膨润土同时去除水中铅、锌、镉、砷及其作用机制研究
程冰冰,莫伟,苏秀娟,余畅,黄钰华,何春彦
(广西大学资源环境与材料学院, 广西南宁530004)
0 引言
随着社会经济的快速发展,我国对矿产资源的需求日益增加,矿产资源在推动经济发展的同时,也带来了日益严峻的矿山环境污染问题[1-4]。我国尾矿废水年排放量巨大,由于尾矿砂颗粒小,因此易氧化分解,释放重金属离子。尤其对于多金属硫化矿尾矿,因金属矿物多以硫化物形式存在其中,而硫化矿物化学活性高,氧化后使水体成酸性,更易使有害重金属离子淋溶出来,进入环境,对环境造成极大危害[5]。硫化矿尾矿废水中的重金属污染物主要有铜、锌、铅、砷、镉、铬、汞、锑等[5]。这些重金属无法降解且易于富集,对人体及动植物危害大,治理成本高,若不妥善处理会导致周边土壤、水体及大气受到不同程度的污染,因此,含重金属离子的硫化矿尾矿废水处理已成为国内外的研究热点。
近些年国内外出现了许多处理重金属废水技术,如化学沉淀法、电解法、吸附法、离子交换法、膜分离法、生物法等[6]。其中,吸附法是处理含重金属离子废水的一种很有前途的方法,具有操作简单、费用低廉等优点[7]。吸附法常用的吸附剂包括活性炭、沸石、膨润土、壳聚糖、生物吸附剂[8]等。在种类繁多的吸附剂中,以膨润土为代表的天然黏土吸附剂具有非常广阔的应用前景。
膨润土的主要矿物组成为蒙脱石,其晶体结构是由两层硅氧四面体片和一层夹于其间的铝氧八面体片构成的2∶1型层状硅酸盐矿物[9]。八面体中有部分Al3+被Mg2+置换,四面体中有部分Si4+被Al3+置换,由此便产生了层间电荷,该不平衡电荷主要由层间阳离子Na+、Ca2+等来补偿[10]。这些可交换阳离子在去除水溶液中的金属阳离子中起着重要作用。研究表明,膨润土的比表面积通常为30~100 m2/g[11-13],比表面积相对较大,从而具有较高的表面能和较大的吸附能力,同时,膨润土还具有较高的阳离子交换容量,因此膨润土在重金属废水处理领域中受到越来越多关注。
国内外大量研究报道了利用膨润土或其复合材料去除水溶液中铅、锌、镉等重金属阳离子。如Esmaeili等[14]研究表明新型天然膨润土(NNB)对Pb(Ⅱ)和Zn(Ⅱ)的最大吸附量分别为8.55、7.90 mg/g。Pawar等[15]采用活化膨润土-海藻酸盐(ABn-AG)复合微球去除Cu2+和Pb2+,结果表明,在pH=2时Cu2+去除率为58%,Pb2+去除率为77%,对Cu2+和Pb2+的最大吸附量分别为17.30、107.52 mg/g,Cu2+和Pb2+是通过与ABn-AG中不同吸附位点相结合而被去除的。Filippidis等[16]研究发现膨润土对单一金属体系中Cd2+、Cu2+、Ni2+和Pb2+的单分子层吸附量分别为31.25、32.26、26.32、85.47 mg/g。Taha等[17]研究表明埃及钠活化膨润土(Na-AB)对Pb(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)的Langmuir单分子层吸附容量分别为5.43、3.14、2.77 mg/g,对受污染海水的应用研究表明,除Pb(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)外,对Cu(Ⅱ)、Mn(Ⅱ)、Cr(Ⅲ)、Zn(Ⅱ)等共存金属的去除率均达到92%~100%。Mu等[18]研究发现膨润土对镉的最大吸附量为15.07 mg/g,吸附机理主要是离子交换。此外也有部分学者对膨润土进行改性后用于砷的去除。如Barakan等[19]利用改性膨润土去除碱性废水中的砷离子,发现其对砷的吸附去除率大于70%,吸附机理主要是络合作用。Mutar等[20]利用纳米膨润土去除水溶液中的砷,采用中心复合设计优化pH(5.5)、膨润土用量(100 mg/L)和接触时间(5 min),并得到最大吸附量为8.659 2 mg/g。Saleh等[21]采用膨润土/壳聚糖/二氧化钛(BT/CS-TiO2)去除水介质中的砷,发现BT/CS由于静电作用和表面络合作用,对As(V)具有较高的吸附量(160 mg/g)。
综上可知,膨润土对含重金属阳离子(如铅、锌、镉等)废水具有很好的去除效果,在尾矿废水处理方面应用广泛,然而,目前膨润土对重金属离子的吸附多为一元、二元、三元离子共存研究,而对重金属阴离子尤其是阴阳离子共存的竞争性吸附研究报道仍较少,作用机制亦不明确。本文旨在通过膨润土对水中共存铅、锌、镉、砷4种重金属离子的吸附特性研究,探讨其对重金属离子吸附能力的差异以及作用机制,为开发利用高效环保的去除重金属阴阳离子新材料提供理论依据。
1 材料与方法
1.1 原料、试剂及仪器设备
试验用原料:试验用膨润土购自辽宁建平某膨润土企业,为干法提纯膨润土,矿样经2 h烘干及混匀缩分后装袋备用。其主要化学元素组成为SiO2(53.4%)、 Al2O3(14.8%)、MgO(7.72%)、Fe2O3(5.23%)等。经测定,样品为钙基膨润土,其中蒙脱石含量为88.14%,阳离子交换容量为121 mmol/100 g,比表面积为109.66 m2/g。
试验用试剂:Zn(NO3)2·6H2O、Cd(NO3)2·4H2O、Pb(NO3)2、HNO3、NaOH等购自天津大茂化学试剂厂,为分析纯;HCl、KBH4、KOH、抗坏血酸(C6H8O6)、硫脲(CH4N2S)等购自上海国药集团化学试剂有限公司,为优级纯;铅、锌、镉、砷等标准溶液购自国家有色金属及电子材料分析测试中心;试验中所用水均为超纯水。
1.2 吸附试验
溶液配制:分别称取(1.598 5±0.000 5) g的Pb(NO3)2、(4.555 7±0.000 5) g的Zn(NO3)2·6H2O、(2.744 2±0.000 5) g的Cd(NO3)2·4H2O及20 mL的砷标液溶解于超纯水中,并定容于1 000 mL,配置成铅、锌、镉离子质量浓度均为1 000 mg/L、砷离子质量浓度为20 mg/L的标准储备溶液。试验采用的一系列不同初始浓度的混合溶液可由上述储备液稀释得到。
吸附实验:准确称取1 g的膨润土,将之加入到50 mL不同初始浓度的混合溶液中,用浓度为1 mol/L的HCl和NaOH调节溶液的pH值,然后在室温下于水浴振荡器上振荡一定时间后,对样品进行离心分离,取上清液经0.45 μm滤膜过滤,测定废水实际初始浓度和滤液中各离子的剩余浓度,并计算各离子去除率及吸附容量。吸附容量和去除率分别按式(1)和式(2)计算。
(1)
(2)
式中:qt为吸附时间为t时,单位质量膨润土的吸附量,mg/g;C0为废水中吸附质的初始浓度(实测浓度),mg/L;Ct为吸附时间为t时,废水中吸附质的剩余浓度,mg/L;m为吸附剂的质量,g;V 为废水的体积,L。
1.3 表征
采用X射线衍射仪(XRD,D8 Advance型,德国)对材料的晶体结构及物相进行了检测,Cu 靶辐射(0.154 18 nm),电压40 kV,电流40 mA,步长0.02°,测试速度0.1 sec/step,扫描范围3°~70°。样品表面官能团由傅里叶红外光谱仪(FT-IR,Nicolet iS5型,美国)测得,采用KBr压片法在400~4 000 cm-1波数范围内检测。样品表面的元素和化学态由X射线光电子能谱(XPS,XPS/INA-X,德国)进行分析。
溶液中重金属阳离子浓度由电感耦合等离子体发射光谱仪(ICP-AES,赛默飞世尔科技,中国)进行测定,砷浓度由原子荧光分光光度计(AFS,AFS-8220型,中国)测定。
2 结果与讨论
2.1 膨润土对水中共存铅、锌、镉、砷的吸附规律研究
2.1.1 吸附时间的影响
Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)配置质量浓度为50 mg/L、As(Ⅴ)质量浓度为1 mg/L,实测质量浓度分别为51.496 3、50.383 7、48.385 2、0.996 5 mg/L,体系pH=2.90条件下,批次称取1 g膨润土分别投入混合溶液中吸附5、10、20、60、120 min后测定重金属离子剩余浓度,结果如图1所示。
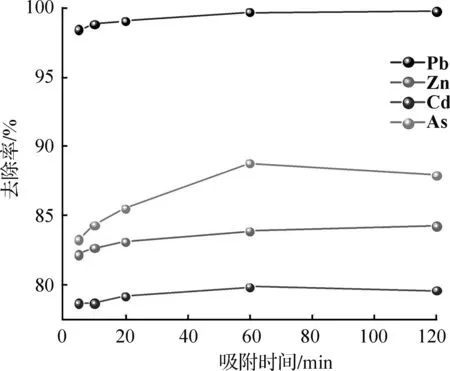
从图1中可以看出,试验条件下,膨润土对Pb(Ⅱ)的吸附速率很快,5 min左右去除率即可达到98%,之后随着时间的延长缓慢增加,最终在60 min达到吸附平衡,此时Pb(Ⅱ)的平衡吸附量为2.567 mg/g;对Zn(Ⅱ)的去除在前10 min增长迅速,10 min后随时间延长速率变缓,至60 min达到平衡,平衡吸附量为2.114 mg/g;对Cd(Ⅱ)的吸附在5~10 min去除率基本不变,10~20 min吸附速率加快,20 min后缓慢增加,在60 min左右达到吸附平衡,平衡吸附量为1.932 mg/g;膨润土对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)3种阳离子的吸附选择性顺序为Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)。对以阴离子形式存在的As(Ⅴ)而言,去除率在前60 min内迅速增加,在60 min时达到吸附量最大值,为0.044 mg/g,60 min后去除率和吸附量有所下降。综合考虑4种离子的吸附去除率和吸附量可知,60 min后基本达到吸附平衡,故后续实验的吸附平衡时间为60 min。
意识形态工作是党的一项极端重要的工作,能否做好意识形态工作,事关党的前途命运,事关国家长治久安,事关民族凝聚力和向心力。全省各级党组织和广大共产党员要牢记,任何时候任何情况下,我们都不能忽视思想的作用和意识形态的力量。要切实增强做好新时代宣传思想工作的自觉性和坚定性,加强理论武装,聚焦重点任务,努力推动我省宣传思想工作守正创新,为建设具有强大凝聚力和引领力的社会主义意识形态、奋力开创我省宣传思想工作新局面提供保障,形成合力。
2.1.2 溶液初始浓度的影响
在吸附剂用量和吸附时间一定的条件下,配置一系列不同初始浓度的混合模拟废水,探究重金属离子初始浓度对吸附效果的影响,结果如图2所示。
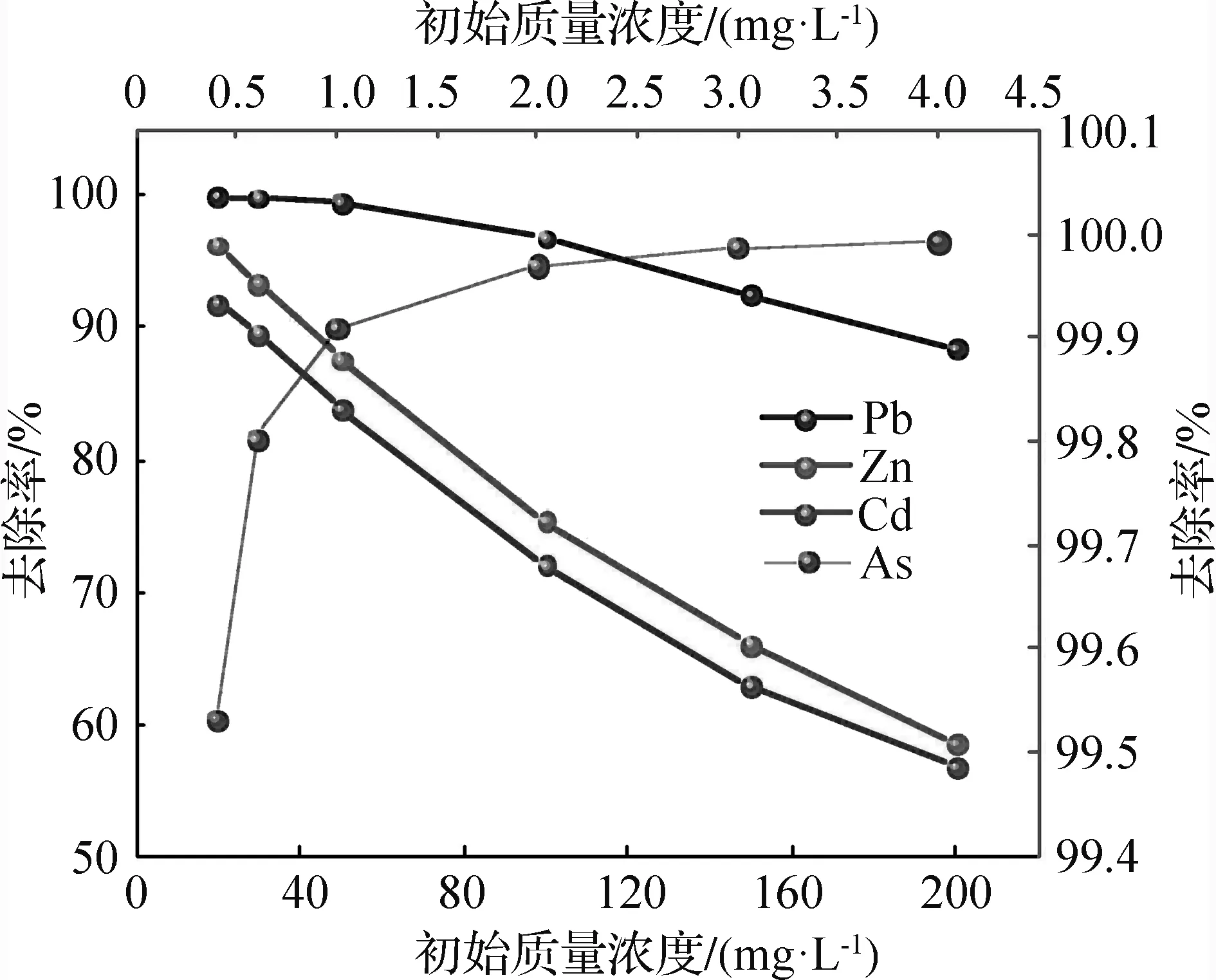
由图2可知,在平衡吸附时间下,膨润土对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ) 3种阳离子的吸附去除率均随着初始浓度的增大而呈下降趋势,只是降幅不同。在初始质量浓度为20~50 mg/L范围内,膨润土对Pb(Ⅱ)的去除率仅下降了0.4%,当初始质量浓度为50~200 mg/L时,其对Pb(Ⅱ)的去除率迅速下降,由99.46% 降至88.35%,说明其它离子的存在对膨润土吸附Pb(Ⅱ)的影响不大;对Zn(Ⅱ)、Cd(Ⅱ)的吸附曲线相似,在初始质量浓度为20~200 mg/L范围内去除率均呈快速下降的趋势,去除率下降了30% 左右,说明其它离子对膨润土吸附Zn(Ⅱ)和Cd(Ⅱ)有一定的抑制作用;对As(Ⅴ)的去除率在初始质量浓度为0.4~1.0 mg/L范围内迅速增加,在1.0~4.0 mg/L范围内增速变缓直至趋于平衡,最大去除率接近100%。同时在试验条件下,膨润土对几种重金属离子的吸附均未达到最大吸附量,可能与重金属离子的初始浓度较低有关,此时其对溶液中Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)的吸附量最大值分别为8.540、4.670、4.556、0.186 mg/g。
2.1.3 溶液初始pH值对吸附效果的影响
Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)配置质量浓度为100 mg/L,As(Ⅴ)质量浓度为2 mg/L,实测浓度分别为98.212 0、87.018 0、85.021 0、1.835 8 mg/L,pH值控制在3~7,探究初始pH值对吸附效果的影响,结果如图3所示。
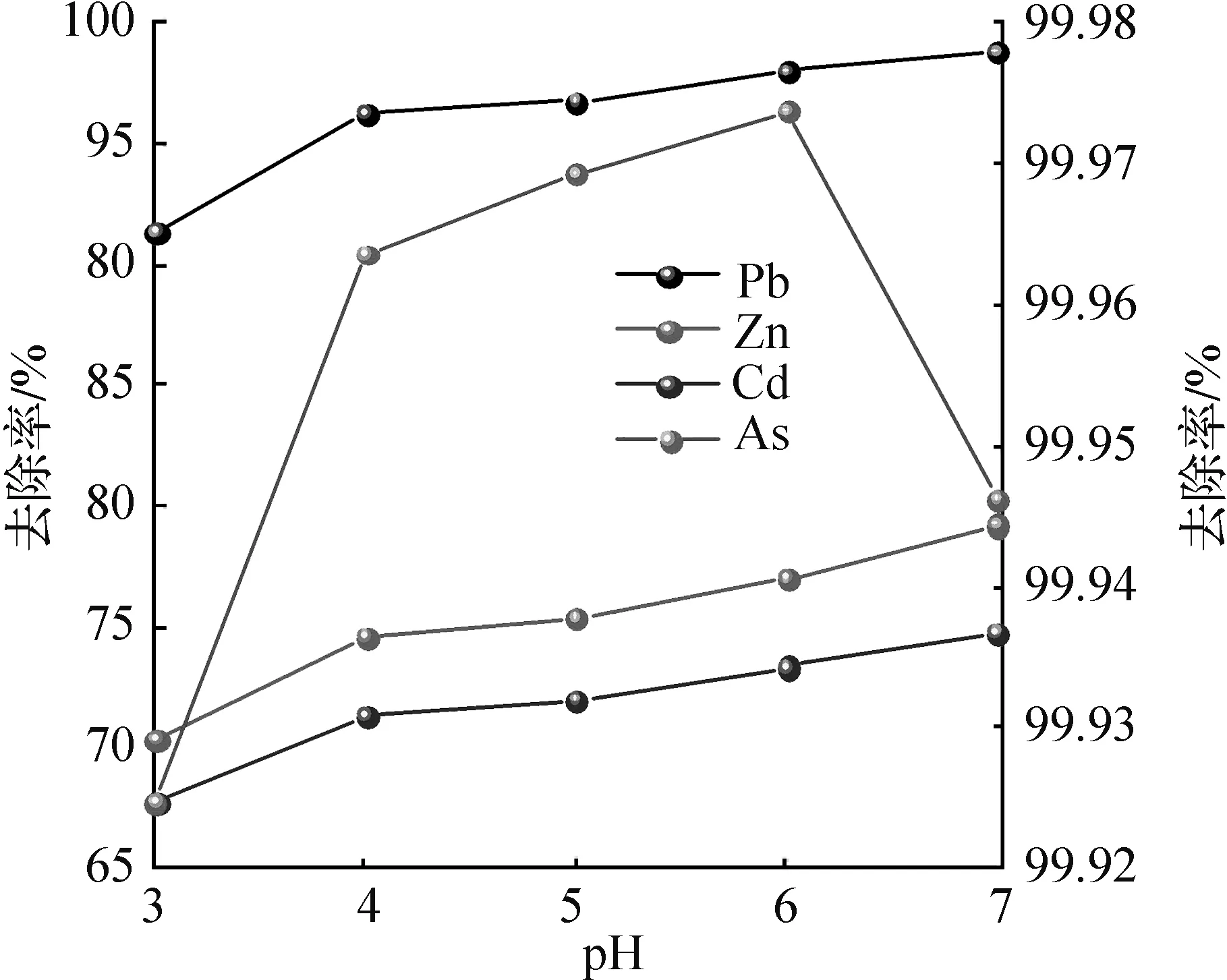
由图3可知,对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)3种离子的去除率在pH<5时缓慢增加,在pH值为5~7时,去除率迅速增大,这是因为在低pH值下,Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)通常以Pb2+、Zn2+、Cd2+及PbOH+、ZnOH+、CdOH+等形式存在于水溶液中,同时溶液中H+含量较高,与重金属离子形成了竞争吸附,不利于膨润土与重金属离子间的离子交换吸附[22],同时查阅相关资料可知,Pb(OH)2、Zn(OH)2和Cd(OH)2开始沉淀pH值均在6~7内,在实验中也发现当调节溶液pH值为6~7时,混合溶液开始变浑浊,此时重金属离子在固体表面发生沉淀[23-25],重金属离子的去除不仅仅有吸附作用,还存在沉淀作用。对As(Ⅴ)的吸附去除率在pH值为3~4时迅速增加,在pH值为4~6时增速变缓,当pH值为6~7时,去除率有所下降但仍不低于99.9%,说明pH值对膨润土吸附砷的影响不大。
2.2 膨润土对水中共存铅、锌、镉、砷的作用机制研究
本文在数据处理过程中发现,利用等温吸附模型和动力学模型对膨润土吸附混合重金属离子的相关数据拟合效果均不佳,说明膨润土吸附混合重金属离子的过程较单一离子复杂,由于各离子间存在相互作用,此无法用单一等温模型和动力学方程解释膨润土对4种离子的吸附机理,因此本试验采用XRD、FT-IR、XPS等表征手段探究膨润土对共存离子的吸附机理。
2.2.1 膨润土吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的XRD分析
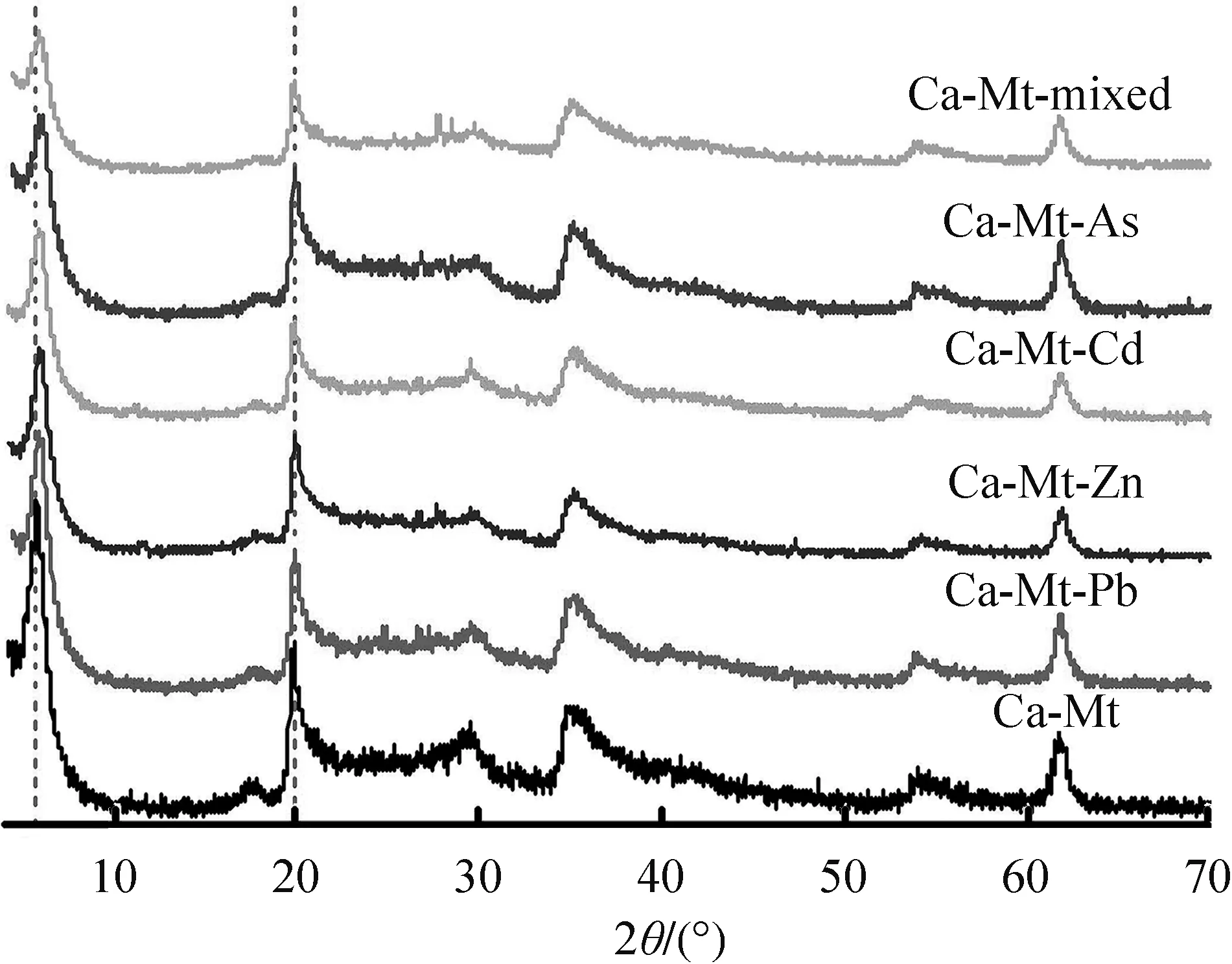
图4 Ca-Mt吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的X射线粉末衍射(XRD)谱图Fig.4 X-ray powder diffraction (XRD) patterns of Ca-Mt after adsorption ofsingle/coexistingPb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)
2.2.2 膨润土吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)前后的FT-IR分析
为探究膨润土吸附重金属离子前后的官能团变化情况,对膨润土吸附单一Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)或As(Ⅴ)以及共存Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的样品进行FT-IR测试分析结果如图5所示,主要FTIR化学键振动法图见表1。
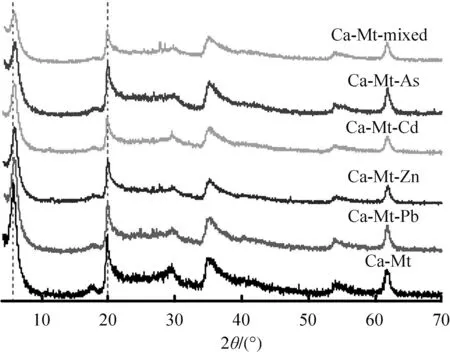
图5 Ca-Mt吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的FT-IR谱图Fig.5 FT-IR spectra of Ca-Mt after adsorption of single/coexisting Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)
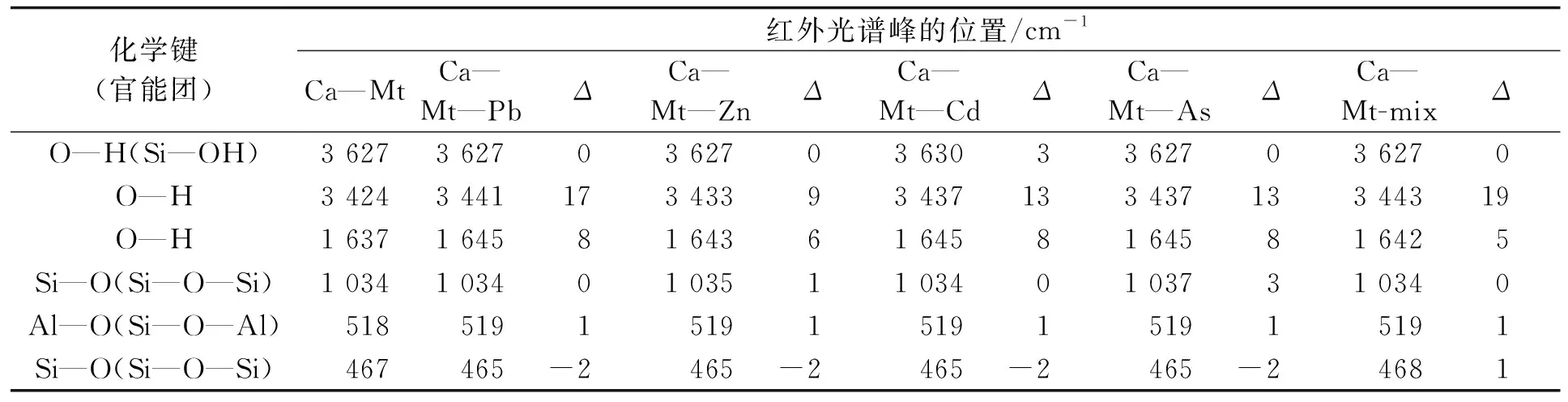
表1 Ca-Mt吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的主要FTIR化学键振动Tab.1 The main FTIR chemical bond vibrations after adsorption of Pb(Ⅱ), Zn(Ⅱ), Cd(Ⅱ) and As(Ⅴ) by Ca-Mt
分析图5可知,膨润土原土在3 627 cm-1处的吸收峰为八面体中的Si—OH伸缩振动吸收峰,3 424 cm-1和1 637 cm-1的吸收峰分别为层间水的伸缩和弯曲振动峰,1 034、518、467 cm-1附近的吸收峰分别为Si—O—Si伸缩振动、Si—O—Al弯曲振动和Si—O—Si弯曲振动吸收峰,表明膨润土表面主要官能团有Si—O、O—H、Al—O。进一步比较可知,当膨润土吸附单一或共存的Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后,相应谱图中并未出现新的吸收峰,仅部分谱带(如518 cm-1处的Si—O—Al/Si—O—Mg,467、1 035 cm-1处的Si—O—Si)出现强度减弱现象;同时还观察到分别位于1 640 cm-1、3 440 cm-1处层间水的吸收峰强度减弱,谱带变宽。此外,由表1可以看出,吸附后,各样品在3 424、1 637 cm-1处的吸收峰(O—H)发生了明显蓝移,说明吸附过程中重金属离子很可能与膨润土表面结合水及吸附水发生了相互作用。
2.2.3 膨润土吸附Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)后的XPS分析
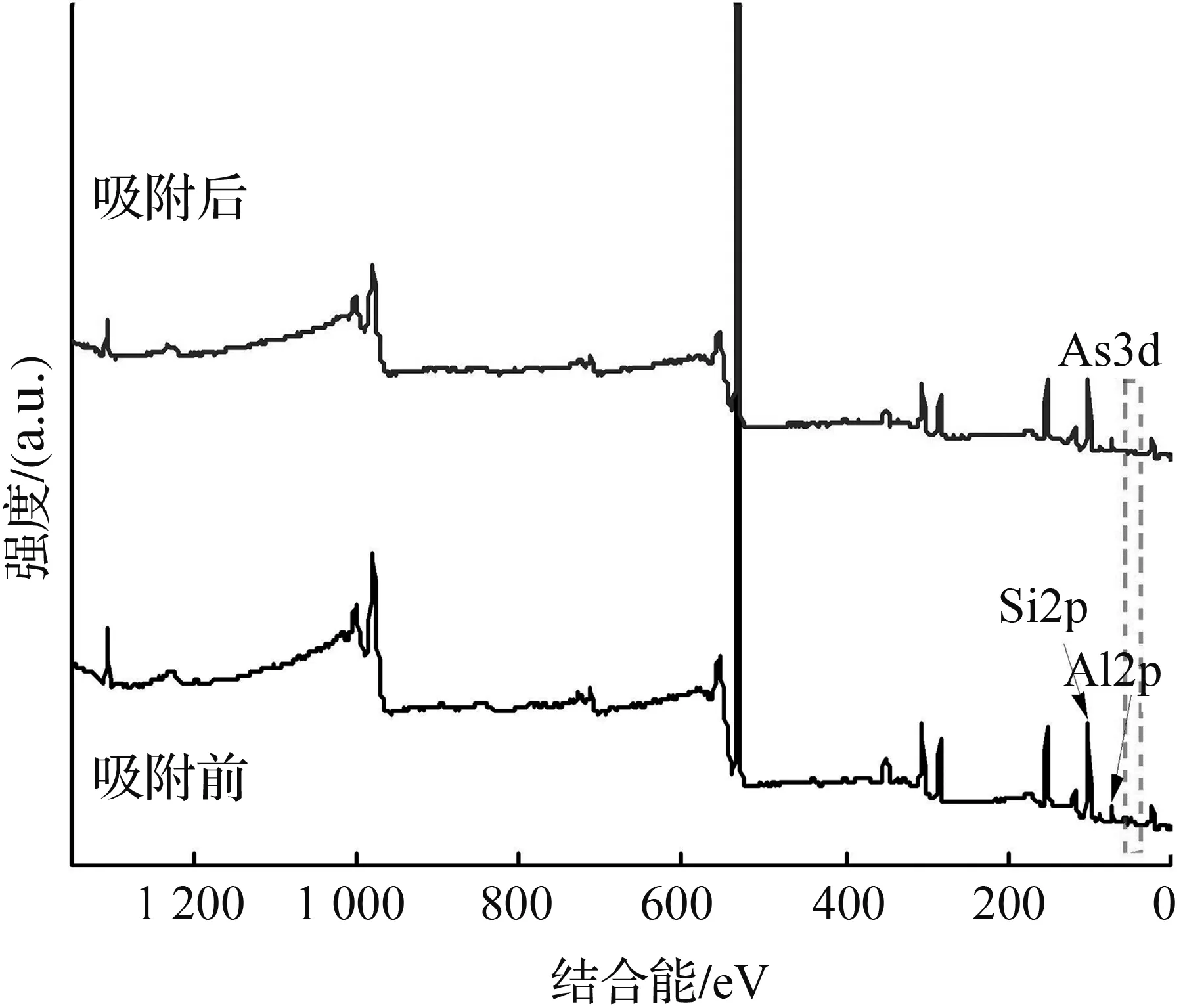
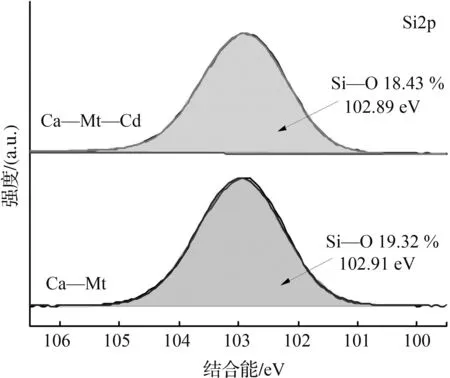
通过XPS分析,可以进一步探讨膨润土对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)的吸附机理。图6为膨润土吸附Pb(Ⅱ)前后的XPS图谱。从图6(a)全谱图可观察到吸附前膨润土含有O1s、Si2p、Al2p这3个主要特征峰,但Al2p的峰值强度较弱,说明铝氧四面体在膨润土表面分布较少,吸附后出现了Pb(Ⅱ)的典型特征峰,说明Pb(Ⅱ)成功吸附到膨润土上。对Pb4f的精细谱进行分峰拟合,结果如图6(b)所示,吸附后Pb4f光谱表现出2种贡献,Pb4f5/2和Pb4f7/2(由自旋轨道分裂产生),归属于Pb—O基团,说明膨润土吸附Pb(Ⅱ)的过程中生成了Pb—O键[26]。对Si2p进行分峰拟合,结果如图6(c)所示,结合能为102.91、102.88 eV的单峰属于Si—O基团[27],比较可知,吸附后Si—O含量略有下降,说明硅氧四面体上的氧与Pb(Ⅱ)发生了络合反应。图6(d)为吸附前后的O1s谱图,比较可知,吸附Pb(Ⅱ)后样品中出现Pb—O特征峰,此时O—H相对含量从吸附前的30.98% 降低为24.12%,由此可推断吸附剂表面的羟基很可能与Pb(Ⅱ)发生了络合反应。综上分析,膨润土对Pb(Ⅱ)的吸附机理可总结如下:①膨润土层板带负电荷,可通过静电作用吸附水中的Pb(Ⅱ);②Pb(Ⅱ)与膨润土层间阳离子发生离子交换反应;③Pb(Ⅱ)与膨润土表面羟基发生络合反应。
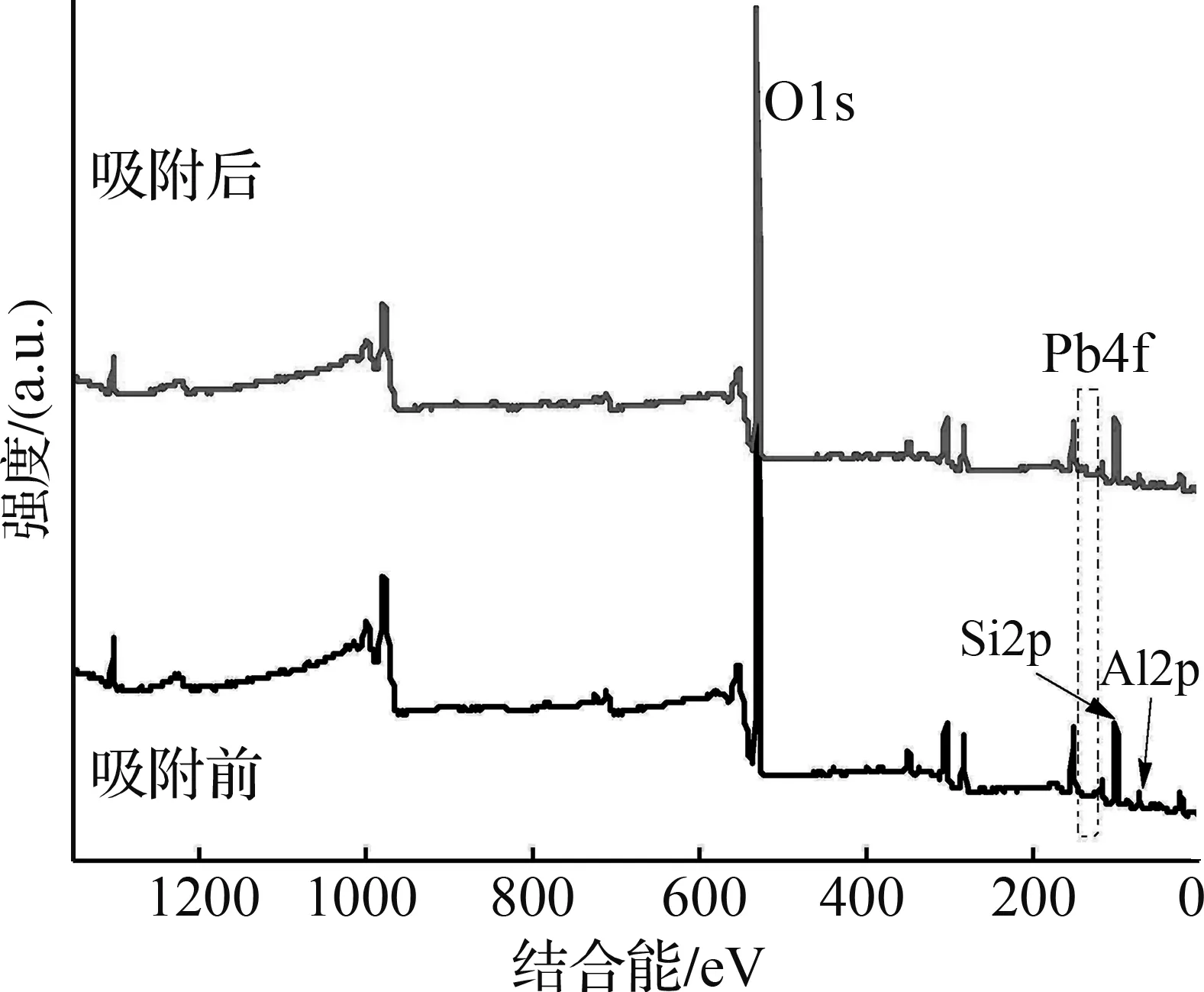
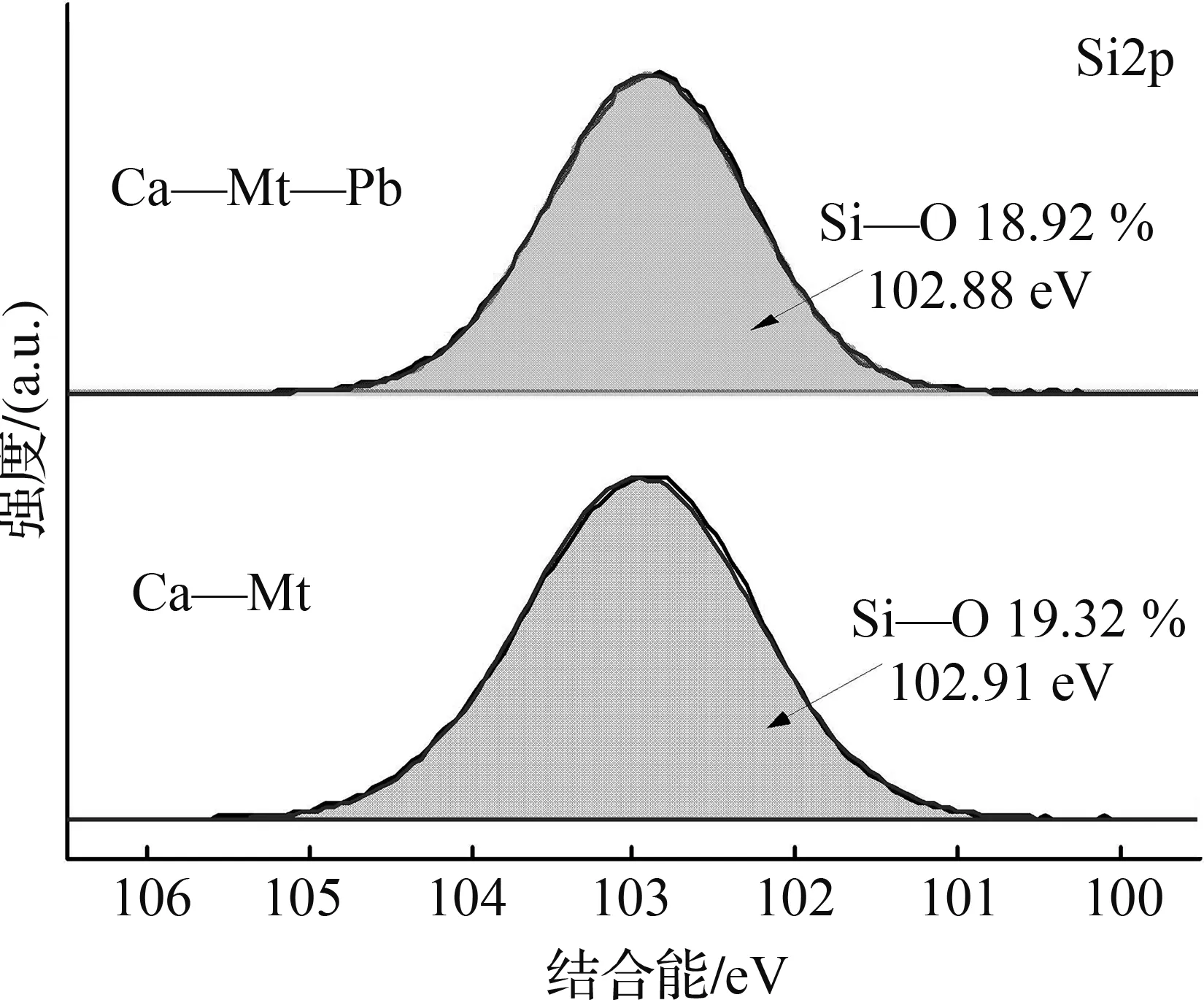
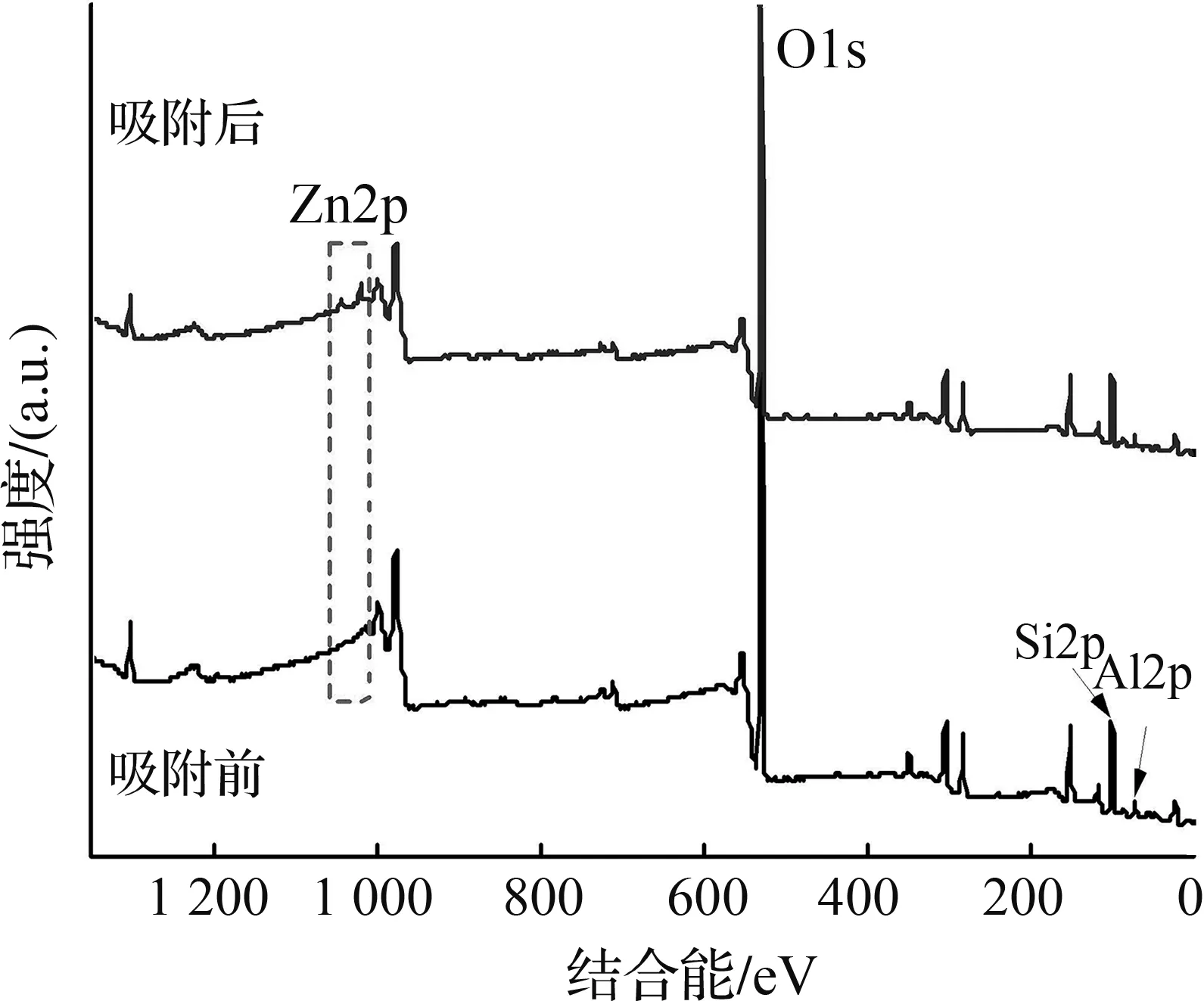
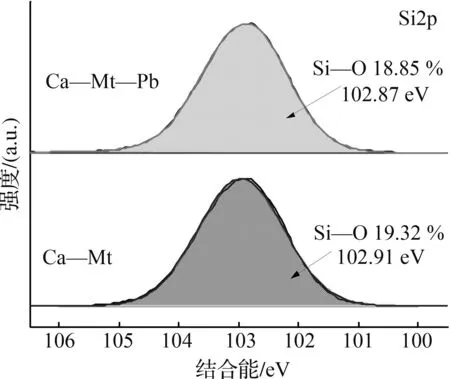
图7为膨润土吸附Zn(Ⅱ)前后的XPS全谱(a)及Zn2p(b)、Si2p(c)和O1s(d)精细谱。由图7(a)全谱图可看出吸附后Zn峰出现。对Zn2p谱进行分峰拟合,结果如图7(b)所示,Zn2p可分出2个峰,结合能分别为1 022.54、1 045.63 eV,均归属于Zn—O基团,表明Zn(Ⅱ)为离子态,且与膨润土表面及层间的羟基氧原子相连。比较吸附前后的O1s谱(图7(d))可看出,吸附后O—H基团含量略有下降,结合能亦有所变化,同时新生成了Zn—O特征峰,说明Zn(Ⅱ)与表面羟基及层间水分子发生了络合反应。
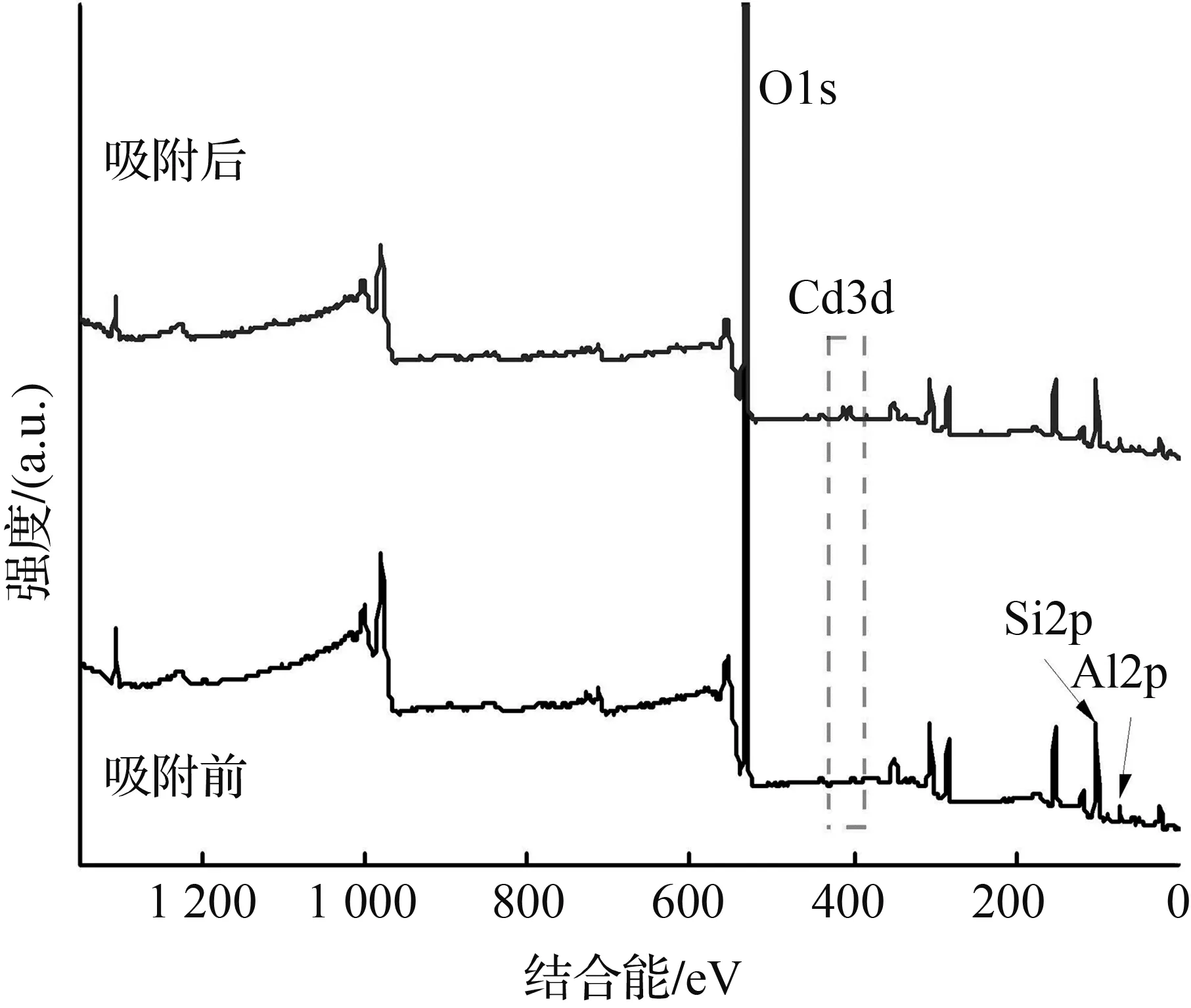
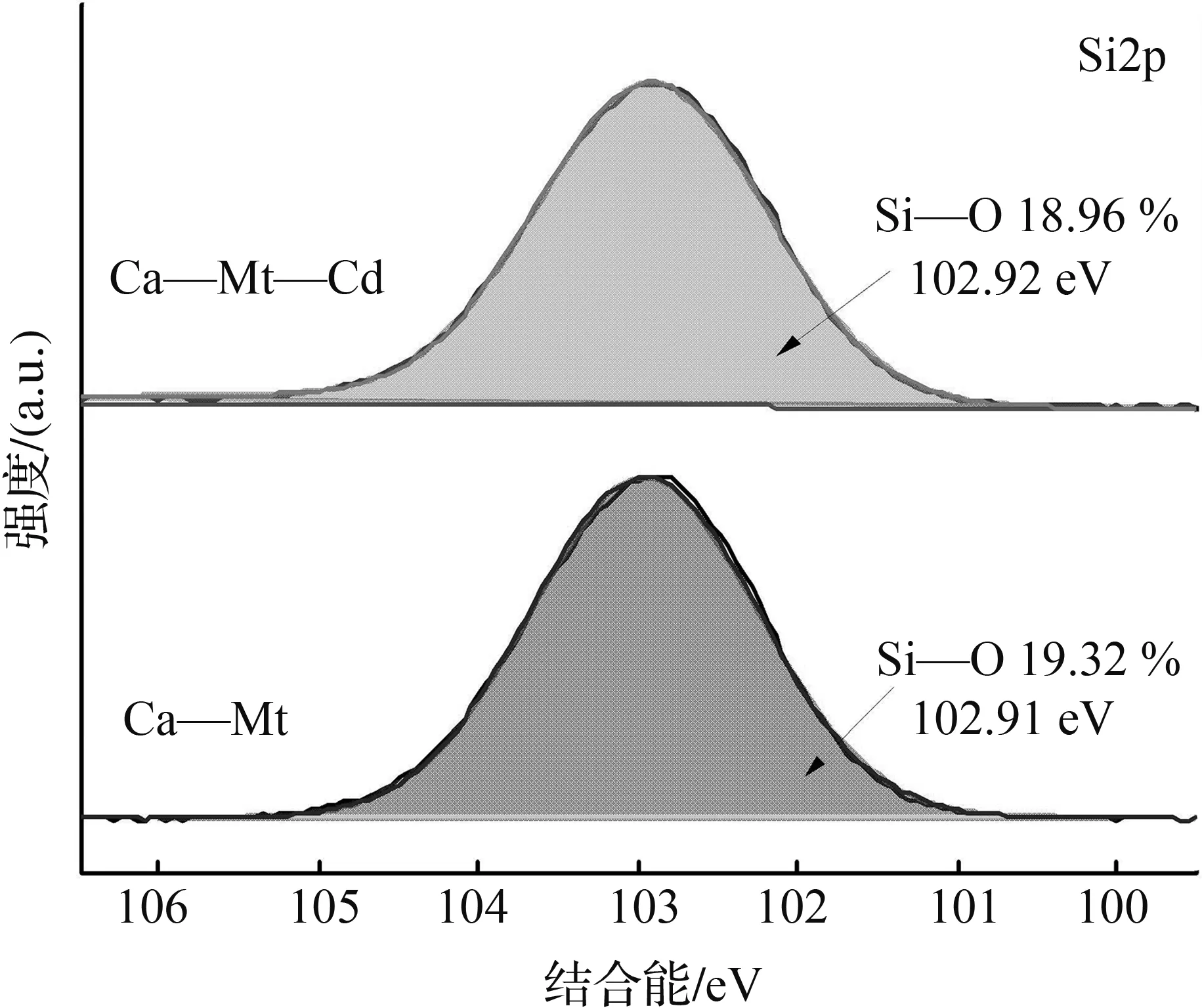
通过XPS研究了膨润土吸附Cd的表面化学特性,进一步证实了膨润土对Cd的吸附机制。膨润土吸附Cd(Ⅱ)前后的XPS谱图如图8所示。XPS全谱(图8(a))显示膨润土由Si、Al、O组成,吸附后的谱图显示了Cd的峰。Cd的高分辨谱如图8(b)所示。在结合能为405.92、412.62 eV处观察到Cd峰,表明Cd通过羟基(—OH)或去质子化形式(O-)的表面络合物吸附在膨润土上[28]。吸附后O1s高分辨谱(图8(d))中出现的Cd—O峰及O—H含量降低进一步证实了膨润土表面羟基和层间水分子与Cd发生了配位作用。
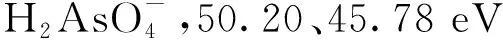
3 结论
为研究开发高效环保的膨润土基复合吸附材料,本文主要开展了膨润土对模拟废水中共存Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)的吸附研究,得出以下结论:
①试验条件下膨润土对重金属阳离子的吸附速率均很快,在5 min后即趋于平衡,对阴离子As(Ⅴ)的吸附速率相对较慢,在60 min时基本达到吸附平衡;膨润土对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ) 4种离子的最大吸附量分别为8.540、4.670、4.556、0.186 mg/g,且其对所考察阳离子的选择性吸附顺序为Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)。
②溶液初始pH值是影响吸附效果的重要因素。当pH值增加时,膨润土对Pb(Ⅱ)、Zn(Ⅱ)、Cd(Ⅱ)、As(Ⅴ)的去除率均显著增加,当初始pH值大于5时,溶液中会出现少量沉淀,此时膨润土对重金属离子同时存在吸附去除和沉淀去除。
③结合XRD、FT-IR及XPS测试分析结果表明,膨润土对Pb(Ⅱ)的吸附主要以静电作用和离子交换为主,同时伴有表面络合反应;对Zn(Ⅱ)的吸附以离子交换和表面络合为主;对Cd(Ⅱ)的吸附以表面络合为主,同时存在离子交换作用;对As(Ⅴ)的吸附主要以表面络合反应为主。

