利用杏鲍菇残渣制备D-氨基葡萄糖盐酸盐的研究*
崔 玮,丁玲强,李佩佩,李学艳,腾 琪,李彩霞,李玉兰
(1.河西学院生命科学与工程学院,甘肃 张掖 734000;2.河西学院实验动物中心,甘肃 张掖 734000;3.甘肃省张掖市甘州中学,甘肃 张掖 734000)
D-氨基葡萄糖盐酸盐 (D-glucosamine hydrochloride,GAH) 呈白色结晶粉末,分子式为C6H13NO5HCl,是甲壳素的一种重要衍生物。氨基葡萄糖化合物类的药物具抗炎、护肝、参与肝肾解毒等作用[1-2]。目前,GAH大多是利用沿海地区动物甲壳中的甲壳素为原料制备[3],具有一定的地理和气候的限制。栽培杏鲍菇(Pleurotus eryngii)时所产生的菌渣中含有大量的菌丝体,而菌丝体细胞壁的主要成分是甲壳素,占细胞壁干重的20%~42%[4],是生产GAH的理想原料。张掖市甘州区是甘肃省最大的杏鲍菇生产基地,每天均会产生许多杏鲍菇残渣,而这些残渣如何进行综合利用需要引起高度关注。目前,尚未有利用杏鲍菇菌渣制备GAH的相关研究。因此,研究旨在探索杏鲍菇残渣中制备GAH的理想工艺,为GAH的生产提供新的方法,同时也为提高杏鲍菇残渣的综合利用价值提供理论依据。
1 材料与方法
1.1 材料
杏鲍菇残渣,于2021年9月由张掖市甘州区张掖市紫家寨农业科技有限责任公司提供。
1.2 试剂和药品
GAH标准品 (纯度≥99%),北京索莱宝科技有限公司;硝酸银 (光谱纯),天津市光复精细化工研究所;氢氧化钠、浓盐酸、乙酰丙酮、碳酸钠、铬酸钾,国药集团化学试剂有限公司;无水乙醇、正丁醇、冰醋酸,天津市致远化学试剂有限公司;对二甲氨基苯甲醛、茚三酮,天津市百世化工有限公司。
1.3 仪器
RE-52AAA旋转蒸发器,温州奥利生物医学仪器厂;AL204电子天平,梅特勒—托利多 (上海)仪器有限公司;JJ-1精密增力电动搅拌器,金坛市城东新瑞仪器厂;DD-5M型大容量离心机,湖南凯达科学仪器有限公司制造;AutopolⅢ-旋光仪,美国鲁道夫公司。
1.4 方法
1.4.1 GAH的制备
1) 杏鲍菇残渣的预处理
预处理时将干燥的杏鲍菇残渣用2%HCl室温浸泡12 h以上,除去无机盐成分,然后用2%的NaOH回流煮沸3 h~4 h,除去蛋白质成分。将经过预处理的原料烘干,粉碎备用[5]。
2) GAH粗品的制备
称取一定量预处理原料,加入三孔反应瓶,按照一定料液比加入一定浓度的HCl搅拌,保持一定温度反应一定时间后,将混合液体移入离心管中,2 500 r·min-1离心10 min,取上清液,在沉淀中加入100 mL蒸馏水淋洗沉淀,离心后将上清液和淋洗液合并过滤,将滤液减压浓缩,待瓶壁析出大量晶体时停止浓缩,将浓缩液与晶体一并转出,加入过量无水乙醇冷却至5℃左右过滤得滤渣即为GAH粗品[6]。
3) GAH的纯化
采取重结晶法[7],将粗GAH晶体溶于沸水中,加入适量活性碳,在60℃下连续搅拌1.5 h脱色。然后将溶液趁热过滤,加入无水乙醇,剧烈搅拌2 h,冷却至5℃左右过滤收集晶体并干燥得白色结晶粉末。
1.4.2 GAH含量的测定
用改进的乙酰丙酮法[8]和Elson-Morgan方法[9]结合测定样品溶液中的GAH含量。
1.4.3 杏鲍菇残渣中GAH得率的测定
GAH得率(G,%) 的计算公式为:

式中:m为实际测得的GAH含量(g);M为杏鲍菇残渣质量(g)。
1.4.4 单因素考察及正交试验
为确定正交试验的因素与水平,考察了反应时间、反应温度、盐酸浓度和料液比 [料液比为质量(g) 与体积(mL) 的比]对GAH粗品得率的影响,分别做3次平行试验。
根据反应结果及统计分析,每个因素下选择3个水平做正交试验。
1.4.5 GAH的层析
采用纸层析法[10]鉴定正交验证试验所得最佳提取条件下制备并纯化的GAH,展层剂为V(正丁醇)∶V(水)∶V(冰醋酸)=4∶3∶1,混合摇匀分层后弃下层。层析后用茚三酮反应试剂显色以及Morgan和Elson反应试剂 [V(正丁醇)∶V(水)∶V(冰醋酸)=4∶3∶1]显色,并计算Rf值,其计算公式为:

式中:s为原点中心至色谱斑点中心的距离(mm);S为原点中心至展层剂前沿的距离(mm)。
1.4.6 氯离子含量的测定
采用硝酸银滴定法测定正交验证试验所得最佳提取条件下制备并纯化的GAH氯离子含量[11]。
1.4.7 GAH样品及标准品的红外光谱分析
在相同条件下测定正交验证试验所得最佳提取条件下制备并纯化的GAH样品和GAH标准品的红外光谱图。
1.4.8 GAH的比旋光度
准确称取1.00 g GAH样品,迅速溶解于重蒸水中,定容至50 mL。每隔10分钟在旋光仪上测定20℃时溶液旋光度,计算出比旋光度,绘制比旋光度随时间的变化曲线[12],比旋光度的计算公式为:

式中:α为旋光度(°);L为旋光管长度(dm);C为测试样品的质量浓度(g·mL-1);D为旋光仪光源钠光的波长(589 nm)。
2 结果与分析
2.1 单因素水平结果与分析
2.1.1 反应时间对GAH得率的影响
不同反应时间对GAH得率的影响结果见图1。
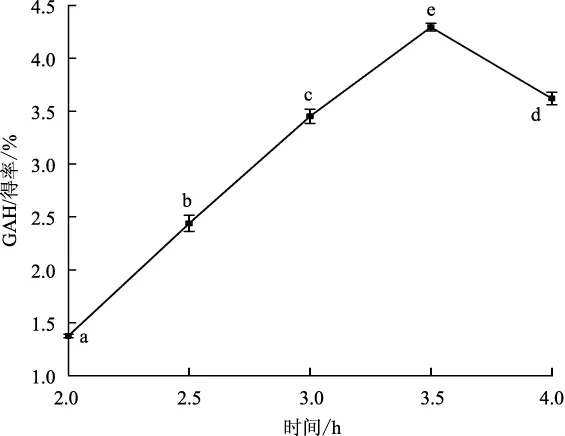
图1 反应时间对GAH得率的影响Fig.1 Effect of reaction time on the yield of GAH
由图1可知,当反应时小于3.5 h,随着反应时间的延长GAH得率呈持续上升的趋势;反应超过3.5 h后,GAH得率开始下降。原因可能是反应时间过长,GAH在水解过程中发生复合与再分解反应[13]。考虑生产效率,选择3.5 h为最适水解时间。
2.1.2 反应温度对GAH得率的影响
不同反应温度对GAH得率的影响结果见图2。

图2 温度对GAH得率的影响Fig.2 Effect of temperature on yield of GAH
由图2可见,随反应温度的升高,GAH得率先增加后降低。温度过高,导致DAH的复合与分解反应增加,生成一些低聚糖与非糖物质,使成品颜色加深[13]。因此,选择100℃为反应的最适温度。
2.1.3 盐酸浓度对GAH得率的影响
盐酸浓度对GAH得率的影响结果见图3。

图3 盐酸浓度对GAH得率的影响Fig.3 Effect of hydrochloric acid concentration on the yield of GAH
由图3可知,当盐酸浓度较低时,GAH得率随着浓度的增大而增高,水解加快。盐酸浓度为30%时,GAH得率较高,而且得到产品的颜色最白。当盐酸浓度大于30%时,其得率呈下降趋势。可能是当盐酸浓度过低时,不易打开酰胺键,而盐酸浓度过高,副反应增多,粘壁碳化现象较严重,造成得率、质量下降[13]。因此加入盐酸的最适浓度为30%。
2.1.4 料液比对GAH得率的影响
料液比对GAH得率的影响结果见图4。
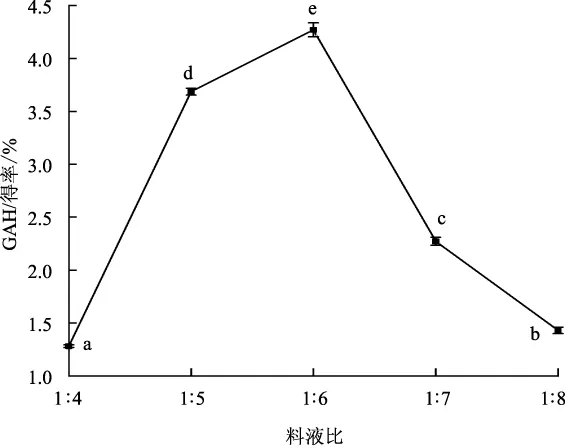
图4 料液比对GAH得率的影响Fig.4 Effect of the ratio of material to liquid on the yield of GAH
图4可知,料液比为1∶6时GAH得率最大。盐酸作为催化剂和水解反应物,用量过少,体系黏度大,反应不充分,且易造成粘壁,增加副反应且得率较低;但用量过高会给后续处理带来困难且明显增加成本,因此最适料液比为1∶6。
2.2 正交试验结果与分析
通过统计分析料液比、反应温度、盐酸浓度以及反应时间4个因素中不同水平对GAH得率的影响,每个因素选择3个水平,设计了4因素3水平的正交试验,分析探究制备GAH的理想工艺,其水平因素设计表见表1,正交试验结果于分析见表2。

表1 正交试验设计因素水平表Tab.1 Factors and levels of orthogonal experiments
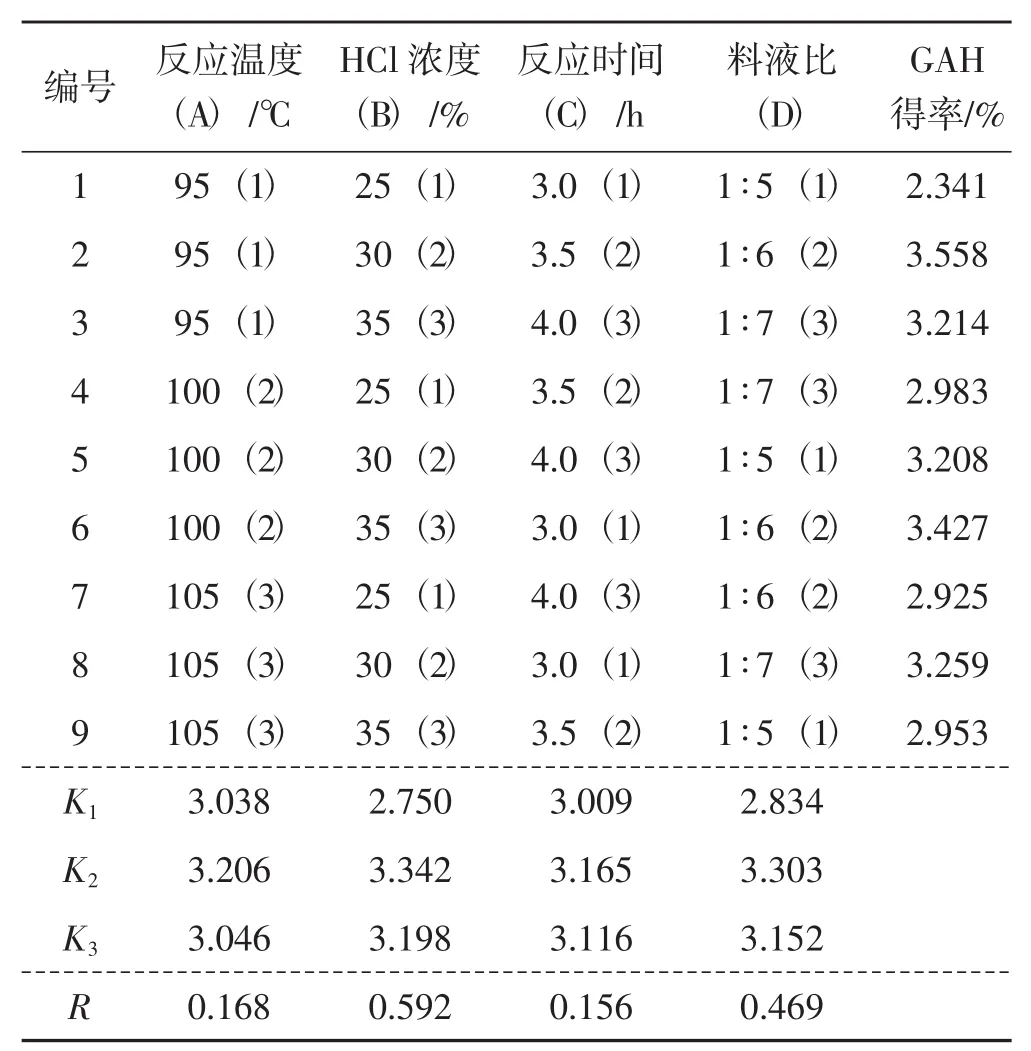
表2 GAH制备工艺优化正交试验结果与分析Tab.2 Results and analysis of orthogonal experiments for GAH preparation process optimization
由表2可知,极差结果R显示:B>D>A>C,即4个因素中对GAH得率影响顺序为:HCl浓度>料液比>反应温度>反应时间,最佳工艺条件为A2B2C2D2,即在料液比为1∶6、盐酸浓度为30%、反应温度为100℃、反应时间为3.5 h时从杏鲍菇残渣中制备GAH的得率最高。对最佳工艺进行验证,进行3组平行试验,GAH的平均得率为5.23%。
2.3 GAH层析分析
根据最佳工艺制备GAH粗品,再采取重结晶法纯化,得白色GAH结晶粉末,以此结晶物进行纸层析分析。纸层析图谱见图5。

图5 GAH层析图谱Fig.5 Paper chromatograms of GAH
由图5可知,用茚三酮试剂显色后样品和标准品均出现一个橘红色斑点,表明该化合物中含有氨基;用Morgan和Elson试剂显色后,样品和标准品也都出现一个红色斑点,说明有氨基葡萄糖存在。2个GAH样品斑点的Rf值均为0.34,与GAH标准品的Rf值一致,说明试验制备的GAH的纯度较高。
2.4 氯离子含量
经计算可得,根据最佳工艺从杏鲍菇残渣制备的GAH(样品)中,氯离子含量为18.14%,接近于标准品中氯离子含量为16.47%。进一步说明试验制备的GAH的纯度较高。
2.5 红外光谱分析
在相同条件下分别测定了GAH标准品和根据最佳工艺从杏鲍菇残渣中制备的GAH样品的红外光谱图,其结果见图6。
由图6可知,所制得的GAH产品在3 280.8 cm-1左右的峰是N-H键的伸缩振动;2 942.7 cm-1左右峰是C-H键的伸缩振动;1 614.8 cm-1左右峰是NH键的面内弯曲振动;1 060.5 cm-1左右峰是C-N键的伸缩振动;912.8 cm-1左右峰是N-H键的面外弯曲振动;与标准品D-GAH红外光谱图相吻合。

图6 红外光谱图Fig.6 Infrared spectrogram
2.6 比旋光度分析
GAH的比旋光度随时间变化的曲线见图7。
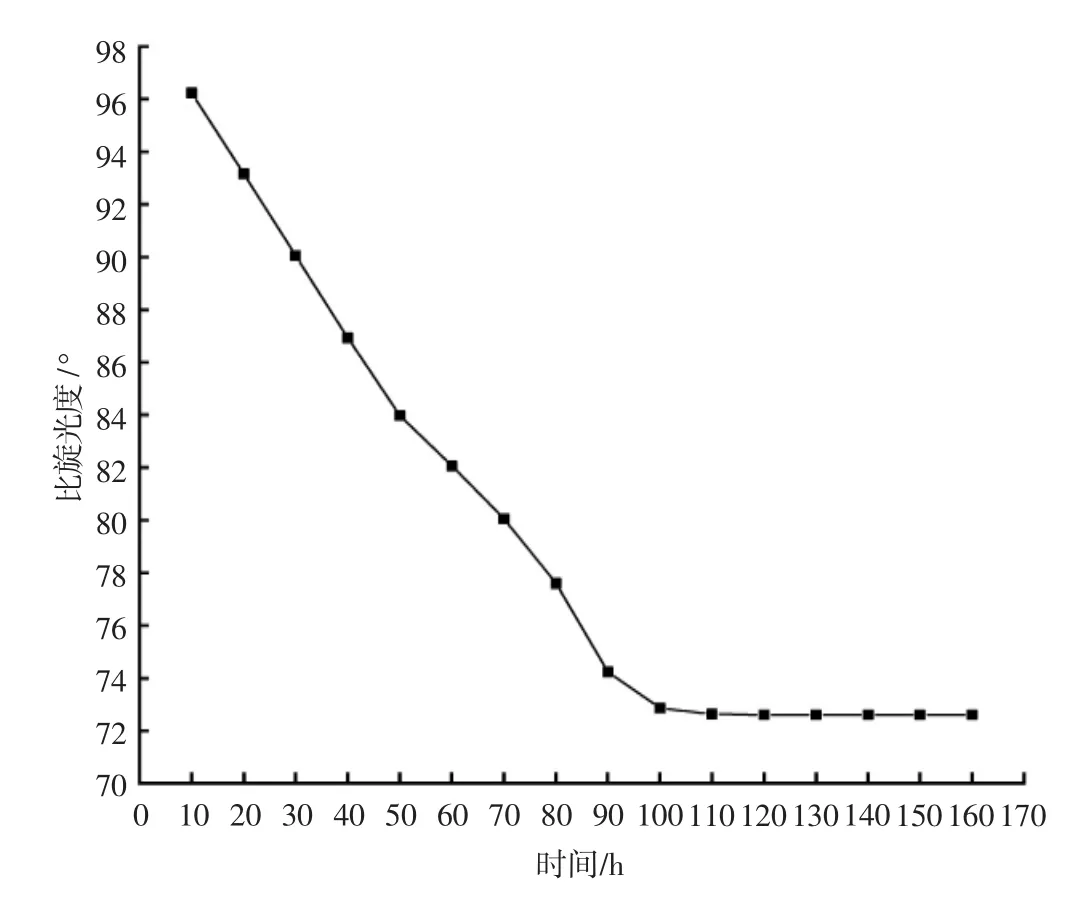
图7 GAH溶液(2%)的比旋光度-时间变化曲线Fig.7 The profile of specific rotatory power of GAH solution(2%)versus time
从图7可以看出,GAH重新溶解于水后出现变旋现象。其刚溶于水时比旋光度值最高,几乎接近100°,随着时间的延长,其比旋光度迅速下降,约2 h后,比旋光度趋于稳定,为71.9°。这一现象可能的原因是,用乙醇进行重结晶的过程中,GAH以α形式析出,当其重新溶解于水中后,α型的GAH将向β型转变,稳定的GAH水溶液是其α型和β型的平衡混合物。
3 结论
试验研究了杏鲍菇残渣制备GAH的反应条件对产物得率的影响,重点研究了反应过程中料液比、盐酸浓度、反应时间和反应温度对得率的影响。通过对工艺条件的探究,通过正交试验及分析,确定最佳反应条件为料液比为1∶6、盐酸浓度为30%、反应温度为100℃,反应时间为3.5 h,在该条件下GAH的得率可以达到5.23%,经层析、氯离子检测、红外光谱和比旋光度分析可知,用该工艺提取的物质为GAH,且纯度较高。因此通过杏鲍菇残渣制备GAH的研究为其制备生产提供了新的方法,从而进一步扩展了制备途径,同时也为提高杏鲍菇残渣的综合利用价值提供理论和必要的试验依据,为工业化生产提供参考。

