还原型谷胱甘肽联合更昔洛韦对巨细胞病毒肝炎患儿肝功能CMV DNA和T细胞亚群的影响
谭细妹, 杨 斌, 祁 云, 梁朝霞
(南方医科大学珠江医院, 广东 广州 510000)
巨细胞病毒(cytomegalovirus,CMV)感染是婴幼儿的常见疾病之一,据报道[1],中国新生儿发生巨细胞病毒感染约占3%。并且因患儿身体状况及感染途径的不同,有先天性感染、围生期感染及生后感染,其临床表现亦有不同,以中枢神经系统症状、运动功能障碍、意识障碍及肝损伤等为主要临床表现,其中以CMV感染造成肝损伤为多见,严重时可引起患儿死亡[2]。更昔洛韦是核苷类广谱抗病毒药物之一,其抗病毒功能较强,对免疫功能缺陷的CMV感染患儿的临床治疗具有重要作用[3,4]。本研究将本院收治的86例CMV肝炎患儿作为研究对象,探讨还原型谷胱甘肽联合更昔洛韦对患儿肝功能、CMV DNA及T细胞亚群的影响。
1 资料与方法
1.1一般资料:将本院2019年1月至2021年5月86例CMV肝炎患儿依据简单随机化分组方法分为对照组(n=43)和联合组(n=43)。纳入标准:符合相关诊断标准;经荧光定量聚合酶链式反应法测定尿CMV DNA为阳性。排除标准:伴有重症肺炎、疱疹病毒感染、风疹病毒感染等;伴有先天畸形、先天性心脏病;伴有遗传性疾病、染色体异常疾病等。其中,对照组男26例,女17例;年龄为0.3~36个月,平均为(7.14±0.64)个月。联合组男24例,女19例;年龄为0.2~34岁,平均为(7.22±0.73)个月。两组患儿性别和年龄的比较,差异均无统计学意义(P>0.05)。见表1。本研究内容已通过本院医学伦理委员会批准,且两组患儿的家属均自愿签署知情同意书。
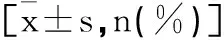
表1 两组患儿一般资料的比较
1.2治疗方法:对照组采取还原型谷胱甘肽(山东绿叶制药有限公司,国药准字H20041265)治疗,静脉滴注0.3~0.6g,每日1次;联合组采取还原型谷胱甘肽联合更昔洛韦(湖北东信药业有限公司,国药准字H20110082)治疗,静脉滴注7.5mg/kg,每日2次,而还原型谷胱甘肽的用法及用量与对照组相同。两组患儿均连续治疗2~4周,或至肝功能恢复正常。
1.3观察指标:①肝功能指标:采用美国贝克曼库尔特公司产全自动生化分析仪(型号为AU5800)分别于治疗前及治疗后1个月,取两组患儿清晨空腹静脉血3mL,检测总胆红素(total bilirubin,TBil)、-谷氨酰转移酶(gamma-glutamyl transferase,GGT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)及谷氨酸氨基转移酶(alanine aminotransferase,ALT)的含量;②尿CMV DNA转阴:采用荧光定量聚合酶链式反应分析仪(美国ABI公司,型号为7500)对两组患儿治疗后尿CMV DNA的转阴情况进行检测,试剂盒购自上海江莱生物科技有限公司;③外周血T淋巴细胞亚群:通过美国 Becton Dicknson公司产流式细胞分析仪(型号为FACSCalibur)对两组患儿治疗前及治疗后1个月外周血CD3+、CD4+、CD8+及CD4+/CD8+进行检测。

2 结 果
2.1两组患儿肝功能指标变化情况的比较:两组患者治疗前血清TBil、GGT、AST及ALT的含量相比,差异均无统计学意义(P>0.05)。治疗后1个月,两组患者血清TBil、GGT、AST及ALT的含量与治疗前相比,差值均为负数,且联合组TBil和GGT的含量与对照组相比,差值均为负数(均P<0.05)。见表2。

表2 两组患儿肝功能指标变化情况的比较
2.2两组患儿尿CMV DNA转阴时间的比较:结果显示,联合组平均尿CMV DNA转阴时间为(17.85±3.83)d,较对照组的(10.04±3.16)d明显缩短(t=10.314,P<0.05)。
2.3两组患儿外周血T淋巴细胞亚群变化情况的比较:两组患者治疗前CD3+、CD4+及CD4+/CD8+相比,差异均无统计学意义(P>0.05)。治疗后1个月,两组患者CD3+、CD4+及CD4+/CD8+与治疗前相比,差值均为正数,CD8+与治疗前相比,差值为负数,且联合组CD4+与对照组相比,差值为正数(均P<0.05)。见表3。
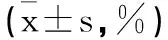
表3 两组患儿外周血T淋巴细胞亚群变化情况的比较
3 讨 论
CMV感染的发生,是与病原体致病力和宿主防御力存在显著关系,当宿主接触CMV后可通过Toll样受体9可识别CMV,对CMV启动特异性及非特异性免疫应答,建立起抗CMV感染的屏障[5]。此外,CMV肝炎在新生儿时期易感疾病,也是人CMV感染的主要临床发病类型,以黄疸消退延长、肝脾肿大等为主要特征,部分患儿伴有肝功能衰竭[6]。目前,临床可通过荧光定量聚合酶链式反应法检测尿CMV DNA有助于对CMV感染进行诊断,若检测结果为阳性则可进一步判定CMV感染并及时采取积极有效的治疗措施[7]。在肝脏发生损伤时,促使氧化应激反应产物增多,细胞外钙离子超载,使得细胞内还原型谷胱甘肽生物合成能力减弱[8]。还原型谷胱甘肽的组成部分包括甘氨酸、谷氨酸及半胱氨酸残基,其具有抗氧化活性、清除氧自由基及抗病毒的作用[9]。更昔洛韦作为近年来新型的广谱抗DNA病毒药物之一,其抗病毒作用较强,其药理作用在于可通过竞争性阻滞病毒DNA聚合酶,亦能掺入至病毒DNA,使得DNA复制终止。
CMV的细胞嗜性较广,其靶细胞主要包括内皮细胞、上皮细胞及成纤维细胞[10]。T淋巴细胞是由不同亚群组成,是机体免疫功能的重要组成,在机体正常免疫反应过程中起到重要作用。按照免疫功能的不同,可将T淋巴细胞分为毒性细胞(CD8+)、效应细胞(CD4+)、辅助性细胞(CD3+)等亚群,其中CD3+可与T细胞抗原受体进行结合,可引起T细胞活化,而CD4+与CD8+比值可用于反映细胞免疫状态,在机体免疫反应中发挥重要作用[11]。在机体受CMV感染后,通过分泌毒性物质可促使CD8+T细胞明显增多,可诱导抑制CD3+与CD4+细胞,使CD3+与CD4+细胞含量减少,而造成机体免疫功能异常[12]。因此,及时采取以积极措施进行抗病毒治疗,以纠正机体T淋巴细胞亚群紊乱状态,改善机体免疫功能显得尤为重要。本研究结果显示,治疗后1个月,两组患者CD3+、CD4+及CD4+/CD8+较治疗前明显升高,CD8+较治疗前明显下降,且联合组CD4+较对照组明显升高。结果表明,还原型谷胱甘肽联合更昔洛韦治疗可有效改善CMV肝炎患儿T淋巴细胞亚群紊乱状态,对机体免疫功能的改善具有重要作用。
TBil、GGT、AST及ALT均为临床常用的肝功能检测指标,及时检测这些指标的含量变化对CMV肝炎患儿病情的评估具有重要作用。本研究发现,治疗后1个月,两组患者血清TBil、GGT、AST及ALT的含量较治疗前均明显减少,且联合组TBil和GGT的含量较对照组均明显减少。此外,本研究中,联合组平均尿CMV DNA转阴时间为(17.85±3.83)d,较对照组的(10.04±3.16)d明显缩短。结果表明,还原型谷胱甘肽联合更昔洛韦治疗可有效减轻CMV肝炎患儿肝功能损害,促进肝功能恢复,对患儿病情的改善具有重要作用。
综上所述,还原型谷胱甘肽联合更昔洛韦治疗可有效减轻CMV肝炎患儿肝功能损害,促进肝功能恢复,具有良好的临床疗效,值得临床应用。

