化妆品中10种α-羟基酸的高效液相色谱检测及质谱确证
郑梅,贾昌平(苏州市药品检验检测研究中心,江苏 苏州 215104)
抗皱、延缓皮肤衰老是大多数亚洲女性一直关注的美容问题之一。α-羟基酸,又称果酸,作为一种能促进皮肤再生的皮肤调理剂广泛用于护肤类化妆品中[1-3]。α-羟基酸是在羧基(-COOH)面第一个(α)碳原子位置上有一个羟基(-OH)的有机酸[4]。近年来α-羟基酸换肤已成为一种美容护肤的新趋势,但诱发的皮肤过敏问题也屡见不鲜[5]。美国FDA在2006年发表了一份关于α-羟基酸的研究报告显示,长期使用α-羟基酸可能会减弱皮肤对紫外线的抵抗力,使皮肤老化,加速细胞的破坏或死亡,导致皮肤发红、起泡及灼伤,可能给皮肤造成永久性的伤害,其长期的安全性无法得到保障[6-7]。因此须严格控制α-羟基酸的含量。
我国2015年版《化妆品安全技术规范》规定化妆品配方中α-羟基酸总量不得大于6%,但只检测了酒石酸、羟基乙酸、苹果酸、乳酸和柠檬酸5种成分[8]。2019年国家药品监督管理局发布的第12号通告中提供了10种α-羟基酸的液相检测方法,但实际应用中发现,部分样品在待测物出峰位置存在杂质干扰,这对检测方法的专属性提出了更高的要求。目前,关于化妆品中α-羟基酸的检测方法主要有高效液相色谱法、高效液相色谱-串联质谱法、气相色谱法、离子色谱法等[9-12],但仅检测了酒石酸、羟基乙酸、苹果酸、乳酸和柠檬酸,远不能满足对化妆品中实际使用的多种α-羟基酸检测的需要。考虑到化妆品基质种类较多,成分复杂,本文采用高效液相色谱法同时测定化妆品中10种α-羟基酸的含量,并对阳性样品进行液相色谱-串联质谱法确证,避免假阳性结果的产生,以期为化妆品中10种α-羟基酸的质量监管提供技术参考。
1 材料
1.1 试药
1.2 仪器
Waters e2695高效液相色谱仪(美国Waters公司);Agilent 6538高效液相质谱仪(美国Agilent公司);KQ-300DA型数控超声波清洗器(昆山市超声仪器有限公司)。
2 方法与结果
2.1 溶液的制备
2.1.1 混合对照品溶液 分别精密称取葡糖醛酸、酒石酸、羟基乙酸、苹果酸、乳酸、柠檬酸、2-羟基丁酸、扁桃酸、二苯乙醇酸、羟基辛酸对照品适量,置于同一50 mL的量瓶中,用水溶解并稀释成质量浓度分别为4.0、2.0、4.0、4.0、5.0、4.0、5.0、0.1、0.1、4.0 mg·mL-1的混合对照品溶液。
2.1.2 供试品溶液 称取样品约1 g(精确到0.0001 g)置于10 mL具塞比色管中,置于90℃水浴中30 min以去除挥发性有机溶剂,加水至10 mL,涡旋混合30 s,60℃超声提取30 min,取适量样品在10 000 r·min-1下高速离心15 min,上清液用0.45 μm滤膜过滤,作为供试品溶液[8]。
2.1.3 阴性样品溶液 取空白膏霜剂作为阴性样品基质,按“2.1.2”项下方法制备阴性样品溶液,即得。
2.2 色谱与质谱条件
2.2.1 高效液相色谱条件 色谱柱:SHISEIDO CAPCELL PAK C18AQ(4.6 mm×250 mm,5 μm);流动相A为0.1 mol·L-1的磷酸氢二铵溶液(磷酸调pH 2.45),流动相B为甲醇;柱温30℃;检测波长214 nm;进样量5 μL;梯度洗脱程序见表1。
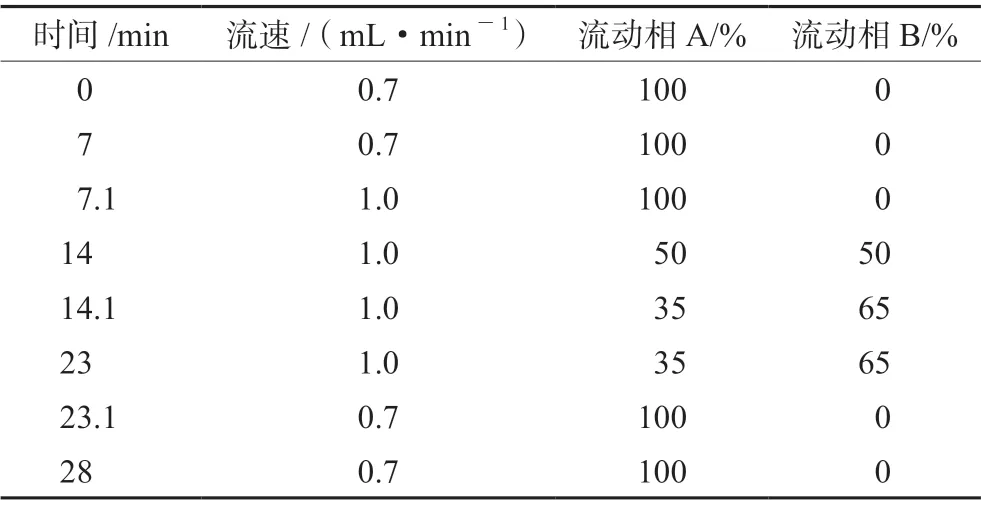
表1 梯度洗脱程序 Tab 1 Gradient elution program
2.2.2 高效液相色谱-串联质谱确证条件 色谱柱:CORTECS UPLC T3(2.1 mm×100 mm,1.6 μm);流动相以0.1%甲酸水溶液为流动相A,乙腈(0.1%甲酸)溶液为流动相B,梯度洗脱(0~5 min,100%A;5~8 min,100%→5%A;8~9 min,5%A;9~9.1 min,5%→100%A;9.1~10 min,100%A);柱温30℃;流速0.3 mL·min-1;进样量5 μL。电离方式:电喷雾离子源(ESI);扫描方式:负离子检测;检测方式:一、二级全扫描;毛细管电压:3.0 kV;脱溶剂温度:350℃;脱溶剂气流速:600 L·h-1。10种α-羟基酸的质谱参数见表2,二级质谱图见图1。

表2 10种α-羟基酸的质谱分析参数 Tab 2 MS/MS parameters for the detection of 10 α-hydroxy acids
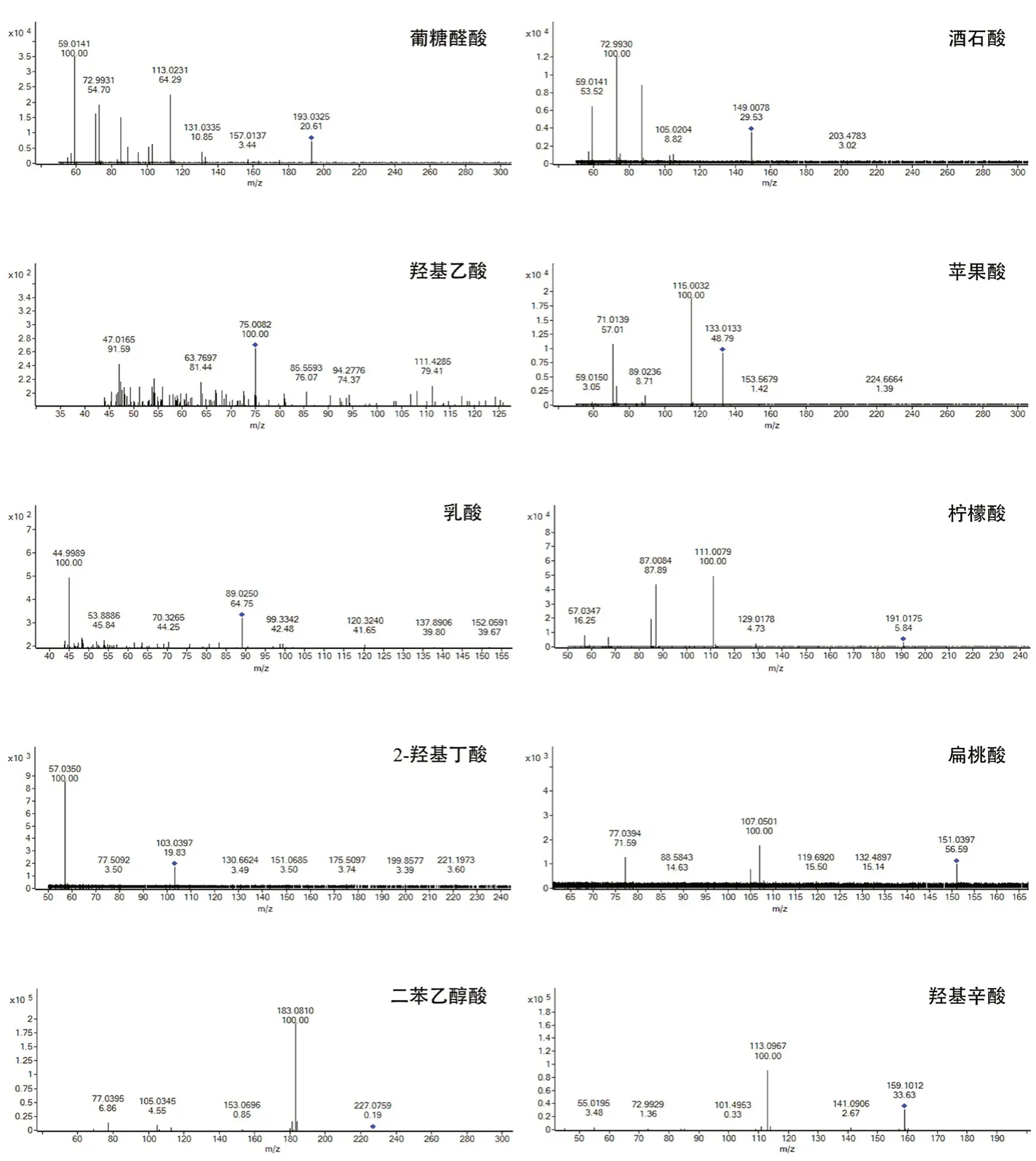
图1 10种α-羟基酸的二级质谱图Fig 1 MS2 spectrum of 10 α-hydroxy acids
2.3 方法学考察
2.3.1 专属性试验 分别取混合对照品溶液、供试品溶液、阴性样品溶液及空白溶剂(水),按“2.2.1”项下方法进样5 μL,结果见图2。空白溶剂和阴性样品溶液不干扰待测物的测定,各峰保留时间适中,分离度良好。

图2 空白溶剂(A)、阴性样品溶液(B)、对照品溶液(C)及供试品溶液(D)典型色谱图Fig 2 Chromatogram of blank solution(A),negative sample solution(B),reference solution(C)and sample solution(D)
2.3.2 线性关系考察 分别精密吸取“2.1.1”项下混合对照品溶液0.25、0.5、1、2、5、10 mL于20 mL量瓶中,加水溶解,稀释至刻度,摇匀,得到系列对照品溶液,分别按“2.2.1”项下方法分别测定,记录色谱图。以质量浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,结果见表3。
2.3.3 定量限与检测限 取“2.1.1”项下混合对照品溶液,用水逐级稀释,按“2.2.1”项下方法测定,以信噪比(S/N)为3和10分别计算仪器的检测限(LOD)和定量限(LOQ),结果见表3。
③企业所得税研发费用加计扣除规定:“企业发生的研究开发费用,未形成无形资产计入当期损益的,在按照规定据实扣除的基础上,按照研究开发费用的50%加计扣除,形成无形资产的,按照无形资产成本的150%摊销。”
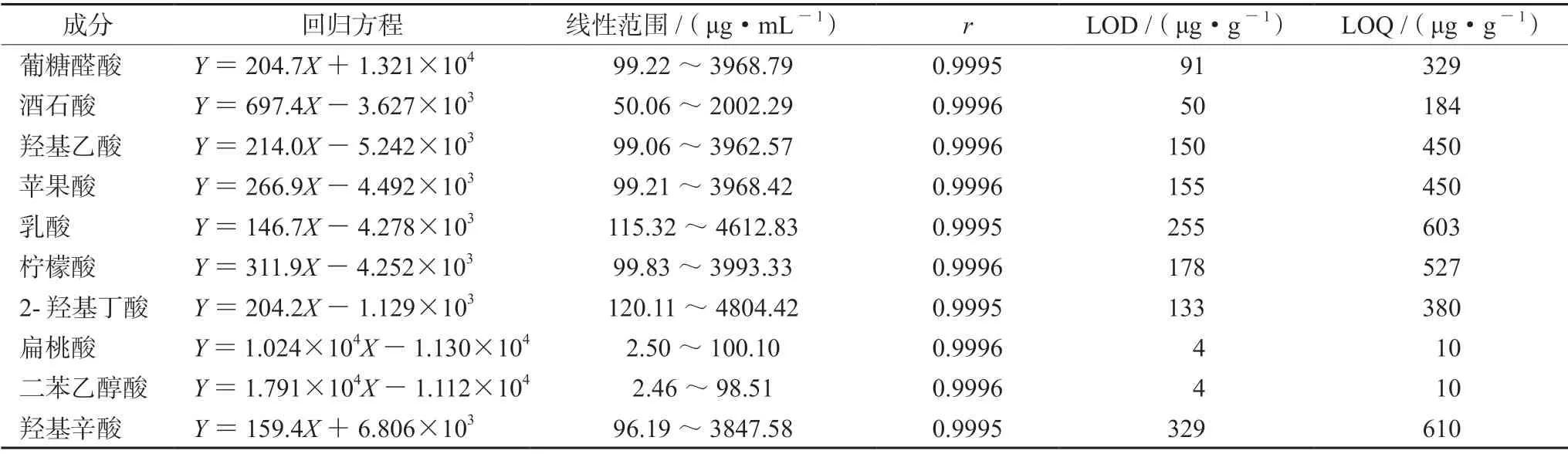
表3 线性关系、检测限和定量限 Tab 3 Linearity,limit of detection and limit of quantization
2.3.4 精密度试验 取“2.1.1”项下混合对照品溶液,按“2.2.1”项下方法重复进样6次,结果10种α-羟基酸峰面积的RSD在0.25%~2.3%,表明仪器精密度良好。
2.3.5 加样回收试验 以空白水剂、膏霜剂、乳剂作为基质考察本方法的回收率。精密称取空白基质1 g于10 mL具塞比色管中,分别加入0.5、2.0、5.0 mL混合对照品溶液,作为低、中、高浓度的加标溶液,按“2.1.2”项下方法制备,每个浓度平行配制3份,进样测定,计算平均加样回收率。结果葡糖醛酸、酒石酸、羟基乙酸、苹果酸、乳酸、柠檬酸、2-羟基丁酸、扁桃酸、二苯乙醇酸、羟基辛酸的加样回收率分别在98.3%~106.5%(RSD在0.40%~4.4%)、100.2%~108.5%(RSD在0.40%~2.2%)、99.6%~108.9%(RSD在0.30%~2.4%)、99.4%~104.6%(RSD在0.30%~3.1%)、102.7%~109.6%(RSD在0.60%~3.0%)、94.7%~105.6%(RSD在1.0%~4.1%)、101.0%~105.3%(RSD在0.60%~4.1%)、94.2%~111.9%(RSD在0.60%~4.8%)、97.5%~106.5%(RSD在0.80%~3.8%)、96.1%~105.6%(RSD在1.1%~4.7%)。
2.3.6 重复性试验 取某批号阳性样品,按“2.1.2”项下方法制备供试品溶液6份,按“2.2.1”项下条件测定,结果样品中乳酸平均含量为0.4%,RSD为1.4%,表明该方法重复性良好。
2.3.7 稳定性试验 取“2.1.1”项下混合对照品溶液,于室温下放置0、1、2、4、8、12、24 h后进样分析,结果葡糖醛酸、酒石酸、羟基乙酸、苹果酸、乳酸、柠檬酸、2-羟基丁酸、扁桃酸、二苯乙醇酸、羟基辛酸峰面积的RSD分别为0.33%、0.25%、2.6%、0.32%、0.47%、0.42%、0.91%、0.65%、1.8%、1.6%,可满足分析测试要求。
2.3.8 样品测定 采用本文建立的方法对30批化妆品进行检测。经高效液相色谱法初筛,3批样品中疑似含有α-羟基酸,需进行液质确证。当样品的提取离子流图中出现与标准品溶液保留时间一致的色谱峰,且色谱峰的一级、二级质谱的特征离子(m/z)信息均一致时,则可判定样品中检出相应的α-羟基酸化合物。结果显示1份样品检出羟基乙酸,含量为0.6%;2份样品检出乳酸,含量分别为0.4%、1.3%;其余样品未检出α-羟基酸。阳性样品液质确证谱图见图3和图4。
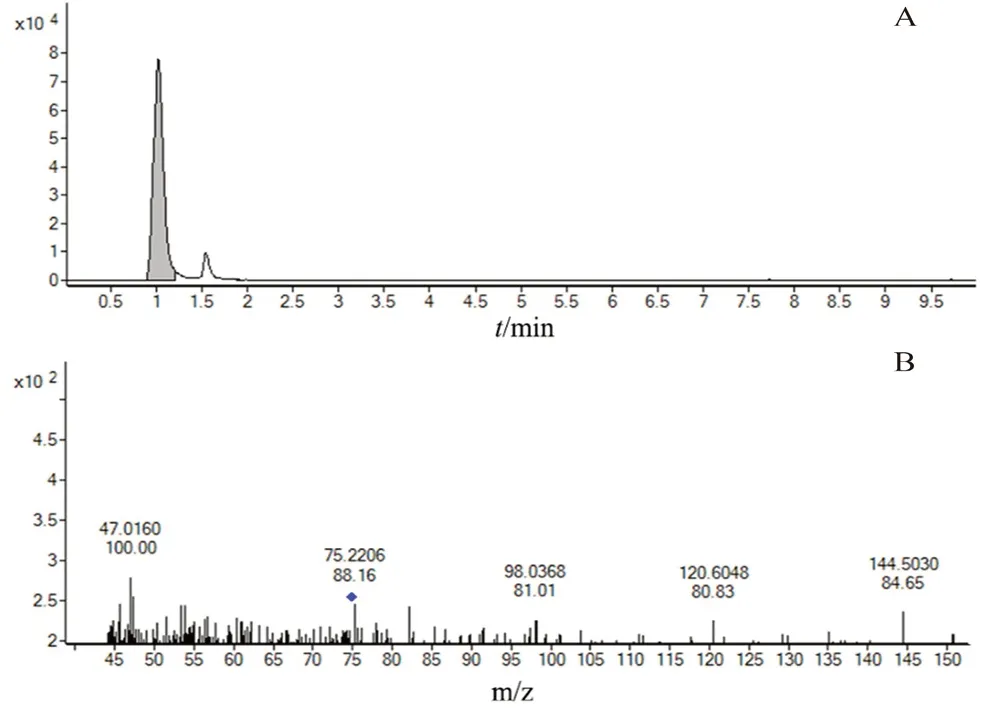
图3 阳性样品中羟基乙酸的提取离子流图(A)和二级质谱图(B)Fig 3 Extracted ion chromatogram(A)and MS2 spectrum(B)of glycolic acid in the positive samples
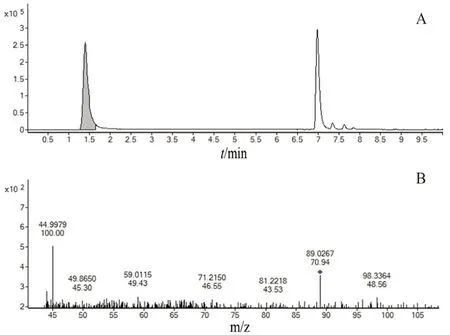
图4 阳性样品中乳酸的提取离子流图(A)和二级质谱图(B)Fig 4 Extracted ion chromatogram(A)and MS2 spectrum(B)of lactic acid in the positive samples
3 讨论
3.1 色谱柱的选择
本试验检测的10种化合物极性均较大,需要选择耐水相色谱柱。本研究考察了Agilent ZORBAX SB-AQ C18(4.6 mm×250 mm,5 μm)、Waters Atlantics T3(4.6 mm×250 mm,5 μm)、SHISEIDO CAPCELL PAK C18AQ(4.6 mm×250 mm,5 μm)三种品牌的色谱柱,以目标化合物分离度和峰形为选择依据,结果显示,当使用Agilent ZORBAX SB-AQ C18柱时,苹果酸、乳酸和柠檬酸稍有拖尾;当使用Waters Atlantics T3柱时,10种化合物的响应均偏低;而当使用SHISEIDO CAPCELL PAK C18AQ柱时,各化合物分离效果较好,峰形对称,出峰时间适中。SHISEIDO CAPCELL PAK C18AQ柱填料为新型聚合物包被的硅胶,在100%的水系流动相中具有良好稳定性,能有效分离高极性化合物,因此是最适用的色谱柱。
3.2 流动相pH的选择
参考文献[6,10],考察磷酸氢二铵溶液不同pH值(2.3、2.45、3.0)对目标化合物色谱行为的影响。结果显示,当pH值为3.0时,酒石酸与羟基乙酸不能完全分离,色谱峰有重叠现象;当pH值为2.3时,二苯乙醇酸和羟基辛酸色谱峰前延,峰形较差;而pH值为2.45时,各成分色谱峰的分离度良好,均能达到基线分离。
3.3 提取方法的选择
以10种α-羟基酸峰面积大小为考察依据,考察了不同提取时间(15、30、45 min)、超声温度(室温、40℃、60℃、80℃)、溶剂用量(10、20、25 mL)对提取效率的影响,结果表明不同溶剂用量对检测结果无明显影响,从操作简便性和成本考虑,最终选择10 mL为溶剂用量。当提取时间30 min、超声温度60℃时,10种α-羟基酸峰面积达到最大值,因此选择30 min为最佳提取时间、60℃为最佳超声温度。
3.4 小结
本研究建立了化妆品中10种α-羟基酸的高效液相色谱检测及液相色谱-串联质谱确证方法,该方法快速、简便、准确度高、专属性强,可为化妆品中α-羟基酸类化合物的测定提供参考,对严格规范我国化妆品市场具有重要意义。

