Nb2O5催化剂的高温选择性催化还原氮氧化物性能
薛 薇,唐钰栋,王 飞,何 虎,郑 拓,薛友祥,杨杭生,王 勇
(1.浙江大学 材料科学与工程学院,浙江 杭州 310027; 2.山东工业陶瓷研究院,山东 淄博 255000)
1 前 言
NOx的过量排放带来了酸雨、光化学烟雾、温室效应等一系列环境问题,同时NOx还具有一定的生物毒性,不利于人类的健康。目前,以NH3为还原剂的选择性催化还NOx是最有效的NOx排放控制技术,简称为NH3-SCR[1]。该技术的核心是SCR催化剂,已实现商业化应用的V2O5-WO3/TiO2催化剂[2],其工作温度范围为300~400 ℃,但该催化剂在高温度下会导致NH3的深度氧化,产生大量的副产物N2O,使脱硝性能下降并降低N2选择性,而且V2O5具有生物毒性,回收处理困难,所以开发环境友好的非钒基催化剂具有实际应用价值和意义。
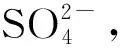
基于此,本研究分别以TiO2、经硫酸处理的TiO2、TiOSO4为载体,以Nb2O5为活性组分,采用机械球磨法制备出三种不同载体的铌钛催化剂,分析比较了在相同Nb2O5含量下、不同载体对300~500 ℃范围内催化剂的脱硝性能,成功优化出高温活性优异的脱硝催化剂,并结合一系列表征手段合理解释了不同载体上催化剂的脱硝活性存在差异的原因,提出了可能的反应路径。
2 实 验
2.1 催化剂的制备

2.2 SCR脱硝活性测试
催化剂的SCR脱硝活性测试在SCR微型反应器中进行,将催化剂粉末过筛,选取40目筛下、60目筛上的催化剂装入石英管中,石英管内径为8 mm;通过质量流量计控制反应气体的含量,各反应气体在混气罐中混合后进入石英反应管,在催化剂表面发生反应;使用testo 340烟气分析仪分别检测石英管出、入口处NO、NO2、O2的浓度,使用Medi-Gas G200 N2O分析仪检测出口处N2O的浓度。实验中各反应气体的设置方式如下:N2为载气,NO和NH3的浓度分别为612和347 mg/m3,氧气体积分数为5%,气体总流量为600 sccm。将催化剂放置在该气流中、500 ℃下保温1 h后,以2 ℃/min的速率降温,从500 ℃开始,每隔25 ℃记录出口处NO、NO2和N2O的含量,记录至300 ℃。实验中催化剂用量为0.5 mL,空速为72 000 h-1。
氮氧化物转化率的计算公式为:
(1)
式中:NOx(入口)表示石英管入口处的NOx浓度,NOx(出口)表示石英管出口处的NOx浓度,NOx浓度为NO、NO2浓度的总和。
氮气选择性的计算公式为:
(2)
式中:N2O表示出口处N2O的浓度。
2.4 催化剂的表征
采用X射线衍射仪Philips XD-98测量催化剂的XRD图谱,其辐射源为Cu Kα,波长为0.15406 nm。采用场发射扫描电子显微镜Hitachi SU70观察催化剂的微观形貌,同时采用配套的能量色散光谱仪对样品进行选区元素分析。采用物理吸附仪TriStar 3020进行比表面积、平均孔径、孔容测试分析。采用X射线光电子能谱仪ESCALAB 250Xi分析催化剂的XPS图谱,光源为Cu Kα,能量为1486.6 eV,C峰校正标准为284.8 eV。采用全自动多用吸附仪tp-5080-D测试催化剂吸附NH3的能力,具体条件为:取100 mg催化剂装样,在450 ℃下、30 sccm的高纯氦气流中预处理1 h后降至50 ℃;随后在流量为15 sccm、NH3浓度为10%的NH3/Ar混合气中吸附0.5 h;吸附结束后气路切换为高纯氦气流,以30 sccm的流量吹扫至基线稳定,以10 ℃/min的升温速率将样品从50 ℃升温至500 ℃,其过程中脱附的NH3信号由热导池(TCD)记录。
采用微型反应器测试NOx的脱附情况。取0.5 mL催化剂装样,在500 ℃下、600 sccm的高纯氮气流中预处理1 h后降至80 ℃;此温度下,催化剂在612 mg/m3的NO、5 vol% O2、N2作为载气的气流中吸附至饱和;吸附结束后以600 sccm的高纯氮气流吹扫,以5 ℃/min的升温速率将样品从80 ℃升温至500 ℃,从100 ℃开始,每隔20 ℃记录出口处NO、NO2、O2的含量,记录至500 ℃。整个测试过程中气体的总流量保持为600 sccm。
采用微型反应器测试NH3的氧化过程,具体测试条件为:取0.5 mL催化剂装样,在500 ℃下、含347 mg/m3的NH3和5 vol% O2的氮气气流中保温1 h;然后以2 ℃/min的速率降温,从500 ℃开始,每隔25 ℃保温20 min并记录出口处NO、NO2、N2O、O2、NH3的含量,记录至300 ℃;实验结束后测量入口处NH3的含量。整个测试过程中气体的总流量保持为600 sccm。NH3氧化率的计算公式为:
(3)
3 结果与讨论
3.1 催化剂的SCR脱硝活性
Nb-Ti体系催化剂上的NO转化率和N2选择性如图1(a)所示。从图可见,在300~500 ℃的温度范围内,三种催化剂的脱硝活性都随温度的升高而升高。Nb1Ti催化剂的脱硝效率较差,在300 ℃时的NO转化率仅有15%,随着温度的升高,NO转化率逐渐提高,在500 ℃时达到了57%。Nb1Ti-S在整个温度区间内催化活性得到了显著提高,300 ℃时达33%,500 ℃时达到了94%,T80(转化率大于80%)的温度窗口为450~500 ℃。而Nb1TiS的催化活性最佳,T80的温度窗口拓宽为375~500 ℃,在425~500 ℃范围内,NO的转化率接近100%。此外,在Nb1Ti-S和Nb1TiS催化剂上整个测试过程中没有检测到N2O的生成,即在300~500 ℃范围内N2选择性达100%,如图1(b)所示。而Nb1Ti在450 ℃以后开始产生N2O,其浓度随温度升高而升高,500 ℃下的N2选择性降至84%。简言之,Nb1TiS显示了优异的高温脱硝性能,可见对于Nb2O5催化剂,TiOSO4是比TiO2更好的催化剂载体。

图1 Nb-Ti体系催化剂上(a) NO转化率和(b) N2选择性,612 mg/m3的 NO, 347 mg/m3的NH3,5 vol%O2,空速为72 000 h-1Fig. 1 (a) NO conversion and (b) N2 selectivity over Nb-Ti catalysts, 612 mg/m3 NO, 347 mg/m3 NH3, 5 vol%O2,GHSV=72 000 h-1
3.2 催化剂的结构与形貌分析
利用XRD对样品进行物相分析,如图2所示。与锐钛矿相TiO2(JCPDS#99-0008)的标准卡片相对比,Nb1Ti和Nb1Ti-S催化剂的衍射峰均与其对应较好,衍射峰的半高宽均相近,通过谢乐公式计算出两种催化剂的晶粒尺寸,分别为42.7和49.6 nm,说明TiO2载体经过硫酸处理后并没有改变其晶体结构和晶粒尺寸。Nb1TiS催化剂同TiOSO4(JCPDS#49-0467)的标准卡相对比,衍射峰也对应较好,并未观察到TiO2相关的衍射峰,说明煅烧过程中没有发生TiOSO4热分解成TiO2的反应,而仅仅能使TiOSO4·2H2O脱除其结晶水,这与文献[16]报道结果相一致。此外,在三个催化剂的XRD谱图中都没有观察到铌氧化物的衍射峰,说明铌氧化物在载体上的分散性良好。

图2 Nb-Ti体系催化剂的XRD图谱Fig. 2 XRD patterns of Nb-Ti catalysts
催化剂的BET比表面积、平均孔径和平均孔容如表1所示。相较于Nb1Ti催化剂,载体经过硫酸处理后的Nb1Ti-S催化剂的比表面积、平均孔径和平均孔容都没有明显变化,说明硫酸化处理并没有显著改变TiO2的晶粒大小,也没有发生明显的化学反应,这与XRD结果一致。当载体为TiOSO4时,催化剂的比表面积达到47 m2/g,远大于另外两种载体,平均孔容也从0.036 cm3/g增加到0.264 cm3/g,结合SCR脱硝活性测试结果,比表面积与SCR脱硝活性呈正相关,大的比表面积为气体在催化剂表面发生反应提供了更多的活性位点,有利于脱硝活性的提高。
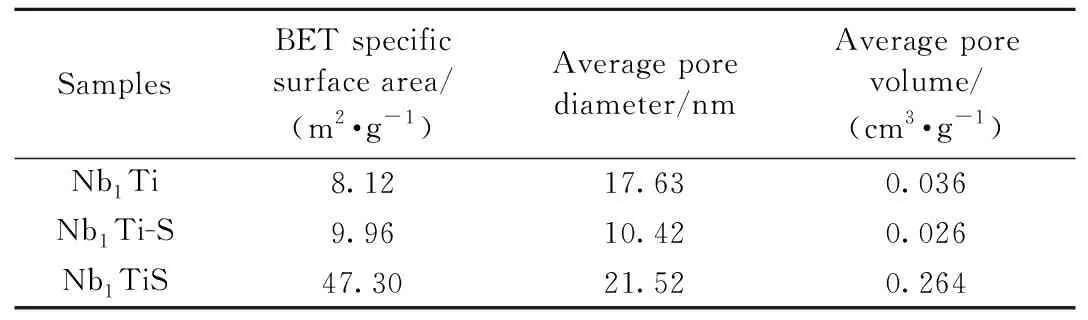
表1 Nb-Ti体系催化剂的BET比表面积、平均孔径和平均孔容Table 1 BET specific surface area, average pore diameter and average pore volume of Nb-Ti catalysts
因为Nb1TiS的脱硝活性优异,采用SEM及EDS元素分析系统研究了Nb1TiS的微结构,如图3所示。从SEM图像可知TiOSO4载体的粒径在微米量级。从EDS能谱图中可以看出,O、S、Ti、Nb元素均匀分布,说明机械球磨法成功实现了活性组分铌氧化物在TiOSO4载体上的高度分散,使催化剂具有优异的脱硝活性和稳定性。

图3 Nb1TiS催化剂的SEM图像以及EDS元素分布图Fig. 3 SEM image and EDS mappings of the Nb1TiS catalyst
3.2 XPS分析
SCR脱硝催化剂的性能取决于反应气体在其表面的吸附和活化,而催化剂表面的元素组成和价态对其有着重要影响。为此,利用XPS研究了催化剂的表面元素组成和价态。S 2p的XPS图谱如图4(a)所示,Nb1Ti-S和Nb1TiS上均只观察到一个峰,峰位分别为168.48和168.58 eV,归属于S6+[17]。Nb1TiS上的S6+的峰相较于Nb1Ti-S向高结合能方向移动了0.1 eV,证明了Nb1TiS的S中心吸引电子的能力很强,增加了中心周围的负电荷密度,产生了以S为中心的电荷富集位点和以Ti为中心的电荷贫乏位点,这个效应是金属氧化物经过硫化后表面能产生丰富的酸性位点的原因[18-19]。O 1s的XPS图谱如图4(b)所示,利用 peak 41软件对该图谱进行分峰拟合,结合能位于527~531.5 eV的峰归属于晶格氧,记为Ob,结合能位于529~533 eV的峰归属于化学吸附氧,记为Oa[20],取这两个峰面积计算化学吸附氧占比Oa/(Oa+Ob)。在Nb1Ti、Nb1Ti-S、Nb1TiS催化剂表面上,化学吸附氧的占比分别为29%、53%、44%,结合SCR活性测试结果,可以确定化学吸附氧含量的增大有利于提高脱硝活性,但不是决定因素。Nb 3d的XPS图谱如图4(c)所示,在207.1和210 eV处的两个峰分别代表Nb 3d5/2和Nb 3d3/2,两个峰均归属于Nb5+物种[21],说明铌元素以+5价的状态存在,即铌氧化物以Nb2O5的形式存在。

图4 Nb-Ti体系催化剂的(a) S 2p (b) O 1s和 (c)Nb 3d的XPS图谱Fig. 4 XPS spectra of (a) S 2p (b) O 1s and (c) Nb 3d for Nb-Ti catalysts
3.3 NH3-TPD分析
高温SCR脱硝催化剂的表面酸性对脱硝活性有关键性影响,中强酸性位吸附NH3的能力强于弱酸位,因此在升温脱附过程中,弱酸位上的NH3首先脱附,接着才是中强酸位上NH3的脱附。催化剂在100~500 ℃的NH3-TPD如图5(a)所示。从图可见,Nb1Ti在整个温度范围内仅有低温区的少量NH3脱附,说明其吸附NH3能力较弱。当TiO2经硫酸处理后,NH3脱附量增加,尤其是在450~500 ℃的区间还存在少量的NH3脱附,说明其氨吸附能力有了显著的提升。Nb1TiS的NH3脱附量明显优于另外两种催化剂,特别是在温度高于300 ℃后,Nb1TiS仍显示出优异的氨吸附能力,说明具有充足的强酸性位,有利于高温SCR反应的进行。
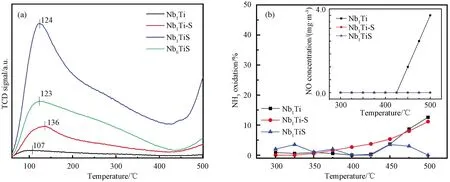
图5 铌钛体系催化剂的 (a)NH3-TPD图谱; (b)NH3氧化和氧化产物NO的浓度Fig. 5 (a)NH3-TPD result and (b)NH3 oxidation and NO concentration of the Nb-Ti catalysts
3.4 NH3的氧化分析
NH3的氧化活化对提高低温脱硝性能至关重要,但高温会导致NH3的深度氧化,不但消耗还原剂NH3,还会额外生成NO和N2O,从而不利于NH3-SCR反应,降低NOx转化率。用NH3的转化率表示其氧化率,铌钛体系催化剂的NH3氧化结果如图5(b)所示。从图可见,当温度达到475 ℃时,Nb1Ti和Nb1Ti-S催化剂上开始出现微弱的NH3的氧化,氧化率分别为8.7%和8.0%,且随温度升高而升高,当温度达到500 ℃时,二者的氧化率分别为12.6%和11.1%。而Nb1TiS氧化NH3的能力更是弱于Nb1Ti-S,在整个测试温度范围内,Nb1TiS催化剂上NH3的氧化率随温度改变,但始终低于4%,几乎可以忽略,这都说明在铌钛体系的催化剂上脱硝时NH3的活化主要不是因为Nb2O5的强氧化能力,而是其弱的氧化性能和强酸性保证在高温下NH3仍被吸附。此外,在Nb1Ti的NH3的氧化产物中检测到了NO,500 ℃时NO浓度为3.7 mg/m3,而在其他两种催化剂上并未检测到NO和N2O,说明Nb2O5确实是一种很弱的氧化剂。这进一步证实通过降低催化剂的氧化性有助于抑制NH3的深度氧化,从而有利于其高温脱硝并提高N2的选择性。
3.5 NOx-TPD分析
利用NOx-TPD研究了NOx在表面的吸附状态。在有氧气参与反应的SCR体系中,NO吸附在催化剂表面可形成亚硝酸盐、硝酸盐类物质,这些吸附物质在较高温度下分解成NO和NO2[22]。在铌钛体系催化剂的NOx-TPD图谱如图6所示,在整个测试过程中没有检测到NO的脱附,所以NOx-TPD图谱的纵坐标为NO2的浓度。在三个催化剂上,只检测到极少量的NO2的脱附,尤其在300 ℃以上的高温区,这说明在脱硝反应过程中,NO没有被吸附和活化,与传统的V2O5基中温催化剂上的SCR反应一致。

图6 铌钛体系催化剂上NOx-TPDFig. 6 NOx-TPD of the Nb-Ti catalysts
3.6 催化剂上SCR的反应路径分析
反应气体在催化剂表面发生的反应属于气固两相反应,涉及扩散、吸附、活化、反应、脱附等过程,当存在多种反应气体时,至少有一种反应气体会在催化剂表面吸附活化,所以SCR反应中存在两种可能的反应路径:L-H路径和E-R路径。L-H路径中反应气体均为吸附态,吸附态物质之间发生反应;E-R路径中反应气体为不同状态,吸附态物质与气体之间发生反应。在传统的V2O5基中温SCR催化剂上,脱硝过程存在两个循环:酸碱循环和氧化还原循环[23],在酸碱循环中,NH3分子被表面酸性位吸附,然后进入氧化还原循环被活化,同时V5+被还原成V4+。活化后的NHX(X<3)与气相中的NO发生脱硝反应。NH3被消耗后,进入下一个酸碱循环,继续吸附NH3。而V4+在氧化还原循环中被空气中的O2氧化后重新生成V5+,实现完整的脱硝过程。在这两个循环中,酸碱循环负责吸附NH3,氧化还原循环负责氧化活化NH3。
对于中温SCR脱硝,反应一般在300~400 ℃进行,需要催化剂在这个温度段仍能够吸附NH3,同时催化剂的氧化能力不能太强,以避免NH3的深度氧化,而V2O5是少数的几个可以满足这两个条件的催化剂。但是,当反应温度继续升高时,就会面临NH3的吸附性能变差,更为严峻的是NH3被深度氧化,直接导致脱硝性能的劣化,并伴随副产物N2O和NO的大量生成[24]。为了拓展SCR的工作温度范围,一个可行的方案是降低反应温度,这就必须提高催化剂的氧化能力。目前针对低温SCR脱硝催化剂的研究就是要寻找具有较强氧化能力的活性组分,以及尽力避免因氧化性偏高而导致SO2氧化后致使的催化剂中毒的问题[25]。而在高温SCR研发过程中,需克服两个难题,一是提高催化剂的酸性强度,保证其在500 ℃的高温下仍能被催化剂吸附。二是降低催化剂的氧化能力,抑制高温下NH3深度氧化的副反应。
目前已有的研究显示Nb2O5是具有合适氧化能力的高温SCR催化剂,但还需优化催化剂或载体以提高其酸强度[26]。文献报导和本研究都显示对TiO2载体进行硫酸化处理有一定的提高催化剂酸强度的效果(图1(a)),从而显著提高其高温SCR脱硝效率。基于该研究思路,本研究发现直接使用硫酸氧钛做载体制备的Nb1TiS,可以兼具高浓度表面强的酸性位(图5(a))和弱氧化性能(图5(b))两大优点,显示出优异的高温SCR脱硝性能。
3.7 催化剂的稳定性分析
在实际使用中,催化剂的稳定性是重要的评价标准之一,而Nb1TiS催化剂在500 ℃下具有优异的脱硝活性和N2选择性,为此对该催化剂进行了500 ℃下长达50 h的稳定性测试,结果如图7所示。Nb1TiS催化剂在50 h内的NOx转化率保持100%,且无下降趋势,证明该催化剂在500 ℃下具有良好的稳定性;另外,整个测试过程中都无副产物N2O生成。将经过稳定性测试后的催化剂过筛,发现催化剂颗粒仍处于40目筛下、60目筛上,证明催化剂在长期高温环境中不发生板结。

图7 Nb1TiS催化剂在500 ℃下的稳定性测试Fig. 7 Stability test of the Nb1TiS catalyst at 500 ℃
4 结 论
本研究采用机械球磨法制备了利用TiOSO4直接负载活性组分Nb2O5的高温SCR脱硝催化剂,T80的温度窗口为375~500 ℃,425~500 ℃范围内的NOx转化率接近100%,且N2选择性为100%。脱硝反应遵循传统的E-R机理,即吸附的NH3和气相的NO之间的反应是脱硝的主要途径。Nb1TiS催化剂具有较大的比表面积,高浓度的表面强酸性位和较弱Nb2O5的氧化能力是其高温条件保持高效率脱硝性能和优异的N2选择性的关键。该催化剂及体系在高温下具有良好的稳定性,可望应用于陶瓷基除尘脱硝一体化技术。

