柱后衍生-液相色谱法测定蔬菜中克百威残留量的不确定度评定
黄小清,王宇,刘佳,谭锦萍,林泽珊,王成龙,黄松,赵金利
(广州市食品检验所,广州 511400)
克百威,又名呋喃丹,属于氨基甲酸酯类杀虫剂,具有良好杀虫、杀螨效果,在农作物种植中被广泛使用。按照中国农药毒性分级标准,克百威属于高毒农药,人体摄入后会改变膜的渗透性与流动性来破坏人体神经环境平衡,进而威胁生命安全[1]。农业部禁止克百威在蔬菜中使用,但是偷用、滥用现象时有发生[2]。GB 2763—2021 《食品安全国家标准 食品中农药最大残留限量》[3]规定,克百威残留为克百威及3-羟基克百威之和,以克百威表示,残留限量值为0.020 mg/kg,因此准确测定蔬菜中的克百威残留量尤为重要。
目前,克百威的检测方法主要有气相色谱-质谱法[4-5]、荧光检测器高效液相色谱法[6-7]、紫外检测器高效液相色谱法[8-9]、液相色谱法-质谱法[10-11]等。其中较常见的是荧光检测器高效液相色谱法,该方法灵敏度高,仪器配备要求不高,但样品处理过程较繁琐,实验周期较长,不利于大批量检测[12]。
测量不确定度是对测量结果准确度的定量表征[13-14],当测量结果处于限量值范围时,方法的不确定度对于测量结果准确性和可靠性评估具有重要指导作用。
笔者基于QuEChERS 原则进行样品处理,采用柱后衍生-液相色谱法测定蔬菜中克百威残留量,该方法快速、简便,适用于大批量检测,能够满足蔬菜中克百威残留的检测要求。同时,为确保检测结果和判定的准确性、可靠性,根据测量不确定度的程序和方法[15-18],对蔬菜中克百威及其残留物3-羟基克百威含量的不确定度进行评估。通过分析和评估不确定度来源,确定影响测定结果的主要因素,为检验结果的准确性及可靠性提供了技术依据。
1 实验部分
1.1 主要仪器与试剂
液相色谱仪:SHIMADZU UFLC-CRB-6A 型,配备柱后衍生系统,日本岛津公司。
电子分析天平:SECURA3102-1CN 型,感量为0.1 mg,德国赛多利斯公司。
高速离心机:2-16KL 型,德国Sigma 公司。
涡旋振荡器:Multi Reax P/N545-10000 型,德国海道夫仪器设备有限公司。
克百威标准溶液:100 μg/mL,农业部环境保护科研监测所。
3-羟基克百威标准溶液:100 μg/mL,美国Accustandard 公司。
氯化钠、氢氧化钠、硼酸:分析纯,广州化学试剂厂。
乙腈、甲醇:色谱纯,美国赛默飞世尔科技公司。
邻苯二甲醛:分析纯,上海安谱实验科技股份有限公司。
3-巯基丙酸:分析纯,阿法埃莎中国化学有限公司。
蔬菜样品:番茄,市售。
0.05 mol/L 氢氧化钠溶液:称取2 g 氢氧化钠,用水定容至1 000 mL。
柱后衍生试剂:称取硼酸3.34 g 和氢氧化钠0.18 g,用400 mL 水溶解,为溶液A;称取0.015 g邻苯二甲醛,用50 mL 甲醇溶解,为溶液B;将溶液A 和溶液B 混合均匀得到溶液C;吸取3-巯基丙酸11 μL 加入溶液C 中,混合均匀。
1.2 样品处理
1.2.1 提取
称量20 g(精确至0.01 g)蔬菜样品于50 mL离心管中,加入20 mL 乙腈,振荡提取20 min,放入冰箱冷冻10 min,加入陶瓷均质子,再加入5~7 g氯化钠,振荡10 min 后,以6 000 r/min 的转速离心3 min,得上清液。
1.2.2 净化
移取6 mL 上清液于15 mL 离心管中,加入N-丙基乙二胺涡旋混合,振荡5 min,以8 000 r/min的转速离心3 min 后,再准确移取4 mL 上清液,于40℃下氮吹至近干,然后准确加入1 mL 甲醇复溶,过0.22 μm 有机相滤膜后,待测。
1.3 仪器工作条件
色谱柱:XSelect HSS T3 型柱(250 mm×4.6 mm,5 μm,美国沃特世科技有限公司);柱温:42℃;检测器:荧光检测器;激发波长:330 nm;发射波长:465 nm;流动相:A 为一级水,B 为甲醇;洗脱方式:梯度洗脱;梯度洗脱程序:0.01~2 min,15%~25%B ;2~8 min,25%~25%B ;8~9 min,25%~40%B;9~10 min,40%~45%B;10~24 min,45%~80%B;24~29 min,80%~80%B;29~30 min,80%~15%B;流动相流量:0.5 mL/min;柱后衍生程序:0.05 mol/L氢氧化钠溶液流量为0.3 mL/min,柱后衍生试剂流量为0.3 mL/min;反应器水解温度为100 ℃,衍生温度为40 ℃。
2 数学模型
采用色谱峰面积外标法定量,建立蔬菜中克百威、3-羟基克百威残留量测定的计算公式(1):

式中:X——样品中被测组分的残留量,mg/kg;
ρ——从标准曲线得到的样品中被测物的质量浓度,μg/mL;
V1——提取溶液体积,mL;
V2——用于检测的提取溶液体积,mL;
V3——样品溶液定容体积,mL;
m——称取的样品质量,g。
3 测量不确定度来源
分析检测过程和数学模型可知,样品测量的不确定度主要来源于样品的称量、标准工作液的配制、样品处理、仪器测量等。每个过程又分别受多种因素影响,整个测定过程中不同阶段的不确定度来源分类如表1 所示。

表1 蔬菜中克百威残留量的不确定度来源分类
4 不确定度分量的评定
4.1 标准溶液稀释过程引入的相对标准不确定度
4.1.1 标准物质纯度引入的相对标准不确定度
克百威标准溶液的标准值ρ1=100 μg/mL,扩展不确定度α=0.09 μg/mL。假设呈均匀分布,包含因子k=,根据文献[15-16]计算公式可得标准品定值引入的相对标准不确定度:
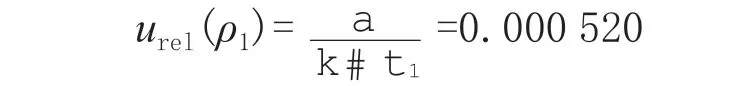
3-羟基克百威标准溶液标准值ρ2=100 μg/mL,扩展不确定度α2为2.0 μg/mL。假设呈均匀分布,k=,根据文献[15-16]计算公式可得标准品定值引入的相对标准不确定度:
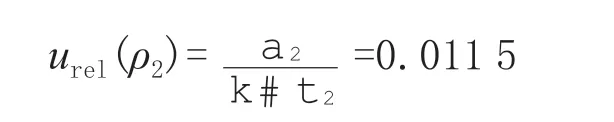
4.1.2 标准溶液稀释过程引入的不确定度
稀释过程中不确定度来源主要是容量瓶、移液器的体积和溶剂由于环境温度波动等因素引起的不确定度。按照JJG 196—2006 《常用玻璃量器检定规程》[19]和JJG 646—2006《移液器》[20]检定规程,玻璃器和移液器均有相应的允许误差。
10 mL 容量瓶(A 级)最大允差α为±0.02 mL,假定为三角形分布,k=,根据文献[15-16]计算公式可得10 mL 容量瓶容量引入的相对标准不确定度:
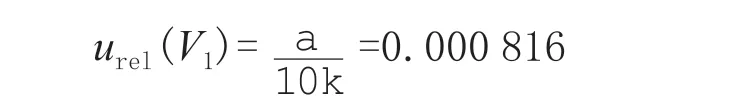
甲醇的膨胀系数为0.001 10/℃,实验室温度为(20±5)℃,假设呈均匀分布,k=,则由温度波动引入的相对标准不确定度:

吸取1 mL(量程为100~1 000 μL 的移液器)质量浓度为100 μg/mL 的标准溶液于10 mL 容量瓶中,配制成标准中间溶液。根据校准证书,1 mL 移液器最大允差α为±1.0%;按照均匀分布,k=,根据文献[15-16]计算公式可得该过程引入的相对标准不确定度:
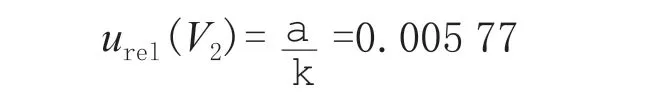
因此标准中间液定容至10 mL 引入的相对标准不确定度:
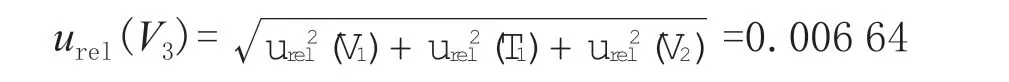
4.1.3 系列标准工作溶液配制过程引入的不确定度
分别用100 μL、1 mL 移液器吸取0.05、0.10、0.20、0.50 mL 和1.00 mL 标准溶液(10 μg/mL)于一系列10 mL 容量瓶中,用甲醇定容至标线,得到质量浓度分别为0.05、0.10、0.20、0.50、1.00 μg/mL的标准工作溶液,移液器和容量瓶引入的相对标准不确定度如表2 所示。

表2 移液器和容量瓶引入的相对标准不确定度
由表2 数据合成得配制系列标准工作溶液引入的相对标准不确定度:

由以上分析可知克百威配制过程引入的相对标准不确定度:

3-羟基克百威配制过程引入的相对标准不确定度:
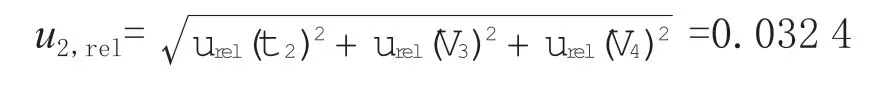
4.2 样品称量引入的标准不确定度
样品称样量m为20 g(精确至0.01 g),天平最大允许误差α为±0.01 g,采用B 类方法评定,假设呈均匀分布,k=,根据文献[15-16]计算公式可得称量引入的相对标准不确定度:

4.3 样品稀释过程引入的标准不确定度
(1)提取溶液体积引入的标准不确定度。样品加入20 mL 乙腈去稀释,使用10 mL 吸管2 次,引入的不确定度主要来源于10 mL 吸管(A 级)。10 mL 吸管允许误差α为±0.05 mL,采用B 类方法评定,假设呈均匀分布,k=,根据文献[15-16]计算公式可得吸管引入的相对标准不确定度:

乙腈的膨胀系数为0.001 37/℃,实验室控制温度为(20±5)℃,假设呈均匀分布,k=,则由温度波动引入的相对标准不确定度:

因此该过程中引入的相对标准不确定度为:
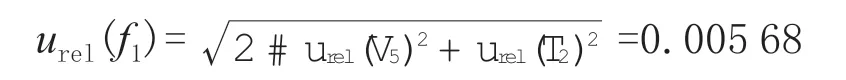
(2)吸取提取溶液体积引入的标准不确定度。准确吸取4.00 mL 液体,在浓缩过程中产生的不确定度主要来源于5 mL 吸管(A 级)。5 mL 吸管允许误差α为±0.025 mL,假设呈均匀分布,k=,根据文献[15-16]计算公式得吸管引入的相对标准不确定度:
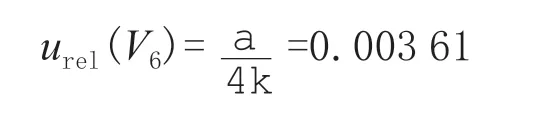
乙腈由温度波动引入的不确定度为0.003 95,因此该过程中引入的相对标准不确定度:
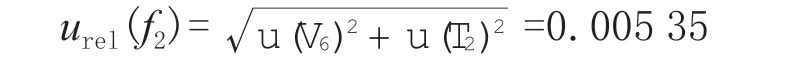
(3)样品溶液定容体积引入的标准不确定度。加入1.00 mL 甲醇复溶的过程所产生的不确定度主要来源于1 mL 移液枪。已知1 mL 移液枪移取1 mL 溶液时允许误差α为±1.0%,假设呈均匀分布,k=,根据文献[15-16]计算公式可得引入的相对标准不确定度:

已知甲醇由温度波动引入的不确定度为0.003 18,因此该过程中引入的相对标准不确定度:

合成得样品稀释过程引起的相对不确定度:

4.4 重复性测量引入的相对标准不确定度
选取番茄为实验样品,克百威和3-羟基克百威在0.020 mg/kg浓度下进行加标,平行进行6组试验,其测定结果见表3。
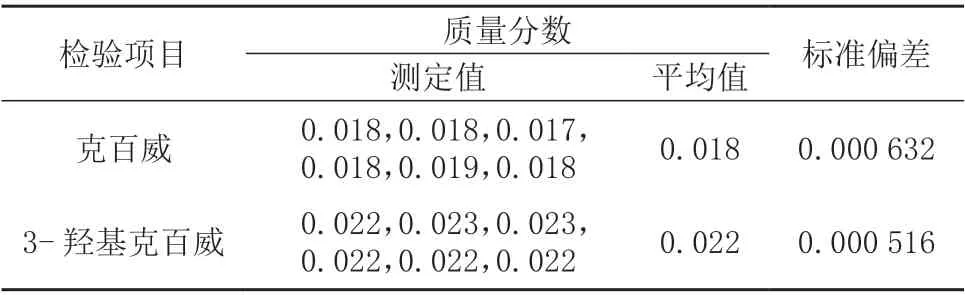
表3 克百威和3-羟基克百威加标回收试验结果 mg/kg
由表3 数据计算可得,克百威重复性测量引入的相对标准不确定度:
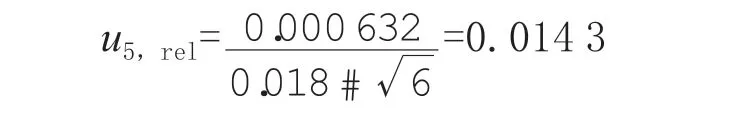
3-羟基克百威重复性测量引入的相对标准不确定度为:
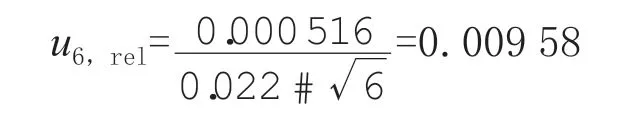
4.5 合成标准不确定度
以上不确定度分量相互独立,没有相关性,因此该方法克百威的合成相对标准不确定度:
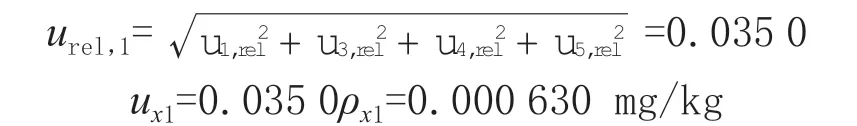
3-羟基克百威的合成标准不确定度:
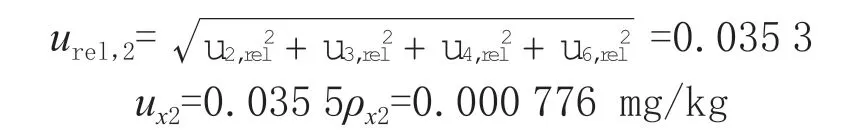
4.6 扩展不确定度
在置信水平为95%下,取k=2,则克百威的扩展不确定度:
Ux1=kux1=0.001 3 mg/kg
3-羟基克百威的扩展不确定度:
Ux2=kux2=0.001 6 mg/kg
最终测量克百威的不确定度报告:
(0.020±0.001 3)mg/kg,k=2
测量3-羟基克百威的不确定度报告:
(0.020±0.001 6)mg/kg,k=2
4.7 数据分析
通过对克百威和3-羟基克百威的测定过程中各个不确定度来源进行分析评定,各不确定度分量的贡献见表4。
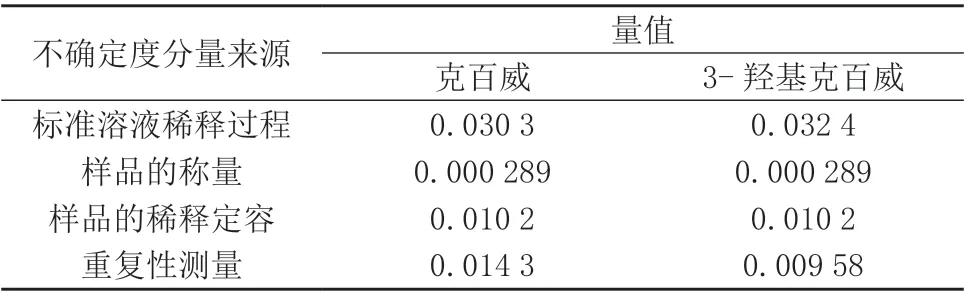
表4 相对标准不确定度分量
由表4 可知,样品的稀释定容过程引入的不确定度分量和重复性测量引入的不确定度分量大于不确定度最大贡献分量的1/3,而样品的称量过程引入的不确定度分量小于不确定度最大贡献分量的1/3,该分量可以忽略[21]。不确定度分量最大贡献来源于标准溶液的稀释过程引入的不确定度分量,因此在实际样品分析测定中,应配制适宜浓度的标准溶液,尽量减少稀释的次数,以保证结果的准确性、可靠性。
5 结语
通过对克百威测定过程中各个不确定度分量进行分析评定,发现液相色谱柱后衍生法测定蔬菜中的克百威的不确定度主要来源于标准溶液的稀释过程。因此在实际样品分析测定中,应配制适宜浓度的标准溶液,尽量减少稀释的次数,以保证结果的准确性、可靠性。

