新型冠状病毒肺炎患者肝功能异常的影响因素及其在不同药物治疗中的动态变化
刘 遥 冯 颖 任 婕 王宪波
(首都医科大学附属北京地坛医院中西医结合中心,北京 100015)
新型冠状病毒肺炎(以下简称新冠肺炎,COVID-19)可引起严重呼吸道疾病。新冠肺炎患者的主要死因是急性肺损伤,其特征是严重的内皮损伤、炎症和肺泡周围毛细血管的大量血栓形成[1-4]。此外,肺外表现如心肌功能障碍和心律失常[5-7]、卒中[8]、肝细胞损伤[9]、急性肾损伤[10-12]、深静脉血栓[13-15]和胃肠道症状[16]等也可见于新冠肺炎患者。
新冠肺炎相关肝损伤是指在病程和治疗过程中发生的肝损伤。其病理机制包括肝中新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)的直接细胞毒性[17],严重炎症反应/全身炎症反应综合征引起的免疫介导的肝损伤[18],呼吸衰竭引起的低氧变化,凝血障碍引起的血管改变,右心衰竭引起的内皮炎或心脏充血,药物引起的肝损伤和既往肝病的恶化[19]。最近的研究[20-23]表明,新冠肺炎患者肝损伤发生率为14.8%~53%,主要表现为丙氨酸氨基转移酶(alanine aminotransferase, ALT)/门冬氨酸氨基转移酶(aspartate aminotransferase, AST)浓度异常,总胆红素(total bilirubin, TBIL)浓度轻度升高[20],血清白蛋白(serum albumin, ALB)浓度在重症患者中下降[21]。重症新冠肺炎患者肝损伤的比例明显高于非重症患者[22],肝功能异常的患者更容易进展为重症肺炎[23]。
现有文献不足以充分阐明影响新冠肺炎患者肝功能异常的因素和肝功能指标的变化。因此,本研究分析了首都医科大学附属北京地坛医院收治的新冠肺炎患者肝功能异常的影响因素及其在不同药物治疗中的动态变化。
1 对象与方法
1.1 研究对象
以2020年1月29日-2020年7月5日收治的615例新冠肺炎患者为研究对象。本研究组在之前发表的一篇论文[20]中阐明了诊断标准、临床分型、纳入和排除标准。轻型和普通型患者被归类为非重症,而重型和危重型被归类为重症。银丹解毒颗粒组是指服用院内制剂“银丹解毒颗粒”的患者。
根据病情应用了以下治疗药物:洛匹那韦400 mg + 利托那韦100 mg/次,2次/d,直到病毒被清除或最长10 d;磷酸氯喹500 mg/次,第1天2次/d,随后2~10 d每天1次;法维拉韦第1天1 600 mg/次,2次/d,次日600 mg/次,2次/d,直到病毒被清除或最多14 d;抗生素7~10 d。患者住院期间应用银丹解毒颗粒治疗,疗程为14 d。
1.2 数据收集
收集患者的人口学特征(年龄和性别),体质量指数(body mass index, BMI),流行病学史(武汉相关或北京新发地相关),合并症(基础肝病、糖尿病、高血压、心血管疾病、慢性阻塞性肺病),从发病到入院的天数,实验室检验(CD4+T细胞计数、C反应蛋白、血清淀粉样A、红细胞沉降率、乳酸、白细胞计数、嗜中性粒细胞计数、淋巴细胞计数、单核细胞计数、血小板计数、中性粒细胞计数与淋巴细胞计数的比率(ratio of neutrophil count to lymphocyte count, NLR)、血小板平均体积、血小板压积、大血小板比率、血小板平均分布宽度、肾小球滤过率、凝血酶原时间、活化部分凝血活酶时间、纤维蛋白原定量和D-二聚体),在住院的第3、7、10、14天检测肝功能指标(ALT、AST、TBIL和ALB)。肝功能异常或肝损伤定义为:ALT>40 U/L,AST>35 U/L,ALB<40 g/L,TBIL>18.8 μmol/L。根据入院时患者肝功能指标情况,分为肝功能异常组(225例,36.6%)和肝功能正常组(390例,63.4%)。本研究方案经由首都医科大学附属北京地坛医院伦理委员会审批,批号:京地伦科字(2020)第(020)-01号。所有患者均签署知情同意书。
1.3 统计学方法

2 结果
2.1 新冠肺炎患者的临床特征
在615例新冠肺炎患者中,88.6%(545/615)患者表现为非重症,22.4%(70/615)患者出现重症表现。非重症患者中有61.7%(336/545)的患者观察到肝功能异常,而重症患者中97.1% (68/70)的患者出现肝功能异常。在615例新冠肺炎患者中,入院时肝功能正常的390例患者中,211例住院期间肝功能持续正常,179例住院期间出现了肝损伤。共有404例患者出现肝功能异常(包括入院时存在肝损伤的225例和住院期间出现肝损伤的179例),其中68例(16.8%)进展为重症。然而,在211例肝功能始终正常的患者中,只有2例(0.9%)进展为重症。
2.2 新冠肺炎患者肝损伤的单因素分析
肝功能异常的患者年龄偏大,BMI偏高,有基础肝病、糖尿病或高血压史,从发病到入院的天数更长,CD4+T细胞水平、淋巴细胞计数、血小板计数、血小板压积和肾小球滤过率较低,并具有较高的NLR、C反应蛋白、血清淀粉样A、红细胞沉降率、血小板平均分布宽度,纤维蛋白原和D-二聚体水平,两组间比较差异有统计学意义(P<0.05),详见表1。
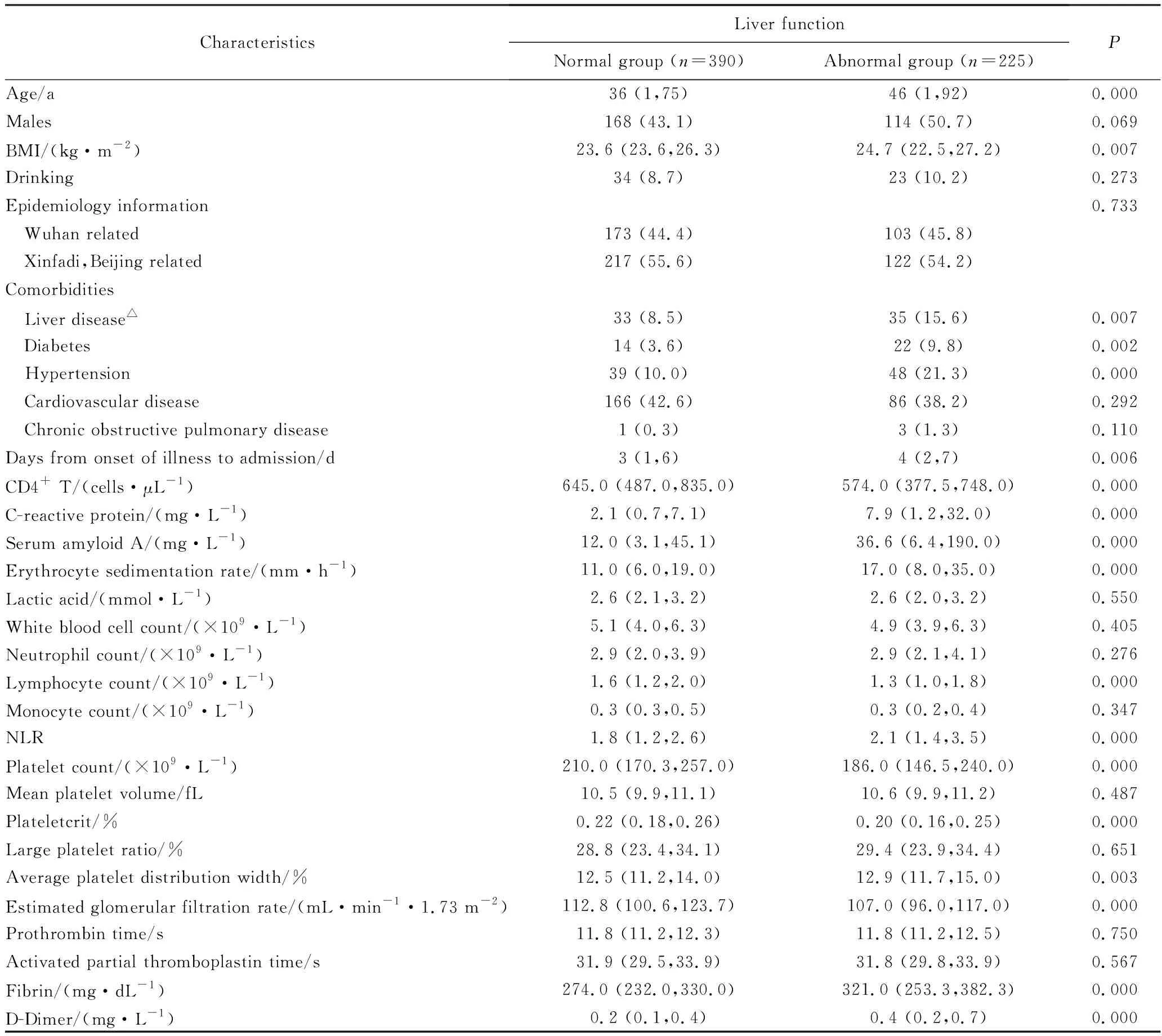
表1 新冠肺炎患者的基线临床特征Tab.1 Clinical characteristic of the patients with COVID-19 at admission according to liver function tests [M(P25,P75),n(%)]
2.3 新冠肺炎患者肝损伤的多因素分析
将基线数据中肝功能正常组与异常组间比较差异有统计学意义的指标纳入多因素Logistic回归分析,包括年龄、BMI、基础肝病、糖尿病或高血压史,从发病到入院的天数、CD4+T细胞水平、淋巴细胞计数、血小板计数、血小板压积、肾小球滤过率、NLR、C反应蛋白、血清淀粉样A、红细胞沉降率、血小板平均分布宽度、纤维蛋白原和D-二聚体浓度。结果表明,年龄、从发病到入院的天数、C反应蛋白浓度和D-二聚体浓度是新冠肺炎患者肝损伤的危险因素(P<0.05),详见表2。

表2 基线时多因素Logistic回归分析筛选肝损伤的影响因素Tab.2 Predictive factors of liver injury by multivariate Logistic regression analysis at admission
2.4 新冠肺炎非重症和重症患者的肝功能指标情况
新冠肺炎重症患者在入院时ALT 和 AST浓度高于轻型及普通型患者,ALB 浓度低于轻型及普通型患者,组间差异有统计学意义(P<0.05);TBIL组间差异无统计学意义(P>0.05)。重型及危重型新冠肺炎患者AST和ALB浓度正常的比例明显低于轻型及普通型患者,差异有统计学意义(P<0.05);ALT和TBIL组间比较差异无统计学意义(P>0.05),详见表3。
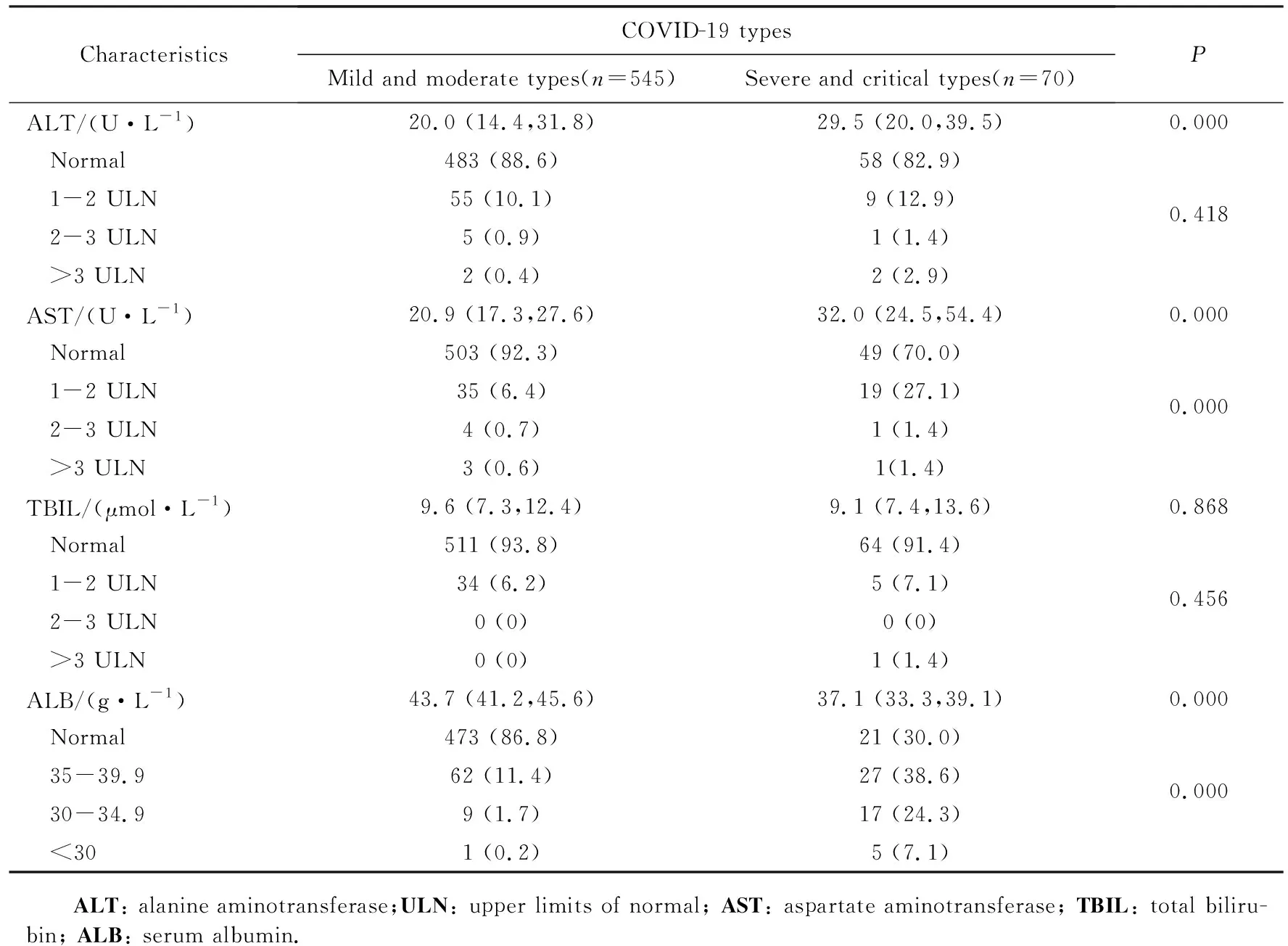
表3 新冠肺炎患者的临床分型与入院时肝功能指标的关系Tab.3 Clinical classification of patients with COVID-19 in relation to liver function test results at admission [M(P25,P75),n(%)]
2.5 应用不同药物时肝功能的动态变化
共有179例患者在住院期间出现肝功能异常。住院第10天,应用洛匹那韦/利托那韦组的ALT浓度明显低于未用洛匹那韦/利托那韦组(P=0.043);法维拉韦组和未用法维拉韦组之间的ALT浓度差异无统计学意义;在第7天(P=0.004)和第10天(P=0.020),磷酸氯喹组的ALT浓度明显低于未用磷酸氯喹组患者。第7天,抗病毒组中的ALT明显低于未抗病毒组(抗病毒组包括应用洛匹那韦/利托那韦、法维拉韦或磷酸氯喹的患者)(P=0.020)。抗生素和银丹解毒颗粒的应用对ALT浓度没有显著影响(P>0.05),详见表4。
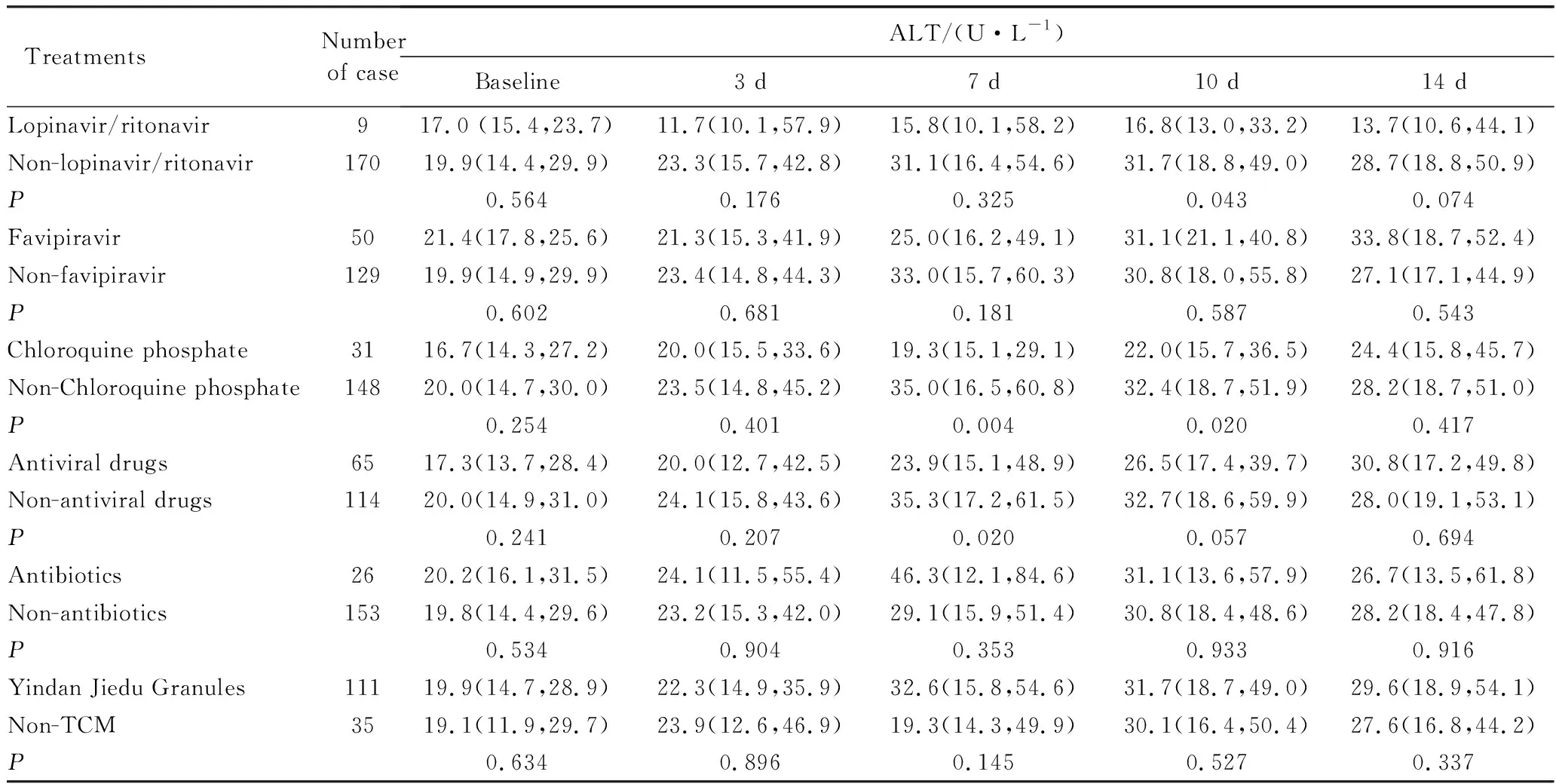
表4 新冠肺炎患者血清丙氨酸氨基转移酶在不同药物治疗中的动态变化Tab.4 Changes of serum ALT in COVID-19 patients treated with different drug M(P25,P75)
ALT: alanine aminotransferase;TCM: traditional Chinese medicine.
洛匹那韦/利托那韦和法维拉韦对AST浓度的影响并不明显(P>0.05);第7天,磷酸氯喹组的AST浓度明显低于未用磷酸氯喹组的患者(P=0.003);第7天,抗病毒组的AST浓度明显低于未抗病毒组(P=0.033);抗生素和银丹解毒颗粒的应用对AST浓度没有显著影响。详见表5。洛匹那韦/利托那韦、法维拉韦、磷酸氯喹、抗生素或银丹解毒颗粒的应用并没有显著升高TBIL的浓度。详见表6。
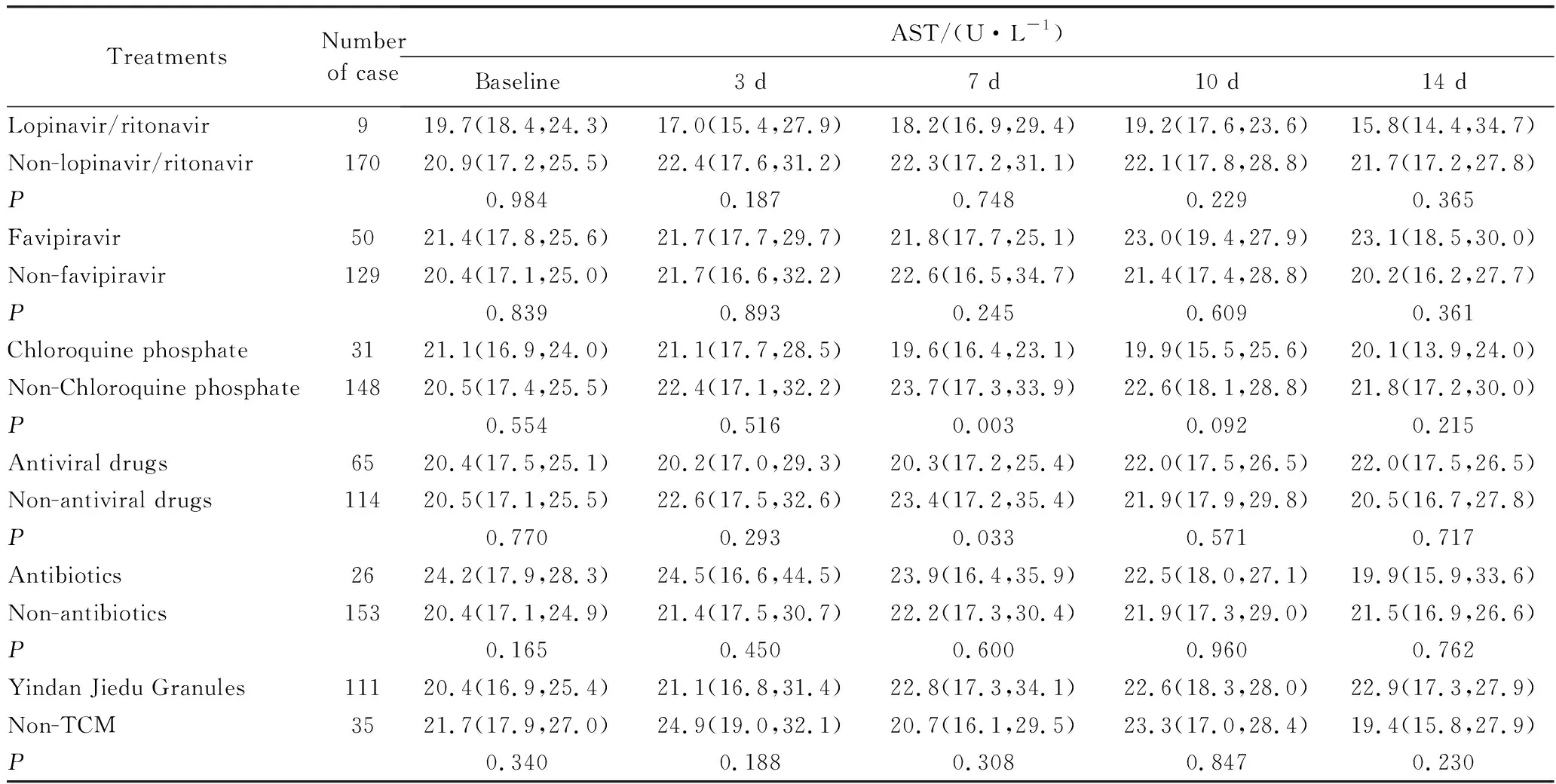
表5 新冠肺炎患者血清门冬氨酸氨基转移酶在不同药物治疗中的动态变化Tab.5 Changes of serum AST in COVID-19 patients treated with different drug M(P25,P75)
表6 新冠肺炎患者血清总胆红素在不同药物治疗中的动态变化Tab.6 Changes of serum TBIL in COVID-19 patients treated with different drug

表6 新冠肺炎患者血清总胆红素在不同药物治疗中的动态变化Tab.6 Changes of serum TBIL in COVID-19 patients treated with different drug
TreatmentsNumber of caseTBIL/(μmol·L-1)Baseline3 d7 d10 d14 dLopinavir/ritonavir97.7(6.2,11.4)11.2(8.5,13.3)6.7(5.8,11.5)7.0(6.2,11.8)6.9(4.6,10.6)Non-lopinavir/ritonavir1708.6(7.0,10.9)8.9(7.0,12.1)8.8(7.0,10.8)8.8(6.9,10.9)9.6(7.7,11.8)P0.4340.1980.2890.4850.071Favipiravir509.0±3.28.9(6.7,11.8)8.6(6.7,9.9)8.8(7.0,12.0)10.6±3.9Non-favipiravir 1299.3±3.19.1(7.1,12.4)9.0(7.0,11.1)8.7(6.8,10.7)9.6±3.5P0.5770.3690.2500.7020.212Chloroquine phosphate318.8±3.29.2(6.7,11.7)8.7(6.7,9.9)9.2(6.4,12.1)8.7(7.2,12.3)Non-Chloroquine phosphate1489.3±3.18.9(7.0,12.2)8.8(7.0,11.0)8.7(6.8,10.6)9.6(7.4,11.6)P0.4240.9530.3860.5880.946Antiviral drugs659.0±3.28.9(6.9,11.9)8.5(6.6,9.9)8.8(6.7,12.0)9.6(7.8,11.8)Non-antiviral drugs1149.3±3.09.0(7.0,12.3)9.0(7.5,11.3)8.7(6.8,10.7)9.4(7.4,11.9)P0.5940.8340.0960.8710.836Antibiotics268.9(7.1,11.6)8.7(6.8,13.0)8.4(6.4,10.5)8.8(7.4,10.4)8.7(7.4,10.1)Non-antibiotics1538.6(6.9,10.9)9.0(7.1,11.9)8.8(7.0,10.8)8.8(6.8,11.0)9.7(7.4,12.0)P0.6280.5790.4850.7590.157Yindan Jiedu Granules1119.6(7.7,11.9)8.9(7.2,11.5)8.8(7.2,10.7)8.6(6.7,10.9)9.6(7.4,11.9)Non-TCM358.2(6.5,10.4)9.4(6.4,12.4)9.1(7.1,11.3)9.4(7.3,12.0)9.8(8.7,12.0)P0.0310.6820.4100.4280.660
TBIL: total bilirubin; TCM: traditional Chinese medicine.
3 讨论
在最近的一项回顾性队列研究[24]中,新冠肺炎的严重急性肝损伤与炎症指标升高显著相关,包括铁蛋白和IL-6。本研究结果表明,与入院时肝功能正常的患者相比,肝功能异常的患者年龄更大,BMI、发病到入院的时间、炎症指标、凝血指标更高,合并症更多,CD4+T细胞计数、淋巴细胞计数和血小板压积较低。本研究筛选了肝损伤的独立危险因素,包括年龄、发病到入院的天数、C反应蛋白和D-二聚体浓度。在615例新冠肺炎患者中,有404例出现肝功能异常,非重症患者中肝功能异常的有336例(61.7%),重症患者中肝功能异常的有68例(97.1%),这表明大多数重症患者都有肝损伤。与非重症患者相比,重症患者在入院时表现出显著升高的ALT和AST浓度,且显著降低的ALB浓度。
为了排除住院前用药的影响,本研究分析了入院时肝功能正常但住院期间发生肝损伤患者的用药情况。研究结果显示,入院后第10天,抗病毒药物洛匹那韦/利托那韦显著降低了ALT的浓度,磷酸氯喹显著降低了ALT和AST浓度。考虑到可能与抗病毒药物抑制病毒可以减少直接肝损伤、缺氧和炎症级联反应等可能会加重肝损伤的因素相关。此外,在这项研究中,没有发现抗生素对肝脏的损伤,亦没有发现银丹解毒颗粒加重肝损伤的不良反应。研究结果表明,新冠肺炎相关肝损伤可能是由直接肝损伤、缺氧和炎症级联反应引起的,与药物相关的肝损伤并不显著。
这项研究有一些局限性。首先,缺乏碱性磷酸酶和γ-谷氨酰转肽酶的数据,其特性无法评估。其次,为了排除住院前用药的影响,本研究分析了179例入院时肝功能正常但住院期间发生肝损伤患者的用药情况,并没有发现住院期间肝损伤是由药物引起的;相反,抗病毒组中的ALT和AST浓度明显低于未抗病毒组。样本量需要进一步增加,也需要外部队列数据进行验证。
结论: 与新冠肺炎患者肝损伤相关的独立危险因素包括年龄、发病到入院天数、C反应蛋白和 D-二聚体。肝功能异常的患者患重症新冠肺炎的风险要更高。入院后,使用洛匹那韦/利托那韦和磷酸氯喹可显著降低ALT和AST浓度。在这项研究中,没有发现抗病毒药物、抗生素或银丹解毒颗粒对肝脏的损害。

