无创心肌做功评估经皮冠状动脉介入治疗后急性ST段抬高型心肌梗死患者心肌节段微血管灌注
孙思瑶,陈旗旗,孙巧冰,魏 虹,陈 娜,付婷婷, 商志娟,孙颖慧,丛 涛
(大连医科大学附属第一医院心脏超声科,辽宁 大连 116021)
经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)后,部分急性ST段抬高型心肌梗死(ST-elevation myocardial infarction, STEMI)患者梗死部位仍存在心肌微血管异常。微血管情况可反映心肌存活状态,影响节段心肌功能及患者预后[1]。心肌超声造影(myocardial contrast echocardiography, MCE)可评价微血管、反映心肌存活状态,预测心肌局部和整体功能恢复情况[2],但需应用超声造影剂,存在致过敏反应风险,且较依赖操作者经验性。相比心肌形变指标,无创压力-应变环(pressure strain loop, PSL)参数心肌做功(myocardial work, MW)能更准确地反映心肌收缩功能[3],现已用于心肌病、心力衰竭等领域[4]。本研究观察无创MW评估PCI后急性STEMI患者心肌节段微血管灌注(microvascular perfusion, MVP)的效能。
1 资料与方法
1.1 一般资料 回顾性分析2017年9月—2019年9月大连医科大学附属第一医院收治的119例急性STEMI患者,男104例,女15例,年龄34~81岁,平均(57.2±11.6)岁;高血压62例、糖尿病26例、高脂血症90例,吸烟68例;心功能Killip分级Ⅰ级101例,Ⅱ级11例,Ⅲ级6例,Ⅳ级1例;62例犯罪血管为冠状动脉左前降支(left anterior descending artery, LAD),13例为左回旋支(left circumflex artery, LCX),44例为右冠状动脉(right coronary artery, RCA)。纳入标准:①STEMI诊断明确[5],经PCI及标准抗凝、抗血小板等治疗并植入药物洗脱支架后,犯罪血管心肌梗死溶栓治疗(thrombolysis in myocardial infarction, TIMI)血流3级;②于PCI后72 h内接受超声心动图及MCE,图像清晰完整。排除标准:①陈旧性心肌梗死;②合并致左心室心肌功能受损疾病;③严重并发症,如室间隔穿孔、乳头肌断裂等;④超声造影禁忌证。检查前患者均签署知情同意书。
1.2 仪器与方法 由2名具有5年以上工作经验的超声科主治医师采用配备频率1.5~4.3 MHz M5S 扇形探头的GE Vivid E9彩色多普勒超声诊断仪进行检查及测量。首先行灰阶超声心动图检查,嘱患者左侧卧,于短暂屏气和稳定心电图下获取胸骨旁和心尖标准切面;以双平面Simpson法测量左心房容积(left atrial volume, LAV)、左心室舒张末期容积(left ventricular end-diastolic volume, LVEDV)、左心室收缩末期容积(left ventricular end-systolic volume, LVESV)及左心室射血分数(left ventricular ejection fraction, LVEF);以频谱多普勒获得二尖瓣血流频谱,测量舒张早期二尖瓣峰值流速(E)、舒张晚期二尖瓣峰值流速(A),计算E/A;以组织多普勒获得舒张早期二尖瓣环侧壁运动速度(Lateral e')和室间隔运动速度(Septal e'),计算二者平均值(e')及E/e'。
连接心电导联,采集心尖左心室长轴切面、四腔心切面、二腔心切面连续3个心动周期图像,以袖带法测量肱动脉血压。于EchoPAC工作站采用Q-Analysis软件以2D-Strain手动描记左心室心内膜边界,测量左心室总体纵向应变(global longitudinal strain, GLS);选择显示牛眼图,输入所测血压值,系统自动根据血压和应变情况绘制左心室PSL曲线,获得整体MW指标,包括左心室整体做功指数(global work index, GWI)、整体做功率(global work efficiency, GWE)、整体有用功(global constructive work, GCW)和整体无用功(global wasted work, GWW);采用左心室18节段模型,得到心肌节段纵向应变(longitudinal strain, LS)及做功指标,包括LS及心肌有用功(constructive myocardial work, CMW)、无用功(wasted work, WW)、MW指数(MW index, MWI)及MW率(MW efficiency, MWE)。
启动机械指数(mechanical index, MI)<0.2的实时超声造影检查模式,将焦点置于二尖瓣环水平,调节增益直至图像出现轻微噪音背景;调节扇区大小和深度,保持图像帧频>25 Hz,尽可能将左心室心腔完整置于扇区中部。经静脉缓慢推注 SonoVue悬浮液0.5~1.0 ml,并以0.9%氯化钠溶液冲洗,发现造影剂完全填充左心室和心肌后,在持续推注的同时选择左心室收缩末期触发“Flash”(帧频为10帧/秒,MI为1.0),采集“Flash”前至少1个心动周期和“Flash”后连续15个心动周期的心尖四腔心切面、二腔心切面和三腔心切面再灌注图像。脱机观察心肌各节段MVP情况,分为MVP正常(造影剂恢复充盈时间≤4 s)组、MVP延迟(造影剂恢复充盈时间>4 s且<10 s)组及MVP减低(造影剂恢复充盈时间≥10 s)组[6];再将前2组归为MVP未减低组。
1.3 统计学分析 采用SPSS 23.0统计分析软件。以中位数(上下四分位数)表示计量资料,组间行Kruskal-WallisH检验。采用多因素logistic回归分析观察MVP减低的独立影响因素,以受试者工作特征(receiver operating characteristic, ROC)曲线评价其评估梗死部位心肌MVP的效能,以DeLong检验比较其曲线下面积(area under the curve, AUC)。随机选择90个心肌节段,由上述医师再次测量心肌节段LS及MW指标,以组内相关系数(intra-class correlation coefficient, ICC)检验观察者间和观察者内测量结果的可重复性,ICC0.8~1.0为可重复性较好。P<0.05为差异有统计学意义。
2 结果
2.1 超声心动图及左心室PSL指标 119例STEMI患者PCI后72 h内超声心动图所检LAV为45.00(37.00,58.00)ml,LVEDV为(119.15±28.33)ml,LVESV为58.00(47.00,70.00)ml,LVEF为(49.87±6.96)%,E/A为0.91(0.78,1.19),E/e'为9.00(6.70,12.70);GLS为-12.00(-15.00,-10.00)%,GWI为(1 133.99±402.63)mmHg%,GWE为90.00(83.00,94.00)%,GCW为1 212.50(908.50,1 587.25)mmHg%,GWW为96.00(61.75,151.00)mmHg%。
2.2 心肌节段LS和MW指标 3组间总体及组间两两比较,心肌节段LS、CMW、WW、MWI及MWE差异均有统计学意义(P均<0.001),见表1及图1。
MVP未减低组与减低组间心肌节段LS、CMW、WW、MWI、MWE差异均有统计学意义(P均<0.001),见表2。

表1 不同MVP水平PCI后STEMI患者心肌节段LS和MW指标比较
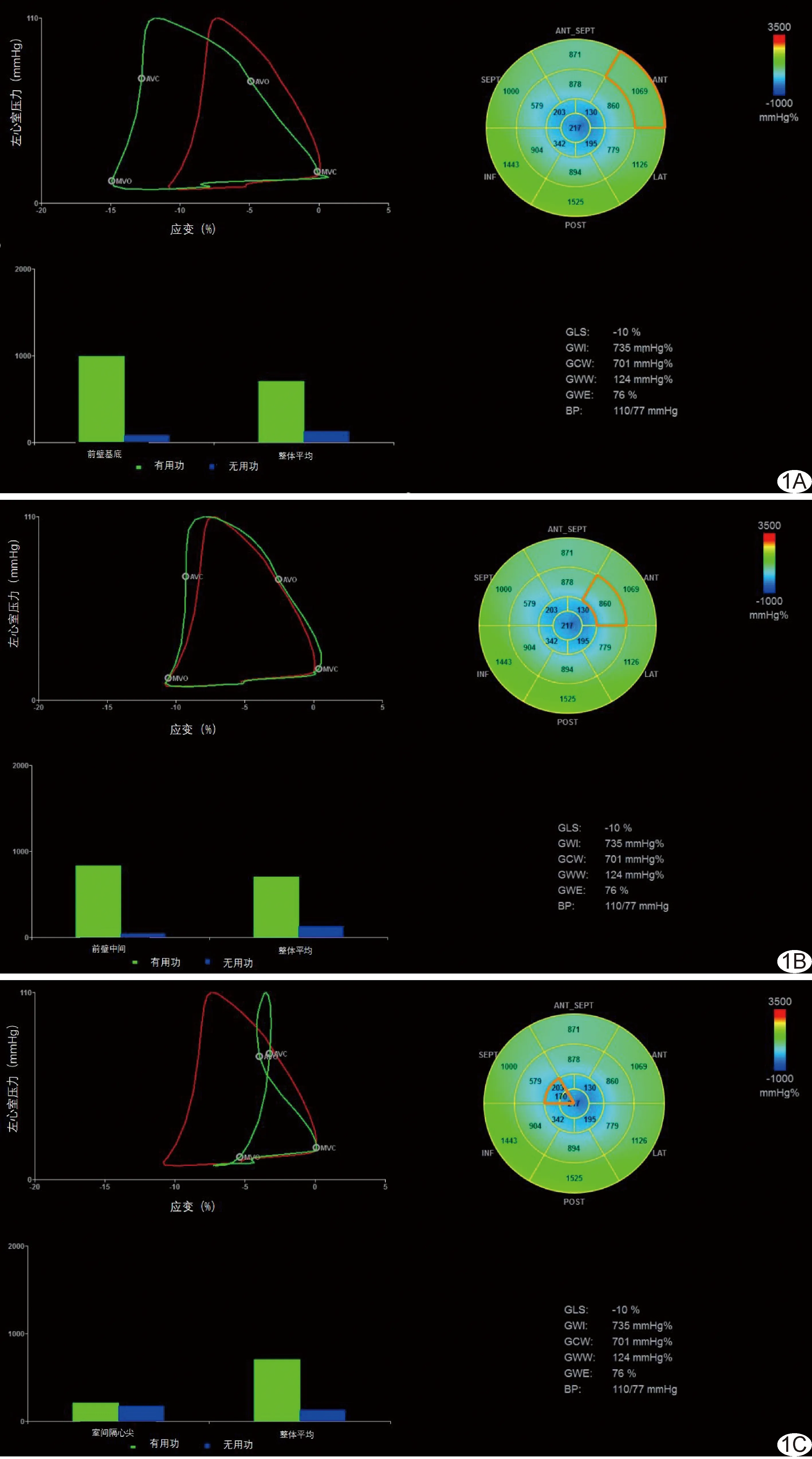
图1 患者男,59岁,急性STEMI,PCI后犯罪血管LAD无创MW图 A~C.分别显示MVP正常(A)、延迟(B)及减低(C)心肌节段(左上图示左心室PSL,红色示整体PSL,绿色示所选心肌节段PSL;右上图为MW牛眼图;左下图为所选心肌节段与心肌整体的CMW和WW柱状图;右下图示整体做功各指标数据)
2.3 心肌节段MVP减低的影响因素 以心肌MVP水平为因变量行多因素logistic回归分析,结果显示MWI[OR=1.00,95%CI(1.00,1.00),P=0.023]、MWE[OR=0.98,95%CI(0.97,1.00),P=0.010]、CMW[OR=1.00,95%CI(1.00,1.00),P<0.001]均为MVP减低的独立影响因素。
2.4 诊断效能 ROC曲线结果显示,MWI(截断值788 mmHg%)、MWE(截断值90%)及CMW(截断值815 mmHg%)评估MVP减低的AUC分别为0.856、0.853及0.877,CMW的AUC大于MWI、MWE(Z=5.246、2.307,P均<0.05),见图2。
2.5 可重复性 观察者间(ICC分别为0.947、0.921、0.957、0.984和0.940,P均<0.05)及观察者内(ICC分别为0.972、0.940、0.979、0.990和0.977,P均<0.05)测量LS、CMW、WW、MWI及MWE结果的可重复性均较好。
3 讨论
发生心肌梗死后,评价存活心肌具有重要临床价值。心肌梗死后存在心肌顿抑,顿抑的心肌虽MVP尚正常,但已存在功能异常,以室壁运动异常评估坏死心肌面积时,可将其误认为坏死心肌[7]而致高估。微血管完整是维持心肌存活的必要条件。MCE可评价微血管情况,有助于判断存活心肌:灌注正常或延迟提示心肌存活可能性大,心肌功能常可恢复,而灌注减低心肌功能常不能恢复[1]。本研究以MCE评估PCI后急性STEMI患者MVP,发现72 h内梗死相关心肌节段存在不同程度MVP异常,MVP异常节段CMW、MWI、MWE显著减低,WW则显著升高。
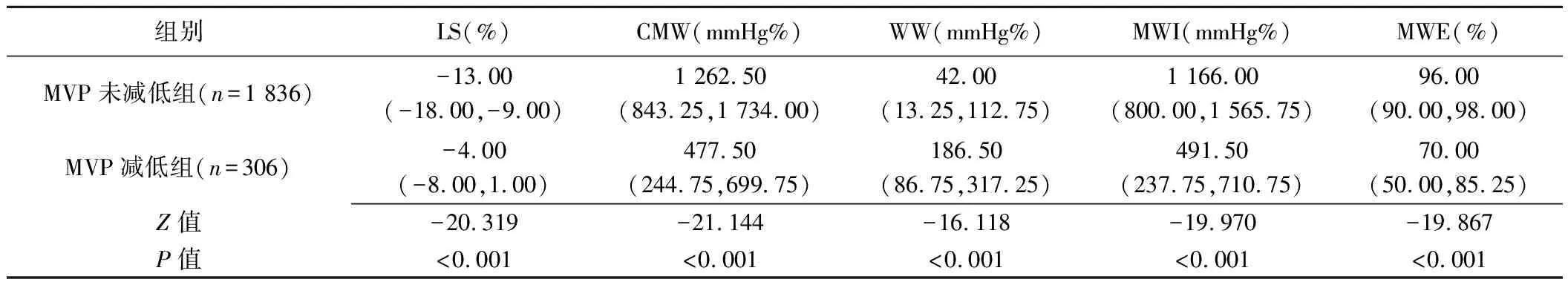
表2 MVP未减低与MVP减低PCI后STEMI患者心肌节段LS和MW指标比较
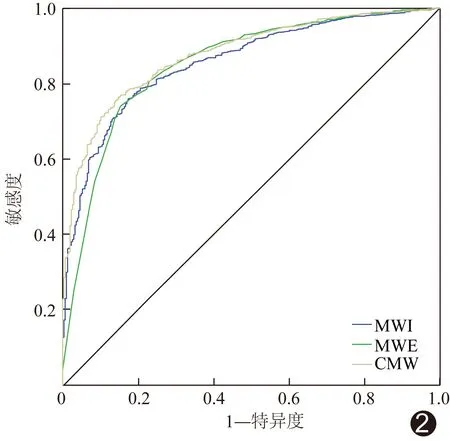
图2 PCI后STEMI患者心肌节段MWI、MWE及CMW评估MVP减低的ROC曲线
MW指标与心肌梗死后左心室重构、左心室功能恢复和临床预后有关[8-11]。MEIMOUN等[11]发现,对因前壁STEMI接受PCI治疗者,CMW是左心室功能恢复的独立预测因素。本研究发现MWI、MWE及CMW均为MVP减低的独立影响因素,且以CMW评价梗死相关心肌MVP的AUC大于MWI、MWE,提示心肌节段MW指标有助于识别存活心肌,尤以CMW效能最佳,而心肌WW并非MVP的影响因素。产生WW的主要原因在于左心室收缩期心肌伸长和/或收缩后心肌缩短。坏死心肌节段存在收缩期伸长和收缩后缩短;受累的存活心肌节段收缩期缩短缓慢、微小,亦存在收缩后缩短;二者均可产生WW,导致依据WW难以准确评价心肌节段存活情况。而CMW仅考虑正性功,反映左心室射血,故以之评价存活心肌的效能较高[12-13]。既往研究[14-15]显示,左心室LS可评价STEMI后心肌梗死范围并预测左心室功能恢复。本研究中LS并非MVP减低的独立影响因素,原因可能是梗死后心肌节段的收缩功能不仅依赖于存活心肌数量,同时受负荷状态影响,后负荷过高可使LS降低[3]。
综上,无创MW可有效评估PCI后STEMI患者心肌节段MVP,有望成为评估存活心肌的新指标。但本研究为单中心回顾性分析,样本量小,且未分析整体MW与MVP的相关性,未进行临床随访,有待进一步完善。

