Eclipse计划系统NTO优化对宫颈癌调强放疗计划的影响
刘可,吴哲,明智,王东
自贡市第一人民医院 肿瘤科,四川 自贡 643000
引言
宫颈癌是我国常见的恶性肿瘤之一[1],在女性恶性肿瘤的发病率中高居第2位。放射治疗技术作为宫颈癌的一种重要的治疗方式已广泛应用于临床[2]。小肠、直肠和膀胱等危及器官(Organ at Risk,OAR)的放疗并发症发生率与照射剂量显著相关,为了在靶区和OAR之间获得更好的剂量跌落,一些学者通过添加辅助限量环结构[3]或者设置等效均匀剂量(Equivalent Uniform Dose,EUD)生物优化函数[4]来保护OAR和保证靶区适形度和均匀性。Eclipse计划系统作为当前主流的计划系统之一,在优化调强放疗(Intensity Modulated Radiotherapy,IMRT)计划时,可以设置的参数很多,如靶区、OAR剂量目标值及优选度、非共面、射野角度、网格分辨率、通量平滑值等,参数的设置直接影响放疗计划的质量。Eclipse 10.0及以上版本内置了一种简单的优化工具正常组织目标(Normal TissueObjective,NTO),NTO是Eclipse中用来限制空间剂量变化,通过形成陡峭的剂量梯度来限制正常组织的剂量。目前少见关于NTO用于剂量优化的报道。基于此,本研究以宫颈癌固定野调强放疗为例,选取NTO函数中不同的剂量跌落值,与系统自带NTO对比,分析NTO跌落值对IMRT计划的剂量学参数影响,旨在为NTO的合理应用提供临床参考。
1 NTO介绍
在Eclipse调强优化系统中,NTO为优化界面内的工具,是优化界面重要的组成部分,它作用于靶区边缘开始至Body边缘,是从定义的靶区边缘距离开始至终端剂量。NTO用于限制正常组织剂量并避免生成高剂量点,同时可以在靶区周围生成较陡峭的剂量跌落区域。NTO为与距离有关的指数衰减函数,见式(1)~(2)[5]。NTO函数为优化罚分函数的一部分,在迭代优化过程中需要满足设立的NTO限定。
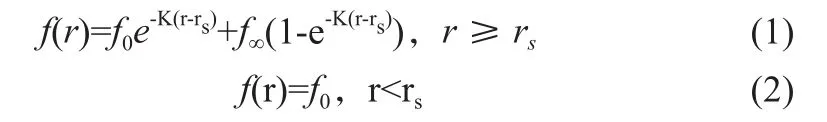
式(1)~(2)中,rs为距离靶区边缘初始距离,r为距离相对于rs边缘的距离,f0为开始剂量(%),f∞为结束剂量(%)。K为剂量衰减常数,即剂量跌落值,跌落速度决定了NTO曲线形状的陡度,修改此值本质上是改变终端剂量的位置接近或远离靶区。
2 材料和方法
2.1 临床资料
选取2020年1月至6月在我院肿瘤科治疗的20例宫颈癌术后患者,年龄41~78岁(中位年龄58岁)。纳入标准:① 有完整的临床病理资料;② 术前病理活检结果为宫颈癌;③ 未发现有远处转移。排除标准:有放射治疗禁忌证。
2.2 CT定位及靶区OAR勾画
使用热塑膜及专用碳纤维板和枕头固定患者,虽然有临床研究表明,采用俯卧位方式对正常组织保护优于仰卧位[6],但考虑IMRT照射时间较长,对摆位的重复性和精确度要求较高,一些患者术后伤口疼痛,仰卧的舒适性更好等因素,故本研究统一取仰卧位,患者定位前均清空直肠,定位前1 h排完小便,再喝适量水憋尿以便充盈膀胱,在Philips precedence 16排CT模拟定位机下增强扫描,CT扫描层厚5 mm,扫描范围为胸11椎体下缘到股骨中段。获得CT影像后,通过专用网络传输至Varian Eclipse 13.6放疗计划工作站,由高年资医生进行靶区和OAR的勾画,靶区包括临床靶区(Clinical Target Volume,CTV)和计划靶区(Planning Target Volume,PTV),其中CTV包括肿瘤原发灶、上段阴道、宫旁组织、髂总、髂内、髂外、骶前和闭孔淋巴引流区,PTV为CTV在三维方向上外放0.5 cm所得。OAR包括膀胱、直肠、左右股骨头、骨盆、小肠和正常组织(Body-PTV)。
2.3 计划设计
基于Eclipse v13.6计划系统和Varian Trilogy加速器,对每个患者制定七组固定野调强计划( fixed field IMRT,ff-IMRT)。第一组(对照组)计划设置为自动NTO;第二组计划跌落值K为0.01;第三组K值为0.1;第四组K值为0.3;第五组K值为0.5;第六组K值为1;第七组K值为5。所有计划Priority为80,后六组计划rs均为0.50 cm,f0均为105%,f∞均为60%,对照组自动NTO计划不需要设置NTO参数。射线质均为6 MV X射线,射野中心位置相同,剂量计算均选择AAA算法,网格大小2.5 mm,剂量率统一为500 MU/min,60对MLC。所有ff-IMRT计划的射野角度均为 27°、78°、129°、180°、233°、282°和 331°,准直器角度均为0°,基于剂量-体积物理优化函数的限制条件均相同。处方剂量均为4600 cGy/25 F。限制条件如下:95%靶区体积达到处方剂量,靶区剂量最大值高于110%的处方剂量体积不超过1%。表1为初始优化目标函数参数设定。
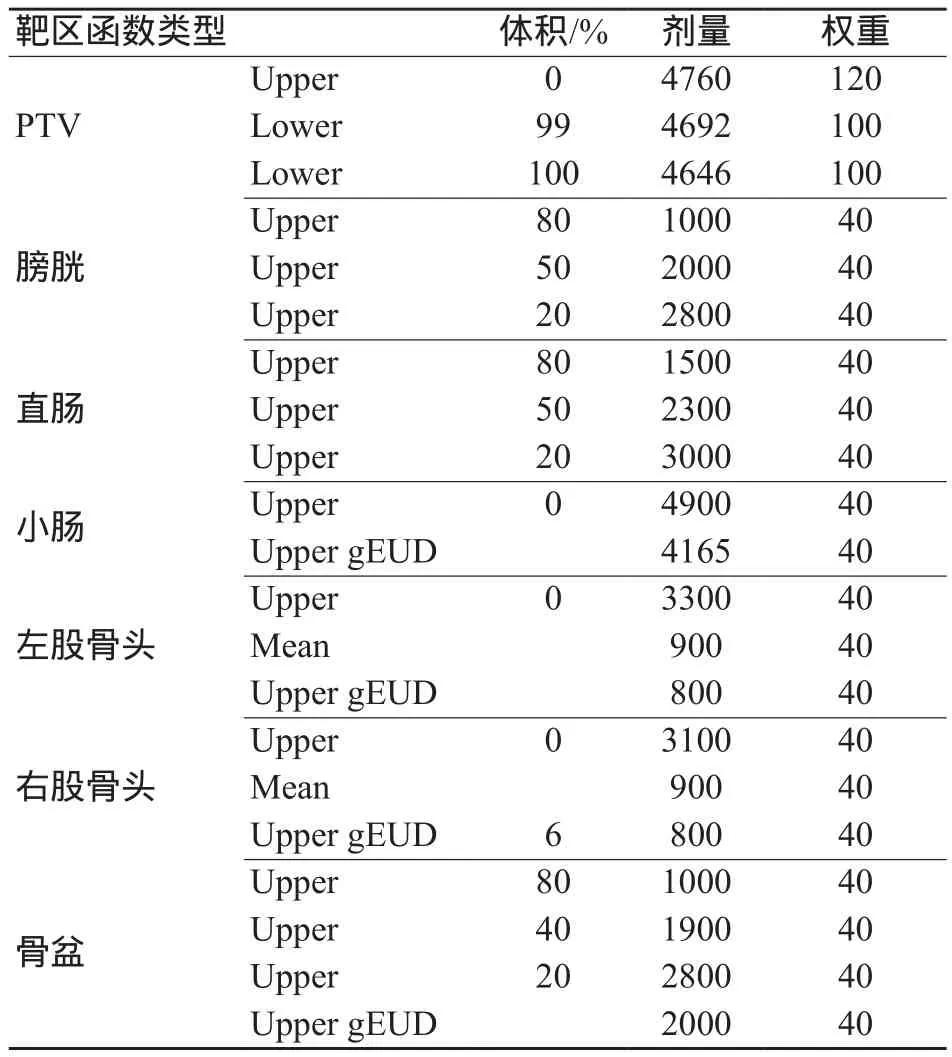
表1 20例宫颈癌术后患者初始优化部分目标函数设定
2.4 计划评估
根据剂量-体积直方图(Dose-Volume Histogram,DVH)来评价靶区和OAR的剂量学参数,参考ICRU83号报告[7]。靶区的剂量学参数:D2、D98、平均剂量Dmean,其中D2、D98分别为包围靶区体积2%、98%的最小剂量;均质性指数(Homogeneity Index,HI)定义如式(3)所示。
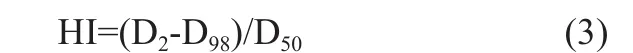
其中,D50为包围靶区体积50%的最小剂量,HI值越接近0,表明靶区的均匀性越好。另外,适形性指数(Conformity Index,CI)定义如式(4)所示。

其中,VT,ref为95%处方剂量所覆盖的靶区体积,VT为靶区体积,Vref为95%处方剂量所覆盖的总体积,CI值越接近于1,说明靶区的适形度越好。各OAR的剂量参数为膀胱D40,直肠D40,左右股骨头D25,骨盆Dmean,小肠Dmax,正常组织 V5、V10、V15、V20、V25、V30、V35和 V40。此外,评估各计划的机器跳数。
2.5 统计学分析
3 结果
3.1 靶区剂量学参数结果
图1所示是某个病例七组计划不同K值(膀胱、直肠、骨盆、正常组织)的DVH,从图中看出,不同K值计划组与对照组基本重合,骨盆差距较大。表2所示是七组PTV的剂量学参数。与对照组相比,K=0.5、1、5计划组D2、Dmean大于对照组,差异均有统计学差异(P<0.05),其他三组计划 D2、Dmean无显著差异(P>0.05);K=0.01、0.1计划组D98高于对照组,结果均有统计学差异(P<0.05),其他四组计划D98均无统计学差异(P>0.05);所有组CI均有统计学差异(P<0.05),其中K=0.01和0.1计划组HI比对照组差,K=0.3及以上时的CI优于对照组;除K=0.01和0.3计划组HI无显著差异,其他组均有统计学差异(P<0.05),K=0.1计划组HI优于对照组,K=0.5及以上计划组HI比对照组差。
表2 靶区剂量学参数比较(±s)

表2 靶区剂量学参数比较(±s)
组别 D2/cGy t值 P值 D98/cGy t值 P值 Dmean/cGy t值 P值自动NTO 4807.59±28.93 - - 4537.79±17.66 - - 4702.59±9.59 - -K=0.01 4807.58±33.04 -0.001 0.999 4546.26±15.38 4.06 0.001 4707.97±49.45 0.461 0.650 K=0.1 4797.75±25.63 -1.935 0.068 4543.29±11.99 2.812 0.011 4709.17±54.17 0.584 0.566 K=0.3 4809.63±27.04 0.389 0.701 4538.74±10.31 0.422 0.678 4707.22±12.40 1.855 0.079 K=0.5 4826.30±34.83 3.233 0.004 4537.55±9.21 -0.088 0.931 4713.66±14.08 3.872 0.001 K=1 4833.25±29.29 3.697 0.002 4534.83±10.10 -1.192 0.248 4719.34±13.79 5.647 <0.001 K=5 4841.08±37.04 4.348 <0.001 4535.22±7.84 -0.92 0.369 4722.14±14.39 5.616 <0.001组别 CI t值 P值 HI t值 P值自动NTO 0.867±0.019 - - 0.057±0.008 - -K=0.01 0.800±0.028 -16.649 <0.001 0.056±0.010 -1.325 0.201 K=0.1 0.851±0.020 -5.774 <0.001 0.054±0.007 -3.458 0.003 K=0.3 0.874±0.013 3.779 0.001 0.057±0.007 0.178 0.861 K=0.5 0.875±0.018 -2.885 0.009 0.061±0.009 3.591 0.002 K=1 0.879±0.014 6.002 <0.001 0.063±0.008 4.13 0.001 K=5 0.880±0.018 4.437 <0.001 0.065±0.009 4.794 <0.001
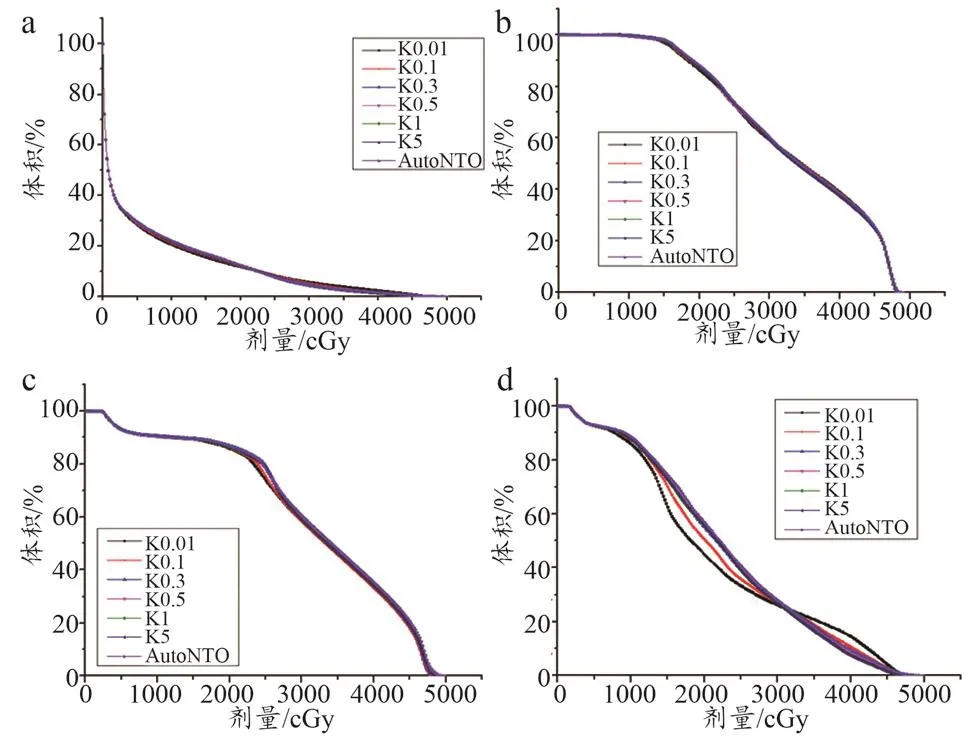
图1 不同K值的DVH
3.2 OAR剂量学参数结果
表3所示为七组计划的OAR剂量学参数。与对照组相比,K=0.01和0.1计划组膀胱D40更高,K=1和5计划组膀胱D40更低,差异均有统计学意义(P<0.05);所有计划组直肠D40均无统计学差异(P>0.05);K=0.1时左右侧股骨头D25较小(P<0.05),K=5时左右侧股骨头D25较大(P<0.05);K=1和5时小肠Dmax较大(P<0.05);K=0.01时骨盆Dmean较小(P<0.05)。
表3 OAR剂量学参数比较(±s)

表3 OAR剂量学参数比较(±s)
组别 膀胱D40/cGy t值 P值 直肠D40/cGy t值 P值 左股骨头D25/cGy t值 P值自动NTO 3809.46±587.06 - - 3889.69±451.02 - - 1798.41±338.76 --K=0.01 3830.48±581.70 3.126 0.006 3907.48±452.09 1.157 0.262 1784.21±378.77 -0.590 0.562 K=0.1 3824.75±584.11 3.140 0.005 3886.60±456.96 -0.321 0.752 1760.74±371.50 -2.350 0.030 K=0.3 3801.14±581.66 -1.232 0.233 3868.24±461.29 -2.041 0.550 1809.37±358.33 0.561 0.581 K=0.5 3796.15±577.44 -1.476 0.156 3875.94±464.05 -0.982 0.339 1834.87±366.88 1.800 0.088 K=1 3786.57±578.56 -2.276 0.035 3862.56±459.45 -2.001 0.060 1856.06±363.16 2.545 0.020 K=5 3784.99±585.31 -2.376 0.028 3861.84±478.68 -1.664 0.113 1868.49±376.71 2.779 0.012组别 右股骨头D25/cGy t值 P值 小肠Dmax/cGy t值 P值 骨盆Dmean/cGy t值 P值自动NTO 1596.99±292.29 - - 4856.64±41.84 - - 2587.16±256.88 - -K=0.01 1573.65±298.08 -0.888 0.386 4864.49±64.83 0.802 0.432 2531.37±313.12 -2.576 0.018 K=0.1 1549.03±302.53 -2.708 0.014 4846.81±48.69 -1.186 0.25 2685.28±601.14 0.726 0.476 K=0.3 1599.49±278.62 0.177 0.861 4851.21±42.63 -0.523 0.607 2577.25±259.44 -1.582 0.13 K=0.5 1625.00±284.86 1.373 0.186 4861.49±43.14 0.571 0.574 2585.30±257.35 -0.222 0.826 K=1 1634.86±255.95 1.668 0.112 4885.83±46.88 2.406 0.026 2581.59±253.78 -0.607 0.551 K=5 1664.31±274.69 2.750 0.013 4888.64±50.73 3.185 0.005 2606.05±267.56 1.420 0.172
3.3 正常组织剂量学参数结果
表4所示为七组计划的正常组织(Body-PTV)剂量学参数,从表中看出,K=0.01、0.1、0.3时,V5、V10、V15和V20与对照组相比更低(P<0.05);V25、V30、V35和 V40与对照组相比更高(P<0.05);K=1、5时V30、V35和V40与对照组相比更低(P<0.05)。因此,本研究认为K值较小时,低剂量体积较小,高剂量体积较大;K值较大时,低剂量体积较大,高剂量体积较小。
表4 正常组织剂量学参数比较[%,(±s)]

表4 正常组织剂量学参数比较[%,(±s)]
注:a表示P<0.05。
组别 V5 V10 V15 V20 V25 V30 V35 V40自动NTO 36.78±7.25 28.86±5.99 23.16±4.90 16.75±3.65 10.36±2.30 6.24±1.40 3.90±0.87 2.23±0.46 K=0.01 36.04±7.07a 27.87±5.84a 21.64±4.68a 16.05±3.74a 11.52±3.06a 8.03±2.17a 5.32±1.43a 3.27±0.88a K=0.1 36.40±7.12a 28.42±5.94a 22.30±4.66a 16.21±3.69a 11.18±2.71a 7.20±1.71a 4.41±1.02a 2.53±0.56a K=0.3 36.69±7.24a 28.65±5.95a 22.85±4.80a 16.56±3.58a 10.62±2.47a 6.34±1.42a 3.73±0.79a 2.08±0.41a K=0.5 36.80±7.27 28.71±5.93 22.97±4.89 16.63±3.68 10.49±2.42a 6.20±1.33 3.62±0.75a 2.01±0.40a K=1 36.85±7.27 28.71±5.89 22.98±4.86 16.64±3.62 10.36±2.37 6.04±1.31a 3.49±0.71a 1.91±0.37a K=5 36.86±7.33 28.71±5.93 22.98±4.90 16.60±3.63 10.35±2.36 6.01±1.28a 3.46±0.70a 1.89±0.37a
3.4 机器跳数
七组计划的机器跳数结果如表5所示。其中,对照组的机器跳数最低。与对照组相比,其他计划组均有统计学意义(P<0.05)。
表5 对照组与其他六组计划跳数比较(±s)

表5 对照组与其他六组计划跳数比较(±s)
组别 机器跳数/MU t值 P值自动NTO 1360.6±109.6 - -K=0.01 1436.5±106.8 5.608 <0.001 K=0.1 1383.5±107.9 2.422 0.026 K=0.3 1381.3±96.0 2.657 0.016 K=0.5 1394.4±98.8 3.164 0.005 K=1 1409.6±101.1 4.594 <0.001 K=5 1418.0±95.2 4.971 <0.001
4 讨论
在设计调强计划时,可以设置的参数很多,如靶区、OAR剂量目标值及优选度、EUD值和NTO值[8]。尽管限量环的使用能够在靶区周围生成较陡峭的剂量跌落区域,但限量环的使用增加了计划设计的时间[9],且限量环的大小、个数等问题对剂量结果有显著影响[10-11]。NTO的使用可以很好地解决此类问题,不需要物理师添加辅助限量环等额外的勾画时间,因此NTO的研究对临床有重要意义。
NTO作为Eclipse 10.0及以上版本放疗计划系统内置的一种简易的优化工具,通过形成陡峭的剂量梯度来限制正常组织的剂量,因此也是影响放疗计划质量的参数之一。NTO涉及的参数较多,五个参数中本研究只改变剂量指数衰减常数K值,其他四个参数固定不变。选择手动NTO改变K值及自动NTO研究宫颈癌术后IMRT计划的影响。近年来,关于NTO的报道不多,早期国外学者Wong等[12]报道了NTO对乳腺癌术后容积旋转调强放疗的影响。Wang等[13]利用限量环和NTO制定脑转移瘤立体定向放射治疗(Stereotactic Body Radiation Therapy,SBRT)外科计划,取得了很好的效果。Caldeira等[14]对比了NTO对前列腺癌放疗计划的影响,发现有无NTO靶区CI、HI、计划指数无显著差异,本研究没有讨论无NTO的影响,讨论了自动NTO与手动NTO的对比结果,前人研究NTO对肺癌SBRT的影响,通过对比不同NTO权重、不同K值以及自动NTO靶区和OAR剂量学参数以及机器跳数,发现没有一组NTO设置对于所有的剂量学参数均是最优的[15-16],这与本研究结果一样,如K为0.3及以上时,靶区CI比对照组好,但是HI结果没有显示优势,且部分OAR结果比对照组高,部分OAR结果比对照组低。叶芝甫[17]选取10例鼻咽癌患者,每位患者分别设置NTO权重分别为1~999,设置跌落值分别为0.01~5.00,设置靶区边缘距离1 mm,开始剂量和跌落剂量分别为100%和10%。结论为NTO权重小于等于100,跌落值0.1~0.3时,可以得到较为理想的计划结果。前人研究SBRT计划推荐K=0.15,权重500[15-16],而本研究推荐自动NTO,这是因为SBRT计划对剂量陡峭的需求更高,不追求均匀性,而本研究为常规分割IMRT计划,当自动NTO启用时,其他参数不会被作用,自动NTO是依靠于患者的结构和优化目标,并自动决定剂量跌落标准。自动NTO会对正常组织的点剂量水平进行动态调整,所以DVH曲线仍然出现一些变化(图2)。手动NTO相对较灵活,如何设置受靶区是多靶还是单靶、靶区与体表轮廓的相对位置关系、靶区与OAR的位置关系、靶区轮廓边缘形态变化是否陡峭等诸多因素影响,本研究中宫颈癌靶区轮廓边缘形态变化较平缓,与直肠、膀胱和小肠等OAR往往存在交叠,靶区位置多位于身体轮廓中央位置并与体表轮廓有一定的距离可满足NTO剂量跌落的距离,故此本研究中自动NTO已经能够满足计划设计要求。而手动NTO受人为因素影响较多,需根据不同的病例进行反复尝试调整,这样优化过程无疑增加了计划设计的时间。相反在头颈部肿瘤的NTO应用中手动NTO优势相对较明显,因为头颈部靶区距离体表轮廓的距离相对较近,临近靶区周围也有较多的OAR,靶区形态轮廓变化较为陡峭,往往在临床中靶区与某些OAR之间的剂量需要非常陡峭的剂量跌落,从靶区和OAR的剂量学结果看,所有组的结果均能满足临床需求。对于正常组织,K值较小时,低剂量体积较小,高剂量体积较大;K值较大时,低剂量体积较大,高剂量体积较小。同样,没有一个K值显示出所有的参数有绝对的优势。自动NTO的机器跳数与其他组相比最小(P<0.05),因此认为自动NTO更适合临床需要。
综上所述,在宫颈癌术后放疗计划中,手动NTO与自动NTO相比,靶区和OAR及正常组织受量没有体现出绝对优势,但是自动NTO的机器跳数更小,能减轻机器负担,建议宫颈癌IMRT临床使用自动NTO。

