miR-25通过TGF-β1途径降低缺氧/复氧诱导的心肌细胞凋亡
徐敏 岳峰 宋勃 周松 黄晶 田水 刘启方
(贵州省人民医院 1康复科,贵州 贵阳 550002;2心内科)
miR-25 在心肌细胞中高表达,参与心肌细胞凋亡和心室重构等病理生理的调节〔1〕。高迁移率族蛋白(HMG)B1是非染色体核蛋白,可导致心肌细胞凋亡及心肌纤维化〔2〕。转化生长因子(TGF)-β1具有诱导生长能力,在心肌间质细胞、心肌细胞中均有表达,在心肌细胞凋亡发生发展过程中有重要作用〔3,4〕。本课题既往研究证实miR-25靶向调控HMGB1的表达〔5〕,miR-25和HMGB1均具有调控心肌细胞凋亡的作用,但二者调控心肌细胞凋亡与TGF-β1有何种关系,本研究将进行探讨。
1 材料和方法
1.1材料 细胞株H9C2心肌细胞来源于胚胎期心脏组织的细胞,购于中国科学院上海细胞库;DMEM 培养基、胎牛血清购自Gibco公司;放射免疫沉淀试验(RIPA)裂解液、考马斯蓝染色(Bradford)蛋白浓度测定试剂盒和二喹啉甲酸(BCA)蛋白浓度检测试剂盒购自江苏碧云天生物有限公司;TGF-β、Smad蛋白、活化的含半胱氨酸的天冬氨酸蛋白水解酶(cleaved caspase)-3、HMGB1和B细胞淋巴瘤/白血病-2基因(Bcl)-2抗体购自Gibco公司;SB-431542试剂购于上海嵘崴达实业有限公司。慢病毒载体由上海吉凯公司构建。
1.2方法
1.2.1分组及转染 H9C2细胞培养24 h 后进行慢病毒感染,向转染组细胞悬液中加入凝聚胺(polybrene)溶液及慢病毒载体。空白对照(control) 组未进行转染;阴性对照(Lv-control) 组转染Lv-control-miRNA模拟物(mimic);Lv-anti-control组转染Lv-control-miRNA-抑制剂(inhibitor);Lv-miR-25组转染Lv-miR-25 mimic;Lv-anti-miR-25组转染Lv-miR-25 inhibitor。按照脂质体转染试剂Lipofectamine2000 试剂盒说明,Contol-shRNA组转染control-shRNA;HMGB1-shRNA组转染HMGB1-shRNA,经培养后筛出稳定细胞系。选取高表达miR-25 H9C2心肌细胞,Lv-miR-25组转染Lv-miR-25 mimic,Lv-miR-25+SB431542组转染Lv-miR-25 mimic后加入TGF-β1/smads抑制剂SB431542共培养。稳定转染后予缺氧/复氧处理,缺氧培养箱(37℃、1% O2、5% CO2、94% N2)培养24 h后行复氧培养箱(95%空气和5% CO2)1 h〔6〕。
1.2.2Western印迹检测蛋白表达 Western 印迹法检测HMGB1、Bcl-2、Cleaved caspase-3、TGF-β1、Smad3、磷酸化(p)-Samd3、细胞外信号调节激酶(ERK)1/2、p-ERK1/2蛋白表达。RIPA裂解液提取细胞总蛋白,蛋白定量后十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,电转聚偏氟乙烯(PVDF)膜,封闭及洗膜后,均加入按照1∶1 000稀释好的cleaved caspase-3、Bcl-2、HMGB1、TGF-β1、Smad3、p-Smad3、ERK1/2、p-ERK1/2抗体,4℃摇床孵育24 h,加入1∶2 000稀释的辣根过氧化物酶(HRP)标记的二抗,室温孵育2 h,电化学发光(ECL)显色。
1.2.3流式细胞术检测细胞凋亡 收集缺氧/复氧处理的细胞,制备成105/ml 浓度的细胞悬液,磷酸盐缓冲液(PBS)洗涤细胞,离心弃上清重悬细胞,加入膜联蛋白(Annexin)V-异硫氰酸荧光素(FITC)5 μl和碘化丙啶(PI)10 μl,室温孵育15 min,上流式细胞仪分析。
1.3统计学方法 应用SPSS20.0软件进行数据分析。Bonferroni法进行组间均数的两两比较,多组数据的比较采用方差分析。
2 结 果
2.1miR-25调控HMGB1及细胞凋亡相关蛋白的表达 Lv-miR-25组HMGB1、Cleaved caspase-3蛋白表达水平明显低于Control组、Lv-control组、Lv-anti-control组、Lv-anti-miR-25组(均P<0.05),Bcl-2蛋白表达水平明显高于Control组、Lv-control组、Lv-anti-control组、Lv-anti-miR-25组(均P<0.05),见表1、图1、图2。
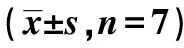
表1 各组H9C2细胞中HMGB1、Bcl-2和Cleaved caspase-3 蛋白表达比较
2.2HMGB1调控TGF-β1、Smad蛋白及细胞凋亡相关蛋白的表达 与Contol-shRNA组相比,HMGB1-shRNA 组HMGB1、TGF-β1蛋白、p-Smad3、Cleaved caspase-3蛋白表达显著下降、Bcl-2蛋白表达显著上升(P<0.05)。两组ERK1/2蛋白表达差异无统计学意义(P>0.05)。见图3、图4、表2。

1~5:Control组、Lv-control组、Lv-miR-25组、Lv-anti-control组、Lv-anti-miR-25组;图2同图1 miR-25高表达对H9C2心肌细胞 HMGB1表达的影响

图2 miR-25高表达对H9C2心肌细胞凋亡 相关蛋白表达的影响

图3 沉默HMGB1表达对H9C2心肌细胞 TGF-β1表达的影响

图4 沉默HMGB1表达对H9C2心肌细胞凋亡 相关蛋白表达的影响
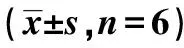
表2 各组H9C2细胞中HMGB1、Bcl-2和Cleaved caspase-3蛋白表达比较
2.3TGF-β1/Smads信号通路调控细胞凋亡 相对于Lv-miR-25组,Lv-miR-25+SB431542组Cleaved caspase-3表达显著增加,Bcl-2蛋白表达显著下降(均P<0.05),提示细胞凋亡减少。相对于Lv-miR-25组,Lv-miR-25+SB431542组凋亡细胞明显减少(16.17%±3.06% vs 6.13%±1.26%P<0.05),见图5、表3。

图5 TGF-β1抑制剂对H9c2心肌细胞凋亡相关蛋白表达及凋亡率的影响
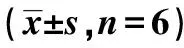
表3 各组H9C2细胞中Bcl-2和Cleaved caspase-3 蛋白表达比较
3 讨 论
细胞凋亡是一个复杂的病理生理过程,涉及多种亚细胞器和细胞分子。研究表明缺血缺氧和再灌注损伤引起的细胞凋亡是通过线粒体途径完成的,Bcl-2家族、caspase家族在细胞凋亡过程中均发挥重要作用。Bcl-2 的表达下调,caspase-3表达上调,引起心肌细胞凋亡;Bcl-2表达上调及caspase-3表达下调对心肌细胞凋亡起抑制作用〔7〕。本研究通过高表达miR-25,检测凋亡相关蛋白表达,结果显示Bcl-2表达上调及caspase-3表达下调,对心肌细胞凋亡具有保护作用。HMGB1 在心血管疾病发生发展的过程中发挥重要的作用。Foglio等〔8〕研究在心肌梗死大鼠模型试验中,给予HMGB1治疗,能够降低caspase-3表达,减轻心肌细胞凋亡率。Hu等〔9〕报道HMGB1在心肌缺血再灌注损伤中扮演着重要的作用,能够导致心肌细胞凋亡,给予HMGB1抗体处理,能够显著增加Bcl-2蛋白表达及较少的凋亡细胞,其作用通过调控白细胞介素-17A。本研究发现通过转染shRNA-HMGB1抑制H9C2细胞HMGB1的表达,检测凋亡相关蛋白表达,Bcl-2表达上调及caspase-3表达下调,心肌细胞凋亡减少。检测TGFβ1、p-Smad蛋白表达下降,HMGB1的表达下降具有下调TGF-β1、p-Smad蛋白的作用。TGF-β1 是一种的具有众多功能的细胞因子,TGF-β1 及受体在心肌间质细胞、心肌细胞中均有表达,它通过调控特殊的信号通路诱导心肌细胞的凋亡〔10,11〕。Wua等〔12〕研究显示,miR-202-3p通过负向调控TRPM6的表达,抑制TGF-β1/smads信号通路减少缺血再灌注损伤所致的心肌细胞凋亡。本研究通过使用TGF-β1抑制剂SB431542与高表达miR-25 H9C2细胞共培养,结果显示相对于单纯高表达miR-25细胞组,使用TGF-β1抑制剂SB431542能够进一步抑制心肌细胞凋亡。由此推断下调TGFβ1表达能够降低心肌细胞凋亡。miR-25具有靶向调控HMGB1的作用。本研究证实HMGB1的表达下降能够下调TGF-β1蛋白的表达,TGF-β1具有调控细胞凋亡的作用,因此得出miR-25通过HMGB1影响TGF-β1/smads信号通路参与保护心肌细胞凋亡的作用。但心肌缺血再灌注损伤导致细胞凋亡是众多因素共同作用的复杂过程,各种细胞因子之间错综复杂的调控关系及转录后的基因调控都扮演着重要的作用,本研究仅仅探讨心肌细胞凋亡调控的一种途径。

