改良阿特金斯饮食对超重/肥胖多囊卵巢综合征患者糖脂代谢、体成分、性激素水平及月经影响
郑小莉 刘永利 张秀智
徐州医科大学附属徐州市立医院(徐州市第一人民医院)(221000)
多囊卵巢综合征(PCOS)中超五成合并超重或肥胖,体质指数(BMI)过高会导致患者代谢紊乱进一步影响生殖功能,患者出现三高概率上升[1-3]。以往临床多采用单纯药物治疗,但药物敏感度不高疗效有限,加上传统的饮食及运动干预对超重/肥胖的PCOS患者来说周期漫长,大多患者无法坚持,未能达到理想的干预效果[4-6]。生酮饮食是一种高脂低碳水化合物的饮食疗法,但因对饮食限制要求较严格,且高脂饮食易带来一系列不良反应[7-8],故许多患者无法完成整个疗程,因其与阿特金斯饮食方式相关性高,而后提出改良阿特金斯饮食(MAD)疗法,后经证实与减脂、改善胰岛素抵抗等有关,并在临床取得一定疗效。目前MAD运用在超重/肥胖PCOS的研究较少,故本文对其进行探究分析。
1 资料与方法
1.1 一般资料
选择2020年6月1日-2021年3月31日在徐州市第一人民医院、徐州市第六人民医院就诊的超重/肥胖且确诊PCOS患者。纳入标准:①符合PCOS诊断标准;②符合《中国成人超重和肥胖症预防控制指南》肥胖或超重定义;③有生育需求;④性生活正常且未采取避孕措施。排除标准:①不孕原因为男性、不育或输卵管异常;②近期使用激素类药物或进行诱导排卵治疗;③合并糖尿病;④合并内分泌、重要器官疾病、肿瘤;⑤合并精神异常。患者及其家属均签署知情同意书,本研究经本院医学伦理委员会批准通过。
1.2 方法
纳入对象随机分两组各40例。对照组给予常规药物治疗和健康生活方式管理的建议。MAD组在对照组基础上根据MAD操作方法给予饮食干预:①MAD前基线评估,排除相关禁忌证。②依据专业营养师及医生提供的饮食方案,按照MAD标准对患者一日三餐饮食食谱进行规定,评价患者营养情况,定期检测体成分指标。③妇科医师持续检测患者月经及妊娠情况,营养师日常监控患者营养状况。④MAD疗法首先摄入较少的碳水化合物,初始以15g/d为标准,1个月后调整为20~30g/d,不需要患者住院及禁食,且不对热量、蛋白和液体的摄入做出规定。⑤使用基础代谢(间接测热法、生物电阻抗法)或公式法计算能量供应标准。将MAD中的脂肪/(蛋白质+碳水化合物)比例设置为1:1或2:1。⑥遵循以上原则,患者可以在保证自己饮食偏好情况下,要求营养师定期更改食谱,完成每日咨询答疑,保证患者接受干预的依从度,确保饮食方案的有效执行。
1.3 观察指标
观察所有患者干预前及干预1、2、3个月后糖代谢[空腹胰岛素(FINS)、空腹血糖(FPG)、胰岛素抵抗指数(HOMA-IR)]、脂代谢[甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)]、体成分[体重、体重指数(BMI)、体脂率、腰围、内脏脂肪区域]、性激素[黄体生成素(LH)、卵泡生成素(FSH)、睾酮(T)、雌二醇(E2)]水平及干预3个月后两组患者自然月经周期、自然成功受孕、排卵率及不良反应发生情况(胃肠道不适、肾结石、脂代谢紊乱)。
1.4 统计学处理
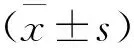
2 结果
2.1 一般情况
MAD组40例,年龄(28.5±3.2)岁(19~39)岁,受教育水平为小学及以下7例(17.5%)、初中及中专20例(50.0%)、大专及以上13例(32.55);对照组40例,年龄(28.2±3.2)岁(20~38)岁,受教育水平为小学及以下6例(15.0%)、初中及中专19例(47.5%)、大专及以上15例(37.5%)。两组比较无差异(P>0.05)。
2.2 两组干预前后糖代谢指标比较
干预前,两组FINS、FPG、HOMA-IR水平无差异(P>0.05);干预后1、2、3个月两组各项水平均呈现下降趋势且MAD组低于对照组(P<0.05)。见表1。

表1 两组干预前后糖代谢指标比较
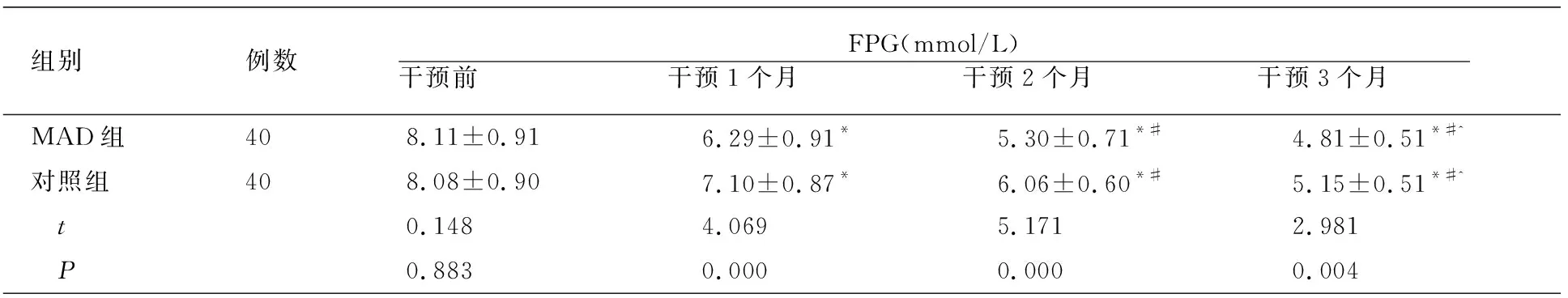
组别例数FPG(mmol/L)干预前 干预1个月 干预2个月 干预3个月 MAD组408.11±0.916.29±0.91*5.30±0.71*#4.81±0.51*#^对照组408.08±0.907.10±0.87*6.06±0.60*#5.15±0.51*#^ t 0.1484.0695.1712.981 P0.8830.0000.0000.004
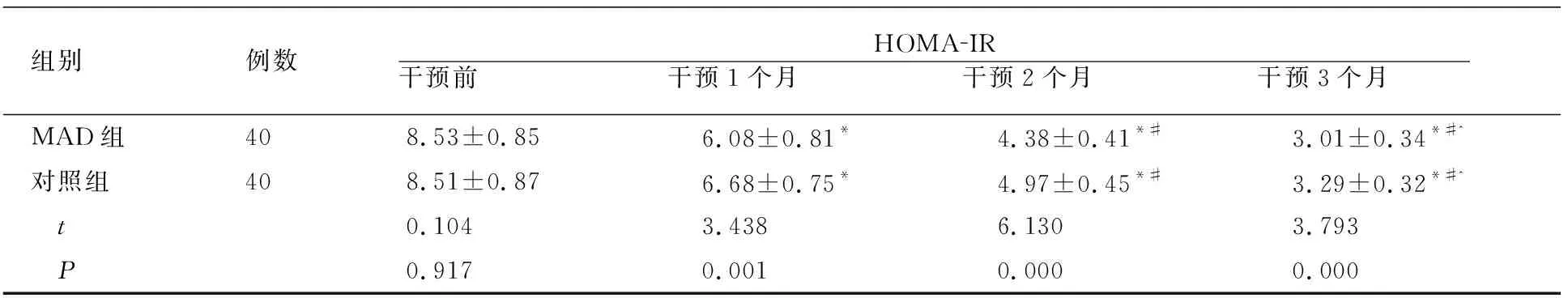
组别例数HOMAIR干预前 干预1个月 干预2个月 干预3个月 MAD组408.53±0.856.08±0.81*4.38±0.41*#3.01±0.34*#^对照组408.51±0.876.68±0.75*4.97±0.45*#3.29±0.32*#^ t 0.1043.4386.1303.793 P0.9170.0010.0000.000
2.3 两组干预前后脂代谢指标比较
干预前,两组TG、TC、HDL-C、LDL-C水平比较无差异(P<0.05);干预后1、2、3个月,两组TG、TC、LDL-C呈现下降趋势且MAD组低于对照组,HDL-C水平呈上升趋势且MAD组高于对照组(P<0.05)。见表2。

表2 两组干预前后脂代谢指标比较
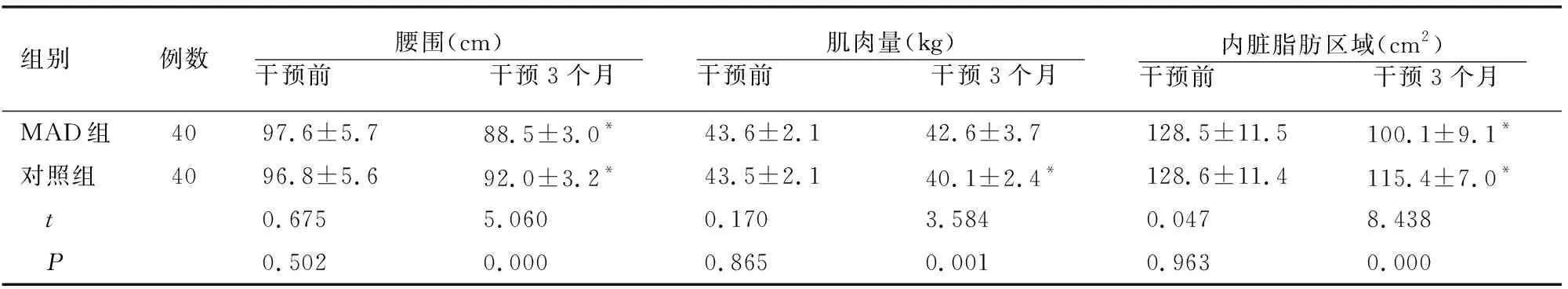
2.4 两组干预前后体成分指标比较
干预前,两组体重、BMI指数、体脂率、腰围、肌肉量及内脏脂肪区域无差异(P>0.05);干预后3个月,两组各项水平均下降且MAD组体重、BMI指数、体脂率、腰围及内脏脂肪区域水平低于对照组,肌肉量水平高于对照组(P<0.05)。见表3。
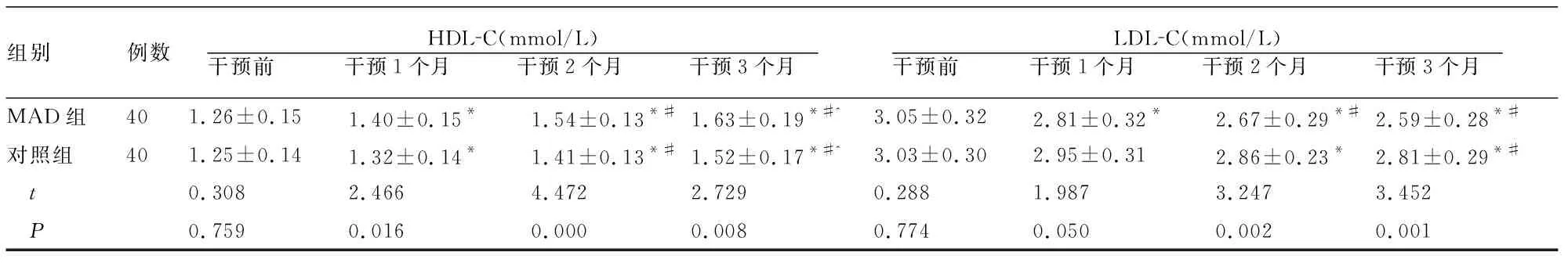
组别例数HDLC(mmol/L)干预前 干预1个月 干预2个月 干预3个月 LDLC(mmol/L)干预前 干预1个月 干预2个月 干预3个月 MAD组401.26±0.151.40±0.15*1.54±0.13*#1.63±0.19*#^3.05±0.322.81±0.32*2.67±0.29*#2.59±0.28*#对照组401.25±0.141.32±0.14*1.41±0.13*#1.52±0.17*#^3.03±0.302.95±0.312.86±0.23*2.81±0.29*# t 0.3082.4664.4722.7290.2881.9873.2473.452 P 0.7590.0160.0000.0080.7740.0500.0020.001

表3 两组干预前后体成分指标比较
组别例数腰围(cm)干预前 干预3个月 肌肉量(kg)干预前 干预3个月 内脏脂肪区域(cm2)干预前 干预3个月 MAD组4097.6±5.788.5±3.0*43.6±2.142.6±3.7128.5±11.5100.1±9.1*对照组4096.8±5.692.0±3.2*43.5±2.140.1±2.4*128.6±11.4115.4±7.0* t 0.6755.0600.1703.5840.0478.438 P 0.5020.0000.8650.0010.9630.000
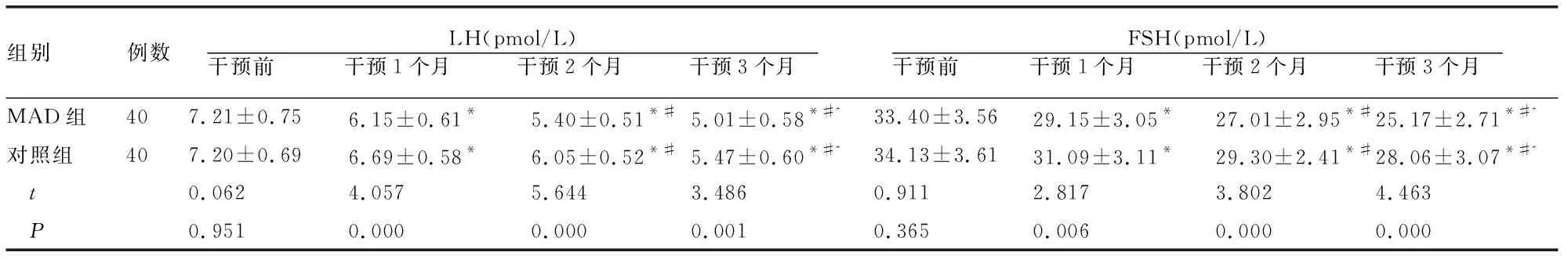
2.5 两组干预前后性激素水平比较
干预前,两组T、E2、LH及FSH水平无差异(P>0.05);干预后1、2、3个月,两组各项水平均呈现下降趋势且MAD组低于对照组(P<0.05)。见表4。

表4 两组干预前后性激素水平比较
组别例数LH(pmol/L)干预前 干预1个月 干预2个月 干预3个月 FSH(pmol/L)干预前 干预1个月 干预2个月 干预3个月 MAD组407.21±0.756.15±0.61*5.40±0.51*#5.01±0.58*#^33.40±3.5629.15±3.05*27.01±2.95*#25.17±2.71*#^对照组407.20±0.696.69±0.58*6.05±0.52*#5.47±0.60*#^34.13±3.6131.09±3.11*29.30±2.41*#28.06±3.07*#^ t 0.0624.0575.6443.4860.9112.8173.8024.463 P0.9510.0000.0000.0010.3650.0060.0000.000
2.6 两组干预后月经与受孕情况比较
干预结束后,MAD组建立自然月经周期37例(92.5%)、自然成功受孕7例(17.5%)、排卵率82.5%(33/40);对照组建立自然月经周期31例(77.5%)、自然成功受孕1例(2.5%)、排卵率65.0%(26/40);MAD组自然成功受孕高于对照组(χ2=5.00,P=0.025<0.05)。
2.7 两组干预后不良反应发生情况比较
干预结束后,MAD组胃肠道不适1例、肾结石1例,对照组胃肠道不适2例、肾结石3例与脂代谢紊乱3例。MAD组不良反应发生率(5.0%,2/40)低于对照组(20.0%,8/40)(χ2=4.114,P=0.043<0.05)。
3 讨论
PCOS的特征为胰岛素抵抗、持续性排卵异常及高雄激素血症为主,常表现为不孕、月经周期异常等,病程漫长且易复发[9-10]。目前POCS病因尚未明确,大多PCOS患者存在超重或肥胖。研究显示,饮食结构异常是该类人群发病的主要原因,降低体重有助于恢复患者月经及妊娠,故适当的营养干预在治疗中尤为关键[11-12]。生酮饮食方案强调高脂与低碳水,但对于饮食有着严格限制,导致患者依从性较低,故需要探索脂肪比例更低的饮食方案。MAD比传统的生酮饮食更接近国内饮食习惯。
本研究结果显示,MAD组干预后各时点糖脂代谢指标水平改善程度均优于对照组,体重、BMI指数、体脂率、腰围及内脏脂肪区域均低于对照组。究其原因:MAD疗法中采取低碳水化合物的营养干预措施,其中脂肪、蛋白质占比较高,饱腹感较强不易因饥饿而过度进食,减少对食物的摄入,且与生酮饮食一样均能产生酮症,使患者机体处于酮体模拟饥饿状态中,加强脂肪分解代谢,通过肝脏合成酮体之后进入血液中供给给肝外组织,达到减脂的目的;酮体还能够调节患者的食欲,MAD方式中限制碳水化合物的摄取,患者肠道单糖吸收能力下降,血糖水平随之下降,进而降低胰岛素水平后,影响脂肪的合成,促进脂肪分解,进而改善患者内分泌情况,因此MAD疗法能够有效降低患者体重、减少内脏脂肪的堆积,从而改进胰岛素抵抗,达到改善糖脂代谢及体成分的效果。此外,MAD组干预后各时点性激素指标水平均低于对照组,自然成功受孕率高于对照组,这可能是因为传统的饮食干预中,饮食受限较多且操作难度大,患者很难坚持到底;但MAD不需要禁食,对蛋白质和脂肪的限制较少,对液体及热量的摄入要求也不高,故患者更易接受,在MAD疗法的调理下,患者建立了较为健康的饮食方式,能够有效改善月经紊乱、调节月经周期恢复正常,保护子宫内膜,促进其排卵及内分泌协调,改善性激素指标,并且降低超重或肥胖患者的体重,保证妊娠不受影响。MAD组不良反应发生率低于对照组,究其原因在于,MAD中脂肪比例较低及蛋白比例相对较高,而常规干预中未对患者饮食进行管理,可能会造成患者食入比例不当的蛋白质而导致肾脏负担沉重,且胃肠道不适感加剧,引发脂代谢紊乱,故使用MAD出现不良反应的概率更低。侯锦等[13]认为,无论患者BMI降低与疗效间相关性是否存在,改良阿特金斯氏饮食均对肥胖或超重的耐药性癫痫患者有较好疗效。这也从侧面印证本研究结论的可靠性。
综上所述,MAD疗法对超重/肥胖的PCOS患者是一种行之有效的干预方式,可使患者糖脂代谢、性激素、体成水平分及月经、妊娠情况均显著改善,不良反应发生率较低。

