体检人群非酒精性脂肪性肝病与心血管疾病发病风险的关联性研究
水明明 石 明 李艳萍 张 晨 党少农
1 西安交通大学医学部公共卫生学院,710061 陕西 西安;2 咸阳市中心医院健康管理中心,712000 陕西 咸阳
非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)是最常见的慢性肝脏疾病。有研究表明,NAFLD患者发生心血管疾病(cardiovascular disease,CVD)的概率高于非NAFLD患者[1-2],而且CVD被列为NAFLD患者的首要死因[3]。若能较准确地预测NAFLD人群未来发生CVD的风险,有利于确定该人群中CVD高风险者,从而对其及时采取有效的干预措施,这对NAFLD人群CVD的防治意义重大。目前,国际上应用的心血管病风险评估方案多基于美国Framingham心脏研究或欧洲SCORE研究建立的预测模型,国内通常采用的是中国人缺血性心血管病(ICVD)10年发病危险评估方法及简易评估工具[4],这些评估模型和工具都有一定的局限性[5]。《中国心血管病预防指南(2017)》给出了新的适合中国人群的CVD 10年发病风险评估方案及评估工具[6],采用该评估模型进行CVD风险评估后分析其与NAFLD关系的研究尚未见报道。本研究根据该评估工具对2019年咸阳市体检人群的心血管疾病相关危险因素进行风险评估,分析NAFLD与未来10年CVD发病风险的关系,探讨使用该工具评估NAFLD人群未来发生CVD风险的可行性,为该人群CVD的早期预防与控制提供理论依据和实践建议。
1 对象与方法
1.1 研究对象
数据来源于2019年1月至12月在咸阳市中心医院健康管理中心体检的受检者19 002例(年龄≥18岁)。排除酒精性脂肪肝、应用乙胺碘呋酮或糖皮质激素等药物、可导致脂肪肝的特定疾病(如基因3型丙型肝炎病毒感染、肝豆状核变性、自身免疫性肝炎等)及资料不完整者3 236例。最终纳入人群为15 766例。纳入人群和排除人群在性别和年龄上略有差异,纳入人群平均年龄(46.39±12.68)岁小于排除人群(58.42±11.71)岁,纳入人群男性比例(61.39%)略低于排除人群(78.80%)。本研究通过咸阳市中心医院伦理委员会审批,(伦)审编号为2022-IRB-17号。
1.2 研究方法
采集受检者基本信息(年龄、性别、既往病史、过量饮酒史、吸烟史),测量血压、身高、体质量,检测空腹血糖、甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、谷丙转氨酶、谷草转氨酶、肌酐、尿素氮、尿酸等指标。应用B型超声诊断脂肪肝。过量饮酒史指过去12个月每周饮用乙醇或酒精男性≥210 g,女性≥140 g。
1.3 研究指标
1.3.1 非酒精性脂肪性肝病诊断标准
采用《非酒精性脂肪性肝病防治指南(2018年更新版)》中NAFLD的诊断标准[7]:有弥漫性肝细胞脂肪变的影像学或组织学证据,无过量饮酒等可以导致肝脂肪变的其他病因。脂肪肝B型超声影像学标准:肝脏前场回声增强(“明亮肝”)、远场回声衰减以及肝内管道结构显示不清楚等特征。
1.3.2 心血管疾病发病风险评估
采用《中国心血管病预防指南(2017)》给出的适合中国人群动脉硬化性心血管病(atherosclerotic cardiovascular diseases,ASCVD)的10年发病风险评估方案及评估工具[6]。在对个体进行风险评估时,已被确诊为ASCVD者(包括急性心肌梗死、冠心病、急性缺血性卒中、有症状的周围动脉疾病)直接列为极高危人群;已确诊糖尿病患者(年龄≥40岁)或单个危险因素水平极高者[LDL-C≥4.9 mmol/L或TC≥7.2 mmol/L、3级高血压者、重度吸烟者(≥30支/d)]列为高危人群。将血压、血清胆固醇LDL-C或TC水平作为危险分层的参数,对剩余人群进一步评估其未来10年ASCVD的发病风险,共计21种组合。其中血压分为有高血压和无高血压,血清胆固醇水平分为3类:3.1 mmol/L≤TC<4.1 mmol/L或1.8 mmol/L≤LDL-C<2.6 mmol/L;4.1 mmol/L≤TC<5.2 mmol/L或2.6 mmol/L≤LDL-C<3.4 mmol/L;5.2 mmol/L≤TC<7.2 mmol/L或3.4 mmol/L≤LDL-C<4.9 mmol/L。
1.3.3 高血压判定标准
有高血压病史或安静状态下,收缩压≥140 mmHg(18.6 kPa)和/或舒张压≥90 mmHg(12.0 kPa)。
1.3.4 糖尿病判定标准
有糖尿病史或空腹血糖水平≥7.0 mmol/L。
1.3.5 超重或肥胖判定标准
BMI≥28 kg/m2为肥胖,24 kg/m2≤BMI<28 kg/m2为超重。
1.3.6 血脂异常判定标准
TC≥3.1 mmol/L和(或)LDL-C≥1.8 mmol/L。
1.4 统计学方法

2 结果
2.1 基本特征
本研究共纳入研究对象15 766人,男性9 734人,占总人数的61.7%,女性6 032人,占总人数的38.3%,男性平均年龄(46.90±12.57)岁,女性平均年龄(46.19±13.08)岁。高血压患病率28.5%,糖尿病患病率7.1%。
2.2 NAFLD的分布特点
本研究中NAFLD人群共6 043例,NAFLD总患病率38.3%。其中男性患病率(43.8%)高于女性(29.6%),差异有统计学意义(χ2=320.85,P<0.001)。NAFLD的患病率存在年龄差异(χ2=272.57,P<0.001)。NAFLD组年龄、BMI、血压、TG、TC、LDL-C、空腹血糖、尿酸、谷丙转氨酶、谷草转氨酶、肌酐、尿素氮、高血压患病率和糖尿病患病率均高于非NAFLD组,HDL-C低于非NAFLD组(P<0.05)。见表1。

表1 NAFLD与非NAFLD体检人群的基本特征
2.3 研究对象未来10年ASCVD发病风险
未来10年ASCVD发病风险低危人群占70.3%,中危占13.4%,高危占14.3%,极高危占2.0%。男性ASCVD风险整体高于女性,且未来10年ASCVD发病风险存在年龄差异,差异具有统计学意义。在单因素分析中,高血压、糖尿病、NAFLD、超重或肥胖、血脂异常和吸烟与未来10年ASCVD发病风险相关(P<0.05)。见表2。
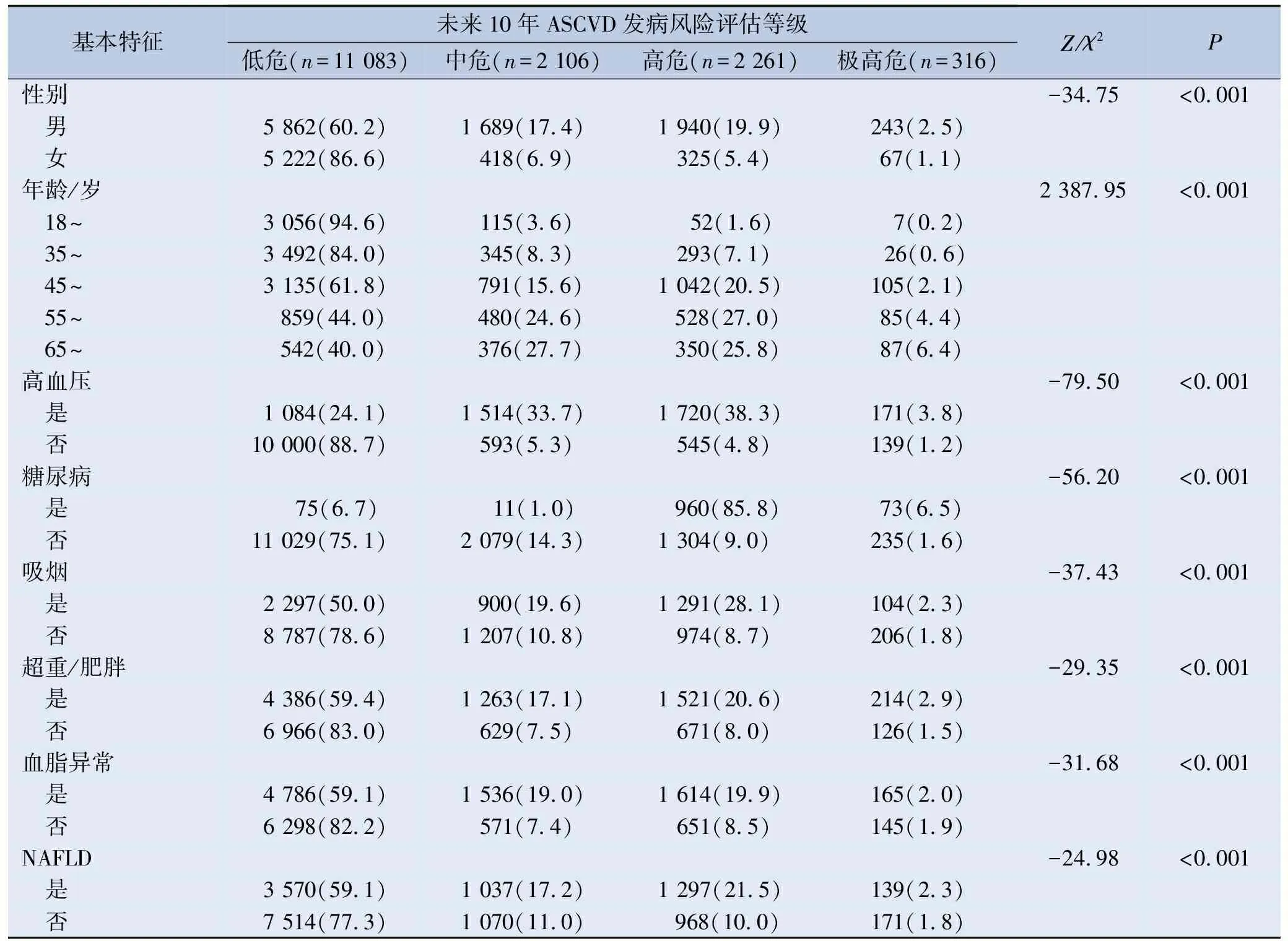
表2 体检人群未来10年ASCVD发病风险评估等级分布
2.4 NAFLD与未来10年ASCVD发病风险的关系
模型1显示,与非NAFLD人群相比,NAFLD人群未来10年ASCVD发病风险增高,OR值为2.36(95%CI:2.20~2.53)。模型2中,在控制年龄、性别混杂因素后,NAFLD与未来10年ASCVD发病风险独立相关,NAFLD对应的OR值为2.74(95%CI:2.53~2.98)。模型3中,将年龄、性别、高血压、糖尿病、血脂异常、超重或肥胖、吸烟作为混杂因素,NAFLD与未来10年ASCVD发病风险仍独立相关,NAFLD对应的OR值为1.31(95%CI:1.12~1.52),说明NAFLD使未来10年ASCVD发病风险增高。将总人群按照性别分层,男性人群在模型1、模型2、模型3中NAFLD对应的OR值分别为2.01(95%CI:1.85~2.18)、2.72(95%CI:2.48~2.99)、1.35(95%CI:1.12~1.61),提示男性人群中NAFLD与未来10年ASCVD发病风险独立相关。控制了可能的混杂因素后,在女性人群中尚未发现NAFLD与未来10年ASCVD发病风险的关联性(OR=1.20,95%CI:0.86~1.68)。见表3。
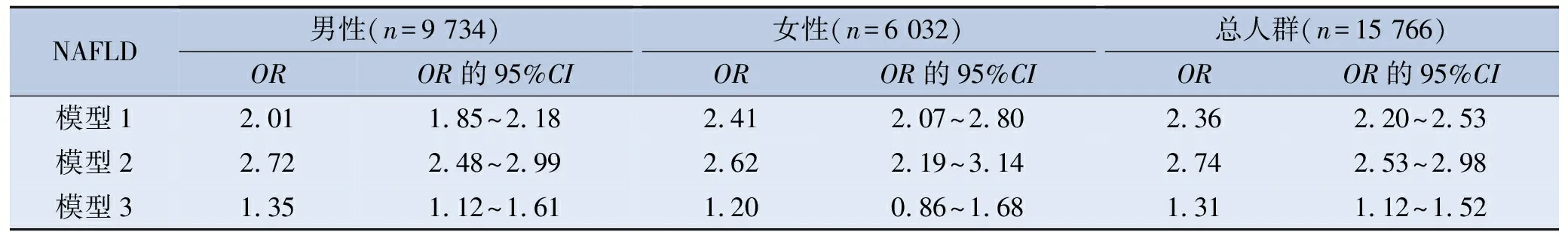
表3 体检人群NAFLD与未来10年ASCVD发病风险的关系
鉴于极高危人群是已经确诊的ASCVD者,为了更好地分析NAFLD与未来10年ASCVD发病风险的关系,将极高危人群排除后进一步分析显示,2者关系仍保持不变。见表4。
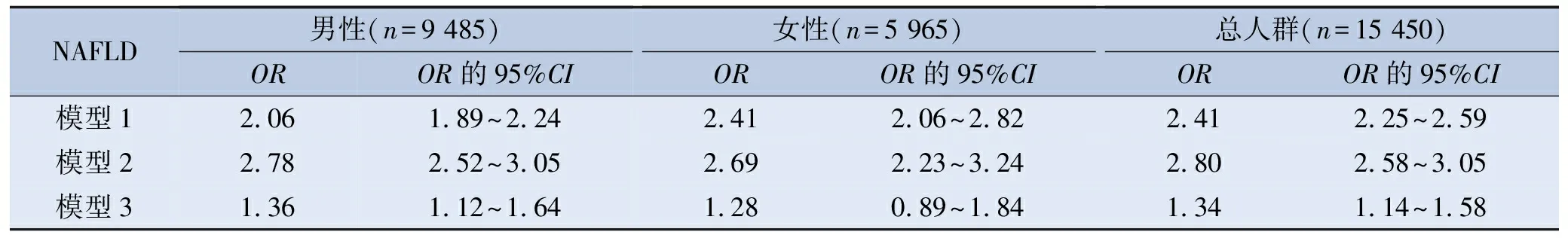
表4 体检人群NAFLD与未来10年ASCVD发病风险的关系(排除极高危人群)
3 讨论
中国NAFLD的患病率为15.0%~54.3%[8-10],本研究中NAFLD患病率为38.3%,处于全国中等水平。其中男性患病率高于女性,NAFLD组年龄、BMI、血压、TG、TC、LDL-C、空腹血糖、谷丙转氨酶、谷草转氨酶等均高于非NAFLD组,这与林苏兰等[9]的研究结果一致,而且本研究也发现NAFLD与代谢综合征和其组成成分相关,有国际专家小组建议将NAFLD命名为代谢功能障碍相关性脂肪性肝病(MAFLD)[11]。本研究中估计的未来10年ASCVD发病风险高危和极高危者占16.4%,与其他采用相同CVD发病风险评估工具的人群比较也处于中等水平[12-14]。
NAFLD和CVD之间存在关联[1-2,15],其潜在联系机制非常复杂,NAFLD可能通过全身炎症、内皮功能障碍、胰岛素抵抗、氧化应激、脂质代谢失调和不稳定斑块形成等多个途径,促进动脉粥样硬化、心肌病和心律失常的发生,进而导致心血管疾病的发生和致死[16-17]。一项NAFLD患者33年的随访研究中指出,43%的NAFLD患者死于CVD,其次是非胃肠道恶性肿瘤(19%),而肝癌、肝硬化等与肝脏相关的疾病死亡率排第三(13%)[3]。
CVD风险评估和危险分层是预防和控制CVD的必要前提,在临床和CVD防治中发挥了重要的指导作用[6]。Jasson等[18]指出,对NAFLD患者开展CVD风险筛查很有必要,有利于对NAFLD患者进行心血管疾病的早期预防和干预。Tamaki等[19]基于健康体检人群,采用Framingham风险评分(FRS)进行CVD评估,表明肝纤维化和NAFLD独立于已知的CVD风险疾病与CVD风险相关。本研究采用《中国心血管病预防指南(2017)》公布的适合我国人群的心血管疾病10年发病风险评估工具,这是目前我国最新的CVD风险筛查工具。单因素分析中,性别、年龄、糖尿病、超重或肥胖、高血压、血脂异常和吸烟与未来10年ASCVD的发病风险相关。在控制这些混杂因素后,NAFLD与未来10年ASCVD发病风险仍独立关联,说明在不依赖于CVD风险已知疾病(高血压、糖尿病、血脂异常)的情况下,NAFLD可以增加未来10年ASCVD的发病风险,与Tamaki等的研究结果相似。进一步按性别分层后发现,男性NAFLD与未来10年ASCVD发病风险存在独立关联,但在女性人群中没有观察到这种关联,这可能是由于男性NAFLD患病率高于女性,男性可能在胰岛素抵抗、脂代谢失调、不稳定斑块形成等NAFLD引发CVD的病因上与CVD关系更密切导致。因此,对于NAFLD体检人群,尤其是男性,有必要同时进行CVD风险筛查。NAFLD的防治基础是改变生活方式,例如减肥、合理膳食和增加体力活动[17]。虽然目前还没有针对NAFLD的特效药,但通过使用他汀类药物、降压药(如ACE抑制剂和血管紧张素受体阻滞剂)来治疗相伴随的CVD危险因素,可以降低和控制CVD的发病风险[20]。
本研究仍存在一些局限性。首先,这是一项现况调查研究,目前只提示NAFLD和CVD风险之间存在显著关联,尚无法进行2者的因果关系推断。其次,本研究纳入人群较为年轻,男性较少,可能会低估2者的关系。第三,本研究对象为体检人群,可能不同于一般的自然人群,故结果可能只适用于体检人群,同时本研究为单中心研究,可能影响了样本的代表性。此外,由于体检人群的一些社会人口基本特征信息不完整,可能存在未知混杂因素引起的偏倚。然而,通常大部分NAFLD患者没有临床症状,多是在体检过程中诊断发现,因此,本研究对于评估该人群中NAFLD患者未来10年CVD发病风险具有一定的参考价值。为了进一步加强NAFLD和CVD风险的因果关系探索,有必要开展更为深入的队列研究。
总之,本研究提示NAFLD与其未来10年ASCVD发病风险可能存在独立关联,建议对NAFLD体检人群,尤其是男性,进行心血管疾病风险筛查,对心血管疾病高危人群采取针对性的干预措施,以达到早期预防和控制心血管疾病的目的。

