极低/超低出生体重儿上肢和下肢静脉留置PICC 的对照观察
印玉静 马月兰 刘小玲
随着围生技术和NICU 生命支持技术的发展,极低/超低出生体重儿的出生率和存活率不断提高。有研究表明[1],我国早产儿出生率为8.1%,低出生体重儿和极低出生体重儿发生率分别为4.4%和6.6%。营养支持是增加极低和超低出生体重儿存活率的关键,但由于其胃肠功能发育不完善,易发生喂养不耐受,因此,肠外营养成为低出生体重儿早期营养供给的重要途径[2]。经外周中心静脉置管(peripherally in-serted central venous catheters,PICC)是一种从外周静脉置入且导管尖端位于中心静脉的深静脉置管术[3],能够在保护血管的同时为早产儿尤其是极低/超低出生体重儿提供长期肠外营养的通路,并且在减轻护士工作量、提高输液安全等方面发挥重要作用。王建荣等[4]指出PICC 的最佳穿刺部位为肘窝下两横指处,首选贵要静脉,其次为肘正中静脉,第三为头静脉,对于无法经过肘部静脉置管的患者,也可以选择颈外静脉、腋下静脉及下肢的股静脉、大隐静脉、腘静脉,但是静脉炎的发生率下肢明显高于上肢。赵京雷等[5]研究报道,下肢静脉一次穿刺成功率低,但具有一次置管到位率高的优点,且并发症发生率与非上肢静脉无差异。而最新指南则推荐优先选择经下肢静脉置管,首选管腔粗直的大隐静脉进行PICC 置管[6]。为再次验证经上下肢不同静脉途径的置管效果及并发症发生情况存在的差异,本研究利用回顾性数据对极低/超低出生体重儿上下肢 PICC 不同部位置管效果及并发症进行比较,以了解不同置管部位对置管综合效果与状态的影响。
1 对象与方法
1.1 研究对象
选取2020 年1—12 月于我科出生的201 例进行PICC 置管的极低/超低出生体重儿,其中男113例,女88 例;胎龄24~36 周,平均29.45±2.04 周;分娩方式:阴道分娩105 例,剖宫产96 例;出生体质量600~1500 g,平均1259.10±255.02 g;置管时日龄平均为5 d;上肢静脉置管者155 例(贵要静脉116 例、头静脉16 例、腋静脉23 例),下肢静脉置管者46 例(大隐静脉41 例、股静脉5 例)。将上肢静脉置管者作为对照组,将下肢静脉置管者做为观察组,两组患儿一般资料比较差异无统计学意义(P>0.05)。
1.2 置管方法
本组极低和超低出生体重儿均选择美德康公司(medcom)1.9Fr 聚氨酯PICC 导管进行穿刺。置管前充分评估患儿并签署家长知情同意书,操作团队由具有PICC 穿刺资质5 年以上的护理人员组成,参照美国静脉治疗护理学会2016 版实践指南进行操作。备齐用物至床边,核对患儿信息后,安置体位;选择合适静脉并测量:上肢为将患儿的手臂外展90°,从预穿刺点沿静脉走向至右胸锁关节,下肢为将患儿下肢外展45°,从预穿刺点沿静脉走向至腹股沟至脐部至剑突,同时测量穿刺肢体和对侧肢体的臂围或腿围;采用最大范围的无菌屏障,PICC 导管按所需长度切割好,安尔碘消毒穿刺侧肢体两遍待干;穿刺时,扎止血带,进针见回血后再送入0.3 cm,确保套管在血管内后松止血带,左手压在套管尖端的血管上,右手退出针芯,助手用无菌镊夹住导管前端,轻轻送入静脉;穿刺上肢静脉送管至腋下时,将患儿头部转向穿刺侧,下颌靠近肩部,避免误入颈静脉;送管至预测长度后抽回血,退出套管,按压穿刺点并止血;穿刺点压一棉签头,“无张力粘贴法”用透明敷贴将弧形固定的导管和导管盘全覆盖,敷贴外用弹力绷带适当加压包扎;X 线确定导管尖端在位后方可使用。置管后48 h 由置管者更换敷料1 次,PICC 使用过程中,每隔7 d由PICC 团队成员更换敷料,如有潮湿、污染、渗血等立即更换,每24 h 用0.9%氯化钠溶液冲管1 次。
1.3 观察指标
(1)置管效果指标:一次穿刺成功率、一次送管成功率、置管所需时间、止血时间及留置时间。①一次送管成功。美国静脉治疗护理学会2016 版实践指南指出[7],PICC 尖端位于上腔静脉与右心房的上壁交界连接点时安全最佳。一次置管到位,即置管送到预置长度,固定后经胸部X 线确认经上肢静脉穿刺的导管尖端位于T4~T6,经下肢静脉穿刺的导管尖端位于T8~T10水平[8];②置管所需时间。从护士扎止血带开始至导管固定完毕[9];③止血时间。从成功退出套管压迫针眼处止血至开始固定导管。
(2)相关并发症:导管堵塞、导管异位、局部渗液、静脉炎、怀疑或明确感染。①导管异位,即置管后或随访行X 线摄片时,导管尖端偏离上下腔静脉[10];②静脉炎,即沿静脉走向出现发红和/或水肿,条索状物形成,有脓液流出[11];③怀疑或明确感染:感染前48 h 内使用过PICC,出现菌血症,经外周静脉抽取血液培养至少1 次结果阳性,同时伴有感染的临床表现,除导管外无其他明确的血行感染源,且导管尖端培养与血培养为同一致病菌[12],若仅有血液培养阳性而导管尖端培养阴性则为疑似感染。
1.4 统计学方法
采用SPSS 25.0 统计学软件对数据进行统计分析,计数资料采用频数(百分率),组间率的比较采用χ2检验或Fisher 精确检验;计量资料采用“均数±标准差”表示,组间均数比较采用t检验。以P<0.05 为差异具有统计学意义。
2 结果
2.1 不同部位留置PICC 一次穿刺成功率和一次送管成功率比较
下肢静脉PICC 一次穿刺成功率高于上肢静脉PICC 穿刺成功率 ,下肢静脉PICC 一次送管成功率高于上肢静脉 ,组间比较差异具有统计学意义(P<0.05),见表1。
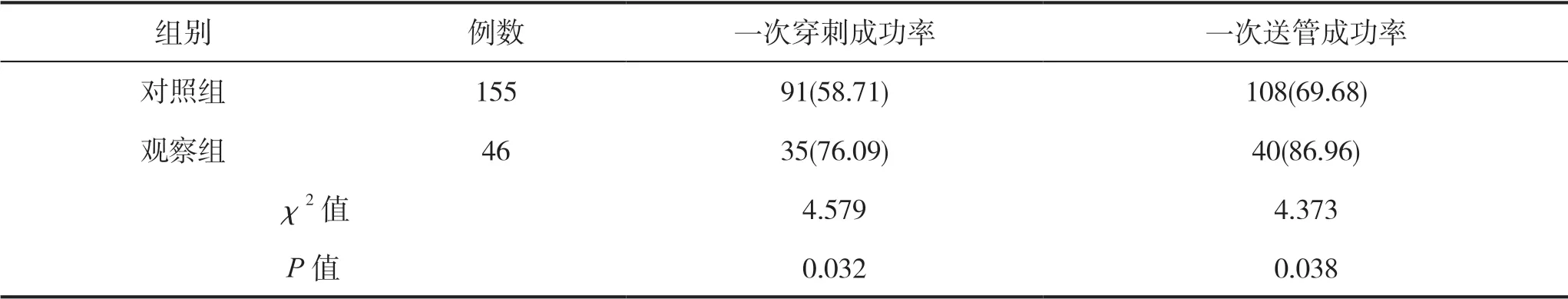
表1 不同部位留置PICC 一次穿刺成功率和一次送管成功率比较
2.2 不同部位留置PICC 时间比较
两组置管所需时间 、上肢静脉PICC 止血时间、留置时间比较差异均无统计学意义(P>0.05),见表2。
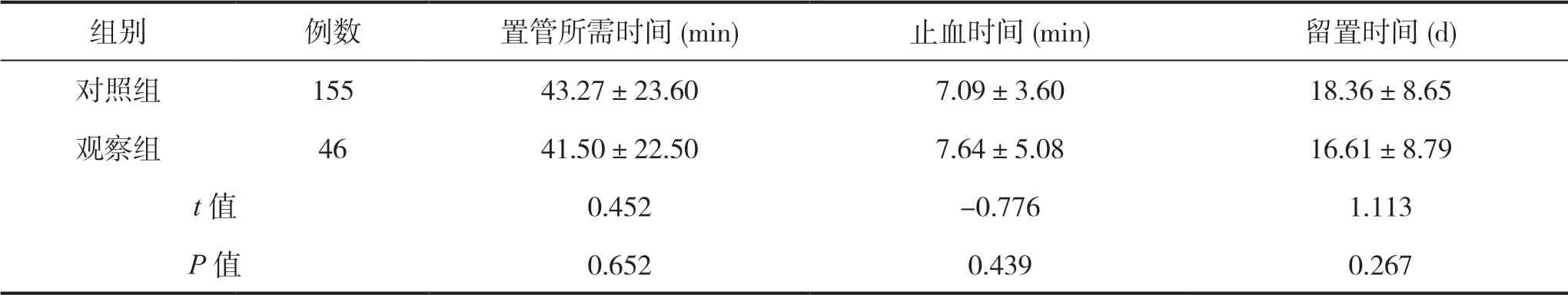
表2 不同部位留置PICC 时间比较
2.3 不同部位留置PICC 导管相关并发症发生情况比较
不同部位留置PICC 导管相关并发症发生情况比较差异均无统计学意义(P>0.05)。说明下肢静脉留置PICC 不会增加并发症发生,见表3。

表3 不同部位留置PICC 导管相关并发症发生情况比较
3 讨论
3.1 经下肢静脉置入PICC 可以提高穿刺效率
本研究结果显示,下肢静脉PICC 一次穿刺成功率和一次送管成功率高于上肢静脉,分析其原因可能是极低和超低出生体重儿上肢静脉比较细且分支多,循环相对较差,针尖进入血管后回血比较慢,而下肢静脉相对于上肢静脉粗直。有研究比较不同外周静脉穿刺PICC 导管发现[13],穿刺成功率由大到小依次为大隐静脉、贵要静脉、腋静脉、肘正中静脉以及颞静脉。大隐静脉起自内踝,穿胫骨内缘,沿大腿内侧缘上行注入股静脉,沿途分支少、管径粗、走向直而置管成功率高[14]。对于危重新生儿或者静脉破坏严重的患儿来说,超声引导的经大隐静脉置管效果也是相当好的[15]。上肢静脉穿刺,虽然在导管送至腋下时,摆放特殊体位可以避免导管误入颈静脉,但却易发生导管送至对侧的锁骨下静脉或者返折至腋静脉,从而影响一次送管的成功率,下肢静脉穿刺则不会发生此类情况,在一定意义上能够减少操作时间。置入PICC 时,止血时间与出血量、操作者的技术水平、患儿的疼痛状态都是有关的,患儿疼痛可引起活动增加,出血增多,止血时间延长。研究显示[16],经下肢静脉置入PICC 时,患儿活动少,疼痛评分低,出血量少。在置管时可以联合采用包括鸟巢姿势、音乐干预、抚触、非营养性吸吮等方法来减轻患儿的疼痛反应[6]。
3.2 经下肢静脉置入PICC 不会增加导管相关并发症发生
本研究结果显示,经上肢和下肢静脉置入PICC在导管相关并发症上比较差异无统计学意义,与赵京雷等[5]的研究结果一致。本研究中,上肢静脉置入PICC 发生1 例导管堵塞,分析原因可能与导管本身管径细、输注营养液及患儿自身的因素有关。2 例继发性导管异位,分析原因可能是,患儿哭闹,上肢活动度大,而新生儿上腔静脉的长度约为1.4~2.3 cm[17],其下腔静脉的长度约为6.78±0.02 cm[18],上下腔静脉的长度差是导致继发性导管异位发生的原因之一。有研究表明[19],极低出生体重儿在置管当日和最后一次胸片时的体质量增长率为11.8%~114.8%,导管末端会出现2~3 个椎体的移位,建议极低出生体重儿优先选择下肢静脉穿刺。静脉炎和导管相关性血流感染是PICC 置管后常见的并发症,本研究中,经上肢静脉置入PICC静脉炎及导管相关性血流感染的发生率高于下肢,但差异无统计学意义。上肢静脉细、分支较多,下肢静脉长、静脉瓣多,置管时均易造成静脉内壁的损伤而发生静脉炎。
综上所述,新生儿尤其是极低和超低出生体重儿,采用经下肢静脉留置PICC 较上肢在置管过程中简化,且不增加并发症发生,未来可以在综合考虑患儿的健康和血管各项因素之后,将经下肢静脉留置PICC 作为其首选置管方式。

