炎症反应源控制对重症肺炎患者血清炎症因子及血气指标的影响研究
周 蕊 馨
(郑州大学第一附属医院综合ICU 郑州 450000)
肺炎作为临床常见呼吸系统疾病,随着机体炎症反应的进行性发展可进展为重症表现,导致患者出现呼吸衰竭及其他系统明显受累。在病理学机制上,促炎/抗炎平衡失调所诱发的全身炎症反应是导致机体免疫功能紊乱的始发因素,而通过炎症反应应激源的控制,抑制炎症风暴是保护器官功能及改善患者预后的关键[1]。临床上,各种生物性因子、非生物因子及内源性致炎因子等均是关键的炎症反应源,本研究以我院收治的90例重症肺炎患者为研究对象,探讨炎症反应源控制的干预方法及临床应用价值,现报道如下。
1 资料与方法
1.1 临床资料
选取2020年6月-2021年6月我院收治的重症肺炎病例中选择90例患者为研究对象。病例纳入标准:(1)经临床综合检查确诊者;(2)对本研究方案知悉且签署知情同意书者;(3)有完整的病历资料者。排除标准:(1)合并免疫系统疾病者;(2)合并其他感染性疾病者;(3)合并精神障碍疾病者。按入院顺序予以患者编号,再根据奇偶数予以分组,分为C组和C+Y组各45例。两组患者的一般资料分布具有一致性(P>0.05),见表1。

表1 C组和C+Y组患者基线资料分布
1.2 方法
1.2.1C组
C组45例患者实施常规护理,主要包括体征持续监测、基础生理护理、呼吸道护理、心理调适等。
1.2.2C+Y组
C+Y组45例患者在C组的基础上联合开展炎症反应源控制护理,具体干预措施:(1)成立炎症反应源控制小组:由管床医生、护士长、责任护士等共同组成护理小组,负责开展炎症反应源控制的统筹规划。(2)炎症反应源识别:从提高患者抗炎效果入手,以循证医学理念为路径,结合临床护理工作经验,准确识别重症肺炎患者炎症反应源:①痰液坠积。呼吸道痰液中含有多种病原微生物和炎症细胞,重症肺炎患者呼吸道大量痰液的坠积是造成炎症持续发展及增加呼吸障碍的主要原因;②呼吸机相关肺炎。重症肺炎患者机械通气过程中气管内插管操作破坏了气道自然的防御机制,使病原体容易接种到下呼吸道而诱发感染,是加剧患者炎症反应及威胁预后的重要因素;③营养不良。重症肺炎患者合并营养不良时造成机体代谢功能障碍,造成机体分泌的脂肪因子从抗炎脂联素转变为促炎瘦素,使局部生成高浓度的促炎症介质,从而加剧机体炎症反应;④合并“三高”。高血压、高血糖、高血脂的合并发生造成血管内皮损伤,并导致机体微循环障碍,进而激活炎症通路,释放大量炎性因子,加剧机体炎症反应。(3)炎症反应源控制:①有效排痰。正确咳痰:指导患者取头低脚高位,将痰液引流入主气道;咳痰前进行5~6次深而慢的呼吸,以增加腹腔压力,让肺部达到最大程度的膨胀,将气道远端的分泌物有效排出,必要时开展吸痰护理。合理拍背:指导患者取半坐位,手掌呈空心状从下往上、由两侧向中间均匀且有节奏的叩击背部,还应根据炎症的部位调整体位,通过震动使肺、支气管内附着的痰液脱落;②预防呼吸机相关肺炎。加强呼吸机管路的清洁与消毒,将人工气道予以妥善固定,防止管道牵拉造成气管插管意外脱出而增加感染风险。同时,患者取仰卧位时将其床头提高30°~45°,增加肺顺应性,定期清理其口鼻内分泌物,防止胃内容物反流;③加强营养支持。根据患者营养状态评估结果,配制合理的营养结构,满足机体营养代谢所需。并在食物的选择上遵循高蛋白、低纤维素、高维生素的原则,保证患者摄入的食物富含维生素、蛋白质、微量元素、矿物质、膳食纤维等营养元素,提高患者营养水平;④调节“三高”。在调查患者疾病史的基础上,加强对患者血压、血糖、血脂的持续监测,从药物(遵医嘱)、作息、饮食、运动等方面提高患者“三高”控制效果,以改善机体微循环,提高血管内皮功能,降低机体炎症反应。
1.3 观察指标
1.3.1病情控制效果
于两组患者护理干预前后,从发热、气促、呼吸困难、咳嗽四项症状予以病情严重程度评分,各症状评分为0~6分,分值越高,提示症状越重。同时统计肺部感染 (CPIS)评分,最高分12分,分值越高,提示肺部感染越重[2]。
1.3.2血清炎症指标
于两组患者护理干预前后,分别采集血液标本,离心分离血清后检测炎症反应指标:降钙素原(PCT)、C反应蛋白(CRP)、白细胞介素-6(IL-6)。
1.3.3动脉血气
于两组患者护理干预前后,分别检测动脉血气指标:氧分压(PaO2)、二氧化碳分压(PaCO2)和氧合指数(OI)。
1.4 统计学方法
2 结果
2.1 病情控制效果
护理前两组患者症状评分、CPIS评分比较,差异无统计学意义(P>0.05);护理后C+Y组患者症状评分、CPIS评分均低于C组(P<0.05),见表2。
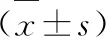
表2 C组和C+Y组患者病情控制效果比较
2.2 血清炎症指标
护理前两组患者血清PCT、CRP、IL-6比较,差异无统计学意义(P>0.05);护理后C+Y组患者血清PCT、CRP、IL-6均低于C组(P<0.05),见表3。
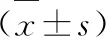
表3 C组和C+Y组患者护理前后血清PCT、CRP、IL-6比较
2.3 动脉血气指标
护理前两组PaO2、PCO2、OI比较,差异无统计学意义(P>0.05);护理后,C+Y组患者PaO2、OI均高于C组(P<0.05),PCO2低于C组(P<0.05),见表4。
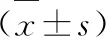
表4 C组和C+Y组患者护理前后PaO2、PaCO2、OI比较
3 讨论
据临床相关调查数据统计显示,过度炎症反应贯穿于重症肺炎病情进展的全过程,导致其病死率高达30%~50%,成为加重社会经济负担的重要疾病因素[3]。2020年,中华医学会呼吸病学分会强调,重症肺炎可由局部感染快速演变为全身多器官炎症反应,甚至感染性休克和多器官功能障碍综合征,因此针对机体炎症反应应激源,采取针对性的抗炎干预对改善重症肺炎患者预后具有重要的意义[4]。而临床上,机体炎症反应表现为复杂的、相互关联的循环网络,各种炎性介质、致炎因子、免疫功能、营养水平等均是该网络的重要调控元素,因此炎症反应控制的关键在于分析重症肺炎病生理机制的基础上,准确识别各种炎症反应源,并采取多途径的炎症干预措施,恢复炎症损伤与免疫调节之间的动态平衡,改善机体过度炎症反应状态[5]。
本研究中,C组、C+Y组患者分别实施常规护理、常规护理+炎症反应源控制护理,研究结果显示:护理后,C+Y组患者症状评分、CPIS评分均低于C组(P<0.05),C+Y组患者血清PCT、CRP、IL-6均低于C组(P<0.05),即通过炎症反应源控制干预可有效提高机体炎症反应的控制效果,减轻肺部感染病情。其中,炎症反应源控制干预旨在通过评估患者病情,收集整理信息,掌握规律,预测趋势,正确识别导致重症肺炎患者炎症反应加剧的危险因素,从痰液坠积、呼吸机相关肺炎、营养不良及合并“三高等方面预计未来可能出现的问题,提前采取措施,采取针对性的炎症反应源控制护理,将可能发生的风险事件消除在萌芽状态中。首先,重症肺炎患者卧床时间长,导致肺底充血水肿,痰液引流不畅、细菌滋生繁殖而加剧炎症反应病情,且气道内大量痰液分泌易引起患者肺通气换气功能障碍,诱发呼吸衰竭,临床护理中通过有效排痰可有效预防痰液坠积性感染,且可有效抑制痰液中炎症细胞的沉积,提高抗生素药物对气道组织的穿透力度,提高药物的生物利用度,从而提高抗炎效果,更好的抑制气道炎症反应[6]。呼吸机相关性肺炎为重症肺炎机械通气患者临床常见的并发症类型,临床上重症肺炎患者机械通气时间长、应用糖皮质激素类药物等因素的影响,极易合并发生呼吸机相关肺炎,临床护理中通过其预防护理可有效降低该并发症的发生风险,避免炎症反应病情加剧。其次,临床上高达50%的重症肺炎患者合并营养不良,而营养不良是造成患者免疫功能下降及炎症病情进展的重要原因,临床护理中通过营养支持不仅可提高患者机体免疫功能,提高炎症抑制效果,且大量蛋白质的补充可发挥抗生素药物的载体功效,提高血药浓度,进而提高抗炎效果[7]。最后,国内外诸多前沿文献报道强调,高血压、高血糖、高血脂均具有促炎机制,持续性高血压、高血糖、高血脂会增加炎症因子表达,加剧炎症反应病情。临床护理中通过“三高”控制可有效改善机体微循环,增强抗炎效果[8]。
同时,本研究结果显示,护理后,C+Y组患者PaO2、OI均高于C组(P<0.05),PCO2低于C组(P<0.05),即通过炎症反应源控制干预可有效改善机体动脉血气。临床上,炎症反应作为身体免疫系统对于疾病或微生物感染的一种正常反应,循环血液中促炎症细胞因子浓度与血氧浓度密切相关,重症肺炎患者通过炎症反应源控制干预可有效改善机体炎症反应,进而提高血氧浓度,改善动脉血气指标。
综上所述,于重症肺炎患者临床护理中实施炎症反应源控制干预能有效提高患者机体炎症反应的控制效果,减轻肺部感染病情,改善临床症状和动脉血气,值得临床推广应用。