口服复方新诺明治疗新生儿耐药肠杆菌败血症9例病例系列报告
刘仕祺 杜 娟 杨子馨 李 耿 陈 璐 齐宇洁 黑明燕
近年来,随着新生儿救治水平的提高,极低甚至超低出生体重儿的存活率逐渐升高,这些患儿住院时间长、免疫功能低下,是发生院内感染的高危人群。同时,随着产前预防性抗菌药物的应用及NICU患儿广谱抗菌药物的应用,抗菌药物耐药的问题日益严峻[1]。新生儿发生广谱耐药菌感染时,其药敏结果提示可选用的抗菌药物种类非常有限,例如仅对黏菌素、磷霉素等敏感,而其他年龄阶段的患儿可选用的抗菌药物,对于新生儿而言则属于超说明书用药[2,3]。由于新生儿具有独特的生理学特点,成人的药代动力学研究结果不能作为新生儿用药的依据,超说明书用药的情况在新生儿科非常普遍。研究显示,即便会增加新生儿发生药物相关不良反应的风险,新生儿超说明书用药的比例仍然很高(38.0%~93.4%)[4,5],更多见于在NICU住院的早产儿。抗菌药物是早产儿最常见的超说明书用药[6]。
复方新诺明(SMZco)是磺胺甲恶唑(SMZ)与甲氧苄啶(TMP)的复方制剂,其中SMZ的药理作用是抑制细菌合成叶酸,从而使细菌无法实现自我复制,TMP则可加强SMZ的抗菌作用,因此SMZco抗菌谱较广。文献报道,SMZco对治疗某些细菌(如嗜麦芽窄食单胞菌、黄杆菌、洋葱伯克霍尔德氏菌、大肠埃希菌等[7-11])引起的新生儿感染有效。但因该药可与胆红素竞争白蛋白结合位点,说明书明确不建议在2月龄以下的婴儿中使用,因此新生儿科医生几乎不选择该药为新生儿经验性一线抗菌药物。同时,近十几年来随着SMZco耐药性的增加,其在儿科的应用也极大减少,仅占儿科用药的0.1%[12,13]。SMZco口服制剂的生物利用度高达90%[14]。
本文总结联合应用口服SMZco治疗新生儿耐药肠杆菌败血症的经验和临床疗效。
1 方法
1.1 纳入标准 通过医院药物管理系统,检索并申领同时符合以下条件的SMZco病历:①2018年1月至2021年6月在首都医科大学附属北京儿童医院(我院)新生儿中心住院、入院时日龄≤28 d或矫正胎龄≤44 周的患儿;②住院期间CRE败血症诊断明确(有明确的细菌感染临床表现+CRE培养阳性);③口服SMZco联合抗感染治疗。
1.2 排除标准 符合以下任1项的病例被排除:①医疗纠纷病例;②预防性口服SMZco(定义:预防机会性致病菌感染,每周口服3 d,暂停4 d)。
1.3 SMZco超说明书用药流程和方案 ①基于CRE败血症诊断明确且面对抗生素选择受限,②经新生儿医生、药师和儿科感染科会诊,认为应用SMZco获益明显,不良反应可控,向患儿家长建议予口服SMZco联合抗感染治疗;③患儿家长接受医生建议,签署超说明书用药知情同意书;④SMZco片剂的规格为每片0.48 g(含SMZ 0.4 g,TMP 0.08 g); ⑤参考>2月龄儿童SMZco推荐剂量,SMZ 20~30 mg·kg-1、TMP 4~6 mg·kg-1,q 12 h,根据患儿病情决定疗程;⑥观察用药期间过敏反应、胆红素脑病表现,每周监测血常规和肝肾功能。
1.4 伦理 本文总结的病例报告经我院伦理委员会批准(2021-E-191-R)。
1.5 临床资料采集 通过医院电子病历系统采集符合本文纳入和排除标准的婴儿的临床资料:性别,胎龄,出生体重,入院日龄/纠正胎龄、主要诊断,手术情况、深静脉置管(PICC,CVC,UVC,PORT,临时透析导管、隧道式中心静脉导管)史,有创通气时间,临床表现(出现肠杆菌感染时的临床症状),口服SMZco前抗生素应用时间,是否延长美罗培南输注时间(超出美罗培南药代动力学建议用药时间以外的时间),中枢神经系统(CNS)感染[15][①CSF的WBC≥20个/mm3、蛋白>1.7 g·L-1(足月儿)、葡萄糖<2.2 mmol·L-1或低于当时血糖的40%;②CSF培养阳性],标本类型,培养阳性时间(从入我院至阳性培养结果出现时间),菌种,药敏试验(哌拉西林/他唑巴坦、头孢哌酮/舒巴坦、氨苄西林、头孢唑林、厄他培南、头孢吡肟、氨曲南、阿米卡星、庆大霉素、环丙沙星、美罗培南、头孢呋辛、氯霉素、SMZco、四环素、替加环素),耐药情况(耐药、敏感、中介),口服SMZco前后WBC、PLT和CRP,口服SMZco时日龄、矫正胎龄、剂量,口服SMZco起止时间,联合用药的名称和种类。用药后出现肝功能损害、肾功能损害、过敏反应、新生儿核黄疸、溶血性贫血、PLT减少等不良反应。根据患儿出院时转归情况分为治愈(包括好转)及未愈(包括因病情危重放弃治疗)。
1.6 统计学方法 应用SPSS 22.0统计软件进行数据分析。计数资料以例数表示,正态分布的计量资料以xˉ±s表示,非正态分布的计量资料以M(Q1,Q3)表示。
2 结果
2.1 一般情况 符合本文纳入和排除标准的病历12例,排除3例因存在原发或继发免疫缺陷,出院时医嘱预防应用SMZco。表1显示,9例应用SMZco的婴儿中,男5例,女4例;入我院时8例为早产儿,平均胎龄为(31.0±4.4)周;6例住院期间曾接受手术治疗,其中腹部手术4例、心脏外科手术1例、心脏外科手术联合腹部手术1例;8例有深静脉置管史;机械通气时间(793±381)h;3例在美罗培南基础上应用SMZco,在美罗培南/利奈唑胺和头孢曲松基础上应用SMZco各1例,4例单独应用SMZco;标本类型:单纯痰3例,单纯血2例,PICC管端、伤口分泌物各1例,血+痰和血+脑脊液各1例。

表1 9例耐药肠杆菌感染新生儿一般资料及病原学结果
9例均接受静脉广谱抗菌药物治疗17~68 (31.6±16.4)d,5例延长美罗培南输注时间,感染依然不能有效控制(临床症状不改善,且血炎症指标不好转或进一步升高); 2例符合CNS感染诊断。
2.2 药物敏感试验 表1显示,9例婴儿入院第39(23.5,49)d(矫正胎龄33~48+6周)均出现耐药菌阳性培养结果,其中6例婴儿CRE败血症均发生在术后;8例培养为肺炎克雷伯菌,1例为大肠埃希菌,均能产生超广谱β-内酰胺酶(ESBL),对碳青霉烯类抗菌药物耐药;对哌拉西林/他唑巴坦、头孢哌酮/舒巴坦氨苄西林、头孢唑林、厄他培南、头孢吡肟、氨曲南、美罗培南和头孢呋辛耐药,对阿米卡星耐药3例、敏感6例,对庆大霉素耐药5例、敏感4例,对环丙沙星耐药6例、敏感3例,对氯霉素中介2例、敏感7例,对四环素耐药3例、敏感5例、中介1例,对SMZco和替加环素均敏感。
2.3 SMZco 应用 表2显示,SMZco 应用前血CRP明显升高7例,WBC异常6例、PLT减少5例;口服SMZco日龄为49(38,70.5)d;3例为序贯口服SMZco;6例为联合碳青霉烯类或三代头孢菌素治疗,5例合并PLT减少,感染程度重;SMZco的剂量以SMZ含量计,为40~60 mg·kg-1·d-1,给药途径为口服。

表2 9例耐药肠杆菌感染新生儿的药敏结果
2.4 SMZco治疗疗程及疾病转归 表3显示,3例自动出院未完成疗程;6例应用SMZco(24.3±11.6)d,其中1例病原标本为深部痰者SMZco应用10 d,另5例均>2周;临床症状均改善,用药后WBC、PLT均恢复正常,7例CRP降至正常,2例自动出院前CRP亦明显下降。4例血培养阳性的婴儿中,1例自动出院,3例治疗后血培养均为阴性。例7自动出院后电话随访,在院外继续口服SMZco治疗,出院3个月后门诊复查血常规正常,脑脊液细胞数明显下降。
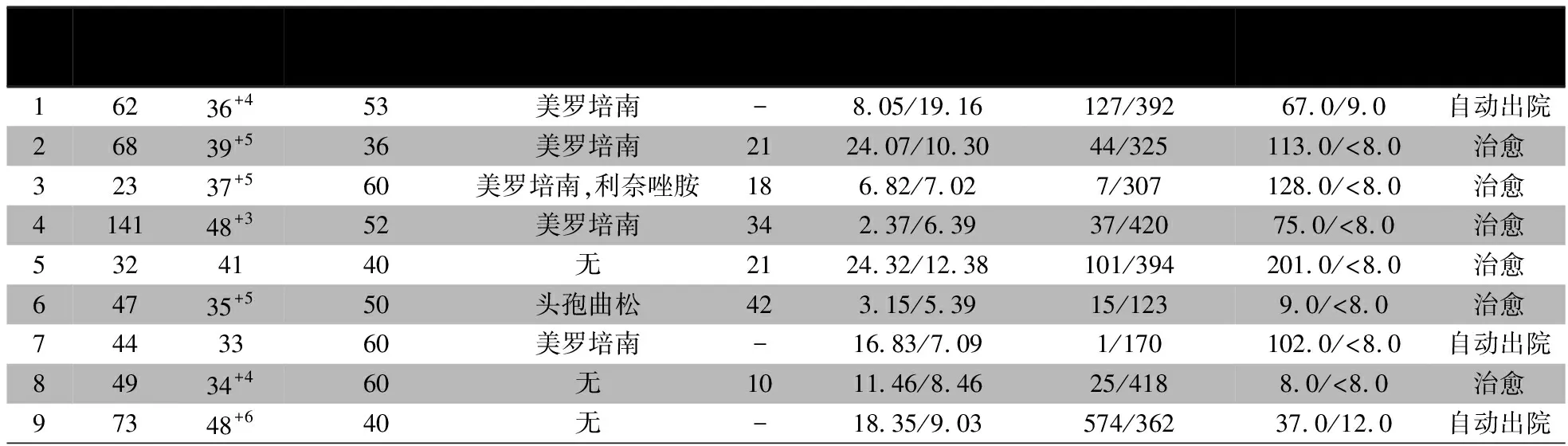
表3 9例耐药肠杆菌感染新生儿应用SMZco治疗情况
2.5 SMZco治疗不良反应 9例SMZco用药期间均未发生过敏反应,无胆红素脑病表现,未出现溶血性贫血、PLT减少,3例仅ALT有2.2~3.5倍的升高,对症治疗后均降至正常,肾功能均正常。
3 讨论
本文总结了9例诊断明确的CRE败血症患儿(明确的细菌感染临床表现+培养阳性)口服SMZco联合抗感染治疗的经验,这些患儿均在新生儿期起病、重症感染入住NICU,均经强广谱抗生素静脉用药治疗仍不能取得满意疗效,面对抗生素选择困难,根据药敏结果、经团队讨论后选择口服SMZco治疗,7例取得了较为满意的临床效果。9例用药期间均未发生过敏反应,无胆红素脑病表现,肾功能均正常,有3例ALT 2.2~3.5倍升高,对症治疗后均降至正常,余未观察到严重的药物不良反应。2例自动出院后临床结局不明。因此,本文9例患儿虽然超SMZco说明书用药,但取得风险与获益的平衡。需要说明的是,仅是病例报告,不足以得出SMZco在新生儿或小婴儿的疗效和安全性的结论,临床选择应当慎重。
肠杆菌(如大肠埃希菌、肺炎克雷伯菌)是新生儿,尤其是早产儿院内感染的常见病原,对早产儿治疗及预后有重要影响[16]。肠杆菌通过基因突变,产生各种β内酰胺酶,如NDM-1、NDM-5等,抑制抗菌药物的活性,从而出现多重耐药[17]。碳青霉烯类药物曾被认为是耐药的革兰阴性杆菌引起严重感染的最后选择[18],但随着其在NICU的广泛应用,碳青霉烯类耐药的细菌感染逐渐成为一个棘手的问题。一项国内儿童专科医院的结果显示,肠杆菌中碳青霉烯耐药株的检出率达27.1%[19]。治疗CRE感染,成人较多应用黏菌素或替加环素,但其可能有肾脏毒性,且在新生儿中因无相关药代动力学结果而应用受限[16]。
SMZco通过抑制叶酸代谢达到抑制细菌生长繁殖的作用,体外药敏试验提示其对CRE具有较好的抑制作用。本研究中88.9%为早产儿,且以极低/超低出生体重儿为主,住院时间均>4周,为SMZco应用的潜在高危人群。9例患儿中,5例为血流相关感染,3例为机械通气下肺部感染,1例为伤口感染,均伴有炎症指标的异常,病原学检查提示均为ESBL阳性的CRE感染,药敏结果提示SMZco具有一定的抗菌疗效。病原学依据为SMZco应用的必备实验室依据。本研究中,患儿足量应用美罗培南治疗>2周,临床症状(包括感染症状、需呼吸支持程度)及实验室指标无好转,规范应用碳青霉烯类抗菌药物治疗效果欠佳,亦是应用SMZco治疗的重要依据。因而,在新生儿,尤其是极低、超低出生体重儿中,住院时间>4周,出现明确CRE感染,尤其是血流相关或肺部感染,在足量、规律应用一线经验性抗感染治疗后,临床症状、实验室指标或培养结果无明显好转时,与家长进行充分沟通并取得知情同意,由临床医生和药师共同决定,作为应用SMZco的主要适应证和依据。
对于>2月龄的儿童,SMZco推荐剂量为每次SMZ 20~30 mg·kg-1、TMP 4~6 mg·kg-1q 12 h。有病理报告显示,对于耐药菌感染的早产儿,受组织浓度的影响,建议提高SMZco的用量[20]。本文SMZco口服剂量均依据2月龄以上儿童的推荐剂量,3例为单独用药,其他均联合美罗培南或三代头孢治疗,均显示了较好的疗效,未出现因重症感染死亡的病例。目前,CRE治疗时采用单一用药还是联合碳青霉烯类药物,尚存在争议[16],本文单独应用SMZco的3例患儿,临床表现相对较轻,且培养阳性的标本为痰液及伤口分泌物,血培养均为阴性。对于临床症状重、明确存在败血症或化脓性脑膜炎的患儿,本研究中仍联合应用了碳青霉烯类抗菌药物,并采取调整剂量及延长输注时间的方法增加其抗感染效果。目前,尚无SMZco在新生儿中应用的疗程推荐,本文除1例痰培养为肺炎克雷伯菌感染的患儿应用10 d,其他患儿疗程均>2周,主要取决于临床症状及感染部位。SMZco说明书中的适应证较多应用于呼吸道、泌尿系感染,本文例7为肺炎克雷伯菌感染引起的化脓性脑膜炎患儿,经SMZco治疗10 d,体温好转,家长自动出院后继续口服SMZco,随访发现炎症指标及脑脊液均明显好转。文献报道1例脑膜炎脓毒性黄杆菌感染引起的早产儿化脓性脑膜炎,经SMZco 3周治疗后治愈,一定程度上反映了其在CNS感染中的应用价值[7]。
SMZco因其在新生儿中潜在的不良反应,如核黄疸、过敏反应、溶血性贫血、肝肾功能损害等,使其在NICU的应用受限。本文观察到轻度肝酶升高3例,予对症治疗后很快降至正常。既往认为,磺胺类药物可以将胆红素从血浆中的白蛋白结合位点移除,导致血浆胆红素升高,从而穿过血脑屏障,到达中枢神经元引起核黄疸,是其在2月龄以下新生儿禁用的主要原因。本文9例患儿均未出现胆红素脑病表现,可能与这些患儿虽为早产儿,但在应用SMZco时日龄均较大、血胆红素水平普遍较低有关。1篇纳入9项口服SMZco治疗新生儿肺炎或败血症研究的综述中,未发现包括神经系统毒性在内的明确不良反应[21]。
本研究局限性:①作为疗效研究,本文为病例系列报告,且仅为出院时结局,缺少远期随访结局;②应用SMZco的日龄均超过了新生儿期,并不能代表在新生儿期使用的经验;③本文未探讨不同的SMZco联合或序贯转换用药策略之间的差异,本文结果仅提示根据患儿全身症状、已接受的抗菌药物治疗效果、其他可选药物种类、是否存在混合感染等因素进行充分的利弊权衡,并遵守正规的超说明书用药和家长书面知情告知流程。
综上所述,对于有明确培养和药敏结果的新生儿CRE感染,在充分应用强广谱抗生素治疗仍不能取得满意疗效的情况下,可考虑联合口服SMZco抗感染治疗,但需严格遵守超说明书用药和家长书面知情告知流程,密切监测不良反应。
致谢感谢我院药剂科、病案室的同行在药物作用机制、电子病历信息收集等方面对本研究的大力支持。

