胃食管反流病对慢性阻塞性肺疾病患者生活质量及肺功能的影响
李 瑛,陈张琴
(陕西省第二人民医院呼吸与危重症医学科,陕西 西安 710005)
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)发病率、病死率高,病情迁延呈持续进展,对患者生活质量有一定影响[1]。2018年由王辰院士牵头的中国肺健康研究是一项全国性的横断面研究,结果显示在中国40岁以上人群中COPD比例正在上升,从2007年的8.2%上升为13.7%[2-3]。COPD急性加重(Acute exacerbation of chronic obstructive pulmonary disease,AECOPD)使患者生活质量下降,肺功能恶化,经济负担与死亡风险增加。AECOPD的病因多与感染或环境有关,但有30%找不到原因。研究[4-6]显示,胃食管反流病(Gastroesophageal reflux disease,GERD)在COPD患者中发生率高,食管症状比其他内科疾病患者更普遍,症状更严重。GERD主要表现为烧心及反流[7]。诊断GERD的主要方式有症状、24 h食管pH监测、质子泵抑制剂诊断性试验、胃镜等。虽然超声、高分辨率放大内镜、染色内镜、内镜窄带成像、阻抗-pH监测等为GERD的诊断提供了更多选择,但目前还没有统一的国际诊断标准,总体而言诊断更倾向于以症状为主。研究[8-9]发现,COPD患者合并GERD时会更频繁地急性发作,生活质量更差,但其因果关系尚不明确,可能与既往研究对GERD诊断的方法缺乏统一标准有关。本研究采用胃食管反流病问卷(GerdQ)[10]的方法作为GERD的诊断标准,分析GERD对COPD患者生活质量及肺功能的影响。
1 对象与方法
1.1 研究对象 本研究在陕西省第二人民医院医学伦理委员会审核通过后进行。选取2019年1月至2020年1月就诊于陕西省第二人民医院呼吸科的AECOPD患者120例为研究对象。所有患者均由专人指导进行GerdQ问卷调查,按照是否合并GERD为GERD组(57例,GerdQ评分≥8分)和非GERD组(63例,GerdQ评分<8分)。病例纳入标准:符合2018年COPD全球倡议(GOLD)定义中的相关诊断标准;签署知情同意书。排除标准:合并肺结核、支气管扩张或其他肺部疾病者;合并严重心脑血管疾病、免疫系统疾病者;合并消化系统其他疾病者;有肺或消化道手术史者;服用质子泵抑制剂、H2受体拮抗剂或其他消化系统疾病相关药物者;肺功能检查无法配合者;无法完成圣乔治呼吸问卷(SGRQ)及GerdQ问卷者;未签署知情同意书者。
1.2 研究方法
1.2.1 资料收集:记录两组患者的一般资料,包括年龄、性别、吸烟指数以及体重指数(BMI)。
1.2.2 SGRQ问卷调查:待患者进入稳定期后开始SGRQ问卷调查,内容包括症状、活动能力、疾病影响三个方面。采用加权平均方法来计算分数。每部分的每个问题需根据以往研究、经验和统计学处理后得到一个权重,权重高则分值大,最后得出总分,范围在0~100分。分数越高说明生活质量越差。不论是单项得分还是总和得分,分值波动在4以上即有临床意义。
1.2.3 肺功能指标检测:待患者进入稳定期后,使用德国Jaeger肺功能仪对所有患者进行检测,指标包括第一秒用力呼气容积(FEV1)、FEV1与用力肺活量(FVC)比值(FEV1/FVC)以及第一秒用力呼气容积占预计值百分比(FEV1%pred)。至少进行3次检测,质量要求符合A级或者B级,取最好的一次结果作为测定值。
1.2.4 COPD急性加重情况:所有入组患者均每2个月随访1次,共随访1年。记录1年内AECOPD发生次数。

2 结 果
2.1 两组患者一般资料比较 见表1。两组患者性别、年龄、吸烟指数、BMI比较,差异无统计学意义(均P>0.05)。
2.2 两组患者SGRQ评分比较 见表2。GERD组SGRQ问卷中症状、活动能力、疾病影响单项评分及总评分高于非GERD组(均P<0.05)。

表1 两组患者一般资料比较

表2 两组患者SGRQ评分比较(分)
2.3 两组患者肺功能指标比较 见表3。GERD组FEV1、FEV1/FVC及FEV1%pred低于非GERD组(均P<0.05)。
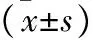
表3 两组患者肺功能指标比较
2.4 两组患者AECOPD发作次数比较 随访1年内,GERD组AECOPD发作(3.46±0.14)次,非GERD组发作(1.97±0.16)次,GERD组AECOPD发作次数多于非GERD组(t=66.460,P=0.0048)。
3 讨 论
中国COPD患者已经接近1亿人,这相当于40岁以上人群中每8个人中就有1例COPD[11]。COPD可导致心功能不全、骨质疏松、骨骼肌萎缩等肺外表现,严重危害患者健康[12-13]。目前,COPD的肺外表现与疾病严重程度及预后的相关性越来越受到重视。AECOPD常会导致疾病进展,加剧患者肺功能障碍,降低患者生活质量[14]。因此,为减慢肺功能下降,就要预防和减少AECOPD发作次数。导致AECOPD的因素常常与感染及环境等有关[15],但其中有30%是不明原因的[16]。
近年来,有多项研究表明COPD和胃食管反流病相关[17-20],COPD合并GERD的发生率为17%~78%[21-22]。早在2017年GOLD指南就已经明确说明,COPD合并GERD会导致患者AECOPD发作风险增高,健康状况恶化[23-24]。Sakae等[25]研究发现,26.6%的COPD患者白天和(或)夜间有GERD症状。然而,它们之间潜在的相互作用机制并不十分明确。研究[26-27]发现,COPD患者的食管蠕动功能降低,食管上括约肌压力降低,气道阻塞,胸腔内负压增高,肺内气体潴留导致膈肌低平,同时削弱了抗反流的屏障,使得反流加重。但也有研究[28]表明,对COPD患者行24 h动态试管内耐酸碱(pH)试验未发现二者间的相关性。这种结果的差异可能与GERD入组及诊断标准不同有关;部分研究甚至尚未提及采用何种方法诊断GERD。目前越来越多的研究证实GERD与COPD具有相关性,然而COPD合并GERD诊断至今仍没有统一标准。采用GerdQ 问卷诊断GERD与AECOPD发作相关性的研究甚少。
本研究采用GerdQ问卷作为GRED诊断标准,分析GERD对COPD患者生活质量及肺功能的影响。所有患者均在AECOPD发作控制、病情平稳进入稳定期后行SGRQ问卷调查及肺功能检查,以评估患者的生活质量及肺功能基础情况。结果显示: GERD组患者FEV1、FEV1/FVC、FEV1%pred和SGRQ评分与非GERD组患者比较差异均有统计学意义,GERD组患者肺功能及生活质量更差;随访1年,GERD组AECOPD发作次数多于非GERD组。GERD不仅加重COPD患者的症状,也极有可能是AECOPD的诱因之一。同时,COPD也会引起GERD,它们互为因果,形成恶性循环,加重了疾病的进展。在今后的COPD防治工作中,对于合并GERD的COPD患者,也许可以通过治疗GERD来减少AECOPD的诱发因素。
综上所述,与不合并GERD的COPD患者相比,合并GERD的COPD患者SGRQ评分更高,肺功能(FEV1、FEV1/FVC、FEV1%pred)更差,急性发作次数更多。但本研究入组患者数量有限,研究的时间周期也较短,存在一定的局限性,后期有必要扩大样本量并延长研究时间对上述结果进行证实。

