大蒜预处理对液体黑蒜保健功能的影响
贾庆超,梁艳美
(1.郑州科技学院 食品科学与工程学院,郑州 450064;2.安阳工学院 计算机科学与信息工程学院,河南 安阳 455000)
大蒜是葱科葱属植物中一种十分有效的功能性食品原料[1],性温味辛,常被人们誉为“天然的抗生素”,医学研究表明[2],大蒜在心血管疾病、感染性疾病、肿瘤及糖尿病等的预防与治疗方面具有活性作用。黑蒜又称为发酵黑蒜,目前发酵黑蒜主要是固态发酵,液体发酵研究较少,黑蒜是将普通新鲜大蒜在发酵箱中发酵2~3个月而成,是一种酸甜可口、毫无酸臭味的保健食品。在发酵过程中,大蒜组织会被破坏,主要发生美拉德反应[3],发酵后期还会有部分的酶促褐变,发酵黑蒜不仅保留了普通大蒜原有的营养物质,而且其含有的营养成分都比普通大蒜增加了很多,抗氧化性也得到了显著提高,并且在降血糖、降血压、降血脂等方面也具有特殊生理功效[4-5]。有研究表明,黑蒜具有防治癌症、促进糖尿病人体质恢复、防治流感、增强免疫力、抗疲劳、抗衰老、防血栓等明显功效[6-7]。目前,对于液体发酵黑蒜的研究鲜少,同时,也并没有将研究重心放在美拉德反应的影响因素上[8-9]。美拉德反应对黑蒜的风味、色泽、营养、安全等方面有重要的影响[10-11],而pH值是影响美拉德反应的主要因素,目前尚没有通过改变大蒜发酵前的pH值来探索发酵黑蒜的保健指标的报道,本文首先在液体大蒜发酵前,加入一定量的食品级柠檬酸和柠檬酸钠,研究其pH值的改变情况,然后研究pH值降低、pH值升高及pH值不改变的情况下,液态黑蒜发酵过程中超氧化物歧化酶(SOD)活性[12]、总酚含量[13]和可溶性糖含量[14]的变化情况,探究pH值对美拉德反应的影响以及对黑蒜抗氧化活性的影响[15],得出大蒜最佳预处理方式和黑蒜保健性能最好的状态。本试验的开展不但弥补了液体发酵黑蒜这一部分的研究空缺,同时也为液态黑蒜的发酵研究提供了有力的数据参考和支持。
1 材料与方法
1.1 材料与试剂
新鲜大蒜:市购;柠檬酸、柠檬酸钠(食品级):潍坊英轩实业有限公司;Tris、福林酚1 mol/L:福州飞净生物科技有限公司;EDTA-2Na、Na2HPO4·12H2O:天津市天力化学试剂有限公司;NaH2PO4·2H2O、无水乙醇:天津市致远化学试剂有限公司;焦性没食子酸、没食子酸:天津市科密欧化学试剂有限公司;无水碳酸钠:郑州派尼化学试剂厂;苯酚:上海展云化工有限公司;浓硫酸、浓盐酸:洛阳昊华化学试剂有限公司;蔗糖:天津市恒兴化学试剂制造有限公司,以上试剂均为分析纯。
1.2 仪器与设备
FA1004 Bsartorius电子天平 赛多利斯公司;PXSJ-216离子分析仪 上海仪点科学仪器股份有限公司;恒温发酵箱 上海科恒实业发展有限公司;Anke TDL-50B离心机 上海安亭科学仪器厂;电热恒温水温箱、电子万用炉 北京市永光明医疗仪器有限公司;KQ5200B机械型超声波清洗器 上海合金超声设备有限公司;UV-4802H紫外分光光度计 尤尼柯仪器有限公司。
1.3 试验方法
1.3.1 液体黑蒜发酵工艺流程
选取新鲜大蒜→去皮→清洗→去根蒂→蒜瓣破碎[16]→装罐→加水→加辅料(柠檬酸、柠檬酸钠)→85 ℃恒温发酵→成品。
1.3.2 柠檬酸和柠檬酸钠对液体大蒜pH值的影响
由于大蒜发酵成黑蒜的过程中发生了美拉德反应,而pH值、温度、浓度是影响美拉德反应的主要因素,本试验中,通过加入食品级柠檬酸和柠檬酸钠来改变发酵前不同料液比的pH值,降低和升高一个pH值,来探究发酵液体黑蒜最佳的大蒜预处理方式。
操作步骤:制备破碎粒度为2 mm,料液质量比为4∶1的蒜汁,混合均匀,过滤取蒜汁2 mL,加入28 mL水,用玻璃棒搅拌均匀后,用离子分析仪测其pH值,记为pH1,可求得料液质量比为4∶1时的原始pH值,记为pH2。在料液质量比为4∶1的蒜汁中加入一定量的食品级柠檬酸,使pH2降低一个数(如从pH 6降到pH 5),记为pH3;在料液质量比为4∶1的蒜汁中加入一定量的食品级柠檬酸钠,使pH2增大一个pH值(如从pH 5升到pH 6),记为pH3。其他不同料液质量比同理。
通过数据分析,得出不同料液质量比的蒜汁降低一个pH值所加入的柠檬酸和柠檬酸钠的量以及升高一个pH值所加入的柠檬酸和柠檬酸钠的量。
1.3.3 pH值的影响
在不同比例的料液质量比发酵原液中,分别加入一定量的柠檬酸和柠檬酸钠,改变发酵液体的pH值。在料液质量比为4∶1的液体蒜泥中分别加入0.06 g柠檬酸和4.5 g柠檬酸钠;在料液质量比为4∶2的 液体蒜泥中分别加入0.05 g柠檬酸和3.0 g柠檬酸钠;在料液质量比为4∶3的液体蒜泥中分别加入0.04 g柠檬酸和1.5 g柠檬酸钠;在料液质量比为4∶4的液体蒜泥中分别加入0.02 g柠檬酸和0.8 g柠檬酸钠;装罐密封,一同放入85 ℃发酵箱中进行恒温发酵。每隔3 d定时取一定量发酵物,测定其超氧化物歧化酶(SOD)活性、总酚含量和可溶性糖含量,来探讨发酵pH值对液体发酵黑蒜的影响。
1.3.4 料液质量比的影响
将破碎粒度为2 mm的新鲜大蒜蒜泥,按照料液质量比为4∶1、4∶2、4∶3、4∶4配制不同的发酵原液,放入85 ℃发酵箱中进行恒温发酵。每隔3 d取一定量发酵物,测定其超氧化物歧化酶(SOD)活性、总酚含量和可溶性糖含量,来探讨料液质量比对液体发酵黑蒜的影响。
1.3.5 破碎粒度的影响
当料液质量比为4∶2时,将破碎粒度为1,2,4 mm的新鲜大蒜蒜泥装罐密封,一同放入85 ℃的恒温发酵箱中,每隔3 d定时取一定量发酵物,测定其超氧化物歧化酶(SOD)活性、总酚含量和可溶性糖含量,来探讨破碎粒度对液体发酵黑蒜的影响。
1.3.6 理化指标的测定
1.3.6.1 超氧化物歧化酶(SOD)活性的测定
采用邻苯三酚自氧化法[17]测定超氧化物歧化酶(SOD)活性。
邻苯三酚自氧化速率的测定:在比色管中依次加入0.1 mol/L Tris-HCl缓冲液4.5 mL和蒸馏水4.2 mL,在25 ℃条件下水浴保温20 min后,加入25 ℃预热过的0.1 mol/L邻苯三酚0.3 mL(对照管用0.1 mol/L盐酸代替),迅速摇匀后,在λ=325 nm处每隔0.5 min测定一次吸光度值A0,共测4 min。测定邻苯三酚自氧化速率ΔA0,平行测3次,取平均值。
称取液体发酵黑蒜4 g,放置于研钵中研磨1 min,加入12 mL 0.05 mol/L 磷酸缓冲溶液,继续研磨3 min后,在60 ℃条件下水浴保温20 min,冷却后用4层纱布过滤,滤液在3000 r/min下离心20 min,取1 mL上清液,稀释5倍后待测。
样液的测定:取1 mL样品液,3.2 mL水,在25 ℃下水浴保温20 min后,加入0.3 mL 25 ℃预热过的0.1 mol/L邻苯三酚(对照共加4.2 mL水),迅速摇匀,立即倾入比色皿中,在波长325 nm处每隔0.5 min测定一次吸光度值A1,共测4 min。测定加样后自氧化速率ΔA1,平行测3次,取平均值。
式中:V1为反应体积(mL);V2为样液体积(mL);D为样液稀释倍数;m为样品质量(g)。
1.3.6.2 总酚含量的测定
采用Folin-Ciocalteu法[18-19]测定总酚含量。
配制标准液:准确称取没食子酸标准样品0.005 g, 用蒸馏水溶解后定容至50 mL容量瓶中,得到浓度为0.1 mg/mL标准液。
建立标准曲线:分别准确量取标准液0.2,0.4,0.6,0.8,1.0,1.2 mL于10 mL容量瓶中,加入6 mL水,摇匀后再加福林试剂0.5 mL。1 min后加入20%碳酸钠溶液1.5 mL,定容后立即混匀,75 ℃下水浴反应10 min,冷却后,于760 nm波长下比色,测定吸光度,建立标准曲线(y=94.893x+0.0096,R2=0.9996),标准曲线见图1。

图1 没食子酸标准曲线Fig.1 Standard curve of gallic acid
样品溶液的制备:用电子天平精确称取样品1.000 g放入50 mL锥形瓶中,加入70%乙醇25 mL,用超声波提取30 min,过滤,反复冲洗锥形瓶后定容至50 mL,准确用吸量管吸取2 mL样液于10 mL容量瓶中,用70%乙醇定容至刻度,待测。
样液的测定:用移液枪准确量取制备好的样品溶液1 mL于10 mL容量瓶中,加入6 mL蒸馏水、0.5 mL福林试剂和1.5 mL 20% Na2CO3溶液,用水定容至刻度,混匀,75 ℃水浴10 min,冷却,在λ=760 nm处测定吸光度。
1.3.6.3 液体发酵黑蒜中可溶性糖含量的测定
采用苯酚-硫酸法[20]测定可溶性糖含量。
糖在浓硫酸的作用下,会脱水生成糠醛或羟甲基糠醛,这两种物质均能与苯酚反应生成一种橙红色化合物,在0~100 μg的范围内反应颜色的深浅与糖含量成正比的关系,而且在λ=485 nm下有最大吸收峰,故可以通过比色法在此波长下进行物质中糖含量的测定。苯酚-硫酸法可用于测定甲基化的糖、戊糖和多聚糖,方法简单,灵敏度高[21],基本不受蛋白质存在的影响,而且产生的颜色能够稳定在3 h左右。
标准曲线的建立:在6支20 mL刻度试管中,分别准确加入0,0.2,0.4,0.6,0.8,1.0 mL 100 μg/mL的蔗糖溶液,依次加入2,1.8,1.6,1.4,1.2,1.0 mL蒸馏水,各加入9%苯酚溶液1 mL,摇匀后,依次加入浓硫酸5 mL,在室温下静置显色,待冷却后,以空白为参比溶液,测定各吸光度值。以糖含量为横坐标,吸光度为纵坐标,绘制其标准曲线(y=0.0054x+0.013,R2=0.9991),标准曲线见图2。

图2 蔗糖标准曲线
可溶性糖的提取(样液的制备):取样品0.3 g于试管中,加入水10 mL,封口后,沸水30 min,冷却后过滤,滤液入25 mL的容量瓶中,并反复冲洗试管壁及残渣并定容,此为样品待测液。
样品的测定:准确吸取0.5 mL样液于25 mL比色管中,加入水1.5 mL,再依次加入1 mL 9%苯酚溶液,摇匀后,沿试管壁缓慢加入5 mL浓硫酸,室温下显色,冷却后,以空白为参比,在λ=485 nm下测吸光度,根据标准曲线方程求出含糖量C。
式中:X为每100 g样品中糖含量(g/100 g);C为标准曲线上计算得含糖量(μg);D为稀释倍数;m为样品质量(g)。
2 结果分析
2.1 柠檬酸和柠檬酸钠对液体大蒜pH值的影响

图3 柠檬酸的量对不同料液质量比pH值的影响Fig.3 The effect of the amount of citric acid on the pHvalues with different solid-liquid mass ratios
由图3可知,当料液质量比为4∶4时,加入0.02 g的食品级柠檬酸可降低一个pH值;当料液质量比为4∶3时,加入0.04 g的食品级柠檬酸可降低一个pH值;当料液质量比为4∶2时,加入0.05 g的食品级柠檬酸可降低一个pH值;当料液质量比为4∶1时,加入0.06 g的食品级柠檬酸可降低一个pH值。

图4 柠檬酸钠的量对不同料液质量比pH值的影响 Fig.4 The effect of the amount of sodium citrate on the pH values with different solid-liquid mass ratios
由图4可知,当料液质量比为4∶4时,加入0.8 g的食品级柠檬酸钠可升高一个pH值;当料液质量比为4∶3时,加入1.5 g的食品级柠檬酸钠可升高一个pH值;当料液质量比为4∶2时,加入3.0 g的食品级柠檬酸钠可升高一个pH值;当料液质量比为4∶1时,加入4.5 g的食品级柠檬酸钠可升高一个pH值。

表1 不同料液质量比的发酵pH值Table 1 The fermentation pH values with different solid-liquid mass ratios
由表1可知通过加入柠檬酸和柠檬酸钠降低和升高一个pH值后不同料液质量比的具体pH值,可以得出本次试验探究的液体发酵黑蒜的发酵pH值范围为4.2~6.3。
2.2 pH值对液体发酵黑蒜理化指标的影响
2.2.1 pH值对液体发酵黑蒜SOD活性的影响
料液质量比为4∶1、4∶2、4∶3和4∶4时,pH值对液体发酵黑蒜SOD活性的影响见图5~图8。

图5 料液质量比为4∶1时pH值对液体发酵黑蒜SOD活性的影响Fig.5 The SOD activity of liquid fermented black garlic as solid-liquid mass ratio of 4∶1

图6 料液质量比为4∶2时pH值对液体发酵黑蒜SOD活性的影响
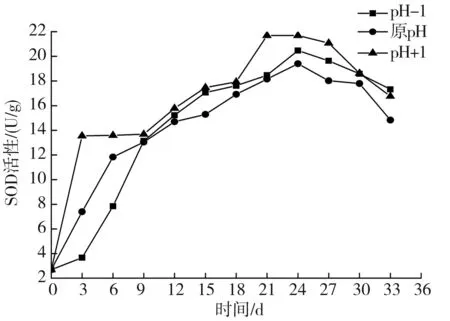
图7 料液质量比为4∶3时pH值对液体发酵黑蒜SOD活性的影响Fig.7 The SOD activity of liquid fermented black garlic as solid-liquid mass ratio of 4∶3
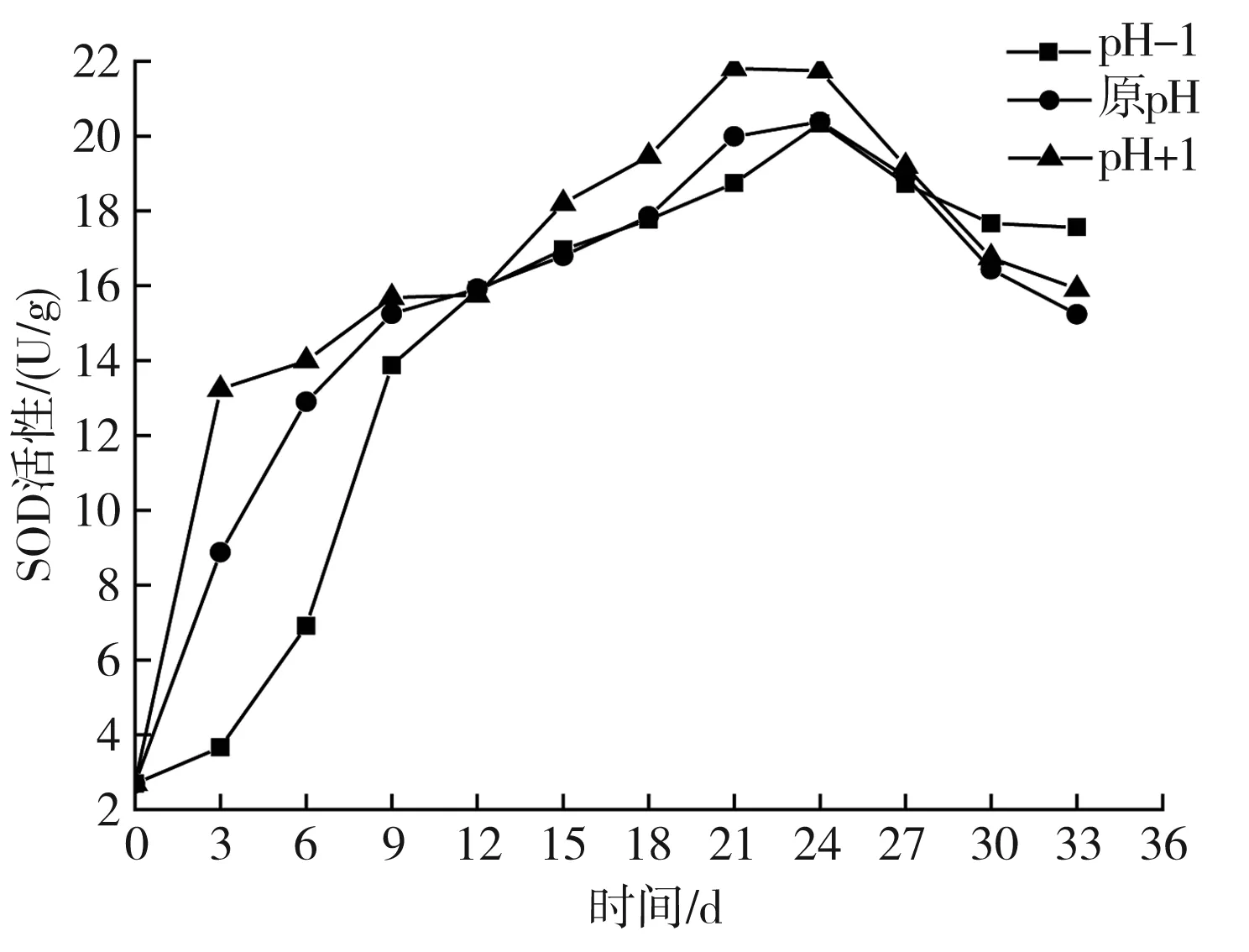
图8 料液质量比为4∶4时pH值对液体发酵黑蒜SOD活性的影响
由图5~图8可知,不同料液质量比时,pH值对SOD活性的影响都是先上升后降低。在发酵前期,pH-1的液体黑蒜SOD活性变化较大,原pH的液体黑蒜SOD活性变化亦较大,而pH+1时,液体黑蒜的SOD活性变化最小,但其SOD活性均高于低pH值时的SOD活性,尤其在发酵3 d时,pH+1的SOD活性明显高于其他pH值,9~18 d的发酵过程中,SOD活性相差不大。直到发酵20 d左右,pH+1的液体黑蒜SOD活性上升到了最大值,料液质量比为4∶1、4∶2、4∶3、4∶4的SOD活性分别为21.552,21.729,21.701,21.806 U/g。在发酵25 d左右,pH-1和原pH发酵的液体黑蒜其SOD活性逐渐达到最大值,最大值在20 U/g左右。
以上分析表明,pH值的升高对液体黑蒜SOD活性的升高有一定的促进作用,pH-1和原pH的液体黑蒜SOD活性均有一些上升,也可以看出,料液质量比对液体黑蒜SOD活性的影响不太显著,料液质量比为4∶4时,SOD活性值略高。同时,通过试验得出未发酵大蒜的SOD活性为2.694 U/g,当pH+1时,在发酵21 d左右,液体发酵黑蒜的SOD活性最高,与未发酵大蒜SOD活性相比提高了7~8倍。
2.2.2 pH值对液体发酵黑蒜总酚含量的影响
料液质量比为4∶1、4∶2、4∶3和4∶4时,pH值对液体发酵黑蒜总酚含量的影响见图9~图12。

图9 料液质量比为4∶1时pH值对液体发酵黑蒜总酚含量的影响Fig.9 The total phenol content of liquid fermented black garlic as solid-liquid mass ratio of 4∶1
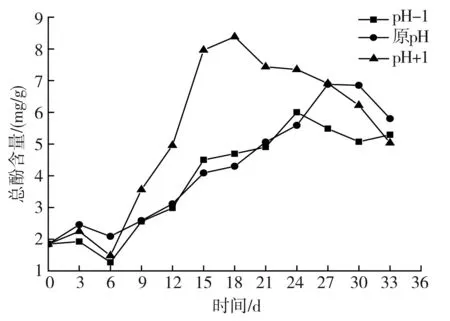
图10 料液质量比为4∶2时pH值对液体发酵黑蒜总酚含量的影响

图11 料液质量比为4∶3时pH值对液体发酵黑蒜总酚含量的影响Fig.11 The total phenol content of liquid fermented black garlic as solid-liquid mass ratio of 4∶3

图12 料液质量比为4∶4时pH值对液体发酵黑蒜总酚含量的影响
由图9~图12可知,4种不同料液质量比的液体黑蒜,pH值对总酚含量的影响基本都是先降低后上升再降低。在发酵前期,不同pH值的液体发酵黑蒜总酚含量变化不明显,基本均在3~6 d时总酚含量呈下降趋势,原因可能是大蒜中的酚类氧化酶未被完全激活。随着发酵过程中美拉德反应的进行以及酚类氧化酶的作用,pH+1时的液体黑蒜总酚含量变化最明显。在21 d左右,总酚含量能够达到最大值,料液质量比4∶1、4∶2、4∶3、4∶4的液体黑蒜总酚含量分别为10.860,8.383,7.344,5.378 mg/g,pH-1和原pH进行发酵的液体黑蒜,其总酚含量基本在27 d左右逐渐达到最大值,其值在4~7 mg/g。在发酵后期,总酚含量均呈现下降趋势,但变化并不明显,可能是因为达到了发酵成熟期,酚类物质可能发生了缩合反应,从而导致总酚含量出现下降趋势。
以上数据表明,升高pH值对液体黑蒜中总酚含量的升高有一定的促进作用,当料液质量比为4∶1时,总酚含量变化最大,并且随着液体黑蒜中水分的增多,总酚含量的最大值呈下降趋势。根据试验得出未发酵大蒜的总酚含量为1.844 mg/g,当pH+1时,在发酵18 d左右,液体黑蒜的总酚含量是未发酵大蒜的2.3~6倍。
2.2.3 pH值对液体发酵黑蒜可溶性糖含量的影响
料液质量比4∶1、4∶2、4∶3和4∶4时,pH值对液体发酵黑蒜可溶性糖含量的影响见图13~图16。

图13 料液质量比为4∶1时pH值对液体发酵黑蒜可溶性糖含量的影响Fig.13 The soluble sugar content of liquid fermented black garlic as solid-liquid mass ratio of 4∶1

图14 料液质量比为4∶2时pH值对液体发酵黑蒜可溶性糖含量的影响
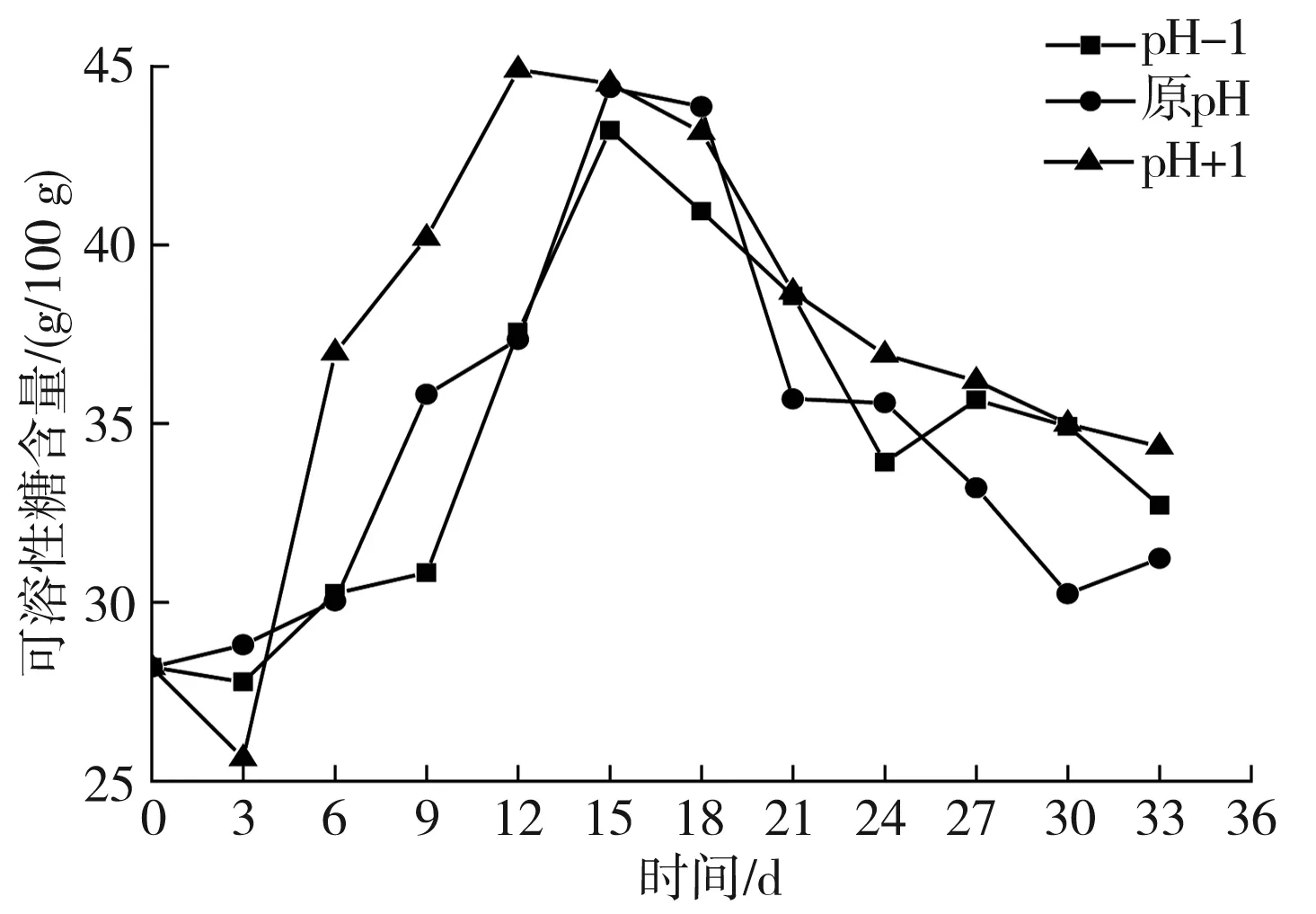
图15 料液质量比为4∶3时pH值对液体发酵黑蒜可溶性糖含量的影响Fig.15 The soluble sugar content of liquid fermented black garlic as solid-liquid mass ratio of 4∶3

图16 料液质量比为4∶4时pH值对液体发酵黑蒜可溶性糖含量的影响
由图13~图16可知,4种不同料液质量比的液体黑蒜,pH值对可溶性糖含量的影响基本均是先上升后降低。在发酵前期,可溶性糖含量会随着发酵时间的变化而迅速升高,这一现象可能是由于大蒜中的多聚糖开始分解为双糖和单糖,使黑蒜的甜度逐渐增加[22-24]。在发酵12 d左右,液体黑蒜的可溶性糖含量最高,可达到48 g/100 g左右,与未发酵大蒜比较,可溶性糖含量可增大32%,之后,液体黑蒜的可溶性糖含量开始呈现下降趋势,可能是因为美拉德反应最为剧烈,消耗的糖较多,在发酵21 d左右,可溶性糖含量开始缓慢下降,可能是由于随着发酵的进行,蒜样中的水分散失引起的。徐丽华等[25]的研究中,将新鲜大蒜置于高温高湿的环境中,25 d时黑蒜的糖含量较鲜蒜增加12.19%。
当料液质量比为4∶1时,在发酵12 d时,pH+1的液体黑蒜可溶性糖含量率先达到了最大值48.969 g/100 g,在20 d后,可溶性糖含量变化不大,与最大值相比下降了35%,而pH-1和原pH的液体黑蒜在发酵15 d时达到最大值,分别为43.217 g/100 g和44.207 g/100 g,在24 d左右,可溶性糖含量基本趋于稳定,与最大值相比均下降了24%;当料液质量比为4∶2时,在发酵12 d时,pH+1的液体黑蒜可溶性糖含量率先达到了最大值49.011 g/100 g,在20 d后,可溶性糖含量变化不大,与最大值相比下降了34%,而pH-1和原pH的液体黑蒜在发酵15 d时达到最大值,分别为43.928 g/100 g和44.425 g/100 g,在24 d左右,可溶性糖含量基本趋于稳定,与最大值相比下降了25%和30%;当料液质量比为4∶3和4∶4时,在发酵12 d时,pH+1的液体黑蒜可溶性糖含量率先达到了最大值,分别为44.899 g/100 g和43.811 g/100 g,在发酵20 d后,可溶性糖含量均变化不大,与各自最大值相比均下降了18%;当料液质量比为4∶3时,pH-1和原pH的液体黑蒜在发酵15 d时达到最大值,在24 d左右,可溶性糖含量基本趋于稳定,与最大值相比分别下降了24%和34%;当料液质量比为4∶4时,pH-1的液体黑蒜在发酵15 d时,可溶性糖含量达到最大值40.275 g/100 g,在24 d左右,可溶性糖含量基本趋于稳定,与最大值相比均下降了18%,原pH的液体黑蒜可溶性糖含量在9 d时达到最大值43.207 g/100 g,在24 d后,可溶性糖含量呈下降趋势,与最大值相比下降了30%。
以上数据得出,pH+1时,当料液质量比为4∶1和4∶2时,更有利于美拉德反应的发生,在发酵21 d左右,可溶性糖含量变化趋于稳定,表示液体黑蒜达到成熟期。
2.3 料液质量比对液体发酵黑蒜理化指标的影响
2.3.1 料液质量比对液体发酵黑蒜SOD活性的影响
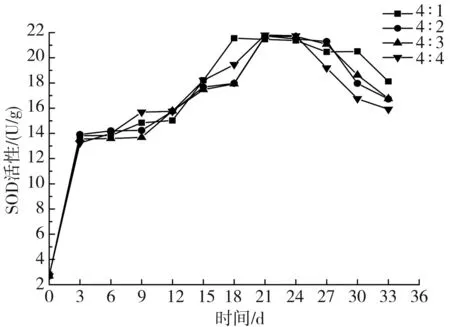
pH-1、原pH和pH+1时,不同料液质量比对液体发酵黑蒜SOD活性的影响见图17。

a

b
c
由图17可知,随着pH值的升高,料液质量比对液体黑蒜SOD活性的影响逐渐明显。在发酵前期,pH-1的液体黑蒜,料液质量比对其SOD活性的影响十分显著,原pH的液体黑蒜,料液质量比对其SOD活性的影响是先迅速升高后缓慢上升,pH+1的液体黑蒜,料液质量比对其SOD活性的影响是先缓慢上升后迅速升高,并且随着pH的升高,越早达到SOD活性最大值。pH-1时,在发酵24 d左右,料液质量比为4∶3、4∶4的液体黑蒜SOD活性最先达到最大值20.469,20.338 U/g,到27 d左右,料液质量比为4∶2、4∶1的液体黑蒜SOD活性达到了最大值19.497,20.964 U/g;原pH时,4种料液质量比的液体黑蒜SOD活性均在24 d达到了最大值,料液质量比从大到小分别为20.260,20.767,19.406,20.382 U/g;pH+1时,料液质量比为4∶1的黑蒜在18 d时SOD活性达到了最大值21.552 U/g,料液质量比为4∶2、4∶3、4∶4的黑蒜在21 d左右SOD活性达到了最大值,分别为21.729,21.701,21.745 U/g。
以上分析表明,不同pH值条件下,料液质量比为4∶1的液体黑蒜SOD活性相对较高,且达到最高值的时间相对较短,其中pH+1时,SOD活性值较其他pH值都略高。
2.3.2 料液质量比对液体发酵黑蒜总酚含量的影响
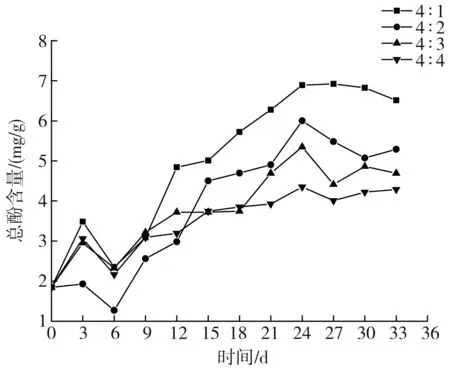
pH-1、原pH和pH+1时,不同料液质量比对液体发酵黑蒜总酚活性的影响见图18。
d

e

f
由图18可知,3种pH值的情况下,不同料液质量比的液体黑蒜随着发酵时间的增加对总酚含量的影响基本均呈先降低后增加再缓慢降低的趋势,并且料液质量比4∶1的液体发酵黑蒜的总酚含量均明显高于其他料液质量比,pH-1时,在发酵24 d时,不同料液质量比的液体黑蒜总酚含量均达到最大值,按料液质量比从大到小分别为6.922,6.002,5.348,4.352 mg/g;原pH的情况下,料液质量比为4∶1、4∶2、4∶3的液体黑蒜总酚含量在27 d达到最大值,分别为7.277,6.883,5.867,4.327 mg/g,料液质量比为4∶4的液体黑蒜在24 d达到最大值4.327 mg/g;pH+1的情况下,料液质量比为4∶1、4∶2、4∶3的液体黑蒜总酚含量在18 d达到最大值,分别为10.860,8.383,7.344,5.378 mg/g,料液质量比为4∶4的液体黑蒜在15 d达到最大值5.378 mg/g。唐仕荣等的研究结果中,固态发酵黑蒜的总酚含量在发酵30 d后达到最大值,仅为3.3 mg/g左右,说明料液质量比对液体黑蒜的抗氧化性有一定的促进作用。
以上分析可以得出,不同pH值条件下,料液质量比为4∶1时,液体黑蒜的总酚含量均最大,且随着料液质量比的减小,总酚含量的最大值也随之减小,但pH+1时,其总酚含量比其他pH值总酚含量均较高。
2.3.3 料液质量比对液体发酵黑蒜可溶性糖含量的影响
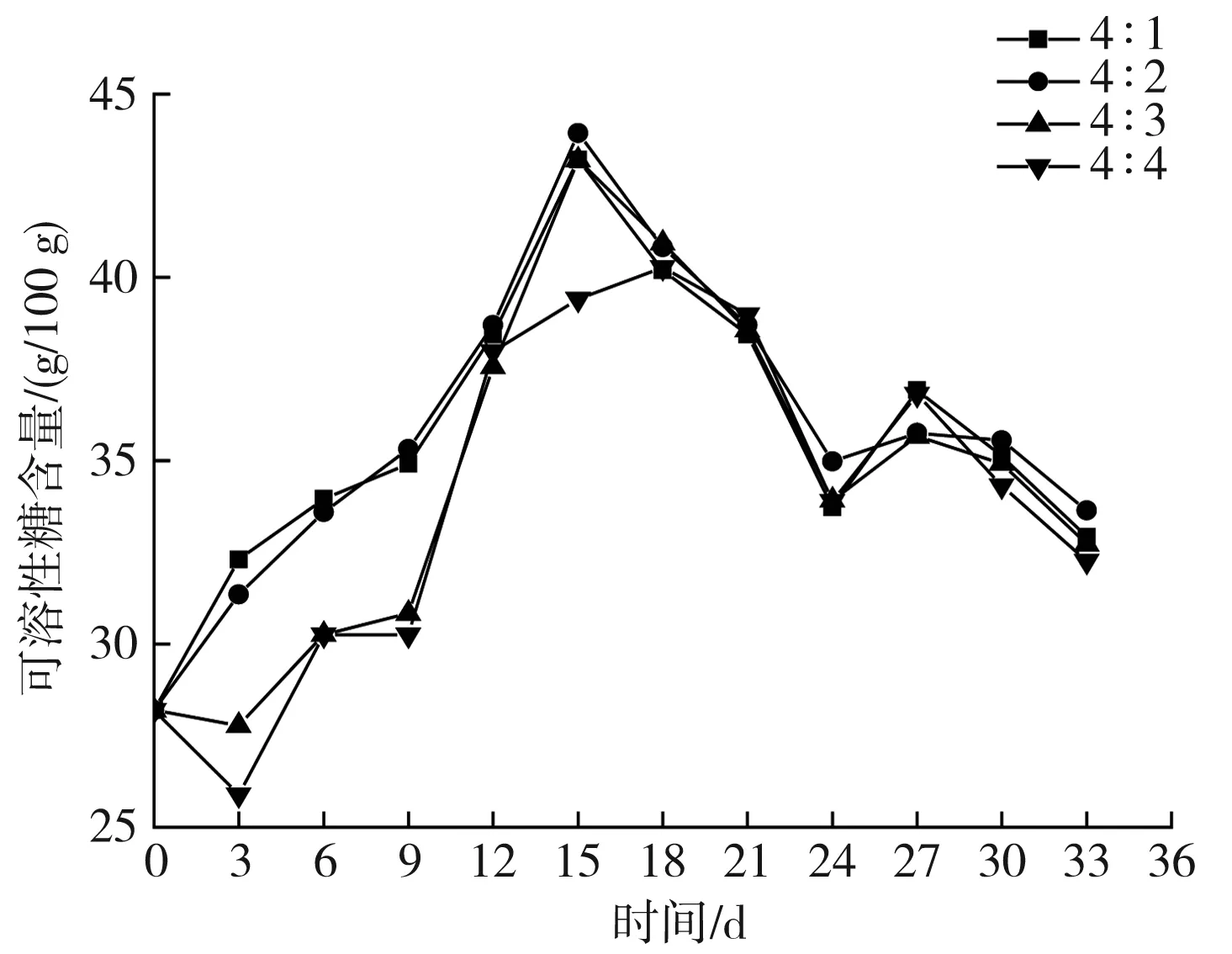
pH-1、原pH和pH+1时,不同料液质量比对液体发酵黑蒜可溶性糖含量的影响见图19。
g

h

i
由图19可知,pH-1时,各料液质量比的液体黑蒜中可溶性糖含量均在15 d达到了最大值,按料液质量比从大到小的顺序分别为43.217,43.928,43.207,40.275 g/100 g,在24 d左右,可溶性糖含量基本趋于稳定,均在33 g/100 g左右,与最大值相比,下降范围分别为24%、25%、24%、18%。原pH时,料液质量比为4∶1、4∶2和4∶3的液体黑蒜可溶性糖含量在15 d左右达到最大值,基本为44 g/100 g,而料液质量比为4∶4的液体黑蒜,其可溶性糖含量在9 d时达到最大值43.207 g/100 g,在24 d后,可溶性糖含量呈下降趋势,与最大值相比,下降范围分别为24%、30%、34%、30%,其中料液质量比为4∶3和4∶4时可溶性糖含量下降的最多。pH+1时,4∶1、4∶2、4∶3、4∶4 4种料液质量比的发酵黑蒜均在12 d达到最大值,分别为48.969,49.011,44.899,43.811 g/100 g,在20 d后,可溶性糖含量均变化不大,与各自最大值相比分别下降了35%、34%、18%、18%。唐仕荣等的研究结果中,糖含量在发酵20 d左右达到最大值,且含量在10 mg/g左右。卢福芝等的研究结果中,可溶性糖含量的最高值在38 g/100 g左右,在本试验结果中,液体黑蒜在发酵20 d左右,可溶性糖含量最大值可达到49.011 g/100 g,在成熟期稳定在33 mg/g左右。与其他人的研究结果相比较,液体黑蒜具有一定的探究价值。
由以上分析可以得出,pH+1时,料液质量比为4∶1的液体黑蒜可溶性糖含量变化更大,其变化幅度大于pH-1和原pH的液体黑蒜。
2.4 破碎粒度对液体发酵黑蒜理化指标的影响
未改变pH值的情况下,破碎粒度对液体发酵黑蒜SOD活性、总酚含量、可溶性糖含量的影响见图20。

j

k

m
由图20中j可知,原pH情况下,随着发酵时间的变化,破碎粒度对液体黑蒜SOD活性的影响是先上升后降低。在发酵前期,SOD活性上升迅速,随后缓慢上升,1,2,4 mm 3种破碎粒度的液体黑蒜SOD活性均在24 d左右达到最大值,分别为21.916,20.767,21.492 U/g。当破碎粒度为4 mm时,在发酵过程中液体黑蒜的SOD活性高于其他破碎粒度。
由图20中k可知,原pH情况下,随着发酵时间的变化,破碎粒度对液体黑蒜总酚含量的影响趋势基本为先上升再降低。其中,当破碎粒度为4 mm时, 液体黑蒜的总酚含量在24 d时率先达到了最大值6.604 mg/g;破碎粒度为2 mm时,液体黑蒜的总酚含量在27 d达到最大值6.882 mg/g;当破碎粒度为1 mm时,液体黑蒜的总酚含量在27 d达到最大值5.986 mg/g。在发酵27 d后,破碎粒度为2 mm的液体黑蒜总酚含量下降缓慢,破碎粒度为1,4 mm的液体黑蒜总酚含量降低的较多。由此可见,当破碎粒度为2,4 mm时,随着发酵时间的变化, 液体发酵黑蒜的总酚含量较高,其液体黑蒜的抗氧化性更好。
由图20 中m可知,原pH情况下,随着发酵时间的变化,破碎粒度对液体黑蒜可溶性糖含量的影响趋势基本为先上升再降低。1,2,4 mm 3种破碎粒度的情况下,随着发酵的进行,液体黑蒜均在15 d左右达到最大值,分别为42.973,44.425,44.357 g/100 g,在27 d之后,可溶性糖含量变化均不大,分别为35.978,33.806,33.217 g/100 g,与最大值相比,下降范围分别为16%、24%、25%,其中破碎粒度为4 mm时,下降范围最大,或许是因为美拉德反应发生的剧烈。
由上述分析得出,当破碎粒度为4 mm时,随着发酵的进行,对液体黑蒜的SOD活性、总酚含量和可溶性糖含量均较好,液体黑蒜的抗氧化性更好,营养价值更高。
3 结论
当料液质量比为4∶1、4∶2、4∶3和4∶4时,降低一个pH值所需要的柠檬酸的量为0.06,0.05,0.04,0.02 g;升高一个pH值所需要加入的柠檬酸钠的量为4.5,3.0,1.5,0.8 g。
pH的升高对液体黑蒜SOD活性和总酚含量的升高有一定的促进作用,而pH-1和原pH的液体黑蒜SOD活性和总酚含量升高的幅度均低于pH+1。而且pH+1时,在发酵21 d左右,可溶性糖含量的变化幅度较大,说明此条件下更有利于美拉德反应的发生。
不同料液质量比的条件下,当pH+1时,在发酵21 d左右,液体黑蒜的SOD活性最高,与未发酵大蒜SOD活性相比提高了7~8倍;当料液质量比为4∶1时,液体黑蒜的总酚含量均最大,与未发酵大蒜相比提高6倍左右,其他料液质量比仅提高3倍左右;pH+1时,料液质量比为4∶1的液体黑蒜可溶性糖含量变化更大,变化幅度大于pH-1和原pH的液体黑蒜,说明此条件下有利于美拉德反应的发生。
当破碎粒度为4 mm时,在发酵过程中,其液体黑蒜的SOD活性高于其他破碎粒度。当破碎粒度为2,4 mm时,随着发酵时间的变化,液体发酵黑蒜的总酚含量较高,说明液体黑蒜的抗氧化性更好。破碎粒度为4 mm时,可溶性糖含量下降幅度最大,说明此时更有利于美拉德反应的发生。
本试验得出的最佳工艺条件是:以新鲜大蒜为原料,当料液质量比为 4∶1,大蒜破碎粒度为4 mm时,加入一定量的柠檬酸钠提高发酵pH值,并且在85 ℃恒温发酵箱中发酵21 d左右,得到的液体发酵黑蒜SOD抗氧化作用更强,营养价值更高,保健性能更好,此时,SOD活性可提高10倍左右,总酚含量可提高6倍左右,可溶性糖含量减少34%左右。

