概念转变视角下的思维框架法教学设计
高韦华 魏建业


摘要:概念是学生认识事物的“基元”,也是学生学习科学知识的媒介。学生在开始构建科学概念之前受诸多已有因素影响,这些因素可能会导致他们在理解和应用新概念时存在不同程度的偏差,进而发展成迷思概念。因此,采用恰当的教学策略及方法转变学生已有迷思概念,进而提高学生对于概念的应用水平具有重要意义。
关键词:概念转变;氧化还原反应;思维框架法
文章编号:1008-0546(2022)12-0046-05
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2022.12.012
化学概念是化学的核心部分,与课程标准提出的五大核心素养之间有着密不可分的联系。而氧化还原反应相关概念的理解和应用是贯穿中学化学知识体系中的一条重要的知识线,是中学化学教学中的重点,也是学生迷思概念较为集中的地方。本文拟介绍一种经证实对转变学生迷思概念有积极作用的教学方法——思维框架法[Teaching Frames Approach(TFA)]。[1]以“氧化还原反应”这一中学化学中重要的基础概念为突破口,尝试应用思维框架法进行教学设计和实践,对学生存在的迷思概念进行转变,旨在帮助学生形成对氧化还原反应相关概念的科学理解,同时为广大一线教师提供概念教学方面的一个参考模式。
一、思维框架法简介
思维框架法是一种利用认知冲突策略使学生的迷思概念外显并转变的系统方法。它的整个过程立足于师生对话和生生对话等启发性社会活动,通过这种社会构建的方式将学生的思维外显,从而为教师的教学重点提供可靠的参考,有利于针对性地转变异质小团体(学生层级存在差异的小组)中存在的迷思概念。
思维框架法的教学模式如下:课程开始之前,教师事先根据教学内容精心设计思维框架法学习单和演示实验,见图1。
在演示实验开始之前,学生根据学习单的指引,分组讨论并预测演示实验结果,按照教师指引完成学习单的相应内容,然后向全班阐述自己这样预测的原因。在观察演示实验后,学生与小组成员讨论、解释实验现象,他们会将经小组讨论后认可的解释,口头阐述给整个班级的学生,老师使用苏格拉底式的提问来引导学生构建科学的模型并完善自己的解释。整个流程大致符合预测—讨论一解释一观察一讨论—解释( Predict- Discuss- Explain- Observe- Discuss- Explain)(PDEODE)策略。教师的提问鼓励学生将科学的本体论模型应用到观察到的现象中,学生通过口头、图片和书面的解释,共同构建科学认知模型,理解科学概念。最后,学生使用一个叫做“水平山”的测量工具来评价自己的课堂表现和收获,[2]见图2。
二、教学背景分析
1.教学内容和学情分析
本节是苏教版必修一专题三“从海水中获得化学物质”第一单元氯气及氯的化合物第三节的内容。氧化还原反应是中学化学概念中的一个核心概念,它贯穿于整个中学化学教材,对于发展学生的核心素养,引导学生有效进行整个高中阶段的化学学习,具有不可替代的作用。
通过初中化学的学习,学生已经掌握四大基本反应类型,他们在高一也已经学习过一些重要元素及其化合物的知识,对化合价并不陌生,能够从得失氧以及化合价变化的角度认识氧化还原反应。但是,由于缺乏相应的原子结构和化学键的知识,往往很难建立起氧化还原反应的本质是电子转移的观念。此外,学生对于化学反应微观层面的认识较少,而且存在着模糊或不科学的认识。
本设计采用思维框架法教学模式,以学生为主体,尝试外显他们头脑中的迷思概念,在教学过程中予以适当的启发问题和引导,帮助他们实现对迷思概念的自我发现和转变。
2.教学目标
(1)认知化学实验中和生活中常见的氧化剂和还原剂,能找出化学反应中的氧化剂、还原剂、氧化产物和还原产物,對于确定的方程式能定量知道它们的比值。
(2)通过实验初步学会设计验证物质的氧化性和还原性的思路,提升证据推理和模型认知的核心素养。
(3)通过对氧化剂和还原剂的研究过程,体会研究物质性质的一般方法,通过渗透化学中的哲学思想,培养学习化学的兴趣,增强科学探究和创新能力。
三、教学流程和教学思路
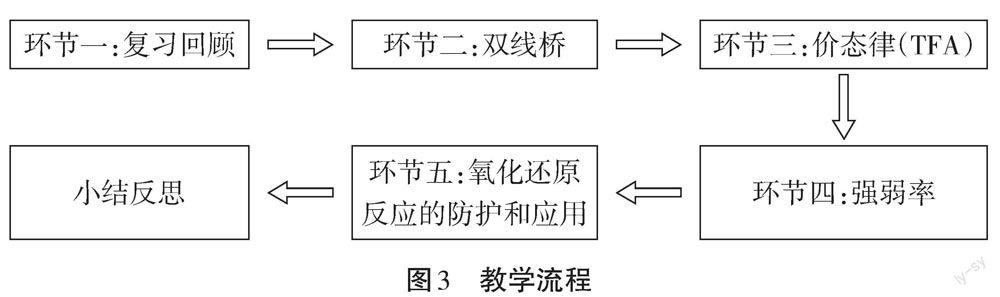
基于学生对物质的氧化性和还原性和物质元素化合价的关系还存在一定迷思概念,本设计把化合价作为切人点,结合两个典型的实验制造学生的认知冲突,启发思维,引导学生从化合价的角度去认识和判断物质的氧化性和还原性,教学流程见图3。设计采用实验法、对比法和化学建模等多种教学方法,传授科学方法的同时,渗透化学中的哲学思想。
四、教学过程
考虑到中国学生的学情,整堂课全部采用思维框架法的模式可能导致不能完成全部教学任务,因此本设计只将“环节三”部分设计为思维框架法教学模式,并将其融合到完整课堂中。下文将重点介绍思维框架法环节的教学片段。
环节三、价态律(TFA教学环节)
【启发性提问】请同学们再思考,实验室制氯气的反应中浓盐酸中氯的化合价是多少?它是否还容易降低?为什么?
【学生交流回答】氯离子最外层电子数是8,达到相对稳定结构,很难再得电子使化合价降低。
【追问】二氧化硫与硫化氢气体的反应中硫化氢中的硫元素的化合价是一2价,是否容易降低?二氧化硫中硫元素的化合价还容易再升吗?还容易再降吗?请同学们结合原子核外电子排布做出科学的解释。
【教师小结】看来物质的氧化性和还原性与元素化合价有一定的关联。接下来用两个实验来探究一下其中的联系。
【实验1】过氧化氢和淀粉碘化钾反应。在盛有2-3 mL碘化钾的试管中逐滴滴加浓度为5%过氧化氢溶液,振荡后观察现象。
【提出问题】实验演示之前我们先分析一下反应物的化合价,预测一下可能会生成的产物,和可能会发生的现象,尝试做出解释完成思维框架表的相应内容。同学们可以小组内讨论5 min。
【学生】小组讨论,头脑风暴,想出与现象有关的关键词,发表预测的看法。
【教师引导过渡】我们看到过氧化氢中的氧是一1价,它既可以升高到0价生成氧气,也可以降低生成一2价的水。
【教师引导提问】你们觉得在这个实验里面它应该是升还是降?氧化还原反应里有升必有降,如果过氧化氢中氢元素的化合价上升那么另一个物质KI里有元素能降低吗?
【学生】分析原子、离子结构发现KI中元素化合价都不容易降低。
【教师追问】那么这里的过氧化氢中氧元素化合价应该是降低的。也就是说KI中有元素要升高,什么元素呢?
【学生】思考、组内讨论、修改自己的预测,再发表看法。
【演示实验】接下来我们就用实验验证一下是不是有碘单质生成。同学们观察到什么现象?与你们预测的实验现象一致吗?如果一致,请你做出科学的解释并完成思维框架表,如果不一致,请思考原因与小组同学交流讨论。
【学生】组内讨论,按照关键词之间的关系和顺序将这些词组成句子和段落,最后完成思维框架表,发表自己的看法。
【教师引导】实验发现无色溶液变成浅黄色。溶液变成浅黄色能说明有碘单质生成吗?检验碘单质的方法是什么?滴加淀粉溶液后溶液变蓝了。说明实验确实有碘单质生成。
【教师追问】请同学分析这个实验过程KI中元素化合价发生了什么变化?作什么剂?体现什么性质?同样反应过程中过氧化氢中的元素发生什么变化?作什么剂?体现什么性质?
【学生】学生讨论、分析、交流。
【实验2】请同学们按照老师刚才的思路从化合价的角度分析第二个实验:酸性高錳酸钾和过氧化氢反应,完成思维框架表的相应部分。
【学生】自主探究,应用科学方法分析变价元素。小组讨论,头脑风暴,发表预测结果的看法。
【教师引导】高锰酸钾中锰元素已经是+7价了,你们见过化合物中锰元素比+7价还要高的价态吗?
【学生】交流、回答。
【教师引导追问】锰元素是不是没有比+7价还要高的价态了呢?所以高锰酸钾中锰元素的化合价可能会发生怎么样的变化?过氧化氢中的氧元素的化合价又会发生什么变化?
【学生】小组内讨论,发表看法。
【演示实验】取1-2 9高锰酸钾于试管,加入15 mL左右蒸馏水,滴加几滴稀硫酸,逐滴滴加浓度为5%的过氧化氢溶液。振荡后观察实验现象。
【提问】同学们观察到什么现象?与你们预测的实验现象一致吗?如果一致请科学地做出解释并完成思维框架表,如果不一致请思考原因并与小组同学讨论。
【学生】高锰酸钾褪色,有气泡产生,带火星的木条伸到瓶口,木条复燃。
说明确实有氧气生成。
【教师追问】请同学分析这个变化过程中高锰酸钾中锰元素的化合价发生了怎么样的变化?作什么剂?体现什么性质?同样这里的过氧化氢发生什么变化?作什么剂?体现什么性质?
【学生】小组讨论,修改自己预测的结果,完善思维框架表,发表自己的看法。
【教师小结】我们可以看到,过氧化氢中氧元素的化合价是一1价,而氧元素常见的价态有0和一2。也就是说一1是处在0和一2之间的中间价态。因此它的化合价可以升高也可以下降。所以在遇到不同的物质或者在不同环境下可以表现出氧化性也可以表现出还原性。过氧化氢在第一个反应充当氧化剂,而到了第二个反应就变成了还原剂。
【追问】所以说,一种物质体现氧化性还是还原性是绝对的吗?
【学生】思考,回答。
【教师总结】很好,氧化剂和还原剂并不是绝对的,不同的反应同一种物质可能是氧化剂也可能是还原剂,但是通过化合价我们可以初步判断物质可能具有氧化性还是还原性或者两者都有。这也是哲学思想渗透在化学中的矛盾的对立统一。
常见的氧化剂有:活泼的非金属单质、含有较高化合价元素的化合物、含有较高化合价金属阳离子的化合物。常见的还原剂有:活泼金属、含有较低化合价元素的化合物、某些非金属单质[3]。具有中间化合价元素的化合物可能既是氧化剂又是还原剂。
【环节设计意图】把学生作为课堂的主体,让学生自主发现自己的迷思概念,教师通过不断地追问和引导,使学生转变自己的迷思概念。氧化剂和还原剂本就是从得失电子的角度对常见物质进行的分类,对它们进一步从价态的角度进行分析有助于学生清晰、有序地认识常见的氧化剂和还原剂,也便于后续对强弱规律的系统学习。同时,加深学生对氧化剂和还原剂的认识,培养学生用哲学的角度看待化学反应,用变化、发展的眼光看问题。使学生认识氧化还原反应中,没有“绝对的”氧化剂和还原剂,根据反应事实所得出的结论一定有它的条件,条件改变,这些结论自然也要随之发生变化。
五、教学反思与建议
1.针对性选题,强化迷思概念转变效果
在教学过程中需要针对学生易产生迷思概念的部分采用思维框架模式。氧化还原反应作为基础性知识应用范围广,能够帮助学生从化合价的角度预测物质的性质,发展学生的微观认识,培养宏观辨识和微观探析的核心素养,有利于建构化学新思维。从氧化还原反应角度认识物质的性质有其独特的化学视角和一般规律。该阶段高一学生对氧化还原反应物质的判断掌握较好,但是没有形成对氧化还原反应的动态认识,知识迁移能力较差。例如:如果他们确定某物质在某一反应中为氧化剂,那么就会认为在其他的化学反应中也是作氧化剂。这个想法会进一步对学生之后的学习,尤其在判断有陌生物质参加的氧化还原反应中的氧化剂、还原剂时,产生很大干扰,造成迷思概念。因此本课时的思维框架教学环节把重点放在解决氧化还原反应中的价态律,基于学生的问题开展教学。这种模式力求从知识本质出发,使学生思维过程外显,并使学生在反思过程中修正自己的迷思概念,有利于摆脱纯粹知识的教学。
2.以学生为中心,培养自主学习化学的能力
在实验前后通过一系列问题串来引导学生的思维活动,全程把课堂交还给学生,只是在学生的讨论过程中给予适当的追问与引导,并在适当的时候做些许补充和小结。整个过程重点放在对学生思维的引导与启发,充分发挥了学生的自主性和课堂参与度,学生在教师的引导下,主動反思并建构科学的认知模型,培养自身证据推理和模型构建的核心素养。整个课堂氛围较好并取得良好的教学效果。
3.手口并用,发展多面能力
思维框架教学法需要学生自己想出与课程相关的关键词,并通过他们适当地处理,形成自己的科学解释。期间,完成思维框架表的过程极大锻炼了学生的想象力和书面表达能力。在学生需要向全班进行解释的时候又锻炼了自身的口头表达能力和在演讲时的信心。因此思维框架法不仅仅立足于知识本身,更锻炼了学生的多方面的能力。
4.结合国情,发挥思维框架法的作用
思维框架教学法在国外科学教育中已经得到了广泛的应用,且已取得了良好的反馈。但目前国内的相关研究尚缺乏。在国外,科学教育的对象大多是儿童,他们有大量的课时进行探究,思维框架教学法往往应用于一个相对抽象庞大的主题,往往需要消耗大半学期甚至一学期的课时。然而,国内化学教学面对的最小年龄的群体都已经是初三的学生,他们面临较大的升学压力,同时教师也面临严峻教学任务,高中的课时更是宝贵。考虑到中国化学教学的形势,笔者建议将思维框架教学法融合到一个课时的某个环节中去,这样既能在一定程度上发挥思维框架法的作用,又不影响正常的教学任务。
综上所述,思维框架教学法有其独特的优势,同时又面临不小的挑战,比如课时环节应如何合理安排以及适合设计成思维框架教学法的主题有哪些等,这需要广大教师继续深入研究、完善与应用,并在实践中进行摸索和改进。
参考文献
[1]Treagust D F,Won M, Mclure F.Multiple representationsand students' conceptual change in science[J]. Convergingperspectives on conceptual change: Mapping an emergingparadigm in the learning sciences, 2017: 121-128.
[2]Mclure F.The Thinking Frames Approach:a case study ofinclusion using student- generated multiple- representations[J]. Journal of Research in Special Educational Needs,2020, 20(1):3-13.
[3]胡海燕.“氧化还原反应”教学设计[J].化学教育,2010,31(S2):146-150.

