pH对乳糖-乳铁蛋白复合物结构及理化特性的影响
黄利华,陈帅,张业辉*,张友胜,江如蓝,钟伟锐,焦文娟,赵甜甜
(1.广州城市职业学院食品科学与美食养生学院,广东广州 510405)(2.广东省农业科学院蚕业与农产品加工研究所,农业农村部功能食品重点实验室,广东省农产品加工重点实验室,广东广州 510610) (3.加州大学戴维斯分校营养系,美国加州 95616)(4.汕尾市五丰海洋生物技术有限公司,广东汕尾 516626)
乳铁蛋白(Lactoferrin,LF)是一种与铁结合的转运糖蛋白,在人的机体中参与铁的转运,并具有抗氧化、抗菌、调节免疫系统等功能活性,是哺乳动物免疫系统中的重要成分。食品中的乳铁蛋白是一种从牛初乳中提取的铁结合性糖蛋白[1],其分子量约为80 ku,由约689个氨基酸组成LF的一级结构。乳铁蛋白的等电点在8.4~9.0之间,高于大多数食品蛋白质[2,3]。LF的三级结构由两个对称的子叶(N叶和C叶)组成,即乳铁蛋白多肽链的N末端和C末端,由一个短α-螺旋连接[4]。LF包含两个热变性温度峰(61和93 ℃),分别对应于N-和C-叶上的展开[5]。乳铁蛋白具有广泛的生理活性,例如抗菌活性、抗氧化活性、抗炎活性、免疫调节特性、抗癌等[6-8],表明它在增强免疫力与抗癌方面可能具有较好的应用价值。此外,LF是一种生物降解性好、生物相容性高、无毒性的天然化合物,在婴幼儿食品、化妆品和医药产品中同样具有广泛的应用[9]。《国家标准GB14880-2012》允许在婴儿配方奶粉中添加乳铁蛋白,其添加量≤1.0 g/kg。
蛋白质的热敏性是限制LF应用的原因之一,蛋白质经过加热处理后暴露了疏水性基团,导致蛋白质聚集,聚集体之间不断发生相互作用,最终导致沉淀的形成[10]。据文献报道蛋白质与多糖结合形成共价或非共价复合物,能提高LF在加工过程中的热稳定性。已有研究表明,多糖的加入可以抑制蛋白质的热变形,提高蛋白质多糖复合物的热稳定[11-13]。此外,在不同的pH条件下,蛋白质多糖复合物还可以形成大小可控的粒子,这有利于研究蛋白质多糖复合物作为食品或药物的载体[14]。因此,本文主要研究了不同pH诱导LF-乳糖复合物的形成过程、微观结构与理化性质的变化规律,研究结果为提高乳铁蛋白在食品中的应用提供一定的参考。
1 材料与方法
1.1 材料与试剂
乳铁蛋白(纯度≥91%),湖北威德利化学科技有限公司;乳糖,天津市福晨化学试剂厂;碧云天试剂盒,上海碧云天生物技术有限公司;甲醇,天津市百世化工有限公司;冰乙酸,天津市富宇精细化工有限公司;β-巯基乙醇,天津市大茂化学试剂厂;考马斯亮蓝,上海源叶生物科技有限公司;十二烷基硫酸钠(SDS),天津市福晨化学试剂有限公司;其余试剂均为分析纯。
1.2 仪器与设备
UV-1800型紫外分光光度计,日本岛津公司;电泳仪,美国Thermo Fisher公司;ST85B3-1型真空冷冻干燥机,美国Milirock公司;JascoJ-815型圆二色谱仪,日本分光公司;VERTEX33型傅里叶变换红外光谱仪,德国Bruker公司;SZ-100纳米颗粒分析仪,美国Malvern Instruments公司;S-3400N型扫描电子显微镜,日本Olympus公司。
1.3 方法
1.3.1 LF-乳糖糖复合物的制备
LF和乳糖分别溶解在蒸馏水中,加入0.02%(m/V)叠氮化钠,以防止细菌生长,室温(22 ℃)搅拌2 h,制备固定浓度为1%(m/V)的原溶液。把制备好的溶液用保鲜膜封口,在冰箱(4 ℃)中保存过夜,以确保完全水合。
1.3.2 浊度测定
浊度的测量采用Li等[15]的方法。使用UV-1800型紫外分光光度计在600 nm处测定不同pH条件下LF-乳糖溶液的浊度。以去离子水为空白对照,对浊度值进行校正。摇匀后测定,每个样品一式三份。
1.3.3 粒径测定
使用美国Malvern Instruments公司的SZ-100纳米颗粒分析仪测定样品的粒径大小及分布。数据报告为平均直径或体积直径。
1.3.4 扫描电子显微镜(SEM)
将冻干的LF-乳糖复合物粉末用双面胶带固定在圆形铝桩上,用离子溅射仪镀金后,在15 kV加速电压下用扫描电子显微镜(日本Olympus公司的S-3400N)进行检查和拍照。
《雷雨》是曹禺先生在“没有太阳的日子里的产物”,无论是哪一个女性形象,都是以悲剧结局收尾。这场命中注定的雷雨,这场无法回避的悲剧,将人世间一切的丑恶揭露开来,无论什么人都无法逃脱命运的囹圄。好一场雷雨,于黑暗中诉说了一个家庭的悲剧,展示了人性的扭曲,揭露了残酷的现实!它是一场暴风雨,是一场文字的雷雨,字字血泪,掷地有声!四凤死了,繁漪疯了,侍萍生不如死。一场雷雨,花谢知多少?花非花,似花,非花无花,梦中泪花,一场雷雨,梦碎一场空;梦非梦,似梦非梦,无梦,梦碎一场空!三十年,走完一场悲哀。
1.3.5 傅里叶变换红外光谱(FT-IR)
将冷冻干燥后的LF-乳糖复合物与溴化钾(KBr)按1:100的比例进行混合压片后,在400~4000 cm-1范围内进行光谱扫描,分辨率为4 cm-1,扫描32次。
1.3.6 圆二色谱测定
分别移取300 μL不同pH条件下的LF-乳糖复合物溶液于光程为1 mm的比色皿中,在波长为190~260 nm,持续通入氮气的条件下,进行样品的圆二图谱扫描,重复两遍实验。
1.3.7 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)
参考Laemmli[16]的方法,根据电泳试剂盒说明书,选用4%浓缩胶和10%分离胶进行配胶。取0.5 mL样品溶液与等体积上样缓冲溶液进行混合,煮沸5 min,于冰水混合物中冷却并恢复至室温后上样,每孔上样量10 μL。采用恒压模式,浓缩胶时电压为25 V,分离胶电压为80 V,凝胶用染色液(含0.02%考马斯亮蓝,45%甲醇和10%冰乙酸)染色2~4 h,随后用脱色液(含45%甲醇和10%冰乙酸)脱色至条带清晰可见并进行拍照。
还原SDS-PAGE中上样缓冲液中加入10%β-巯基乙醇,其他同上。
1.4 数据分析
测定和分析结果采用Origin 8.0、CDNN和Prodata软件处理数据,SPSS V20.0软件进行单因素差异性及相关性分析。
2 结果与讨论
2.1 不同pH条件下LF-乳糖复合物的浊度变化
如图1a所示,所有溶液在热处理前都是透明的。相比之下,加热后B1和B2组仍然澄清,B3/B4/B5出现浑浊。此外,在B3/B4/B5玻璃瓶可以观察到大的聚集体,而且聚集体随着pH的增大也逐渐增多,这显然是热处理后LF分子的变性和聚集所致[17,18]。
热处理前后不同pH值条件下样品的浊度变化如图1b所示。加热前,pH值对LF-乳糖复合物的浊度基本没有影响,复合物溶液在的吸光值大约在0.05左右,溶液呈澄清透明状态。加热后,随着混合溶液中pH值的增加,LF-乳糖复合物的浊度逐渐变大。特别是在pH值6时,复合物溶液的浊度开始急剧增加(吸光值约pH为2时的30倍),直到pH值为10,吸光值增加到2.4左右。从图中可以看出,高pH值条件下,热处理后LF-乳糖复合物的变性和聚集更易发生,这可能与LF分子在碱性环境中对热不稳定的原因有关[19]。
2.2 不同pH条件对LF-乳糖复合物粒径的影响
在不同pH条件下热处理后LF-乳糖复合物的平均粒径如图2a所示,从图中可以明显的得出,环境中pH对LF-乳糖复合物颗粒的形成具有促进作用。随着混合溶液中pH的增加,LF-乳糖复合物颗粒呈显著增大的趋势,在pH=10时,LF-乳糖复合物颗粒粒径达到最大值465 nm。在强酸性环境中(pH=2和pH=4),LF和乳糖分子呈共溶状态,颗粒平均直径基本维持在10 nm左右。在弱酸和碱性环境中(pH=6、pH=8和pH=10),LF-乳糖复合物的粒径形成,并逐渐变大(224增加到467 nm),这可能与LF在弱酸和碱性环境中不稳定相关[20,21]。当复合物中静电相互作用较弱且净电荷相对较高时,可溶复合物就会形成。相反,当静电相互作用较强且净电荷较低时,就会形成共聚物[22]。热处理导致LF-乳糖复合物聚集体的形成,弱酸和碱性环境降低了LF本身的正电荷,从而引起了LF-乳糖复合物聚集体间的静电斥力降低,聚集体之间不断相互作用,最终到导致沉淀的生成。从图1a中瓶底部的沉淀也可以说明,pH值越大LF-乳糖溶液中沉淀越多。
为了更好地说明不同pH值对LF-乳糖复合物颗粒形成的影响,我们测定了样品的尺寸分布,如图2b所示。在pH=2和pH=4,溶液的粒径基本一致,分布很窄;随后随着pH值的增加粒径分布的峰值明显向大尺寸方向移动,同时也发现更宽的尺寸分布,这也表明LF-乳糖复合物的形成。
2.3 不同pH条件下LF-乳糖复合物的微观结构
采用扫描电镜表征不同形态的LF-乳糖复合物微观结构。图3显示,LF、乳糖均呈球状或椭圆状,LF分子相对较大。图3b和3c中,LF和乳糖分子呈无规则状态,这是由于在强酸环境中LF和乳糖分子均被质子化,静电斥力阻碍了LF与乳糖的结合,它们处于共溶状态[23]。在宏观图1a中,也可以明显在的看到LF-乳糖呈透明状态。图3d和3e中,可以明显看到LF和乳糖结合在一起,NaCl附着在其表面形成盐桥促进LF-乳糖复合物的形成。并且随着pH值的变大,LF-乳糖复合物之间进一步发生相互作用,形成更大的聚集体。但是在粒径结果中,在pH=6和pH=8时,LF-乳糖复合物的粒径变化不大,说明测聚集体之间主要靠盐键连接,聚集体在水溶液中部分溶解。在图3f中(pH=10),观察到长条状聚合物,由于LF分子在碱性条件中不稳定,加热处理后,LF分子完全变性,导致蛋白分子间聚集,生成沉淀。图2a和图1a中复合溶液的粒径的突然增大以及玻璃瓶底部有大量沉淀的生成也可以说明了这点。除此之外,有关报道指出,LF在90 ℃ 10 min条件下就完全变性,丧失其原有的空间结构[4],但在LF-乳糖复合物中发现LF的原有的球形结构(pH=6和pH=8),因此可以推测,乳糖的加入一定程度上抑制了LF的热变性。
2.4 不同pH条件下LF-乳糖复合物的红外光谱分析
乳铁蛋白、乳糖及不同pH条件下LF-乳糖复合物的红外光谱图如图4所示。LF和乳糖在酰胺A带(3000~3700 cm-1)内有个很宽的峰,这是由于-OH的伸缩振动引起的。LF在酰胺一带(1600~1700 cm-1)和酰胺二带(1500~1600 cm-1)均有峰值,这是LF分子中的肽键产生的,其中酰胺一带(1652.77)主要由C=O伸缩振动产生的,酰胺二带(1542.51)是由N-H的弯曲振动和C-N伸缩振动产生的[24]。乳糖在酰胺一带有峰值(1654.97),这是乳糖中C=O伸缩振动引起的,在890 cm-1吸收峰是乳糖中β-糖苷键的特征峰[25]。在所有复合物样品中都存在酰胺带(酰胺一带和酰胺二带)和890 cm-1处β-糖苷键的特征峰,这说明LF与乳糖发生了相互作用形成了LF-乳糖复合物。
如表1所示,总的来说,当混合溶液的pH值为酸性时,LF-乳糖复合物的酰胺Ⅰ带和酰胺Ⅱ带略有蓝移现象,酰胺A带由3410.33 cm-1蓝移至3396.36 cm-1。当混合溶液的pH值为碱性时,LF-乳糖复合物的酰胺Ⅰ带和酰胺二带略有蓝移现象,而酰胺A带由3410.33 cm-1红移至3421.32 cm-1,这表明混合溶液的酸碱性影响了LF-乳糖复合物的-OH。可能是由于混合溶液中环境的酸碱性改变了-OH伸缩振动的大小,从而导致酰胺A带的蓝移或红移现象。
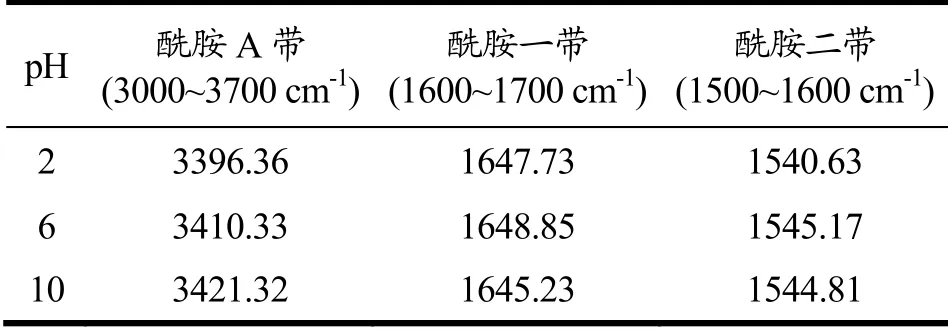
表1 不同pH下LF-乳糖复合物对应的光谱带分析Table 1 Spectral band analysis of LF-lactose complex at different pH values
2.5 不同pH条件对LF-乳糖复合物二级结构的影响
LF-乳糖复合物不同pH值条件下二级结构的变化如图5所示。有报道称LF的远紫外图谱含有两个特征吸收峰,在195 nm左右的正峰带和210 nm左右的负峰带[26],这是蛋白质二级结构的典型峰。从图中可以明显看出,随着溶液中pH值逐渐增大,195 nm左右的正峰带强度变化较小,210 nm左右负峰带的强度逐渐减弱,这说明随着溶液中pH值逐渐增大,更多的二级结构遭到破坏,这与LF在碱性条件下不稳定是一致[19]。氢键是维持蛋白质二级结构最主要的作用力。这种变化可能是因为酸性环境中增强了氢键作用力,从而保护了LF的二级结构不受破坏;而碱性环境中,降低了氢键作用力,破坏了LF的二级结构。此外,在酸性条件下(pH=2和pH=4)210 nm左右负峰带有蓝移现象,这与红外分析结果一致。
通过Prodata和CDNN软件处理圆二图谱计算二级结构的变化,如表2所示。可以得出,α-螺旋含量逐渐降低,同时无规则卷曲和β-折叠含量逐渐增大,β-转角基本保持不变。由于LF-乳糖复合物中LF分子在碱性环境中不稳定,热处理加大了蛋白分子变性的程度,导致α-螺旋展开,蛋白质中其他结构向无规则卷曲和β-折叠转变,引起其含量增加[27]。黎庆等[28]和刘猛等[4]在研究LF的热变性时,也发现其二级结构中α-螺旋含量降低,β-折叠含量升高,与本研究结果相似。
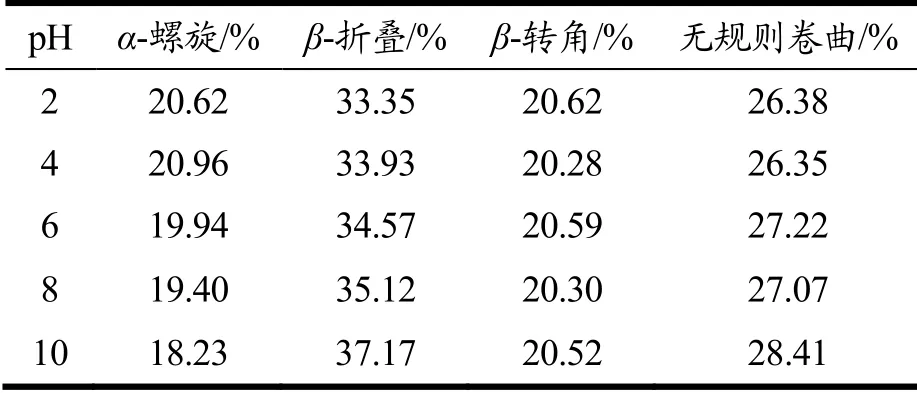
表2 热处理后不同pH条件下LF-乳糖复合物的二级结构变化Table 2 Secondary structure changes of LF-lactose complex at different pH after heat treatment
2.6 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)
由图6a可以看出,LF在66~95 ku区域内有一条密度较高的宽大条带。在pH为2时,条带的密集度明显降低,这可能由于在强酸性环境中LF发生降解。有研究报道表明,LF在pH=2时,部分高级结构展开,释放大量结合的铁离子[29,30]。在pH为4时条带密度与LF相同,pH为6时,条带密度略微减低,这说明LF-乳糖合物在pH=6时出现变性。在pH为8时,只有一条很浅的条带,同时在浓缩胶顶端也有条带,这说明LF-乳糖合物形成大量聚集体,且大部分聚集体不能进入分离胶。在pH为10时,LF-乳糖合物几乎全部形成了更大的聚集体,聚集体堆积在浓缩胶顶端,不能进入分离胶。
弱酸和碱性环境中LF-乳糖分子均发生交联,碱性越强交联越紧密,导致形成聚集体,且相对分子质量增大,不能通过浓缩胶。但在还原性电泳图谱中(图6b),只有pH为8时条带明显加深,pH为6时条带略微加深,而且在pH为8和10时,在浓缩胶顶端仍发现聚集体,这说明在碱性环境中形成了不被β-巯基乙醇破坏的聚集体。闫旭东等[31]研究表明,较强烈的热处理打断了LF分子内的二硫键从而释放出游离的巯基,导致了LF分子结构的巨大改变。因此可以推测这种聚集体可能以非二硫键的共价键或以静电作用和疏水相互作用为主的非共价键作用形成[28]。倪娜等[32]在研究pH对羊血浆蛋白热诱导凝胶特性时,也发现在pH=5.0、85 ℃的持续加热导致了凝胶中非二硫共价键的形成。
3 结论
pH值可以调控LF-乳糖复合物的粒径大小,随着pH值(2~10)逐渐增大,LF-乳糖复合物的粒径也不断增大(从10到460 nm)。弱酸性环境中,LF-乳糖复合物中仅有少量的蛋白分子变性,LF-乳糖复合物主要以盐键和氢键作用形成。碱性环境中,蛋白分子大量变性,形成大量聚集体,聚集体间主要以静电作用及疏水作用形成。不同的pH值条件,影响了形成LF-乳糖复合物的主要作用力,改变了LF-乳糖复合物结合状态,导致其在水溶液中不同的存在形式。本研究结果对探索多羟基物质对LF分子结构和功能的变化提供一定的理论参考,也拓宽了乳铁蛋白在食品中的应用。

