黏质沙雷氏菌对稀土废水中Dy(Ⅲ)的生物吸附性能及吸附机理分析*
沈吉利 梁长利,2 任嗣利#
(1.江西省矿冶环境污染控制重点实验室,江西理工大学资源与环境工程学院,江西 赣州 341000;2.黄淮学院生物与食品加工工程学院,河南 驻马店 463000)
稀土元素镝(Dy)被广泛应用于核能、冶金、电子、化学工程和计算机等领域[1],是工业生产的重要原材料。随着经济与科技的发展,Dy的需求量逐年增加。目前,稀土冶炼企业通常将低浓度稀土废水直接排放,不但造成了严重的稀土资源浪费,并且对周围生态系统的安全和人类健康构成了严重威胁[2-3],因此迫切需要寻找一种经济有效的从废水中回收稀土元素的方法。
针对稀土废水处理,微生物吸附法因具有操作成本低、吸附和解吸速率快、选择性高、对稀溶液处理效果好、可再生、环境友好等特点具有良好的应用前景[4]。目前已有一些针对微生物吸附稀土离子的研究[5-6],但主要集中在轻稀土领域,针对重稀土吸附的研究较少。对于Dy这种具有重要经济价值的重稀土元素则多采用无机合成材料吸附[7-8],应用微生物吸附的研究鲜有报道。为此,本研究以赣南稀土矿区废水中分离的黏质沙雷氏菌作为生物吸附剂吸附稀土废水中的Dy(Ⅲ),研究废水pH、吸附时间、Dy(Ⅲ)初始浓度和细菌生物量对吸附效果的影响,通过吸附动力学和吸附等温线研究了黏质沙雷氏菌对Dy(Ⅲ)的吸附动力学行为和吸附作用方式,从而为微生物吸附法在稀土废水处理和稀土资源回收中的应用提供理论指导。
1 材料与方法
1.1 主要试剂与材料
实验材料:牛肉膏、蛋白胨、琼脂均为市售产品直接使用;NaCl、HCl、HNO3和NaOH均为分析纯;Dy2O3纯度为99.9%;实验过程中的用水为超纯水(18.25 MΩ/cm)。
菌株培养:从赣南某稀土矿区筛选分离黏质沙雷氏菌,在牛肉膏蛋白胨平板上活化24 h,挑取生长较好的单克隆转接于液体培养基中,在30 ℃、200 r/min的条件下于水浴恒温振荡器中培养48 h,最后在4 ℃、10 000 r/min下离心10 min后收集菌体,用无菌水洗涤3次去除表面残留培养基后离心收集备用。
Dy(Ⅲ)储备液:用含一定HCl的去离子水配置Dy(Ⅲ)储备液,Dy(Ⅲ)质量浓度为1 000 mg/L,根据实验设计,利用Dy(Ⅲ)储备液配置不同浓度的Dy(Ⅲ)溶液。
1.2 吸附实验
单因素吸附实验在100 mL锥形烧瓶中进行,烧瓶内装有20 mL Dy(Ⅲ)溶液,调节溶液pH、Dy(Ⅲ)初始浓度、吸附时间和吸附剂用量后充分吸附,吸附结束后在4 ℃、10 000 r/min低温离心机上离心10 min,测定上清液中剩余的Dy(Ⅲ)浓度,计算Dy(Ⅲ)去除率及吸附量,所有实验均进行3次取平均值。
1.3 样品表征
用Zetasizer Nano ZS90型Zeta电位仪分析不同pH溶液中黏质沙雷氏菌表面的Zeta电位;采用MLA650F型场扫描电子显微镜(SEM)和X射线能谱仪(EDS)对吸附前后黏质沙雷氏菌的表面形貌和元素组成进行了分析;采用傅立叶红外光谱(FTIR)和X射线光电子能谱(XPS)研究黏质沙雷氏菌表面官能团的组成和元素变化。
2 结果与讨论
2.1 Zeta电位分析
不同pH溶液中,黏质沙雷氏菌表面Zeta电位变化见图1。黏质沙雷氏菌表面Zeta电位随着溶液pH的升高逐渐降低,pH=4.18为黏质沙雷氏菌的零电荷点,低于该pH时Zeta电位为正值,而当pH>4.18时,Zeta电位为负值且电负性随着pH的增加而增强,因此适当提高溶液pH有利于带正电荷的Dy(Ⅲ)通过静电作用吸附在黏质沙雷氏菌表面[9]。
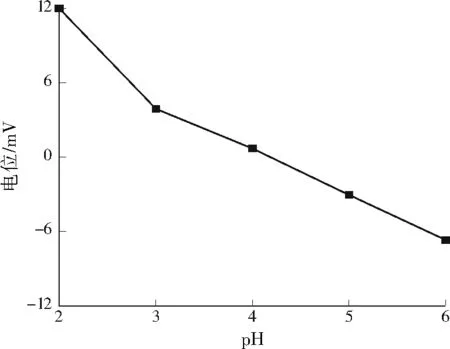
图1 黏质沙雷氏菌在不同pH溶液中的 Zeta 电位Fig.1 Zeta potentials of Serratia marcescens in solution with different pH
2.2 黏质沙雷氏菌对Dy(Ⅲ)的吸附行为研究
配置初始质量浓度为30 mg/L的Dy(Ⅲ)溶液,调节黏质沙雷氏菌用量为0.4 g/L,利用HCl、NaOH调节Dy(Ⅲ)溶液pH分别为2.00、3.00、4.00、5.00、6.00,充分吸附120 min后测定剩余Dy(Ⅲ)浓度,计算黏质沙雷氏菌对Dy(Ⅲ)的吸附量,结果见图2。
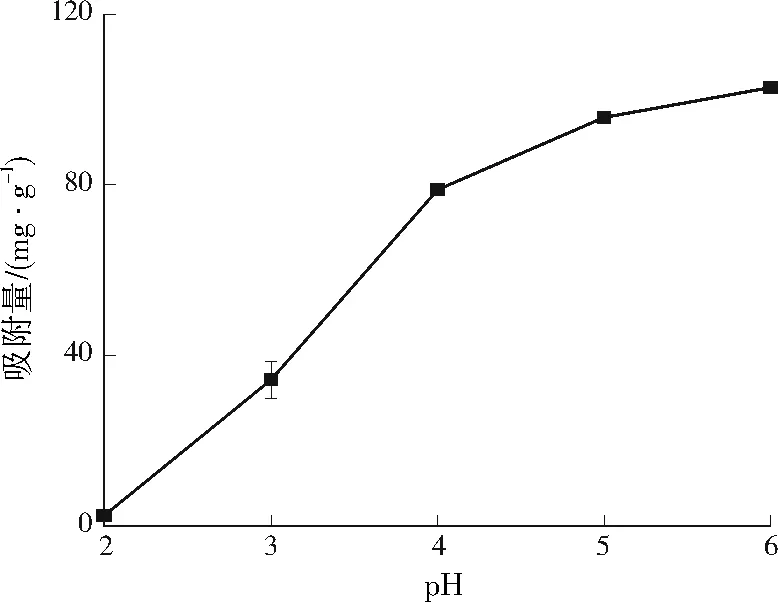
图2 溶液pH对黏质沙雷氏菌吸附Dy(Ⅲ)的影响Fig.2 The effects of pH on the adsorption of Dy(Ⅲ) by Serratia marcescens
由图2可见,当Dy(Ⅲ)溶液pH从2.00增加到6.00时,黏质沙雷氏菌对Dy(Ⅲ)的吸附量由2.50 mg/g迅速提高到102.79 mg/g,这是因为pH越高,黏质沙雷氏菌表面的电负性越大,越有利于Dy(Ⅲ)通过静电吸引作用吸附到黏质沙雷氏菌上。XU等[10]在利用农杆菌HN1吸附La(Ⅲ)和Ce(Ⅲ)时也发现类似现象。当Dy(Ⅲ)溶液pH高于5.50时,Dy(Ⅲ)易出现沉淀干扰现象。因此,选择pH为5.00进行后续吸附实验。
配置初始质量浓度为30 mg/L的Dy(Ⅲ)溶液,调节Dy(Ⅲ)溶液pH为5.00,黏质沙雷氏菌用量为0.4 g/L,充分吸附360 min,期间不定时取样测定Dy(Ⅲ)浓度,计算黏质沙雷氏菌对Dy(Ⅲ)的吸附量,结果见图3。

图3 吸附时间对黏质沙雷氏菌吸附Dy(Ⅲ)的影响Fig.3 The effects of adsorption time on the adsorption of Dy(Ⅲ) by Serratia marcescens
由图3可见,随着吸附时间的增加,黏质沙雷氏菌对Dy(Ⅲ)的吸附分为两个阶段。首先,吸附量在前90 min内迅速增大,此后缓慢增加并在120 min时基本达到吸附平衡。在吸附初始阶段,溶液中Dy(Ⅲ)浓度较高,黏质沙雷氏菌表面存在大量吸附活性位点,有利于Dy(Ⅲ)的吸附,因此吸附速率较快。随着吸附过程的进行,黏质沙雷氏菌活性结合位点数量逐渐减少,从而降低了吸附剂与金属离子相互碰撞的概率[11],吸附速率逐渐降低,直到达到平衡。因此,选择吸附时间为120 min进行后续吸附实验。
利用Dy(Ⅲ)储备液配置初始质量浓度分别为10、20、30、50、70、90、110 mg/L的Dy(Ⅲ)溶液,调节Dy(Ⅲ)溶液pH为5.00,黏质沙雷氏菌用量为0.4 g/L,充分吸附120 min后取样测定溶液中Dy(Ⅲ)浓度,计算黏质沙雷氏菌对Dy(Ⅲ)的吸附量,结果见图4。
由图4可见,随着Dy(Ⅲ)初始质量浓度从10 mg/L增加到110 mg/L,黏质沙雷氏菌对Dy(Ⅲ)的吸附量从38.71 mg/g提高到97.97 mg/g。随着Dy(Ⅲ)浓度的进一步增加,黏质沙雷氏菌对Dy(Ⅲ)的吸附量逐渐稳定,说明黏质沙雷氏菌表面结合位点对Dy(Ⅲ)的吸附基本达到饱和,吸附过程达到平衡。

图4 Dy(Ⅲ)初始质量浓度对黏质沙雷氏菌吸附Dy(Ⅲ)的影响Fig.4 The effects of initila Dy(Ⅲ) mass concentration on the adsorption of Dy(Ⅲ) by Serratia marcescens
配置初始质量浓度为30 mg/L的Dy(Ⅲ)溶液,调节Dy(Ⅲ)溶液pH为5.00,控制黏质沙雷氏菌用量分别为0.1、0.2、0.3、0.4、0.5、0.6 g/L,充分吸附120 min,吸附结束后取样测定Dy(Ⅲ)浓度,计算Dy(Ⅲ)的去除率,结果见图5。
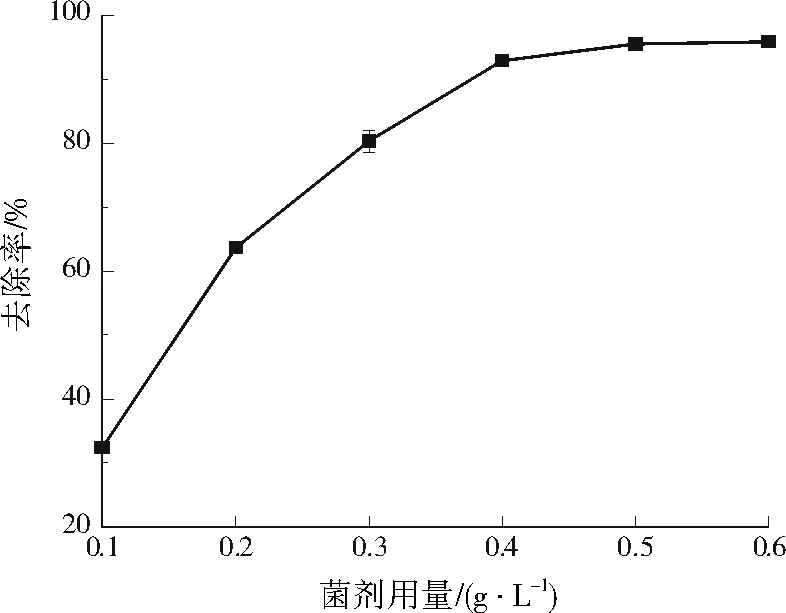
图5 不同黏质沙雷氏菌用量下Dy(Ⅲ)的去除率Fig.5 The removal rate of Dy(Ⅲ) under different Serratia marcescens dosage
由图5可见,当黏质沙雷氏菌用量从0.1 g/L增加到0.6 g/L时,Dy(Ⅲ)的去除率由32.43%上升到95.86%。这是由于溶液中Dy(Ⅲ)的浓度固定,黏质沙雷氏菌用量增加,吸附剂总表面积增加,能够吸附更多的Dy(Ⅲ),因此Dy(Ⅲ)去除率相应提高。在实际应用中,应根据稀土废水中Dy(Ⅲ)浓度调整吸附剂的用量,以平衡处理成本和效率。
综合以上实验结果,当Dy(Ⅲ)溶液pH为5.00、吸附时间为120 min、Dy(Ⅲ)初始质量浓度为30mg/L、0.4 g/L黏质沙雷氏菌对Dy(Ⅲ)的吸附量和去除率可分别达到95.81 mg/g和95.86%。

表1 黏质沙雷氏菌对Dy(Ⅲ)的吸附等温线参数Table 1 Isotherm parameters of Dy(Ⅲ) adsorption by Serratia marcescens
2.3 吸附动力学和吸附等温线
2.3.1 吸附动力学
为了研究黏质沙雷氏菌吸附Dy(Ⅲ)的动力学行为,并分析吸附过程中是否存在粒子内扩散过程,分别用准二级动力学模型(见式(1))[12]2460和颗粒内扩散动力学模型(见式(2))[13]1577对吸附数据进行了拟合:
(1)
Qt=kit0.5+C
(2)
式中:t为吸附时间,min;Qt为吸附t时的吸附量,mg/g;k2为准二级吸附速率常数,g/(mg·min);Qe为平衡吸附量,mg/g;ki为第i个吸附阶段的颗粒内扩散吸附速率,mg/(g·min1/2);C为颗粒内扩散速率常数,C为与界面层厚度相关的常数,C值越大,吸附边界效应越大。
根据吸附数据拟合结果,准二级动力学模型的相关系数为0.99接近于1,说明可以用该模型描述黏质沙雷氏菌对Dy(Ⅲ)的吸附动力学行为,该吸附过程主要为化学吸附[12]2466,准二级吸附速率常数为0.012 g/(mg·min)。颗粒内扩散动力学模型拟合结果表明,黏质沙雷氏菌对Dy(Ⅲ)的吸附过程包含3个阶段,第1、2、3阶段的颗粒内扩散吸附速率分别为5.27、0.62、0.15 mg/(g·min0.5),第1阶段(0~50 min)为颗粒外扩散阶段,Dy(Ⅲ)吸附速率最快,因为吸附初期溶液中Dy(Ⅲ)浓度较高,在浓度驱动力的作用下,Dy(Ⅲ)迅速吸附到细菌表面,初始30 min内Dy(Ⅲ)的吸附率可达68.55%;第2阶段(50~120 min)为逐渐吸附阶段,已吸附的Dy(Ⅲ)阻碍了溶液中的Dy(Ⅲ)向细菌表面的扩散,减缓了扩散速度;第3阶段(120 min后)吸附量基本保持不变,意味着吸附达到平衡。此外,颗粒内扩散模型中,Qt与t1/2的拟合线均未通过原点,说明颗粒内扩散不是黏质沙雷氏菌吸附Dy(Ⅲ)的限速步骤[13]1579。
2.3.2 吸附等温线
采用Langmuir方程和Freundlich方程两种等温吸附模型对黏质沙雷氏菌吸附Dy(Ⅲ)的过程进行了拟合,Langmuir方程和Freundlich方程表达式分别见式(3)、式(4)[14-15]:
1/Qe=1/(QmKLce)+1/Qm
(3)
lgQe=1/nlgce+lgKF
(4)
式中:Qm为理论最大吸附量,mg/g;KL为Langmuir吸附常数,L/mg;ce为吸附平衡时溶液中Dy(Ⅲ)质量浓度,mg/L;KF为Freundlich吸附常数,mg1-1/n·L1/n/g;n为经验参数,与吸附体系性质有关。
Langmuir方程、Freundlich方程的拟合结果见表1。可以看出,Langmuir方程拟合相关系数为0.99,更接近于1,表明黏质沙雷氏菌对Dy(Ⅲ)的吸附更符合Langmuir模型,吸附过程为单分子层的化学吸附[16]。用Langmuir方程计算黏质沙雷氏菌对Dy(Ⅲ)的理论最大吸附量为96.45 mg/g,与实际最大吸附量95.81 mg/g更加吻合。ZAKI等[17]利用腐殖酸吸附稀土废水中的Dy(Ⅲ),平衡吸附量为18.3~39.1 mg/g,LIU等[18]发现壳聚糖膜对Dy(Ⅲ)的最大吸附量为23.3 mg/g,比较可知黏质沙雷氏菌在吸附Dy(Ⅲ)上具有相当大的优势,有望用于稀土废水中有价稀土元素的回收。
2.4 吸附机理研究
2.4.1 SEM分析
图6为黏质沙雷氏菌吸附Dy(Ⅲ)前后的SEM图。吸附前,黏质沙雷氏菌表面相对光滑,而吸附后的黏质沙雷氏菌表面变得粗糙,细胞表面有沉积物,这可能是由于吸附在黏质沙雷氏菌表面的Dy(Ⅲ)所致。根据EDS分析结果(见表2),黏质沙雷氏菌细胞表面Dy的质量分数从吸附前的0增加到吸附后的3.39%,进一步证实了Dy(Ⅲ)成功地吸附在黏质沙雷氏菌表面。此外,Na、Ca、K质量分数大幅下降,说明Dy(Ⅲ)可能通过与Na+、Ca2+、K+等金属离子发生离子交换而吸附在细胞表面。大肠杆菌、枯草芽孢杆菌和酿酒酵母菌对Cd2+的吸附中也存在类似的离子交换现象[19]。

图6 黏质沙雷氏菌吸附Dy(Ⅲ)前后的SEM图Fig.6 SEM images of Serratia marcescens before and after adsorption of Dy(Ⅲ)

表2 黏质沙雷氏菌吸附Dy(Ⅲ)前后表面元素质量分数Table 2 The mass percentage of various element of Serratia marcescens before and after adsorption of Dy(Ⅲ) %
2.4.2 FTIR分析
黏质沙雷氏菌吸附Dy(Ⅲ)前后的FTIR图谱见图7。吸附前,黏质沙雷氏菌在3 200~3 600 cm-1的强宽带可以归因于—OH/—NH的拉伸振动[20],该宽峰的存在表明黏质沙雷氏菌中存在大量的羟基和氨基。2 924、2 857 cm-1处的双峰是甲基或亚甲基的典型不对称和对称拉伸振动峰[21]。1 646 cm-1处为酰胺Ⅰ带中C=O的伸缩振动峰,1 548 cm-1为酰胺Ⅱ带中N—H的弯曲振动峰[22]2282。黏质沙雷氏菌吸附Dy(Ⅲ)后,1 646 cm-1处特征峰峰位移至1 643 cm-1,1 548 cm-1处特征峰位移至1 534 cm-1,这与氨基中—NH的弯曲振动有关[23],可能是Dy(Ⅲ)与黏质沙雷氏菌蛋白质上的氨基发生了络合作用所致。此外,1 384 cm-1处特征峰表示蛋白质酰胺Ⅲ带中的C—N伸缩振动吸收峰[22]2282,吸附Dy(Ⅲ)后峰强度明显增强,可能是Dy(Ⅲ)与酰胺基团中的氮成键,使得酰胺基团C—N键两端电负性差别增大,偶极矩变大,导致振动强度增强。由此表明,氨基和酰胺基团在Dy(Ⅲ)吸附过程中发挥了重要作用。
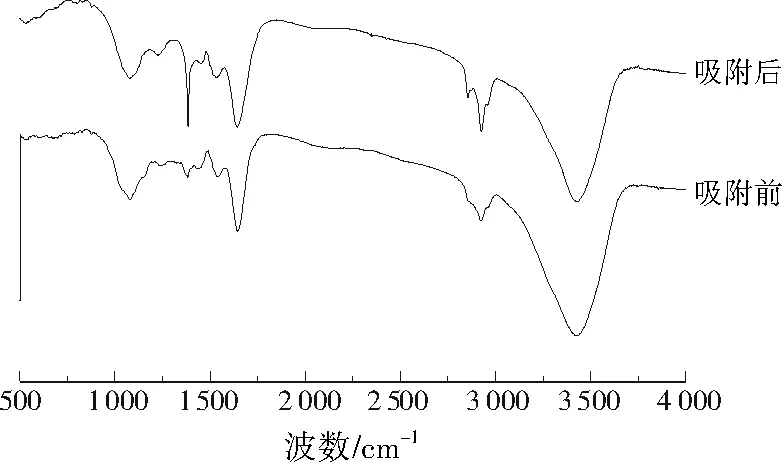
图7 黏质沙雷氏菌吸附Dy(Ⅲ)前后的FTIR图谱Fig.7 FTIR pattern of Serratia marcescens before and after adsorption of Dy(Ⅲ)
2.4.3 XPS分析
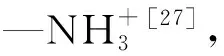
2.4.4 黏质沙雷氏菌对Dy(Ⅲ)的吸附机理
黏质沙雷氏菌对Dy(Ⅲ)的吸附机理有3种:(1)在适宜pH下,黏质沙雷氏菌表面具有较高的电负性,可有效吸引带正电荷的Dy(Ⅲ)离子,即黏质沙雷氏菌可通过静电吸引作用促进Dy(Ⅲ)的吸附;(2)Dy(Ⅲ)与黏质沙雷氏菌中Na+、Ca2+、K+、Mg2+等金属离子发生离子交换进入生物吸附材料;(3)Dy(Ⅲ)与黏质沙雷氏菌中的—NH2和—COOH等活性官能团发生配位作用,增强了黏质沙雷氏菌对Dy(Ⅲ)的吸附。
本研究中黏质沙雷氏菌对Dy(Ⅲ)的生物吸附能力明显高于其他材料,可以较好满足从稀土废水中回收Dy(Ⅲ)的要求。分析原因,黏质沙雷氏菌株从江西省稀土矿山废水中筛选出来,在Dy(Ⅲ)溶液中长期驯化处理,因此对Dy(Ⅲ)表现出良好吸附能力;其次黏质沙雷氏菌与无机合成材料相比,其表面含有大量活性官能团从而提供了更为丰富的吸附活性位点。研究结果为微生物法在稀土废水处理的实际应用提供了科学参考和数据支撑。
3 结 论
采用黏质沙雷氏菌吸附去除稀土废水中的Dy(Ⅲ),考察了溶液pH、Dy(Ⅲ)初始浓度、吸附时间和吸附剂用量等对吸附过程的影响。结果表明,当Dy(Ⅲ)溶液pH为5.00、吸附时间为120 min、Dy(Ⅲ)初始质量浓度为30 mg/L、0.4 g/L黏质沙雷氏菌对Dy(Ⅲ)的吸附量和去除率可分别达到95.81 mg/g和95.86%。黏质沙雷氏菌对Dy(Ⅲ)的吸附过程为Langmuir单层吸附,遵循准二级吸附动力学模型。黏质沙雷氏菌对Dy(Ⅲ)的吸附主要通过静电吸引作用和离子交换作用进行,此外黏质沙雷氏菌表面分布的—COOH、—NH2基等含N、O的基团可通过配位作用吸附Dy(Ⅲ)。

