CO2加氢合成甲醇催化剂的助剂效应
宋 敏,安晓琪,刘 振
[中国石油大学(华东),山东青岛 266580]
人类的生存与发展都和能源有密切关系,随着人口数量激增、社会迅速发展、工业经济主导[1],社会需要的热量和动能不断增加,人类对能源的需求量呈几何倍数增长,而风力、水力等新能源受到条件限制不能大规模使用[2],因此,能源已呈过度开采的趋势,这一经济载体将在21世纪迅速接近枯竭[3-4]。
CO2作为碳源,比煤炭、石油和天然气总储量都高。这就使得在能源危机和环境危机的双重作用 下[5-7],全球的科学研究人员将目光聚集在二氧化碳的转化利用上[8],力图寻找出CO2利用的新途径和新技术。CO2作为被世界组织认证的亲和性气体,其在精细化工[9]、医药行业、食品行业、农业、工业中均是一种宝贵的资源。
甲醇可以煤为原料[10-11],尤其是以高硫煤和炉烟气为原料可以带来经济和环境双重效益。另外,甲醇也可以以生物质为原料,由此可以对有机垃圾等进行回收处理[12]。目前工业上几乎全部采用CO催化加压加氢合成甲醇的方法。美国南加州大学教授Olah团队曾前瞻性地提出转化CO2的“甲醇经济”理念[13],该技术成为全球CO2转化技术关注的焦点。近几年来,各个能源企业尤其是煤化工对CO2催化加氢制甲醇技术表现出极大的关注。然而,对于目前的CO2催化加氢制甲醇技术来说,除去H2的来源制约过程和成本之外,催化剂转化率和选择性差的问题更是科学研究者极大的困扰[14]。
20世纪中叶,英国推出了Cu基甲醇合成催化剂,促进了CO2催化加氢制甲醇的研究进展[15]。且现有世界上对于CO2加氢催化制甲醇的方法主要为沉淀法和浸渍法。沉淀法虽然可以在低压下得到高活性[16],但同时也面临着抗毒性差、机械强度低和易失活的缺陷。浸渍法可以采用合适性能的载体,利用率高且成本低,但易产生废气和发生活性物质转移。本文旨在CO2催化加氢制甲醇的以Cu/ZrO2为载体的催化剂的助剂改性研究,试图改进传统的合成甲醇催化剂的方法及性能[17-18]。
1 CO2合成甲醇反应机理
1.1 合成甲醇反应
按相关研究[4]看来,CO2加氢合成甲醇反应可以由以下3个反应组成:
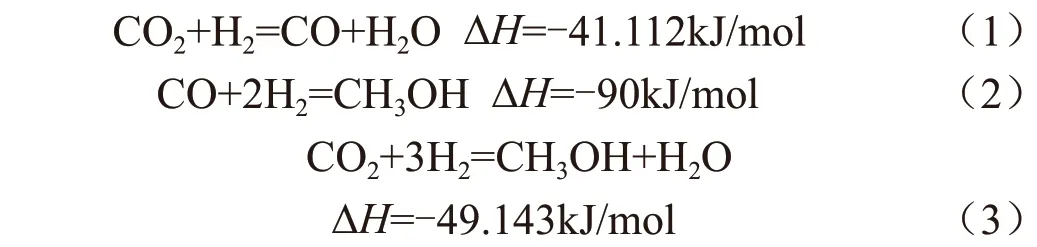
1.2 反应机理
目前,对于CO2加氢催化合成反应的争议主要在于CO2在催化过程中是否有解离中间体CO和中间产物的产生。但随着研究的不断深入,很多研究者对于此项争议的共识越来越趋向于CO2在催化剂上加氢直接催化合成甲醇,而不经过解离中间体CO和中间产物的产生过程。Deluzarche研究ZnO-Cr2O3催化剂催化此反应时,在催化剂上发现了甲酸盐物种和甲氧基物种[5]。而Ramarson也在Cu-Zn催化剂催化此反应时发现有甲酸盐物种出现,并提出了如图1的反应机理[6]。
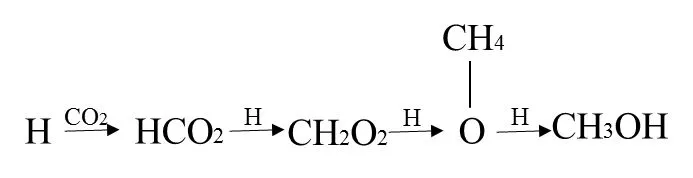
图1 Deluzarche等提出的CO2催化加氢机理
2 实验部分
2.1 催化剂的制备
2.1.1 分散沉淀法(SR)制备催化剂
将研磨后的ZrClO2·8H2O和NaOH按摩尔比1∶4混合,迅速搅拌使其反应。将反应产物在110℃下晶化48h。抽滤,110℃干燥12h得到ZrO2。
把ZrO2分散到Cu(NO3)2溶液中,搅拌1h。在70~75℃的条件下把Na2CO3溶液滴到混合溶液中。抽滤,在110℃条件下干燥12h,在350℃温度下焙烧3h得到Cu/ZrO2催化剂。进行压片、造粒(40~60目)。
2.1.2 固态反应法(DP)制备催化剂
研磨Cu(NO3)2、ZrClO2、NaOH,将研磨后的Cu(NO3)2、ZrClO2迅速混合,再加入NaOH快速搅拌,然后进行晶化,之后经过急冷、抽滤、干燥、焙烧后得到Cu/ZrO2催化剂,晶化与焙烧条件与分散沉淀法条件相同。最后冷却、压片、造粒(40-60目)。
2.2 催化剂的表征
氮气等温吸脱附采用美国ASAP3020介孔物理吸附仪。比表面积采用BET公式计算,孔容积和孔径分布采用BJH方法通过氮气等温脱附曲线计算。
XRD采用荷兰帕纳科锐影X-射线衍射仪。射线源为Cu Kα,扫描范围为2θ=5°~75°,扫描速度 2(°)/min,功率2.2kW。
H2-TPR 采用天津市先权公司的TP-5080-D全自动多用吸附仪。将0.05g催化剂,载气为He,还原气为10% H2-90% N2,待基线稳定后,升温速率为2℃/min。
XPS采用美国赛默飞世尔X射线光电子能谱仪。仪器激发源为Al Kα,分辨率为1.15eV。
2.3 催化剂活性评价
本实验评价采用美国麦克公司Particular Systems Microactivity Effi反应器进行评价。取1.0g催化剂,装入反应管。先在常压 300 ℃用H2还原4h。然后切换反应气,压力升到2MPa,温度降为250℃,反应气质量流量为45mL/min,开冷凝器冷凝液体产品,在此条件下反应持续6h以上。待反应系统稳定,运行色谱。每15min采集一次气体样品,通过色谱TCD在线分析反应后气体的组分及含量。反应结束后,收集液体样品,离线分析液体产品中组分及含量。
3 结果与讨论
3.1 助剂对CO2加氢催化剂的影响
3.1.1 氮气等温吸脱附
如图2~图5所示。从孔径分布可以看出,所有催化剂孔分布曲线相似,孔分布集中,均集中在4nm左右。从催化剂等温吸附图看来,无论采用何种方式引入助剂所得催化剂的吸附等温线均属于Ⅳ型,带有明显的滞后回环为介孔孔结构类型,且滞后环在P/P0=0.4位置闭合表明催化剂存在较小的介孔。而从比表面和孔结构数据来看,除Mn外,浸渍法方式引入的催化剂比表面稍微优于共沉淀法方式引入,这可能是因为共沉淀法引入助剂时,助剂物种部分进入ZrO2孔道内,堵塞了一部分孔,导致其比表面积降低,而Mn作为结构性助剂在共沉淀过程中有利于铜物种的分散,提高了催化剂比表面[19],而浸渍法引入Mn、K助剂催化剂比表面积降低的原因可能是助剂量引入过多,不利于形成大比表面积催化剂,如表1所示。
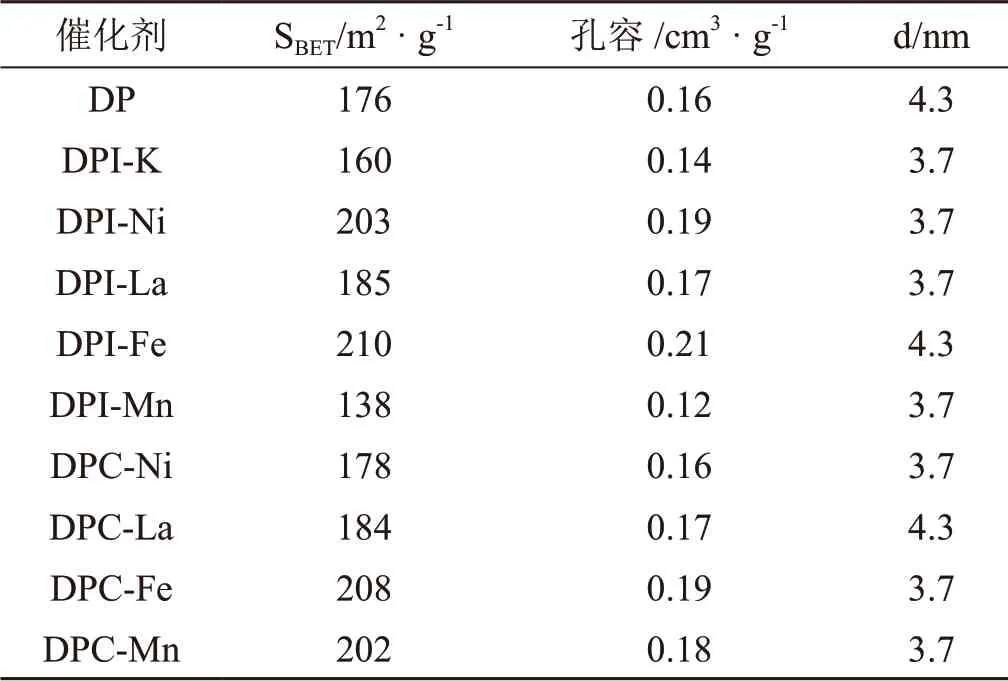
表1 M/CuO/ZrO2催化剂比表面积和孔结构

图2 DPI法M/Cu/ZrO2催化剂等温吸附曲线
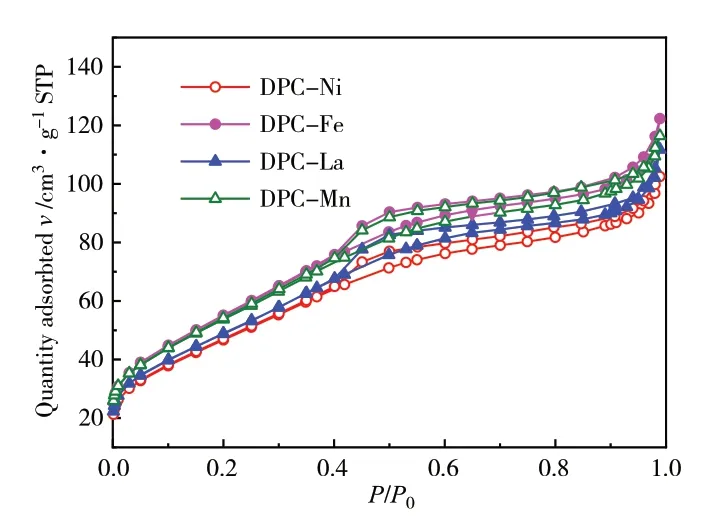
图3 DPC法M/Cu/ZrO2催化剂等温吸附曲线
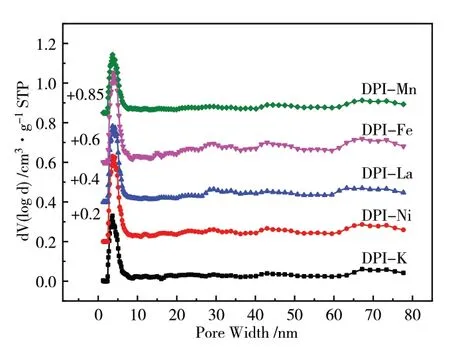
图4 DPI法M/Cu/ZrO2催化剂孔径分布曲线
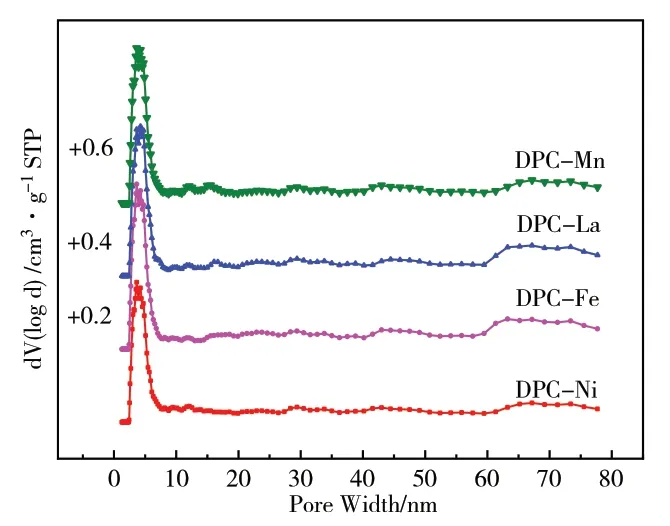
图5 DPC法M/Cu/ZrO2催化剂孔径分布曲线
3.1.2 XRD表征
分别采用浸渍法和共沉淀法引入助剂,从图6和图7可以看出,两种引入方式对催化剂的物相结构存在不同的影响,浸渍法引入助剂所得催化剂CuO的衍射峰基本没有变化,这是因为助剂是通过浸渍方式引入催化剂前驱体中,在浸渍之前,ZrO2和CuO前驱物晶粒已经形成,助剂的引入对其晶粒尺寸大小基本没有影响。而通过共沉淀法引入助剂所得催化剂CuO衍射峰有些许宽化,尤其是Mn助剂作用比较明显,这是因为助剂通过共沉淀法引入与CuO前驱物溶液混合比较均匀,起到了“栅栏”作 用[20,21],避免铜物种团聚,因此共沉淀法引入助剂有助于形成小晶粒CuO。
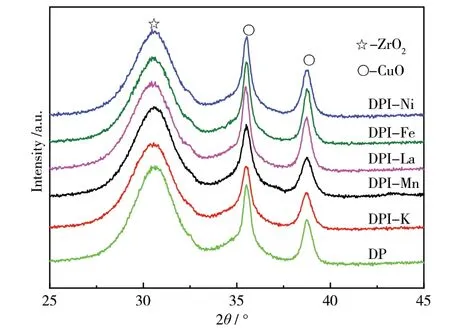
图6 CuO/ZrO2催化剂XRD谱图
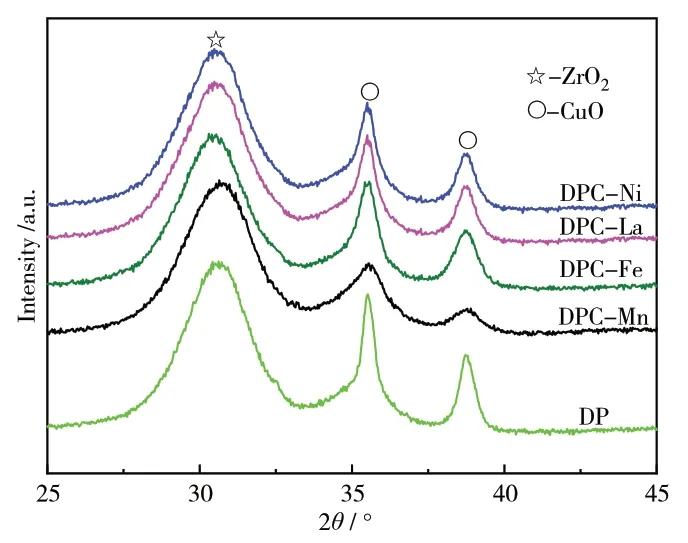
图7 CuO/ZrO2催化剂XRD谱图
3.1.3 H2-TPR表征
从催化剂的还原性质来看,浸渍法引入助剂所得催化剂在引入不同助剂后双还原峰均向高温方向移动,尤其是K,只出现了单还原峰,且向高温方向移动,这是因为碱金属量加入较多时大部分分布在催化剂的表面,可能会覆盖催化剂表面的活性组分,则会减少还原气体H2与活性组分的接触面积,进而会对催化剂的还原产生不利影响。此外,La和Ni引入后出现了三原峰,推测可能是因为催化剂表面在还原的过程中出现了Cu+物种[22]。
而共沉淀法方式引入助剂,所有催化剂均出现了双还原峰,其中Fe、Ni改性催化剂两个还原峰均向低温方向移动,且两种助剂的引入使催化剂的高温、低温还原峰不易区分。La助剂对催化剂表面CuO的还原基本没有什么影响,Mn改性的催化剂低温还原峰向低温方向移动,且相对含量较高。文献中提到,Mn是结构性助剂,Mn的引入促进了催化剂表面CuO的分散,提高了其还原性能;Fe、Ni是调变性助剂,能调节Cu物种的电子性质[23-26],促进催化剂的还原;La也是调变性助剂,但在该催化剂体系中,La的作用不明显,如图8所示。
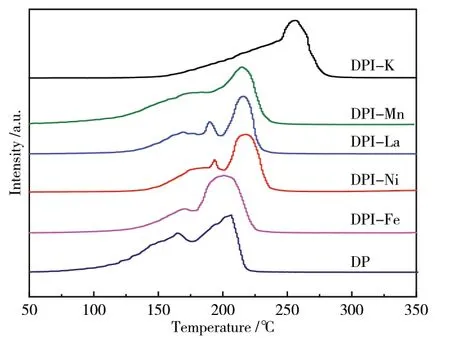
图8 M/Cu/ZrO2催化剂H2-TPR图
3.2 催化剂反应评价
从图9和图10可以看出,采用共沉淀法方式引入助剂催化剂的CO2转化率高于采用浸渍法引入助剂,这可能与催化剂的还原性有关,共沉淀法引入助剂催化剂的CuO颗粒分散较好,表面CuO容易还原,催化活性较好,尤其是Mn但浸渍法引入方式引入助剂,催化剂的初始活性较好,这表明助剂引入方式的不同会影响催化剂还原之后的活化程度。
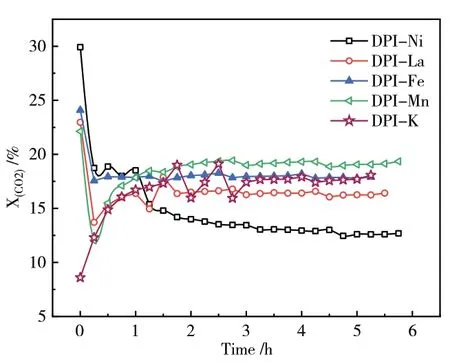
图9 浸渍法引入助剂CO2转化率
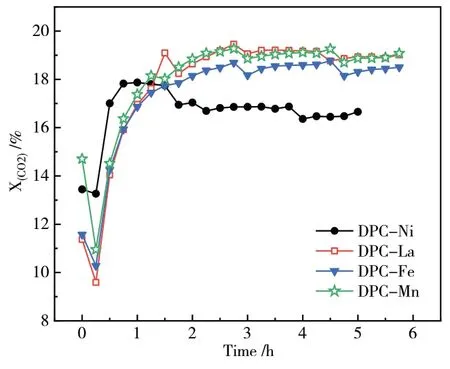
图10 共沉淀法引入助剂CO2转化率
从图11和图12可以看出,总醇选择性呈现逐渐减小的趋势,对醇类的选择性在反应最初时最大,可达90%以上,这可能是因为在初始反应阶段活性中心上生成的CO首先迁移并吸附到载体表面,部分脱附成为产物,部分加氢生成醇类,随着CO吸附量的增加,从表面脱附的CO越来越多,尾气中CO浓度也越来越高,当达到饱和吸附时,尾气中CO含量达到稳定值,相应的,加氢生成醇类的CO量就越来越少。
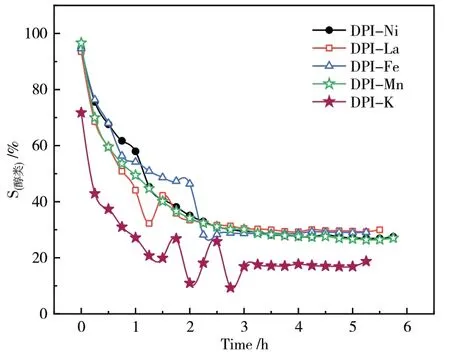
图11 浸渍法引入助剂总醇选择性
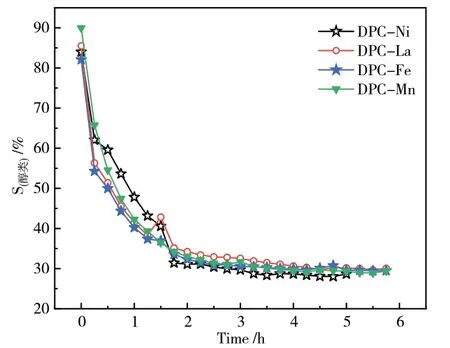
图12 共沉淀法引入助剂总醇选择性
从图中可以看出,采用浸渍法引入La、Ni后,甲醇选择性明显优于其他催化剂,结合H2-TPR,采用浸渍法引入La、Ni后还原曲线出现了三个还原峰,猜测可能出现了新的Cu物种,此外选取了转化率最好的浸渍法引入Mn助剂的催化剂和同样是La助剂,甲醇选择性最差的共沉淀催化剂研究了催化剂组分之间的相互作用。
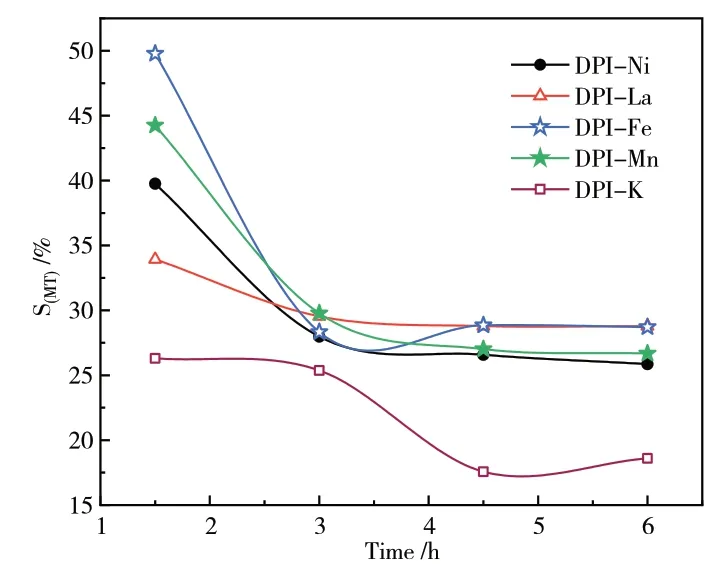
图13 浸渍法引入助剂甲醇选择性
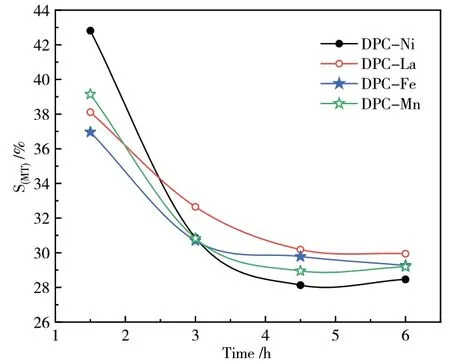
图14 共沉淀法引入助剂甲醇选择性
4 结论
1)助剂的引入明显提高了催化剂的反应活性,但影响了产物分布。MnO、La2O3、Fe2O3和NiO的几何效应提高了催化剂的比表面积,尤其是采用沉淀法引入助剂的方式抑制了CuO晶粒的聚集,得到了较小尺寸的CuO晶粒。助剂对活性组分Cu之间的电子调变作用,增强了Cu和Zr之间的相互作用,尤其是采用沉淀法引入助剂的方式降低了催化剂的还原温度,且La和 Mn的引入明显提高了反应活性。
2)关联催化剂理化性质和活性组分Cu的价态与反应性能得到,催化剂中Cu与ZrO2的相互作用越强,催化剂还原温度越低,CO2转化率越低,CO2转化率与Cu与ZrO2之间相互作用强弱有关。此外,乙醇选择性与Cu+活性位有关,甲醇选择性与Cu0活性位有关。

