锰胁迫下盐肤木锰富集及生理响应特征
王悟敏,胡佳瑶,刘文胜,曾文斌
(中南林业科技大学 生命科学与技术学院,长沙 410004)
锰矿的无序开采导致生态环境恶化,土壤锰(Mn)污染愈来愈严重,锰甚至会通过食物链危害人类的健康。如何有效修复大面积重金属污染土壤已成为当前急需解决的关键问题。植物修复具有高效、环保和廉价等优点,是重金属污染土壤治理的有效方法之一,具有广阔的应用前景[1]。筛选出优良的修复植物并揭示其耐受机制是采用该技术修复重金属污染土壤的关键。
锰作为植物必需的元素,参与植物的多种代谢过程,主要包括光合作用、叶绿素合成以及作为酶的辅因子,少量的锰可促进植物的生长[2]。然而,过量的锰元素会对植物造成胁迫。锰胁迫环境下植物体内会积累大量活性氧自由基(reactive oxygen species,ROS),使膜结构受到破坏,严重时会引起植株的死亡。植物锰毒性主要表现为生物量和光合作用减少,叶绿体的结构造成破坏以及生理生化机制紊乱[3]。而对于锰耐受性强的植物,植物体内会发生一系列生理生化反应来应对锰胁迫环境,如植物体内渗透调节物质含量、抗氧化酶活性以及丙二醛含量等均发生不同程度的变化[4-6]。植物对于重金属锰具有一定的吸收累积能力,通常以Mn2+的离子态吸收。不同植物对重金属锰的富集与转运能力不一样。一般植物体内锰含量为30~500 mg·kg-1,而锰耐受性植物对锰的积累远远超过这一值[7]。例如,美洲商陆(Phytolaccaamericana)[5]、短毛蓼(Polygonumpubescens)[8]和木贼(Equisetumhyemale)[9]等对锰均有较强的富集作用。但不同的植物积累锰的部位有所不同,锰被贮存在根系细胞或是被转运到地上部分,由此耐锰性植物对锰的积累类型主要分为地上部富集型、根部囤积型和规避型3种[9]。
盐肤木(Rhuschinensis)是漆树科盐肤木属落叶小乔木或灌木,高可达10 m。该植物在中国境内分布广泛,资源丰富,是中国主要经济树种。盐肤木适应能力强,耐干旱、耐贫瘠,抗逆性强。之前的研究表明该植物在重金属铬、铜、铅胁迫下均表现出良好的耐受性,是废弃地恢复的先锋植物[10-12]。研究显示该植物对铜、铅、镉、铬均具有一定的富集与转运能力[11-13]。Zhou等[14]研究发现盐肤木可通过生理生化机制来减轻铅的毒害作用。我们的前期研究表明,盐肤木在锰矿区有较好的锰耐受性,同时该植物相比与草本植物具有生物量高、根系发达等特点,在重金属污染土壤修复中具有较高的应用潜力。然而,目前对盐肤木在锰胁迫下的耐性机制、对锰的富集与转运能力以及锰积累类型尚未开展系统研究,这限制了该植物在锰污染土壤修复中的应用前景。
本试验以盐肤木作为研究对象,研究不同浓度锰胁迫下盐肤木的生长、生理响应与重金属积累特征的变化规律,旨在揭示盐肤木对锰胁迫的耐受性机制和累积特征,为利用盐肤木进行重金属锰污染土壤的植物修复提供理论依据。
1 材料和方法
1.1 试验材料
盐肤木果实于2019年11月中旬采自湖南省湘潭市锰矿废弃地(27°58′N,112°51′E,海拔26 m),该区土壤锰含量达52 319.25 mg·kg-1,盐肤木种群平均高度约5 m。将采回的果实进行风干,待其呈褐色时去除果皮及其他杂质,将得到的种子装入种子袋中于室温保存。
1.2 盆栽试验
2020年10月,参照徐莉清等[15]的方法将预处理后的盐肤木种子放入人工培养箱中进行萌发。2021年4月初,选取高度为10 cm、5~6片真叶、长势一致的半年生盐肤木幼苗为试验材料。将这些幼苗转移至直径20 cm、高14 cm的花盆中,每盆3株盐肤木幼苗。盆中培养基质由纯沙和珍珠岩按照2∶1混合而成,幼苗适应生长2周,待其生长稳定后加入锰溶液进行胁迫。锰浓度梯度设置为0(CK)、1、5、10和20 mmol·L-1,用Hoagland营养液溶解MnCl2·4H2O进行胁迫处理,对照组(CK)施以等量Hoagland营养液,每个浓度处理12盆。在胁迫20 d后测定幼苗的生物量、生理指标以及锰含量。胁迫期间使用去离子水保持培养基质湿润,每3 d添加1次Hoagland营养液。
1.3 测定项目与方法
1.3.1 生物量将胁迫后植株收获,分成地上部分和地下部分。用去离子水充分洗净,地下部分用0.2% EDTA浸泡2 h去除表面吸附锰离子,经105 ℃杀青5 min,75 ℃烘干3 d至恒重,称取地上部分和地下部分干重,并计算根冠比。 根冠比=地下部分生物量/地上部分生物量
1.3.2 光合色素含量取新鲜叶片用80%丙酮研磨提取,在紫外分光光度计下测646、663和470 nm处的吸光值,按Chavoushi等[16]的方法计算叶绿素含量[mg·g-1(鲜重)]和类胡萝卜素含量。
1.3.3 渗透调节物质含量参照Pan等[17]的方法,用蒽酮比色法测定盐肤木叶片中可溶性糖含量;考马斯亮蓝法测定可溶性蛋白含量,以牛血清白蛋白(BSA)为标准;酸性茚三酮显色法测定游离脯氨酸含量。
1.3.4 抗氧化物酶活性参照Gao等[18]的方法,取新鲜叶片于预冷的研钵中,用5 mL磷酸盐缓冲液(0.05 mol·L-1,pH 7.8)将叶子研磨至匀浆,4 ℃下8 000 r·min-1离心15 min,取上清液待测。超氧化物歧化酶(SOD)活性用氮蓝四唑(NBT)法测定,以抑制NBT光还原的50%为一个酶活性单位(U·g-1);过氧化物酶(POD)活性用愈创木酚法测定,以每分钟内OD470升高0.01为一个酶活性单位(U·g-1·min-1);过氧化氢酶(CAT)活性用紫外吸收法测定,以每分钟内OD240减少0.01为一个酶活性单位(U·g-1·min-1)。
1.3.5 丙二醛含量参照Gao等[18]的方法,取新鲜叶片用5%三氯乙酸磨成匀浆状,3 000 r·min-1下离心10 min,获得提取液。用硫代巴比妥酸法测定丙二醛(MDA)含量。
1.3.6 锰含量、生物富集系数和转运系数将植株分成地上部分与地下部分烘干至恒重,用粉碎机打碎过筛(20目)后称重。在马福炉中300 ℃开炉门1 h,再500 ℃关炉门5 h,呈灰白色。冷却后加2 mL 50% HCl,用水过滤至25 mL容量瓶,用原子吸收分光光度计(AA-70000,Shimadzu,Japan)测定锰含量[17]。并据此计算生物富集系数和转运系数。生物富集系数为植物体内锰含量与基质锰含量的比值;转运系数为地上部分锰含量与地下部分锰含量的比值。
1.4 数据处理
用SPSS 22.0对测量数据进行单因素方差分析(ANOVA),不同浓度之间用LSD法进行多重比较(P<0.05),使用SigmaPlot 12.5绘图。
2 结果与分析
2.1 锰胁迫对盐肤木生长的影响
胁迫处理20 d后,盐肤木在Mn2+浓度为0、1、5和10 mmol·L-1条件下生长发育状况良好,地上部分没有出现明显的重金属中毒现象,而且盐肤木在5 mmol·L-1Mn2+条件下叶片舒展,叶片颜色较深;而在20 mmol·L-1Mn2+条件下盐肤木部分叶片出现褐色斑点、萎蔫卷边的现象(图1)。

图1 锰胁迫下盐肤木叶片形态的变化Fig.1 Morphology changes of R. chinensis leaves under Mn2+ stress
表1显示,盐肤木生物量随Mn2+浓度升高呈先增加后下降的趋势。其中,盐肤木地上部分干重在不同Mn2+浓度之间差异不显著;地下部分干重和总干重在Mn2+浓度为5 mmol·L-1时最高,分别比CK显著增加42.72%和31.73%,其余处理均与CK无显著差异;根冠比在Mn2+浓度为1 mmol·L-1时最高,此时比CK增加13.32%,但各浓度胁迫处理与CK之间均无显著差异(P>0.05)。这说明锰胁迫下盐肤木生物量有下降的趋势但没有表现出明显的毒害效应,表明其对高浓度锰具有一定的耐性。

表1 锰胁迫下盐肤木单株生物量的变化
2.2 锰胁迫对盐肤木叶片生理响应的影响
2.2.1 光合色素含量盐肤木叶中叶绿素a、叶绿素b和类胡萝卜素含量均随Mn2+浓度升高呈先升后降的变化趋势,并均在Mn2+浓度为5 mmol·L-1时最高,此时分别比CK增加15.38%、7.33%和27.04%,且均在20 mmol·L-1Mn2+时最低,分别比CK降低12.19%、13.33%和10.24%,但各浓度胁迫处理大多与CK无显著性差异(图2,Ⅰ)。同时,盐肤木叶中叶绿素a/b也在不同Mn2+浓度处理下无显著变化(图2,Ⅱ)。这说明各浓度锰胁迫对盐肤木叶中光合色素含量无显著影响,光合作用仍然能够正常进行。
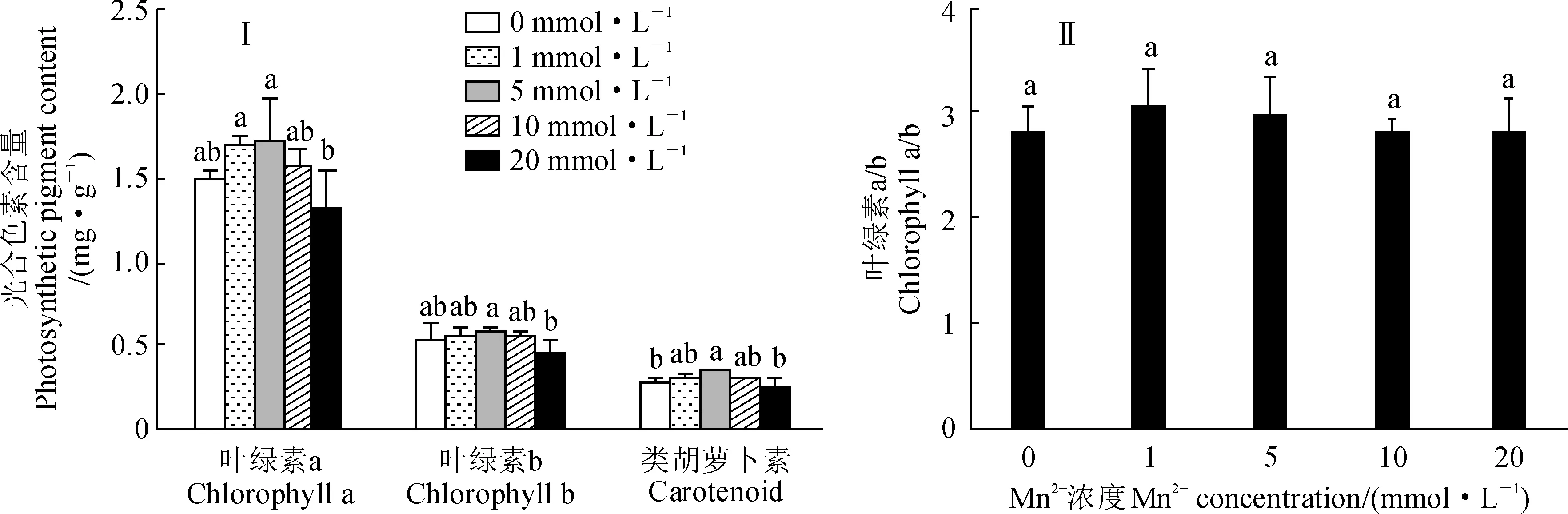
小写字母表示不同浓度间差异显著(0.05),下同图2 锰胁迫下盐肤木幼苗叶中光合色素含量及叶绿素a/b的变化Different normal letters indicate significant differene among trecuments at 0.05 level, the same as belowFig.2 Changes of photosynthetic pigment content and chlorophyll a/b in leaves of R. chinensis seedling under Mn2+ stress
2.2.2 渗透调节物含量图3显示,盐肤木叶中可溶性糖含量在Mn2+浓度为1 mmol·L-1时显著低于CK,在5、10、20 mmol·L-1时均显著高于CK,分别是CK的1.98、2.32和1.75倍(P<0.05);其可溶性蛋白含量在各浓度下均不同程度高于CK,并在10、20 mmol·L-1时差异达到显著水平,分别是CK的2.80、2.49倍;其游离脯氨酸含量在1、5 mmol·L-1时均稍低于CK,在10、20 mmol·L-1时显著高于CK,分别是CK的1.85、1.18倍。其中,各渗透调节物含量均在10和20 mmol·L-1Mn2+时比CK显著增加,并在10 mmol·L-1时达到最高。说明盐肤木能够在1~5 mmol·L-1Mn2+条件下正常生长,在10~20 mmol·L-1Mn2+胁迫条件下能够通过积累可溶性糖、可溶性蛋白和游离脯氨酸来有效缓解锰胁迫的伤害,但在浓度为20 mmol·L-1时各渗透调节物含量有降低趋势。

图3 锰胁迫下盐肤木幼苗叶中可溶性糖、可溶性蛋白和游离脯氨酸含量的变化Fig.3 Changes of soluble sugar, soluble protein and free proline contents in leaves of R. chinensis seedling under Mn2+ stress

图4 锰胁迫下盐肤木幼苗叶中超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性变化Fig.4 Changes of the superoxide dismutase (SOD), peroxidase(POD) and catalase(CAT) activities in leaves of R. chinensis seedling under Mn2+ stress
2.2.3 抗氧化物酶活性盐肤木幼苗叶中SOD、POD和CAT活性均随Mn2+浓度升高呈先增加后下降的趋势(图4)。其中,叶片SOD活性在Mn2+浓度为1~20 mmol·L-1时均显著高于CK,是CK的1.27~1.44倍,并在10 mmol·L-1时最高;叶片POD和CAT活性均在5~20 mmol·L-1时显著高于CK,分别是CK的2.12~3.15倍和1.81~3.40倍,并分别在5和10 mmol·L-1时达到最高。说明在1~10 mmol·L-1Mn2+胁迫下盐肤木能够通过提高抗氧化物酶活性来抵抗逆境,但当Mn2+浓度达到20 mmol·L-1时部分抗氧化物酶活性有降低趋势。
2.2.4 丙二醛含量盐肤木叶中MDA含量随Mn2+浓度升高呈增加的趋势(图5)。其中,叶片MDA含量在Mn2+浓度为1~5 mmol·L-1时均与CK无显著差异,在20 mmol·L-1时则比CK显著增加(P<0.05);在Mn2+浓度为5、10和20 mmol·L-1时,MDA含量分别是CK的1.45、1.89和2.30倍。说明当Mn2+浓度达到10 mmol·L-1后,盐肤木受到一定程度的损伤,叶片细胞膜脂过氧化,导致盐肤木体内的MDA含量增加。

图5 锰胁迫下盐肤木幼苗叶中MDA含量变化Fig.5 Changes of MDA content in leaves of R. chinensis seedling under Mn2+ stress
2.3 锰胁迫对盐肤木富集特征的影响
2.3.1 锰含量盐肤木幼苗地上部分、地下部分锰含量以及总锰含量均随Mn2+浓度升高呈逐渐增加的趋势,且各浓度锰胁迫处理均显著高于CK,分别为CK的12.93~60.30倍、9.20~24.65倍和11.10~40.51倍(图6)。其中,Mn2+浓度为20 mmol·L-1时,盐肤木幼苗地上部分、地下部分以及总锰含量分别为3 116.88、3 709.97和3 316.01 mg·kg-1。
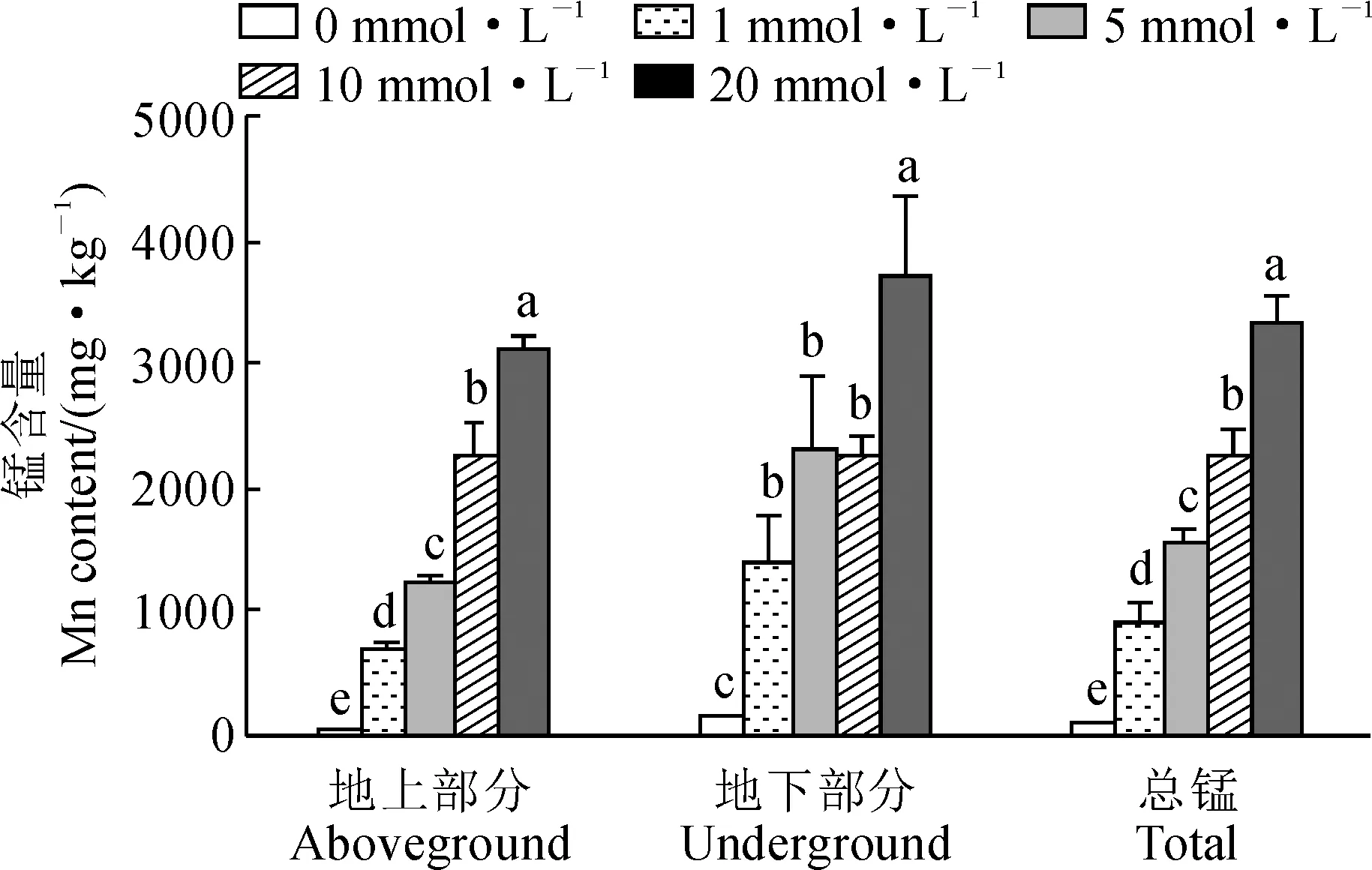
图6 锰胁迫下盐肤木各部位锰含量的变化Fig.6 Changes of Mn content in parts of R. chinensis plant under Mn2+ stress
2.3.2 生物富集系数和转运系数盐肤木幼苗锰生物富集系数随Mn2+浓度升高呈逐渐大幅下降的趋势,且各胁迫处理均显著低于CK;Mn2+浓度为20 mmol·L-1处理下时,富集系数最低为4.02;同时,锰转运系数随Mn2+浓度升高呈逐渐增加的趋势,除1 mmol·L-1浓度处理外均与CK差异显著,但各Mn2+浓度处理的转运系数总体上小于1(表2)。这说明盐肤木在高浓度锰胁迫下对于Mn2+具有较强的富集与转运能力,其锰积累部位主要为地下部分。

表2 锰胁迫下盐肤木富集系数和转运系数
3 讨 论
3.1 锰胁迫条件下盐肤木幼苗生长情况
植物叶片能够表现出对锰毒性响应最直观的变化。在本研究高浓度锰胁迫下,盐肤木叶片出现褐色斑点、叶边缘卷曲萎蔫的现象。Blamey等发现在施加30 mmol·L-1锰胁迫时,白羽扇豆(Lupinusalbus)、窄叶羽扇豆(Lupinusangustifolius)等4种植物叶柄和叶片上有明显的黑棕色斑点,叶片数量减少,在叶片坏死区有大量的锰积累[19]。Führs等同样发现植物大量积累锰会导致其叶片出现褐色斑点、幼叶变形等中毒症状[20]。植物锰中毒的典型表现是在植物老叶上出现褐色斑点,随后是黄化、坏死和叶片脱落,褐色斑点是植物细胞壁中氧化锰和氧化酚的局部积累,尤其是表皮[21]。这种坏死的褐斑被作为植物受到锰毒害作用的标志[22]。
植物生长状况能够综合反映出植物对锰胁迫环境的适应能力。本研究中,盐肤木干重、根冠比在1、5 mmol·L-1Mn2+处理下比CK增加,而当Mn2+浓度为20 mmol·L-1时生物量比CK有所降低,说明在一定程度Mn2+有利于盐肤木的生长。余轲等在对青葙(Celosiaargentea)[23]的锰耐性和富集特征研究中同样也发现低浓度锰会促进青葙生长以及生物量增加的现象;酸模叶蓼(Polygonumlapathifolium)[24]总生物量和株高也随着Mn2+浓度的增加而增加。这是由于锰作为植物生长的必需元素,参与多个代谢过程,适量的锰能促进植物的生长,提高生物量。但由于多种金属转运蛋白分子在植物细胞中具有转运Mn2+的能力,Mn2+具有较强的结合能力,过量的锰使得植物吸收Ca2+、Mg2+、Fe2+等其他营养元素的能力受到影响[25-26]。这导致高浓度锰胁迫下植物生长受到抑制,表现出生物量减少、生长迟缓、植株矮小等现象[27]。
3.2 锰胁迫条件下盐肤木幼苗的生理生化特征
锰在光合作用和叶绿素合成中起着重要作用[28]。本研究结果表明,在1、5 mmol·L-1Mn2+处理下盐肤木叶片叶绿素a、叶绿素b、类胡萝卜素含量有增加的趋势。在本研究最高Mn2+浓度(20 mmol·L-1)处理下,盐肤木叶绿素含量有所下降,但与CK之间没有显著差异,各处理的叶绿素a/b则均没有显著变化。有研究表明,在锰胁迫条件下,柚(Citrusgrandis)[29]叶片中的叶绿素含量没有受较大的影响;各锰浓度下水稻(Oryzasativa)[30]叶片叶绿素a/b没有显著的变化;耐性较强的菠菜(Spinaciaoleracea)品种在海水胁迫下光合含量变化幅度较小[31]。综上所述,高浓度的锰胁迫会阻碍对锰敏感型植物的叶绿素合成,从而影响植物光合作用[32],但对于具有一定锰耐受性植物的叶绿素含量则没有明显的抑制作用。本研究表明,盐肤木幼苗在较高的锰胁迫下叶绿素含量下降幅度较小,说明其具有较高的锰耐受性,从而能够保持其相对正常的光合能力。
渗透调节是植物应对逆境的一种重要机制。在植物遭受逆境胁迫时都会直接或者间接地造成水分缺失,此时为了对抗外界的不利环境,植物会迅速产生并积累大量的可溶性糖、可溶性蛋白、游离脯氨酸等渗透调节物质,来保持细胞内水分平衡,从而减轻渗透失水而造成的胁迫损害,以维持细胞正常生命代谢活动[4]。随着Mn2+浓度的升高,本研究中盐肤木叶片中可溶性糖、可溶性蛋白和游离脯氨酸大量积累,当Mn2+浓度为20 mmol·L-1时,可溶性糖、可溶性蛋白和游离脯氨酸含量与10 mmol·L-1处理下相比虽显著下降但仍显著高于1、5 mmol·L-1处理。这与锰胁迫下黄花草(Cleomeviscosa)[33]、小飞蓬(Conyzacanadensis)、杠板归(Polygonumperfoliatum)、美洲商陆[34]叶片渗透调节物质含量变化趋势相同,也与构树(Broussonetiapapyrifera)[35]渗透调节物质含量的变化趋势一致。其原因是低浓度的锰胁迫能够促进渗透调节物质的合成,从而通过提高其含量来增强盐肤木在逆境下的耐受性;而过高浓度的锰胁迫会破坏叶片细胞结构,阻碍了渗透调节物质的合成,使渗透调节失衡,对盐肤木产生危害。
3.3 锰胁迫条件下盐肤木幼苗的富集特征
除本身的生长、生理状况外,植物对重金属的富集特征是决定其是否适用于植物修复技术的另一主要因素。随着Mn2+浓度的升高,本研究中盐肤木地上部分、地下部分锰含量显著增加。同样,在锰胁迫条件下,垂序商陆[40]各器官中锰含量、冬青(Ilexparaguariensis)[41]叶片中锰含量也随Mn2+浓度的增加而增加。这是因为植物对于锰的吸收与其他营养元素不同,锰转运蛋白基因的表达通常不受外部锰浓度的影响而下调,这使得植物能在高锰浓度下积累大量的锰[42]。因此,盐肤木对锰具有一定的富集能力。
在本研究中,盐肤木锰生物富集系数随Mn2+浓度升高呈下降的趋势,且其值均大于1。这与锰胁迫下短毛蓼[8]、青葙[23]富集系数变化规律一致。同时,盐肤木锰转运系数则随Mn2+浓度升高呈现出增加的趋势。这说明Mn2+浓度的增加促进了盐肤木体内锰的迁移,锰被转运至地上部分。但是,整体上转运系数小于1,又表明盐肤木根部锰含量高于地上部分锰含量,锰主要积累于盐肤木根部。同样,重金属耐性植物木贼[9]根部铅含量明显高于地上部分铅含量,芒(Miscanthussinensis)和乌蕨(Stenolomachusanum)[43]根部对锰的吸收能力大于地上部分。这类植物在根部囤积重金属,以此来减轻重金属胁迫对地上部分的伤害。可见,盐肤木属于锰根部囤积型植物。
4 结 论
随着环境中Mn2+浓度升高,盐肤木幼苗生物量、叶绿素含量、渗透调节物质含量以及抗氧化物酶活性均呈先增加后下降的趋势,MDA含量则显著增加。同时,随着环境中Mn2+浓度的升高,盐肤木地上部分、地下部分锰含量增加。盐肤木生物富集系数随Mn2+浓度的升高而降低,且在各种Mn2+浓度胁迫处理下均大于1;其转运系数随Mn2+浓度升高却呈增加的趋势,且总体小于1,该植物属于锰根部囤积型耐重金属植物。盐肤木具有一定的锰富集能力和耐受性,其主要通过合成大量渗透调节物质、增强抗氧化物酶活性以及在根部囤积锰的方式来减轻锰的毒害作用。

