由松针制取三种叶绿素钠盐及其稳定性的研究
占汝真,武 健,付成钰,方丽颖,王 吉,欧阳杰,*
(1.北京林业大学生物科学与技术学院食品科学与工程系,北京100083;2.林业食品加工与安全北京市重点实验室(北京林业大学),北京100083)
叶绿素是一种从绿叶中提取的天然食用色素,其安全无毒,除被广泛用作食品、化妆品的着色剂外,还具有抗诱变、抗氧化等活性[1]。但是,叶绿素不稳定且不溶于水,所以常常将其制成叶绿素铜钠盐以提高其稳定性。叶绿素铜钠盐是联合国粮农组织、世界卫生组织(FAO/WHO)和我国食品添加剂标准委员会批准使用的天然绿色素,也是我国食品工业中唯一允许使用的绿色素[2-4]。但基于Cu2+的毒性,如果能将叶绿素制成其他金属盐,安全性将更高。锌是人体所必需的微量元素,是体内多种酶的组成部分,参与机体内的各种新陈代谢,若将叶绿素改造为叶绿素锌钠盐,可以使其兼具色素和锌制剂的双重作用[5]。同样,制备出叶绿素铁钠,也可作为一种具有补铁保健功能的天然绿色色素。叶绿素铁钠具有抗菌、抗病毒、抗过敏和促进组织再生等作用,是一种良好的造血细胞复合剂,对各种原因引起的白细胞减少症及各种贫血有治疗作用[6-7]。
迄今为止,从毛竹、红松、榆树等叶子制备叶绿素锌钠和叶绿素铁钠已经有了一定的研究,还有人利用蚕砂制备叶绿素铁钠,其叶绿素含量约为1%[8],但蚕砂只分布于南方养蚕的地区。我国松树资源分布广泛,松针叶绿素具有抗菌、止血、降血压、刺激细胞生成和清除体内超氧自由基等作用[9-10]。
此外,国内外有部分针对叶绿素钠盐稳定性的研究,但将三者稳定性进行对比的较少,且采用的方法是在实验处理一段时间后进行一次测定,无法确定三种叶绿素钠盐稳定性随处理时间延长产生的影响。因此,本研究以松针为原料制备叶绿素铜钠、叶绿素锌钠和叶绿素铁钠,并比较它们对光、热、pH和氧化剂在一段时间内的稳定性。
1 材料与方法
1.1 材料与仪器
松针 采摘于北京地区的马尾松;无水乙醇、氢氧化钠、石油醚、硫酸、盐酸、丙酮、硫酸铜、硫酸锌、硫酸亚铁 均为分析纯,北京化学试剂公司。
UV2550紫外可见分光光度计 日本岛津公司。
1.2 实验方法
1.2.1 叶绿素铜钠、叶绿素锌钠和叶绿素铁钠的制取
1.2.1.1 松针的预处理 将新鲜松针用水洗净风干,再用60℃热风烘干至含水率12%左右;除去发黄的松针,粉碎后过60目筛,即得松针粉,备用。
1.2.1.2 叶绿素的萃取 称取100g松针粉,将其置于1000mL烧杯中,加入450mL无水乙醇和50mL水拌匀,静置12h,再用闪式提取器提取300s,抽滤;把滤液转入蒸馏装置浓缩,55℃减压蒸馏,蒸至原滤液体积的1/3,即得叶绿素软膏,其主要成分有叶绿素、β-胡萝卜素、叶黄素等。
1.2.1.3 皂化分离提纯叶绿酸钠 向叶绿素软膏中加入0.3mol/L NaOH调节pH至10~11,65℃皂化40min,稍冷却转入分液漏斗中,加入等体积的石油醚,激烈振摇,以萃取其中不皂化物。静止分层,上层的石油醚层主要含未皂化的叶黄素、β-胡萝卜素等,下层为已转变的叶绿素钠盐——叶绿酸钠。
1.2.1.4 叶绿素铜钠、锌钠和铁钠的制备 将上述叶绿素钠盐用0.5mol/L HCl调节pH为6.0~6.5,65℃搅拌1h,此时生成脱镁叶绿素钠。再调节pH为2.0~3.0,搅拌反应1h。再滴加20g/100mL CuSO4溶液,逐渐析出结晶;当整体颜色由黄绿色变成墨绿色时,再多加2~3mL CuSO4液体,结晶1h,过滤、水洗、干燥得叶绿素铜酸[11]。将上述叶绿素铜酸溶于适量丙酮中,加入5%NaOH-乙醇溶液,随着溶液的加入叶绿素铜酸逐渐溶解,当调至pH=10.0时,又开始变稠,析出结晶,调到pH=11.0时结晶1h,过滤、用丙酮洗涤三次、真空干燥得蓝黑色的叶绿素铜钠结晶[12]。分别用ZnSO4和FeSO4代替CuSO4,以同样的方法分别制备得到墨绿色有金属光泽的叶绿素锌钠和墨色有金属光泽叶绿素铁钠结晶[13-14]。
1.2.2 紫外-可见吸收图谱的测定 将按上述制得的叶绿素铜钠、叶绿素锌钠、叶绿素铁钠盐加蒸馏水配成一定浓度溶液,以蒸馏水作参比,分别在200~700nm波段进行全波长扫描。
1.2.3 叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的稳定性研究 分别将叶绿素铜钠、叶绿素锌钠、叶绿素铁钠配制成1×10-4g/mL的溶液,分别:a.置于黑暗、实验室自然光(500Lux)和灯箱(4000Lux)中;b.置于50、60、70、80℃下;c.各用HCl和NaOH调节成pH为3.0、5.0、7.0、10.5和12.5;d.以H2O2(30%)为氧化剂,配制含有不同质量分数H2O2的叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稀溶液。每隔一定的时间间隔,分别在其最大吸收波长处测吸光度。
保存率(%)=色素溶液不同时间点时在最大吸收波长处测得的吸光值/色素溶液在最大吸收波长处的初始吸光值×100
2 结果与讨论
2.1 从松针制备叶绿素铜钠、叶绿素锌钠和叶绿素铁钠
以松针为原料,经过叶绿素提取、皂化、酸化、铜代(或锌代、铁代)、加碱成盐等步骤,可分别制得叶绿素铜钠、叶绿素锌钠和叶绿素铁钠。其中,叶绿素铜钠为墨绿色具有金属光泽的结晶,以松针原料计产品得率为1.99%,其水溶液呈深绿色;叶绿素锌钠为绿色具有金属光泽的结晶,得率为1.74%,水溶液呈翠绿色;叶绿素铁钠为黄褐色具有金属光泽的结晶,得率为2.24%,水溶液呈茶黄色。
2.2 叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的紫外-可见吸收光谱

图1 紫外-可见光吸收图谱Fig.1 UV-Vis absorption spectra
叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的紫外-可见吸收光谱如图1所示。叶绿素铜钠的最大吸收波长为402nm,叶绿素锌钠的最大吸收波长为415nm,叶绿素铁钠在405nm处有一微弱吸收峰。文献中,叶绿素铜钠的最大吸收波长为405nm和630nm[15],叶绿素锌钠的最大吸收波长为410nm[16],叶绿素铁钠的最大吸收波长为405nm,三者的最大吸收波长均与文献中的较为一致[17]。
2.3 光照对叶绿素铜钠、叶绿素锌钠和叶绿素铁钠稳定性的影响
将叶绿素铜钠、叶绿素锌钠、叶绿素铁钠放置在不同光照条件下检查其稳定性,结果见图2。叶绿素铜钠、叶绿素锌钠、叶绿素铁钠在黑暗条件下稳定性较好,10h后保存率均在80%以上;在室内自然光和强光照射下,三者均加快分解,其中叶绿素铜钠的稳定性最好,自然光照10h后保存率为78.76%,强光照射10h后保存率为73.24%。叶绿素锌钠、叶绿素铁钠的光稳定性明显不如叶绿素铜钠。
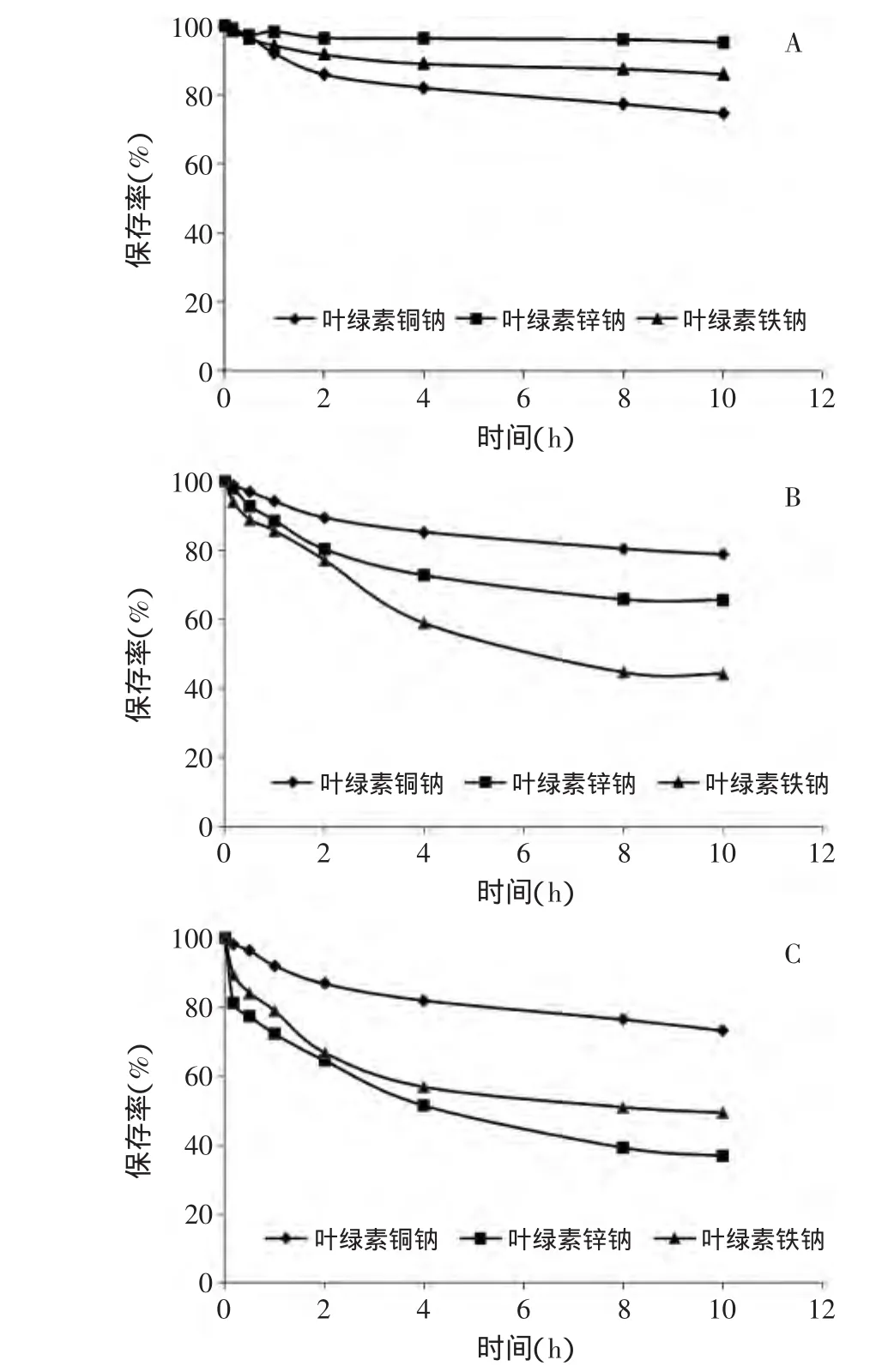
图2 不同光照条件对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响Fig.2 Effect of light irradiation on the stability of sodium copper chlorophyllin,sodium zinc chlorophyllin and sodium iron chlorophyllin
2.4 温度对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响
将叶绿素铜钠、叶绿素锌钠、叶绿素铁钠放置在不同温度条件下检查其稳定性,结果见图3。叶绿素铜钠、叶绿素锌钠、叶绿素铁钠在50℃下稳定性较好,其中叶绿素锌钠的稳定性最好,12h后保存率为88.99%,叶绿素铜钠12h后的保存率为80.49%。在70℃以下叶绿素锌钠和叶绿素铜钠的保存率均在80%以上。叶绿素铁钠对温度的稳定性较差,70℃条件下12h后保存率只有57.40%。超过80℃后,三者均分解加剧,溶液褪色[18-19]。

图3 不同温度对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响Fig.3 Effect of heat treatment on the stability of sodium copper chlorophyllin,sodium zinc chlorophyllin and sodium iron chlorophyllin
2.5 pH对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响
叶绿素铜钠、叶绿素锌钠、叶绿素铁钠配制成一定浓度溶液后为碱性溶液,再将叶绿素铜钠、叶绿素锌钠、叶绿素铁钠配制成不同pH溶液检查其稳定性,结果见图4。pH的变化会引起叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的异构化。对于叶绿素铜钠、叶绿素锌钠、叶绿素铁钠来说pH越高,异构化后得到的物质吸光值越大,在酸性条件下,溶液的吸光值降低,且酸度越高,溶液的颜色越浅,吸光值越小。

图4 不同pH对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响Fig.4 Effect of different pH on the stability of sodium copper chlorophyllin,sodium zinc chlorophyllin,and sodium iron chlorophyllin
2.6 不同浓度氧化剂对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响
将叶绿素铜钠、叶绿素锌钠、叶绿素铁钠配制成含有不同浓度H2O2的溶液,检查其稳定性,结果见图5。H2O2会使叶绿素铜钠、叶绿素锌钠、叶绿素铁钠分解,且浓度越高分解越剧烈。在不同浓度情况下,叶绿素铁钠相对较为稳定,叶绿素铜钠稳定性较差。当H2O2的溶液浓度为0.02%时,8h后叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的保存率均在50%左右;当H2O2的溶液浓度为0.1%时,8h后只有叶绿素铁钠的保存率大于50%;当H2O2的溶液浓度为0.5%时,8h后叶绿素铁钠的保存率为46.21%,而叶绿素铜钠只有21.17%。
3 结论
以松针为原料制备叶绿素铜钠、叶绿素锌钠、叶绿素铁钠的得率分别为1.99%、1.74%和2.24%。相比之下,叶绿素铜钠的光稳定性较好,叶绿素锌钠对温度的稳定性好,叶绿素铁钠对氧化稳定性较好。从颜色来考虑,叶绿素锌钠的水溶液颜色为翠绿色,与叶绿素铜钠的颜色相差不大,且其具有色素和锌剂双重作用,因此若将其应用作食品添加剂,将具有广阔的发展前景。
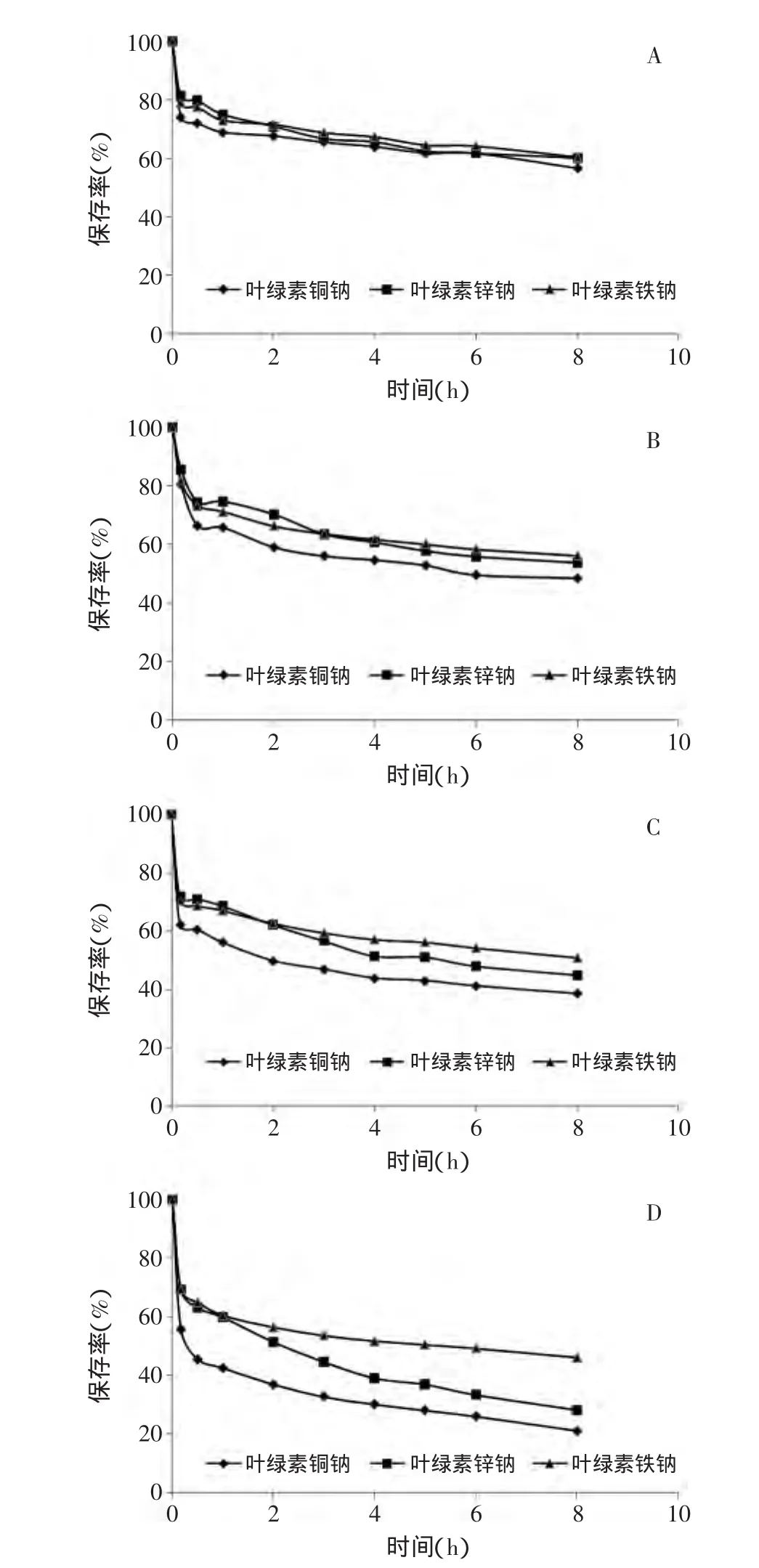
图5 不同浓度H2O2对叶绿素铜钠、叶绿素锌钠、叶绿素铁钠稳定性的影响Fig.5 Effect of H2O2on the stability of sodium copper chlorophyllin,sodium zinc chlorophyllin and sodium iron chlorophyllin
[1]Pimentel E,Cruces M,Zimmering S.A study of the inhibition/promotion effects of sodium-copper chlorophyllin(SCC)-mediated mutagenesis in somatic cells of Drosophila[J].Mutation Research/Genetic Toxicology and Environmental Mutagenesis,2011,722(1):52-55.
[2]杨立荣,胡斌,韩兆熊,等.叶绿素铜钠盐的制备[J].浙江大学学报,1998,32(6):745-752.
[3]Tadashi Kunieda,Toyoki Amano,Yuzo Shioi.Search for chlorophyll degradation enzyme,Mg-chelatase,from extracts of chenopodium album with native and artificial substrates[J].Plant Science,2005,169:177-183.
[4]Simon D,Hellwell S.Extraction and quantification of chlorophyll a from freshwater green algae[J].Water Res,1998,32(7):2220-2223.
[5]王效山.新型食品添加剂叶绿素锌研究[J].食品科学,1995(9):48-49.
[6]向纪明,王琳,潘晓辉,等.蚕沙中叶绿酸铜钠、叶绿酸铁钠的提制及应用[J].安康师专学报,1999,11(3):41-42.
[7]迟翠翠,翟二林,李春燕,等.芹菜叶绿素铁钠与其他补血药物功效的比较研究[J].食品科学,2013,34(7):289-292.
[8]胡丰林.松针的利用价值分析[J].生物学杂志,1996(2):25.
[9]刘晓庚,陈梅梅.我国松针的开发利用研究进展[J].粮食与食品工业,2003(3):25-29.
[10]郑光耀,何玲,薄采颖,等.松针叶绿素-胡萝卜素软膏体外清除自由基及体内抗氧化作用的研究[J].时珍国医国药,2013,24(4):815-817.
[11]Owen R Fennema.Food Chemistry[M].Beijing:Light industry Press,2003:552-557.
[12]张海英,蒋申蓉,朱嘉玉,等.荷叶叶绿素铜钠盐的制备和稳定性研究[J].内江师范学院学报,2010,25(10):55-57.
[13]曾家豫,武伟国,孔维宝,等.红三叶叶绿素锌钠的制备及其稳定性研究[J].西北师范大学学报,2012,48(6):82-88.
[14]李祥,文星,房媛,等.叶绿素铁钠盐的制备[J].食品与发酵工业,2012,38(4):77-81.
[15]邓文灿,朱僚辉.松针叶绿素铜钠的制备[J].山东化工,2001,30(4):7-8.
[16]游秀花,林瑞余,蔡碧琼,等.杉木叶绿素锌钠的制备工艺及稳定性[J].福建林学院学报,2007,27(2):126-129.
[17]王立娟,李坚,叶结旺.松针叶绿素铁钠的制备及稳定性研究[J].林业科技,2004,29(2):43-45.
[18]王修东,楼飞群,贾天亮,等.叶绿素铜钠稳定性影响因素研究[J].中国药业,2012,21(14):20-21.
[19]Ferruzzi M G,Schwartz S J.Thermal degradation of commercial grade sodium copper-chlorophyllin[J].Journal of Agricultural and Food Chemistry,2005,53(18):7098-7102.

