原发性纤毛运动障碍患儿及其父母焦虑抑郁影响因素分析
林雅丽 郭卓瑶 王立波 钱莉玲
原发性纤毛运动障碍(PCD)是一种纤毛数量、结构或摆动功能异常的罕见病,临床主要表现为反复呼吸道感染、鼻窦炎、中耳炎、内脏排布异常、不孕不育、支气管扩张等,其发生率为 1/20 000~1/15 000,无明显性别差异[1-3]。
慢性呼吸系统疾病[如囊性纤维化(CF)、非囊性支气管扩张等]患儿及其父母焦虑、抑郁的发生率较高,对治疗依从性、疾病管理、患儿生活质量及疾病转归等存在负面影响[4-6]。CF人群焦虑、抑郁症状发生率为正常人群的2~3倍[7]。欧洲CF协会专家共同制定了CF国际心理健康指南,建议对CF患儿及其照顾者进行年度心理健康评估和治疗[8]。而同样为黏液纤毛病的PCD,目前研究主要集中于临床表型、诊断过程和致病基因[9-10],心理状况相关的研究很少。本研究主要探讨我国PCD患儿及其父母焦虑、抑郁的现状及影响因素。
1 方法
1.1 研究设计 病例对照研究。以确诊的PCD患儿及家长分别为PCD儿童组和PCD父母组,以确诊的哮喘患儿及家长分别为哮喘儿童组和哮喘父母组,以健康儿童及家长分别为对照儿童组和对照父母组。以儿童焦虑性情绪障碍筛查表(SCARED)、儿童抑郁量表(CDI)及焦虑自评量表(SAS)、流调用抑郁自评量表(CES-D)作为评价工具,评价3组儿童及其父母的焦虑和抑郁状况,并分析影响因素。
1.2 诊断标准
1.2.1 PCD诊断标准 符合以下PCD临床特征中至少2项:①足月儿发生不明原因的新生儿呼吸窘迫综合征,② 6月龄之前开始全年持续性的季节性咳嗽、咳痰且抗感染效果不佳,③ 出生后不久(通常6个月内)出现全年持续性非季节性鼻窦炎,且抗感染治疗效果不佳,④内脏排布异常;结合以下任1项阳性结果可确诊为PCD:①典型的纤毛超微结构异常,包括外动力臂缺失,内外动力臂联合缺失、内动力臂缺失并伴有微管转位,②有PCD相关基因中双等位基因致病性突变[11]。
1.2.2 哮喘诊断标准 依据呼吸道症状、体征和肺功能检查证实存在可逆的呼气气流受限,并排除引起相关症状的其他疾病。临床表现不典型者,应至少具备以下1项:①证实存在可逆性气流受限,②支气管激发试验阳性,③最大呼气流量(PEF)每日变异率 (连续监测2周)≥13%[12]。
1.3 纳入和排除标准
1.3.1 入组儿童共同纳入和排除标准 同时满足以下条件者纳入:①2020年3月至2022年1月于复旦大学附属儿科医院(我院)就诊或体检的儿童,②年龄>7岁(焦虑和抑郁量表年龄最低要求),③口头知情同意参与问卷调查。符合以下任1项排除:①合并其他慢性疾病(包括CF、糖尿病、慢性肾病、肿瘤等)或严重急性躯体疾病(如急性心衰、急性阑尾炎等),②智力低下,③近2周有突发负性生活事件,④有精神疾病史(如焦虑、抑郁、双相情感障碍等),⑤有精神类药物、可致幻觉等药物使用史。
1.3.2 3组儿童分别纳入标准 除符合入组儿童共同纳入和排除标准外,PCD组还需符合PCD确诊标准;哮喘组还需符合哮喘诊断且目前药物控制良好或部分控制;健康组为健康体检且结果正常儿童。
1.3.3 3组儿童父母纳入和排除标准 同时满足以下条件者纳入:①父亲和/或母亲入组前至少6个月内是儿童生活起居的主要照顾者,②具备正常沟通和读写能力,③口头知情同意参与问卷调查。同时≤7岁PCD儿童的父母也纳入。符合以下任意1项排除:①智力低下,②近2周有突发负性生活事件,③有精神疾病史(如焦虑、抑郁、双相情感障碍等),④有精神类药物、可致幻觉等药物使用史。
1.4 测量工具 本文儿童和成人焦虑、抑郁、负担量表均为自评量表。
1.4.1 儿童测量工具 ①SCARED:用于6~18岁儿童、青少年,包含惊恐、广泛性焦虑、分离性焦虑、社交恐惧、学校恐惧5个因子,评估项目41项,总分≥23分为有焦虑症状,中国标准化常模信度0.88,效度良好[13]。②CDI:用于7~17岁儿童、青少年,包含快感缺乏、负面情绪、低自尊、效能低下、人际问题5个因子,评估项目27 项,总分≥19分为有抑郁症状,中国标准化常模信度0.85,效度良好[14]。
1.4.2 成人测量工具 ①SAS:评估成人焦虑情绪,包括正向评分15项及反向评分5项,标准分<50分为正常,~59分为轻度焦虑,~70分为中度焦虑,≥70分为重度焦虑,中国标准化常模信度0.93,效度良好[15]。②CES-D:评估成人抑郁情绪,共20项,包括4个反向评分项,总分≤15分为无抑郁症状,~19分为可能有抑郁症状,≥20分为肯定有抑郁症状,中国标准化常模信度0.90,效度良好[16]。③Zarit负担量表:评估照顾者照顾负担,共22项,得分越高表示照顾者负担越重,中国标准化常模信度0.87,效度良好[17]。
1.5 测量方法 儿童先后完成SCARED和CES-D 2个量表,成人先后完成SAS、CES-D和Zarit负担3个量表。由1名熟悉本研究测评量表条目及指导语的儿科医生主试、监督并当场回收量表。PCD组儿童来源于我院PCD患儿微信群,于慢性肺部疾病专科门诊就诊后完成测量;哮喘组儿童来源于我院哮喘专科门诊,就诊后完成测量;对照组儿童来源于我院疫苗门诊体检儿童成人测量人群;来源于当天陪同儿童来我院就诊或体检的父母,鼓励父母均填写3个成人量表。
1.6 资料采集 3组父母在完成成人量表测量的同时,完成人口学资料的填写,包括儿童年龄、BMI和有无兄弟姐妹,父母性别、年龄、受教育程度(高中及以下,大学专科及以上)、职业(稳定工作,无业),家庭年收入(≤10万/年,>10万/年),PCD组和哮喘组加填患儿运动频率(每周数次,偶尔或几乎不),近1年住院频率(<1次,≥1次)、是否规律随访(<1次/年,≥1次/年)。从医院门诊电子病历系统中提取PCD患儿第1秒用力呼气量(FEV1)预计百分比、气道护理情况、有无中耳炎、支气管扩张等资料。

2 结果
2.1 一般情况 符合本文PCD组、哮喘组和对照组纳入和排除标准的儿童分别为38例、76例和76名,男女生各占50%。表1显示,3组儿童年龄和有无兄弟姐妹差异无统计学意义,BMI哮喘组和PCD组低于对照组,差异有统计学意义;PCD组FEV1预计百分比(76.1%±15.3%),每天1~2次规律气道护理21例(55.3%),合并支气管扩张11例(29.8%),合并中耳炎30例(78.9%),Zarit得分21.5±11.7。
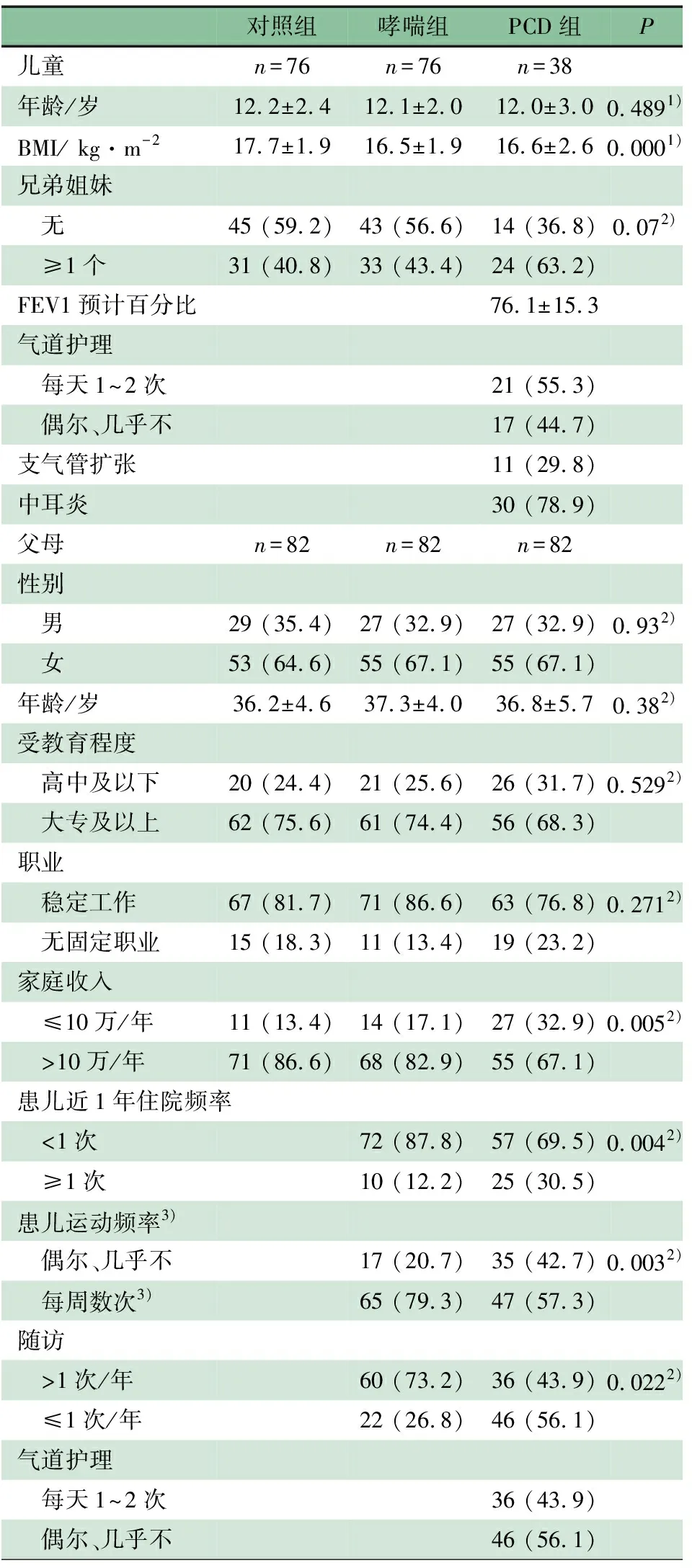
表1 PCD组、哮喘组和对照组儿童及其父母一般资料[n(%)]
符合本文PCD组、哮喘组和对照组纳入和排除标准的父母均为82名。PCD组父亲27名,母亲55名;哮喘组父亲27名,母亲55名;对照组父亲29名,母亲53名。需要说明的是,本文共纳入4~17岁PCD患儿62例,其中38例(7~17岁)符合SCARED和CDI测量年龄要求,其父母43名;4~7岁24名,其父母39名。3组父母性别、年龄、受教育程度、职业差异均无统计学意义,家庭年收入PCD组低于哮喘组和对照组,差异有统计学意义。
2.2 3组儿童CDI、SCARED得分及焦虑、抑郁发生率比较 表2显示,焦虑发生率PCD组高于哮喘组(P=0.048)及对照组(P=0.007),SCARED得分PCD组高于哮喘组(P=0.001)及对照组(P=0.009)。哮喘组与对照组焦虑发生率和SCARED得分差异均无统计学意义,3组儿童CDI得分及抑郁发生率比较差异均无统计学意义。
2.3 3组父母CES-D、SAS得分及焦虑、抑郁发生率比较 表2显示,父母焦虑发生率PCD组高于哮喘组(P=0.033)和对照组(P=0.003)。SAS得分PCD组高于对照组(P=0.000),PCD组与哮喘组差异无统计学意义。父母抑郁发生率PCD组高于哮喘组(P=0.024)和对照组(P=0.013)。CES-D得分PCD组高于哮喘组(P=0.037)和对照组(P=0.001)。父母SAS得分哮喘组高于对照组(P=0.008)。哮喘组与对照组焦虑、抑郁发生率及CES-D得分差异均无统计学意义。
表3显示,82名PCD患儿母亲CES-D评分、SAS评分和Zarit得分均高于父亲,母亲焦虑和抑郁发生率高于父亲,差异有统计学意义。

表2 PCD组、哮喘组和对照组儿童及父母SCARED、CDI、CES-D、SAS
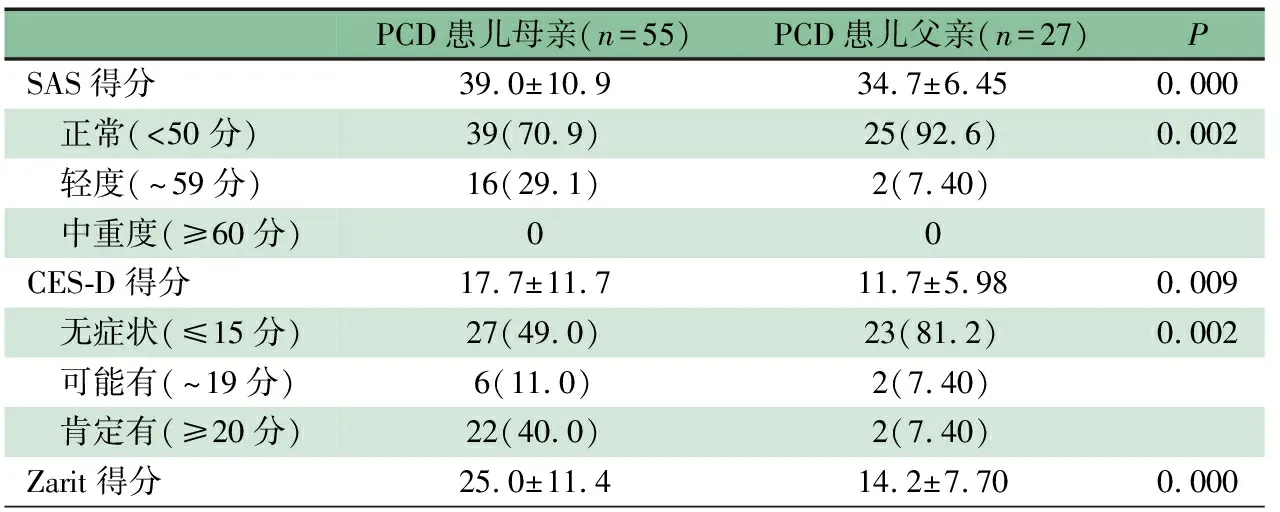
表3 PCD患儿父和母CES-D、SAS、Zarit得分及焦虑、抑郁发生率比较[n(%)]
2.4 PCD患儿及其父母焦虑、抑郁的单因素分析 表4显示,PCD组患儿是否焦虑和抑郁纳入了11个变量,焦虑单因素分析显示,性别、近1年住院<1次、每天1~2次气道护理差异有统计学意义;抑郁单因素分析显示,每天1~2次气道护理差异有统计学意义。PCD患儿父母是否焦虑和抑郁纳入了10个变量,焦虑和抑郁单因素分析显示,性别、近1年住院<1次、每天1~2次气道护理、父/母受教育程度、有稳定职业、Zarit负担量表得分差异均有统计学意义。

表4 PCD患儿及父母焦虑、抑郁的单因素二元Logistic回归分析

续表 无中耳炎-0.0360.9650.965(0.192~4.839)-0.2880.7580.750(0.120~4.691)父母(n=82) 女性1.6350.0395.128(1.085~24.24)1.7860.0035.963(1.821~19.53) 年龄-0.0210.6730.980(0.890~1.078)0.020.6171.020(0.943~1.103) 近1年住院<1次-2.42200.089(0.027~0.297)-2.37200.093(0.031~0.282) 每周数次运动-2.39800.091(0.024~0.350)-2.09100.124(0.045~0.338) 每天1~2次气道护理0.5780.2831.783(0.620~5.123)0.5380.2451.713(0.691~4.247) 每年>1次随访-0.3150.5560.730(0.256~2.083)0.2190.6331.245(0.507~3.057) 大专以上教育程度-2.3220.0010.098(0.030~0.325)-1.9100.148(0.053~0.415) 有稳定职业-3.22400.040(0.011~0.151)-1.6130.0040.199(0.065~0.603) 家庭年收入>10万0.3090.61.362(0.430~4.315)-0.3660.4820.714(0.280~1.823) Zarit负担量表得分高0.1301.139(1.071~1.211)0.10301.108(1.054~1.164)
2.5 PCD患儿及其父母焦虑、抑郁的多因素分析 将表4中P<0.2的因素纳入多因素Logistic回归分析,表5显示,7~17岁PCD患儿,规律气道护理是避免焦虑和抑郁发生的保护因素,男孩较女孩易发生焦虑。4~17岁PCD患儿父母,受教育程度高、有稳定职业、患儿规律运动是避免焦虑发生的保护因素,受教育程度高、患儿近1年住院<1次、患儿规律运动是避免抑郁发生的保护因素,Zarit负担量表得分高是焦虑和抑郁发生的危险因素。
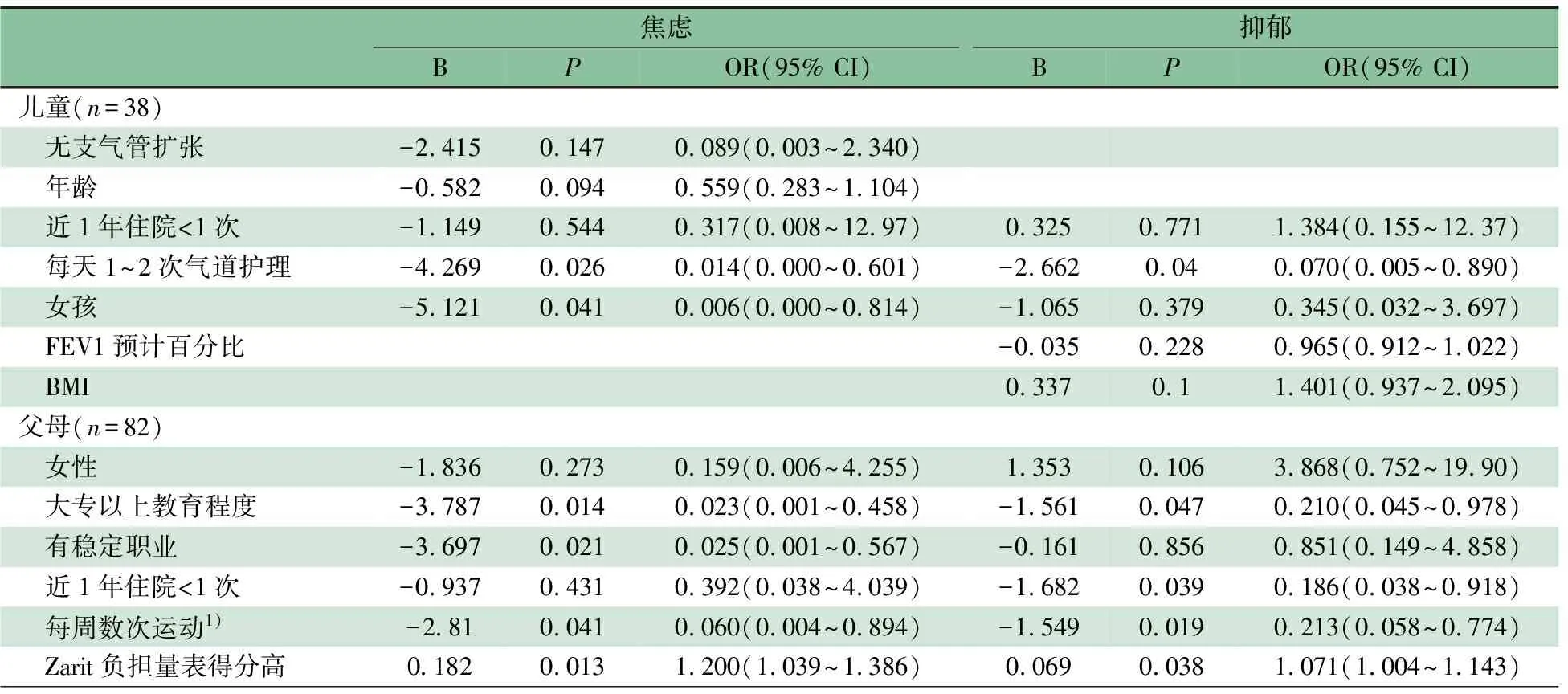
表5 PCD患儿及其父母焦虑、抑郁的多因素二元Logistic回归分析
3 讨论
PCD不仅影响患儿躯体健康,患儿预后的不确定、对病情恶化的恐惧、成年后的生育问题以及公众场所难以控制咳嗽、咳痰的尴尬等还可能影响患儿的心理健康[18,19],降低其生活质量。
Carotenuto等[6]发现,与健康儿童相比,PCD患儿更易焦虑、抑郁。本研究与文献[6]有所不同,一是对照组除了正常儿童以外,还纳入了哮喘患儿,结果显示,PCD儿童组焦虑发生率和SCARED得分不仅高于对照儿童组,也高于哮喘儿童组;二是儿童CDI得分及抑郁发生率PCD组、哮喘组和对照组差异均无统计学意义,说明中国PCD患儿以焦虑情绪为主要表现。目前PCD的主要治疗方法包括气道护理、控制感染等,气道护理包括拍背、体位引流、规律运动及雾化等[1]。本研究显示,对于7~17岁PCD患儿,规律气道护理是避免焦虑和抑郁发生的保护因素,症状的缓解也可以缓解PCD患儿的焦虑和抑郁。缓解心理症状可能带来的改善不仅在心理方面,同时可提高患儿依从性,提高患儿生活质量,有益于疾病管理。本研究中PCD男孩较女孩易发生焦虑,还需更大的样本量予以证实。既往研究提示,慢性呼吸系统疾病患儿焦虑、抑郁情绪与患儿肺功能呈负相关[20-22],本研究中PCD患儿焦虑抑郁与其肺功能无明显关联,可能提示PCD患儿日常活动不受明显影响,也可能是由于未对患儿年龄进行分组。
慢性病患儿父母的心理症状同样会对患儿心理状态产生负面影响[23],心理症状与患儿及其父母较差的依从性有关,较差的依从性一定程度上会减少患儿气道护理频率及气道护理方式,从而可能导致患儿病情加重[24,25]。本研究显示,父母焦虑和抑郁发生率PCD组高于哮喘组和对照组,但哮喘组父母焦虑、CES-D得分和抑郁发生率与对照组差异无统计学意义,与Marieke等[26]研究结果一致。PCD是一种慢性疾病,治疗更耗时、耗力,更加依赖于父母协助。在PCD患儿父亲和母亲的角色中,母亲焦虑、抑郁发生率、CES-D评分、SAS评分均高于父亲,母亲Zarit得分高于父亲,说明母亲承担着PCD患儿更多的生活照护。本文结果显示,PCD患儿父母受教育程度高和规律运动是避免焦虑和抑郁情绪发生的保护因素,父母有稳定职业是避免焦虑情绪发生的保护因素,患儿近1年住院<1次是避免抑郁情绪发生的保护因素。
本研究不足与局限性:①PCD患儿及其父母影响因素OR值及其95%CI宽泛,说明样本量不足;②研究对象主要来源为上海周边地区,PCD患儿及其父母焦虑和抑郁的影响因素也受地域文化和经济影响。

