扶正解毒颗粒对鸡安全性和影响大肠杆菌抗药性的研究
骆延波 张印 胡明 李璐璐 张庆 赵效南 齐静 陈义宝 许晓晖 刘玉庆
摘 要:将1日龄健康雏鸡80只,随机分为四组,每组20只。其中1~3组为试验组,分别在饮水中全程添加推荐剂量1倍(4 g/L)、3倍(12 g/L)和5倍(20 g/L)的扶正解毒颗粒;4组为不用药对照组。试验期8周,每天观察并记录各组鸡的临床体征,每周末称重1次,8周末试验结束时心脏采血测定各组鸡的血液生理生化指标,剖检鸡只,通过组织切片观察各脏器有无变化。从试验组2(即3倍推荐用药剂量组)和不用药对照组鸡只肠道中采集内容物分离大肠杆菌,进行抗药性分析。结果显示,各组试验鸡的行为、采食、粪便性状与空白对照组相比,均未见异常变化。1倍剂量组和3倍剂量组试验鸡的体重均显著高于不用药对照组(P<0.05或P<0.01)和5倍剂量组(P<0.05或P<0.01);而1倍剂量组和3倍剂量组间在各日龄段均无显著差异(P>0.05)。试验各组和不用药对照组鸡只血液生理生化指标红细胞数、血红蛋白、白细胞数、淋巴细胞比例均无显著性差异(P>0.05)。试验各组脏器颜色、形状、大小、位置等均未见异常变化。显微镜观察组织切片,细胞符合正常组织形态和结构特点。大肠杆菌对8种药物的MIC值均未有显著差异(P>0.05)。以上结果表明,扶正解毒颗粒对靶动物鸡无明显不良影响,对大肠杆菌抗药性水平影响不显著。
关键词:扶正解毒颗粒;鸡;血液;生理指标;大肠杆菌;抗药性
中图分类号:S853.7 文献标识码:B文章编号:1673-1085(2022)04-0012-07
扶正解毒颗粒是由《中国兽药典·二部》(2015版)中的扶正解毒散经过剂型改造而制成。按照农业部442号公告发布的《中兽药、天然药物分类及注册资料要求》属于申报四类传统中兽药复方制剂。扶正解毒散具有扶正祛邪、清热解毒之功效,临床上用于鸡传染性法氏囊病的治疗[1-2]。经过剂型改造后,本制剂在临床上主要用于提高鸡的免疫力,与疫苗协同使用提高疫苗抗体水平,并延长抗体在禽类体内的持续作用时间。为了全面评价本制剂在临床上的确切功效,本试验首先通过靶动物安全试验考察受试兽药扶正解毒颗粒用于靶动物鸡的的安全性及安全剂量范围,为临床试验给药方案的制定提供依据。随着我国养殖业的迅速发展,抗生素使用量剧增,在一定程度上造成细菌抗药性程度较高,急需细菌抗药性防控技术[3-7]。研究发现,添加中药在一定程度上减缓细菌抗药性的增加速度,或部分消除抗药性[8-10]。因此,本研究通过添加扶正解毒颗粒观察是否对大肠杆菌抗药性产生影响。
1 材料与方法
1.1 试验材料
1.1.1 试验动物及饲料 1日龄体重相差±5 g的海兰灰蛋鸡雏:购自保定市浔源禽业有限公司,严格按照管理标准进行饲养。饲料:市场购进雏鸡全价饲料。
1.1.2 供试药品及试剂 扶正解毒颗粒:山东明发兽药股份有限公司提供,规格:100 g/袋,含量:1 g,相当于原生药0.5 g。批号:20170901。
1.1.3 试验仪器 OLYMPUS生物显微镜:日本制造。全自动生化分析仪:日本东芝TBA-120FR。电子天平:Precisa 92SM-202A。
1.2 试验方法
1.2.1 试验分组与处理 根据《兽用中药、天然药物临床试验技术指导原则》中对靶动物安全试验的分组要求,从新购进的1日龄雏鸡中选取体重相近、健康活泼的雏鸡80只,随机分为4组,每组20只。其中1~3组为试验组,分别在饮水中全程添加推荐剂量1倍(4 g/L)、3倍(12 g/L)和5倍(2 0g/L)的扶正解毒颗粒;4组为不用药对照组,全程饮用新鲜自来水。试验期8周,每天观察并记录各组鸡的临床体征,每周末称重1次,8周末试验结束时心脏采血测定各组鸡的血液生理生化指标;同时进行剖检,通过组织切片观察各脏器有无变化。在试验开始前以及试验结束时,从试验组2(即3倍推荐用药剂量组)和空白对照且鸡只肠道中采集内容物分离大肠杆菌,并进行抗药性分析。
1.2.2 指标测定方法[11-14] 红细胞总数的测定:采用试管法,即将供检血稀释200倍后,用血细胞计数板计数一定容积内的红细胞数,最后计算出每升血液中的红细胞数。红细胞总数的计算公式:红细胞总数(×1012个/L) = X×10 000。式中的X为5个中方格的红细胞总数。
白细胞总数的测定:采用试管法,即将供检血稀释20倍后,用血细胞计数板计数一定容积内的白细胞数,最后计算出每升血液中的白细胞数。白细胞总数的计算公式:白细胞总数(×109个/L) = X×50×106。式中的X为4个大方格中的白细胞總数。
淋巴细胞比例的测定:用未抗凝血,制作血涂片,姬姆萨染色法染色,采用白细胞分类法对白细胞计数,计算淋巴细胞比例。
血红蛋白含量的测定:采用比色法。红细胞遇酸溶解后会游离出血红蛋白,并被酸化为褐色的酸性血红素,稀释后与标准比色柱比色,即可求得血红蛋白的含量。
最低抑菌浓度(minimum inhibitory concentration, MIC)值测定:根据美国临床和实验室标准协会 (Clinical and Laboratory Standards Institute,CLSI) 建立的标准药敏方法,采用微量肉汤稀释法[15],测定多黏菌素、多西环素、头孢噻呋、庆大霉素、氟苯尼考、恩诺沙星、氨苄西林和新霉素等8种抗生素对这些分离菌株的抗药性水平。
1.3 数据分析
用SPSS软件对数据进行统计分析。
2 试验结果
2.1 扶正解毒颗粒对鸡临床体征的影响
在试验过程中每天观察并记录各组鸡的临床体征,结果发现,各组试验鸡的行为、采食、粪便性状与空白对照组相比, 均未见异常变化。说明扶正解毒颗粒对靶动物鸡的状况无明显不良影响。
2.2 扶正解毒顆粒对鸡体重的影响
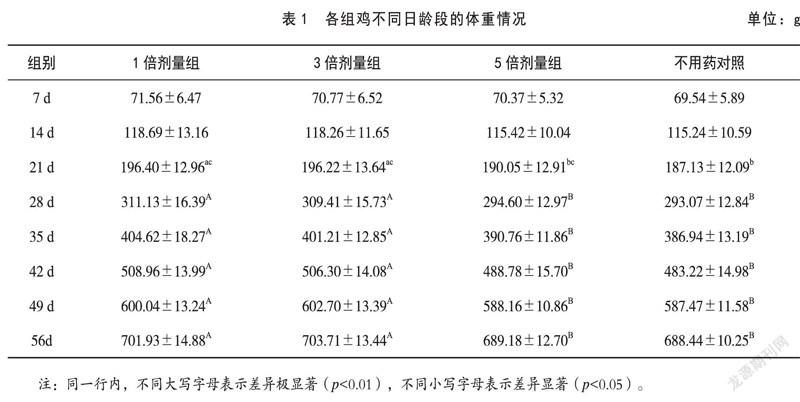
在试验期间每周对各组试验鸡称体重1次, 通过计算每个周末试验鸡的平均体重可知,受试鸡在试验期前2周内各组间的平均体重均无显著性差异(P>0.05)。从21日龄开始到试验结束,1倍剂量组和3倍剂量组试验鸡的体重均显著高于不用药对照组(P<0.05或P<0.01);从28日龄开始到试验结束,1倍剂量组和3倍剂量组试验鸡的体重均显著高于5倍剂量组(P<0.05或P<0.01);而1倍剂量组和3倍剂量组间在各日龄段均无显著差异(P>0.05)。5倍剂量组和对照组间均无显著性差异(P>0.05)。详见表1。
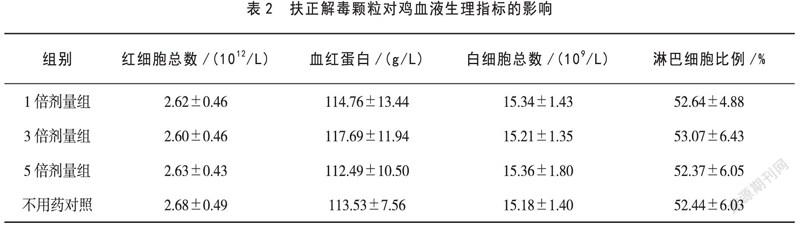
2.3 扶正解毒颗粒液对鸡血液生理指标的影响结果见表2。
由表2可以看出,从1~56日龄在试验鸡饮水中全程添加推荐剂量1倍、3倍、5倍的扶正解毒颗粒,其血液生理指标红细胞数、血红蛋白、白细胞数以及淋巴细胞比例均与不用药对照组无显著性差异(P>0.05),且3个用药剂量组间也均无显著性差异(P>0.05)。
2.4 病理学检查结果
试验结束时对各组雏鸡剖检,进行肉眼病理学观察。通过观察发现,各组脏器颜色、形状、大小、位置等均未见异常变化。
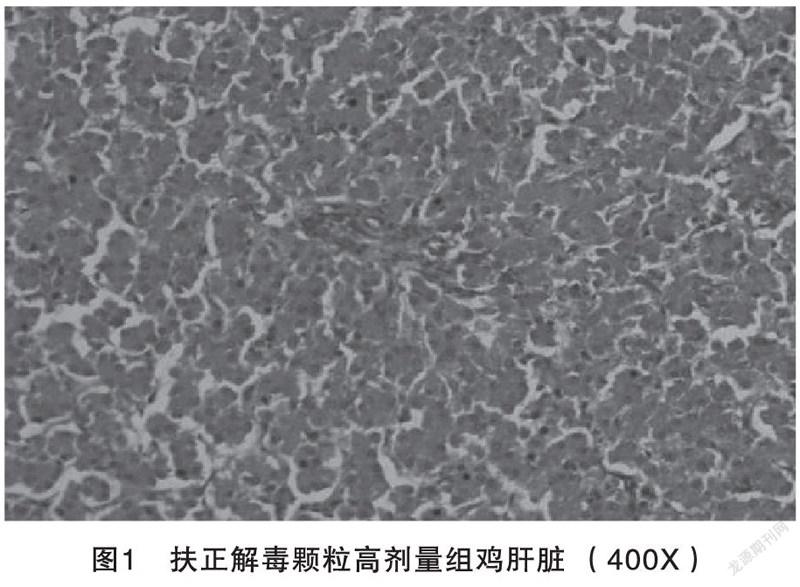
显微镜观察组织切片,可见细胞轮廓完整,排列有序;胞质丰满,细胞核结构清晰,符合正常组织形态和结构特点。可以认定药物对所采集组织无毒性作用(图1~4)。
2.5 大肠杆菌抗药性结果
2.5.1 分离鉴定细菌 在试验前和试验结束时,从3倍推荐剂量组和空白对照组分别分离到大肠杆菌各20株。编号分别为试验1~20号,对照1~20号。
2.5.2 细菌抗药性检测结果 8种抗生素对分离菌株大肠杆菌的MIC值对比见图5。
从图5可以看出,3倍推荐剂量试验组中鸡源大肠杆菌对多黏菌素、多西环素、氟苯尼考、头孢噻呋、氧氟沙星抗药性水平基本上没变化,而对氨苄西林、庆大霉素、新霉素的抗药性水平略有下降,但不显著(P>0.05)。
3 讨论
《中华人民共和国兽药典》(2010版)中收录的扶正解毒散,方中的黄芪有提升免疫力的作用[17-19],淫羊藿有滋补肾阳气功效[16],二者配合使用具有明显的提升免疫力的能力;板蓝根内含有多种抗病毒物质,具有良好的清热解毒、降火功能,可单独使用,也可与其它药配伍使用,对多种病毒引起的疾病都有较好效果。三味药相互组合,在提升免疫力的基础上清热解毒,降低了细菌性疾病和病毒性疾病感染的机会。
本试验以临床推荐剂量的1倍(4 g/L)、3倍(12 g/L)和5倍(20 g/L)在试验鸡饲养的56 d中,全程在饮水中添加扶正解毒颗粒。结果发现,各用药组试验鸡的外在表现、采食、粪便性状与空白对照组相比, 均未见异常变化;各用药组试验鸡的红细胞数、血红蛋白、白细胞数以及淋巴细胞比例均与不用药对照组无显著差异(P>0.05);组织学观察心肝脾肾也均未见异常。表明扶正解毒颗粒对试验鸡无不良影响。
试验过程中,从21日龄开始,1倍剂量组和3倍剂量组试验鸡的体重均显著高于不用药对照组(P<0.05或P<0.01)。这种结果的出现,不是受试药品不良反应的表现,而是由于组方中补气健脾的黄芪增加了鸡群脾胃的运化和吸收功能[16],从而导致其体重比不用药对照组显著增加。
本试验结果中1倍剂量组和3倍剂量组试验鸡的体重较不用药对照组显著增加(P<0.05或P<0.01),而5倍剂量组却与对照组鸡的体重无显著性差异(P> 0.05),从另一个角度进一步证明了实验室临床试验所推荐的4 g/L饮水剂量的合理性。这主要是因为许多中药的药效与用药剂量呈钟罩状关系,即在一定剂量范围内药效随着剂量的增加而显著增大,当用药剂量达到某一定范围时,药效不再随着用药剂量的增加而增大;当用药剂量超过一定范围后,药物的药效随着剂量增加反而降低。本试验结果中,1倍和3倍剂量可显著提高试验鸡的体重,而5倍剂量却没有明显作用,就属这种情况。
本试验添加扶正解毒颗粒,对于鸡肠道大肠杆菌的抗药性水平影响不明显,可能与中药的成分和使用时间较短有关系。尽管扶正解毒颗粒对于大肠杆菌的抗药性影响很小,但可通过提高鸡体免疫力,增强机体抗菌抗病毒的能力,提高生产性能。随着抗生素的广泛使用,导致严重的多重抗药性和药物残留,以至于欧盟以及我国出台了相关法规政策禁止饲料中添加任何抗生素促生长剂,全球范围内抗生素的从严处方化管理和抗药性监测渐成常规[20-21],因此具有免疫功能的扶正解毒颗粒能够抗药抗病毒,是一种很好的抗生素替代产品。
4 结论
靶动物安全试验结果表明,即使在饮水中添加3倍和5倍推荐剂量的受试药品扶正解毒颗粒对靶动物鸡仍无明显不良影响。
3倍推荐剂量的受试药品扶正解毒颗粒在8周作用时间下其对8种药物的抗药性水平未发生显著变化。
参考文献:
[1] 田美湛,张秀英,蒋月,等.扶正解毒散超微粉对人工感染传染性法氏囊病预防试验[J].中国兽医杂志,2007,41(11):31-33.
[2] 欧伟莲,戴光文,江精华.扶正解毒散对 CSF、PRRS、PR与FMD免疫效果试验[J].中兽医学杂志,2019,5:11-12.
[3] LIU YY, WANG Y, WALSH TR,et al.Emergence of plasmid-mediated colistin resistance mechanism MCR-1 in animals and human beings in China:a microbiological and molecular biological study[J].The Lancet Infectious Diseases,2015,16(2):161-168.
[4] KAGEYAMA C,SATO M, SAKAE H,et al.Increase in antibiotic resistant Helicobacter pylori in a University Hospital in Japan[J].Infection and Drug Resistance,2019,12:597-602.
[5] BOULANT E,DAVIN RA,PAGES JM,et al.Efflux pumps,a bacterial resistance mechanism[J].Revue Francophone des Laboratoires,2020,519:39-48.
[6] ENJAMIN H, THANDO N, TANYA C,et al.Exploring the antimicrobial resistance profiles of WHO critical priority list bacterial strains[J].BMC Microbiology,2019,19:303-313.
[7] OSHUA B,ALINA B,ISAAC I. B.Endometritis and Bacteremia With a New Delhi Metallo-Beta-Lactamase 1 (NDM-1)–containing Organism in a Remote Traveler[J].Journal of Obstetrics and Gynaecology Canada, 2019,41(6):753-754.
[8] 杨帆,杨玉荣,赵振升,等. 中草药消除细菌耐药性质粒研究进展[J]. 动物医学进展,2013,34(12):160-164.
[9] 刘昊,王秀东,曹凯捷,等.中药及其有效成分抗细菌耐药性的研究进展[J]. 现代畜牧兽医,2019,9:54-57.
[10] 刘金平,吕世明,谭艾娟,等.中药提取物恢复耐药大肠杆菌对氨基糖苷类药物敏感性的研究[J].畜牧与兽医,2018,50(3):107-111.
[11] 王红梅,钟秀会,尹卫卫,等. 加味扶正解毒散对肉仔鸡生理和生产性能的影响[J].中国家禽,2010,32(9):22-24+28.
[12] 王勇.藍马鸡和藏马鸡血液生理生化指标测定[J].畜牧与兽医,2001,33(2):31-32.
[13] 袁进,吴清洪,徐名衬,等. 广州地区藏鸡血液生理和生化指标测定分析[J]. 中国比较医学杂志,2018,28(4):69-72.
[14] 冼琼珍,计慧琴,陈胜峰,等.阳山鸡血液主要生理生化指标的测定[J].畜牧与兽医,2012,44(S1):46-48.
[15] CLSI.Performance standards for antimicrobial disk susceptibility tests.27th edition.CLSI document M100[S].Wayne:Clinical and Laboratory Standards Institute,2017.
[16] 胡明,付晓杰,张庆,等.大肠杆菌持留菌株与抗药菌株生长优势的比较[J].山东农业科学,2019,51( 7):108-112.
[17] 马飞,李玉保.黄芪对肉鸡免疫力的影响[J].安徽农学通报,2007,5:81-82+74.
[18] 骆延波,胡明,齐静,等. 扶正解毒颗粒对小鼠血液指标影响的研究[J].山东农业科学,2017,49(4):116-119.
[19] 李群道,单安山.中药复方对鸡增重和免疫功能的影响[J].中国兽医杂志,2005,8:29-30.
[20] 佟建明,沈建忠. 饲用抗生素研究与应用[M].北京:中国农业大学出版社,2000.
[21] 陈燕军.对欧盟禁用动物抗生素添加剂的再思考[J].中国禽业导刊,2006(21):9-10+53.
Study on Toxicity of Fuzheng Jiedu Granules to Chickens and
to drug Resistance of Escherichia coli
LUO Yanbo, ZHANG Yin,HU Ming,LI Lulu , ZHANG Qing,ZHAO Xiaonan,
QI Jing ,CHEN Yibao,XU Xiaohui,LIU Yuqing
(Institute of Animal Husbandry and Veterinary Medicine, Shandong Academy of Agricultural Sciences/Shandong Key Laboratory of Animal breeding and diseases Control, Shandong Jinan 250100 China)
Abstract: 80 healthy 1-day-old chicks were randomly divided into four groups, with 20 chickens in each group. Among them, 1-3 groups are the experimental group, and Fuzheng Jiedu granules with the recommended dose of 1 times (4 g/L), 3 times (12 g/L) and 5 times (20 g/L) are added to the drinking water respectively,but the drug is not added in group 4. Control group. During the 8-week test period, the clinical signs of each group of chickens are observed and recorded and chickens are weighed once every weekend.At the end of the 8-week,blood are collected to determine the blood physiological and biochemical indicators of each group of chickens. Microscopic observation of tissue sections also will be done.At the same time,Escherichia coli was isolated from the intestinal tract of chickens in experimental group 2 (that is, three times the recommended dosage) for drug resistance analysis. The results showed that the behavior, feeding, and fecal traits of the test chickens in each group showed no abnormal changes compared with the blank control group. The body weight of the test chickens in the group 1and the group 3 was significantly higher than that in the control group (P <0.05 or P <0.01) and the 5-dose group (P <0.05 or P <0.01); while there was no significant difference between the group 1 and group 3(P> 0.05). The blood physiological and biochemical indexes of red blood cells, hemoglobin, white blood cells and lymphocyte ratio were not significantly different in the chickens of each experimental group and the drug-free control group (P> 0.05). There were no abnormal changes in the color, shape, size and position of organs in each group. Microscopic observation of tissue sections, cells conform to normal tissue morphology and structural characteristics. There was no significant difference in the MIC values of E. coli against the eight drugs (P> 0.05). The above results indicate that Fuzheng Jiedu Granules have no obvious adverse effects on the chickens, and have no significant effect on the level of E. coli resistance.
Keywords: Fuzheng Jiedu Granules; Chicken; Blood; Physiological indexes; E. coli; Drug resistance

