冠状动脉低开口患者行经导管主动脉瓣置换术的结果分析
牛冠男,王墨扬,赵庆豪,张倩,叶蕴青,宋光远,张洪亮,罗彤,滕思勇,赵杰,安云强,吕滨,吴永健
经导管主动瓣置换术(TAVR)已成为外科手术中高危主动脉瓣狭窄患者的首选治疗方案,也是所有高龄症状性重度主动脉瓣狭窄的首选治疗方案[1-2]。近年来,TAVR 治疗量的迅速增长,总体疗效良好,但各种并发症的出现仍影响患者的生活质量甚至导致患者死亡[3]。其中,冠状动脉阻塞是致死率最高的并发症,冠状动脉低开口(≤10 mm)是TAVR 围术期冠状动脉阻塞的危险因素[4]。需要通过细致的术前评估及恰当的冠状动脉保护,以预防TAVR 后冠状动脉阻塞[5]。本研究通过回顾性分析单中心经术前影像学筛选后冠状动脉低开口(≤10 mm)患者的手术效果,并与冠状动脉开口高度>10 mm 患者对比,分析出现冠状动脉阻塞事件和术前评估为冠状动脉阻塞高风险并进行冠状动脉保护的患者CT影像学特征,总结避免TAVR 冠状动脉阻塞的方法。
1 资料与方法
1.1 研究对象
回顾性收集2012 年12月至2021 年12 月我院接受TAVR 治疗的患者。纳入标准:(1)症状性重度主动脉瓣狭窄,平均跨瓣压差≥40 mmHg(1 mmHg=0.133 kPa)或峰值跨瓣流速≥4 m/s 或主动脉瓣有效瓣口面积≤1.0 cm2;(2)NYHA 心功能分级≥Ⅱ级;(3)术前CT 评估自体瓣环面积及直径符合器械的使用范围。排除标准:(1)术前1 个月内存在急性心肌梗死;(2)妨碍导引鞘安全置入的髂股动脉血管特征;(3)近期脑卒中或短暂性脑缺血发作病史(距手术<3 个月);(4)存在抗凝及抗栓禁忌等;(5)外科生物瓣损毁患者;(6)无完整主动脉根部CT 影像。
术前通过增强CT 评估排除解剖结构不适宜行TAVR 的患者,本研究共筛选687 例患者,排除无主动脉根部CT 影像或影像治疗较差者46 例,另有生物瓣术后患者19例(均使用具有瓣架的生物瓣膜,该类瓣膜对冠状动脉开口有一定的保护作用,而外科手术往往会相对降低冠状动脉开口高度,将对结果造成偏移,故排除该部分患者),最终共纳入患者622 例,其中冠状动脉开口高度>10 mm 患者556例(89.40%,冠状动脉开口高度>10 mm 组)。经术前影像学筛选,排除冠状动脉阻塞高风险后接受TAVR 治疗的冠状动脉开口高度≤10 mm 患者66例(10.60%,冠状动脉开口高度≤10 mm 组)。
1.2 术前评估
术前通过超声心动图及临床评估诊断为症状性重度主动脉瓣疾病,通过增强CT 对患者主动脉根部及入路进行解剖学评估。基础评估参照通用评估方法[6]。冠状动脉低开口定义为冠状动脉开口下缘至瓣环平面的垂直距离≤10 mm。对瓣叶高度>冠状动脉开口水平高度的患者,测量同水平瓣叶厚度,窦部最远端至冠状动脉开口距离;如患者同水平瓣叶间存在融合,测量融合长度,并计算剩余窦部宽度,如为三叶式主动脉瓣(三叶瓣)、功能性二叶式主动脉瓣(二叶瓣)及1 型二叶瓣,剩余窦部宽度=冠状动脉开口水平窦部最远端至冠状动脉开口距离-瓣叶间融合长度-瓣叶厚度(图1A);如为0型二叶瓣畸形,剩余窦部宽度=冠状动脉开口水平两侧窦部之间最远距离-瓣叶厚度1-瓣叶厚度2(图1B)。比对剩余窦部宽度与拟置入瓣膜大小,同时观察瓣叶形态。
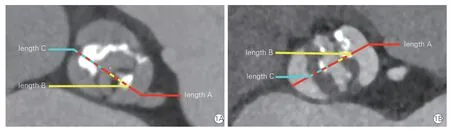
图1 CT 主动脉剩余窦部宽度、主动脉瓣瓣叶厚度及融合长度测量方法
1.3 手术方法及观察指标
依据患者临床基本情况,选择适当的麻醉方式、手术入路并依照标准TAVR 流程完成手术[7]。术后观察手术成功率、安全性终点并应用经胸超声心动图评价瓣膜血流动力学及心功能情况。手术成功标准参照瓣膜学术研究联盟-3(VARC-3)标准[8]定义,手术成功的定义为单一生物瓣膜置入恰当的位置且血流动力学无明显异常、术后30 d 内无死亡、无需再次介入或外科手术治疗、无严重的心血管并发症。
1.4 统计学方法
应用Prism 8 统计软件进行分析,符合正态分布的连续型变量以表示,采用t检验;计数资料用百分率表示,采用χ2检验或Fisher 精确检验;P<0.05 为差异有统计学意义。
2 结果
患者基线临床资料(表1):622 例患者中男性352例(56.59%),平均年龄(75.15±7.29)岁,均有明显的临床症状,冠心病、糖尿病、高血压、高脂血症等合并症比例较高,心功能差,NYHA 心功能分级Ⅲ级以上患者共510例(81.99%)。冠状动脉开口高度≤10 mm 组和冠状动脉开口高度>10 mm 组在性别、年龄、NYHA 心功能分级及合并症的发生率等方面差异均无统计学意义(P均>0.05)。

表1 两组患者基线临床资料比较[例 (%)]
两组患者术前增强CT 数据及超声心动图比较(表2):全部患者术前增强CT 测量显示收缩期主动脉瓣瓣环周长(77.35±8.67)mm,瓣环面积(423.60±70.37)mm2。与冠状动脉开口高度>10 mm组比较,冠状动脉开口高度≤10 mm 组主动脉瓣瓣环长径[(27.68±3.07)mm vs.(26.15±2.31)mm,P<0.01]、收缩期瓣环周长[(77.74±8.77)mm vs.(74.02±6.99)mm,P<0.01]及主动脉窦部直径[(32.73±4.41)mm vs.(30.78±3.73)mm,P<0.01]均较小,差异均有统计学意义。冠状动脉开口高度≤10 mm 组患者左冠状动脉开口高度为(8.63±1.08)mm。两组患者术前及术后30 d 超声心动图结果差异均无统计学意义(P均>0.05)。术后30 d 超声心动图提示,与同组术前比较,全部患者、冠状动脉开口高度>10 mm 组及冠状动脉开口高度≤10 mm 组主动脉瓣平均跨瓣压差均明显减低(P均<0.01),主动脉瓣瓣口面积均明显增加(P均<0.01)。
表2 两组患者术前增强CT 数据及超声心动图比较()
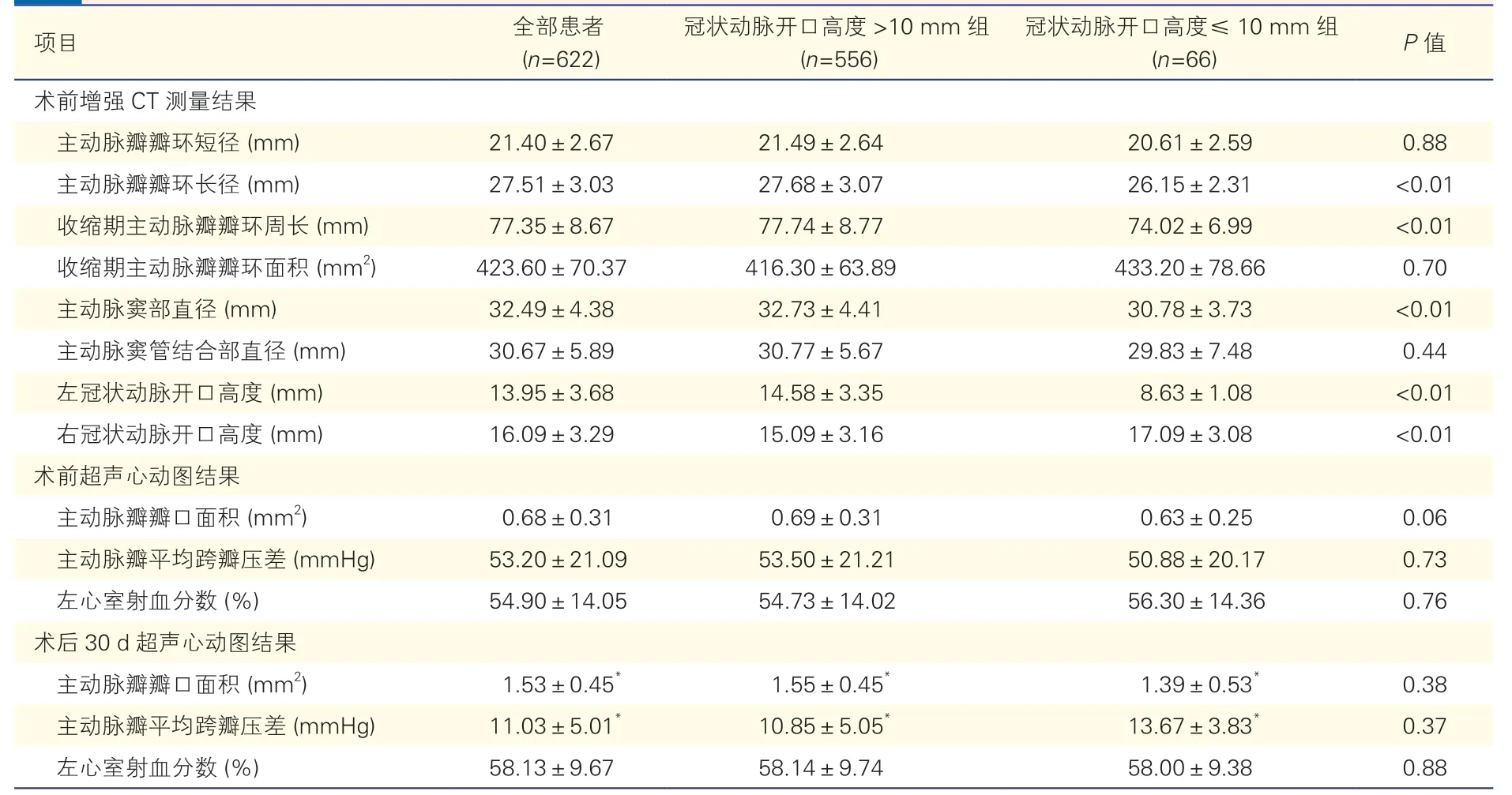
表2 两组患者术前增强CT 数据及超声心动图比较()
注:与同组术前比较*P<0.01。1 mmHg=0.133 kPa
冠状动脉开口高度≤10 mm 组患者主动脉瓣瓣叶及窦部特征(表3):冠状动脉开口高度≤10 mm 组66 例患者中共有二叶瓣患者32例(48.48%),其中功能性二叶瓣21例(65.63%),1型二叶瓣9例(28.13%),0 型二叶瓣2例(6.25%)。66 例患者中剩余窦部宽度小于拟置入瓣膜型号患者19例(28.79%);19 例患者中,二叶瓣畸形患者为14例(73.68%),其中1例(7.14%)为0 型二叶瓣,其余13例(92.86%)患者均可见冠状动脉低开口对应瓣叶与毗邻瓣叶间融合;其余5例(26.32%)为三叶瓣患者,这5 例患者剩余窦部宽度与拟置入瓣膜差值<1 mm,且均置入自膨胀式瓣膜。
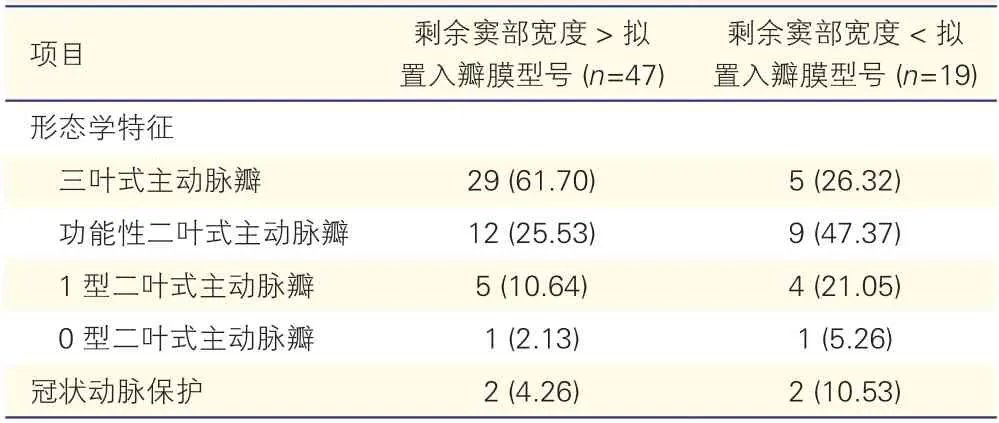
表3 冠状动脉开口高度≤10 mm 组患者主动脉瓣瓣叶及窦部特征[例 (%)]
两组患者手术成功率和早期安全性终点比较(表4):全部患者早期手术成功518例(83.28%),术中使用第二枚瓣膜的患者77例(12.38%),术后早期植入起搏器的患者74例(11.90%);这些指标在冠状动脉开口高度>10 mm 组和冠状动脉开口高度≤10 mm 组间差异均无统计学意义(P>0.05)。早期全因死亡率、脑卒中、严重血管并发症的发生率,两组间差异均无统计学意义(P均>0.05)。全部患者共4例(0.64%)发生了冠状动脉阻塞,均发生于冠状动脉开口高度>10 mm 组,但与冠状动脉开口高度≤10 mm 组比较差异无统计学意义(0.72% vs.0%,P=0.49)。术中共使用冠状动脉保护技术12例(1.93%),其中冠状动脉开口高度≤10 mm 组4例(6.06%),冠状动脉开口高度>10 mm组8例(1.44%),冠状动脉开口高度≤10 mm 组需要进行冠状动脉保护比例较高[6.06% vs.1.44%,P<0.01],差异有统计学意义。经冠状动脉保护后无患者出现冠状动脉阻塞或围术期死亡、脑卒中等并发症。
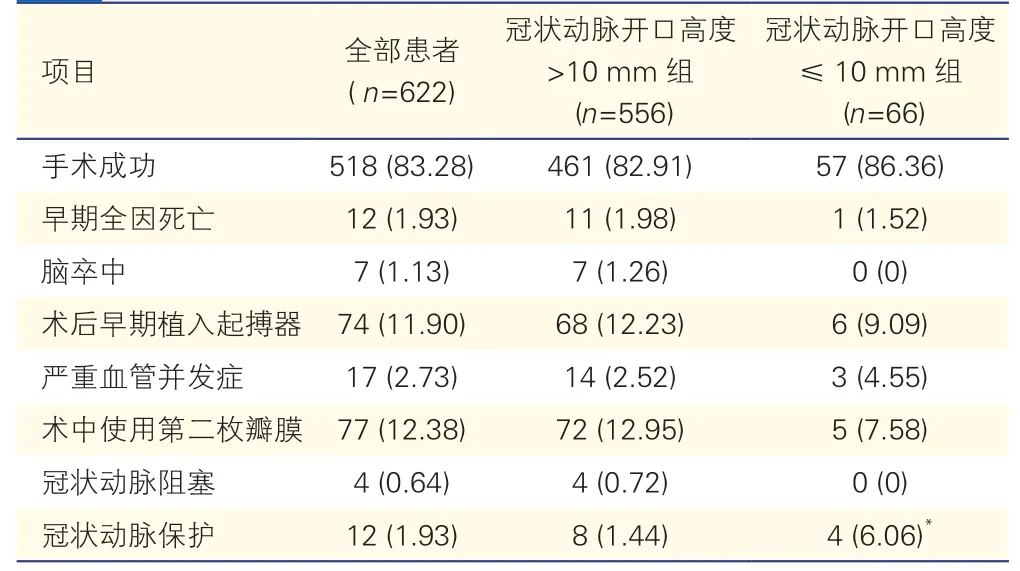
表4 两组患者手术成功率和早期安全性终点比较[例(%)]
3 讨论
冠状动脉阻塞是一种罕见但致命的TAVR 并发症,其发生率不足1%,但预后极差,在发生冠状动脉阻塞且未能成功进行经皮冠状动脉介入治疗(PCI)或冠状动脉旁路移植术(CABG)的患者中死亡率为100%[4]。尽管部分冠状动脉阻塞患者成功进行了血运重建,但接受PCI 的冠状动脉阻塞患者30 d死亡率仍高达22.2%,而接受CABG 的患者30 d死亡率为50%[4]。冠状动脉阻塞的发生率在各种不同类型的瓣膜中发生率不尽相同,球囊扩张式瓣膜的发生率高于自膨胀式瓣膜的发生率(0.81% vs.0.34%,P=0.023),而外科生物瓣术后TAVR 围术期冠状动脉阻塞发生率高于原位TAVR(2.48% vs.0.62%,P=0.045)[4]。外科瓣膜术后TAVR 围术期冠状动脉阻塞主要见于免缝合瓣或无瓣架类型的外科生物瓣膜,该瓣膜在我国使用较少。而我国常使用的有瓣架的外科生物瓣膜,对冠状动脉开口有一定的保护作用。
冠状动脉阻塞的已知危险因素包括使用球囊扩张式瓣膜、冠状动脉低开口(<10 mm)及瓦氏窦狭小(<30 mm)[4,9-12]。此外,对于外科生物瓣术后患者,虚拟瓣膜至冠状动脉开口距离<4 mm 也是冠状动脉阻塞的危险因素。
本研究中发现,冠状动脉开口高度≤10 mm 病例占全部接受TAVR 治疗患者的10.6%,平均冠状动脉开口高度为(8.63±1.08)mm,其术后早期临床结局与冠状动脉开口高度>10 mm 的患者相似,并未增加冠状动脉阻塞的发生率。但需要注意的是,我中心进行TAVR 治疗前会对患者进行细致的影像学评估,已排除部分冠状动脉阻塞高风险患者,在开展TAVR 早期,对冠状动脉开口高度≤10 mm 患者的主动脉瓣瓣叶长度、瓣叶形态学特征、冠状动脉开口水平瓣叶形态、窦部宽度等因素进行分析,排除了冠状动脉阻塞高危患者5 例,从而降低了冠状动脉开口高度≤10 mm患者冠状动脉阻塞的发生率,也是导致冠状动脉开口高度≤10 mm 患者术后早期临床结局与冠状动脉开口高度>10 mm 患者相似的重要原因。而在学习了冠状动脉保护技术后,对冠状动脉阻塞高风险患者实施该技术,避免了患者术中出现冠状动脉阻塞的情况,因此,患者发生冠状动脉阻塞比例较低,且冠状动脉开口高度≤10 mm组无冠状动脉阻塞发生。
虽然冠状动脉阻塞发生率不高,但其高致死率仍引起了极高关注。近年来,冠状动脉保护技术已开始应用于冠状动脉阻塞高风险患者当中。BASILICA 是将原生主动脉瓣或外科生物瓣膜进行切割,使瓣叶在TAVR 人工瓣膜置入时向两侧横向分离,避免瓣叶向冠状动脉开口方向移动,从而避免冠状动脉阻塞[13]。前瞻性多中心研究显示,在30 例冠状动脉阻塞高危患者中,对37 个瓣叶(部分患者进行双瓣叶切割)尝试进行BASILICA 操作中,35 个瓣叶成功切割,全部患者均未出现冠状动脉阻塞[14]。烟囱支架技术是在近冠状动脉开口处置入支架并延伸至主动脉,用以避免冠状动脉动脉阻塞进而引起心原性休克或死亡的方法。在近期的一项研究中,在12 800 例TAVR 治疗中,有60 例 (0.5%)采用了烟囱支架技术,避免TAVR 期间冠状动脉阻塞。在这60 例患者中,35例(58.33%)经术前评估考虑为冠状动脉阻塞高危患者,预先进行了烟囱支架保护,其余25例(41.67%)患者在发生冠状动脉阻塞后补救性进行了烟囱支架置入,全部患者中3 例 (5.0%)患者死亡,13 例 (21.6%)患者发生心肌梗死,均发生于补救性行烟囱支架置入组。14 例 (23.3%)患者发生心原性休克,其中13 例发生于补救性行烟囱支架置入组。而缺乏冠状动脉保护是冠状动脉阻塞高危患者30 d 死亡、心肌梗死和(或)心原性休克的独立危险因素。
综上所述,经过细致的术前影像学评估筛选的冠状动脉开口高度≤10 mm 患者接受TAVR 治疗安全、有效,与冠状动脉开口高度>10 mm 患者的早期临床结局差异无统计学意义。但需要注意,本研究仅对实施TAVR 患者进行了分析,部分冠状动脉开口高度较低,且冠状动脉阻塞风险较高的患者已排除在外,而冠状动脉阻塞高风险患者在接受TAVR 治疗过程中进行了冠状动脉保护,从而降低了并发症的发生率。在TAVR 治疗前应对患者实施细致的影像学评估,综合患者冠状动脉开口高度、主动脉窦部大小及冠状动脉开口水平主动脉瓣瓣叶特征,预测患者TAVR 治疗中冠状动脉阻塞风险的发生风险,对冠状动脉阻塞高风险患者在术中进行冠状动脉保护或建议实施外科主动脉瓣置换术治疗,可有效避免冠状动脉阻塞的发生。
冠状动脉阻塞风险评估注意事项:(1)测量冠状动脉开口距离瓣环平面的垂直距离,若≤10 mm 应高度警惕;(2)测量主动脉瓣瓣叶长度,并与相应冠状动脉开口高度对比,如瓣叶长度明显大于冠状动脉开口高度,应警惕冠状动脉阻塞风险;(3)观察冠状动脉低开口瓣叶是否与毗邻瓣叶间存在融合,如融合长度较长,则降低冠状动脉阻塞风险;此外,如患者为0 型二叶瓣畸形,冠状动脉阻塞风险降低;(4)如主动脉瓣瓣叶高度高于冠状动脉开口高度,计算剩余窦部宽度,与拟置入瓣膜型号进行对比,如剩余窦部宽度<瓣膜直径,建议关注术中球囊与扩张时冠状动脉血流非选择性造影结果。(5)球囊预扩张并主动脉根部造影时注意冠状动脉血流非选择性造影结果,如冠状动脉非选择性造影血流消失,建议实施冠状动脉保护或终止手术,评估外科主动脉瓣置换术的可行性;如冠状动脉非选择性造影见左主干部分受阻,建议实施冠状动脉保护;如冠状动脉非选择性造影仍可见冠状动脉血流通畅,但瓣叶结构贴近冠状动脉开口,建议实施冠状动脉保护。
利益冲突:所有作者均声明不存在利益冲突

