塑料餐盒中邻苯二甲酸酯的迁移风险研究
蓝敏怡, 李会茹, 应光国
(华南师范大学环境学院/广东省化学品污染与环境安全重点实验室/环境理论化学教育部重点实验室, 广州 510006)
邻苯二甲酸酯(PAEs)在增加塑料可塑性和柔韧性方面性能优越,是目前使用量最大的增塑剂,市场份额约占80%,在塑料中的质量分数高达20%~30%[1],目前全球年产量已超过200万吨。PAEs作为环境内分泌干扰物,会引起人体和动物体内分泌失调、生殖细胞基因损害、卵子质量异常变化等,进而阻碍生殖发育等机能,最终导致习惯性流产、停产、早产和胎儿畸形(遗传变异)等[2],长时间的累积暴露甚至有引发恶性肿瘤与生物绝种的危害[3]。有学者发现雄性大鼠围产期接触PAEs后的症状与人睾丸发育不良综合症有显著的相似之处,说明PAEs能够通过抑制胎儿睾丸的睾酮合成,破坏雄激素依赖性结构的发育,导致男性胎儿出现尿道下裂、睾丸停止发育、精子数量减少、阴茎变小等症状[4-6]。此外,PAEs还会产生有毒物质,对人或动物的神经系统造成影响,从而削弱人和动物的可逆记忆[7]。鉴于PAEs的致癌、致畸、致突变效应,国际癌症研究署和美国环保署均将其列为人类可能的促癌剂或致癌物质。欧盟指令2007/19/EC和我国《食品安全国家标准 食品接触材料及制品用添加剂使用标准》(GB/T 9685—2016)均对PAEs应用于食品接触材料中的迁移限量进行规定。
塑料是使用最多的食品包装材料,我国现有食品包装中塑料占比超过50%[8],截至2020年12月,我国网上外卖用户规模达4.19亿人,外卖市场交易规模达8 352亿元,同比增长14.8%[9-10]。然而,因包装材料与食品直接接触,其中的化学成分(尤其是增塑剂等)可通过接触迁移至食品中,从而威胁人体健康[11-12]。在我国江苏、安徽、浙江、陕西等省抽取的聚氯乙烯(PVC)和复合材料塑料食品包装样品中分别检出了邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二异丁酯(DIBP)[13]。在塑料保鲜袋(膜)、一次性塑料杯[14]、一次性餐盒中均检出PAEs[15],但低于国家限定的迁移量。研究表明:PAEs的迁移量受食品类型、pH、温度、储藏时间的影响[16-17];接触时间越长,迁移量越大[18-19]。DEHP极易迁移至食品中,其在食品中的质量分数容易超过欧盟安全限量标准委员会的限制[19]。食品保鲜膜中的主要增塑剂二乙基羟胺(DEHA)也极易迁移到其所包裹的肉类、鱼类、奶酪和即时食品中[20]。鉴于此,本研究测定了市售塑料餐盒中16种PAEs的质量分数,通过食品模拟物浸出实验研究了样品中PAEs的污染释放特征和影响因素,以客观评估其对人体的健康风险。
1 实验部分
1.1 材料与试剂
本研究采集了全国不同地区14个厂家的一次性塑料餐盒样品,其中8批次随机购自大型餐饮用品批发市场,6批次购自淘宝网销量较高的商铺。各塑料餐盒样品具体来源:广东5个,福建2个,江西、江苏、广西、湖南、安徽、湖北、山东各1个。
16种PAEs的正己烷混标溶液,包括邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二(2-甲氧基)乙酯(DMEP)、邻苯二甲酸二(4-甲基-2-戊基)酯(BMPP)、邻苯二甲酸二-2-乙氧基乙酯(DEEP)、邻苯二甲酸二戊酯(DPP)、邻苯二甲酸二己酯(DHXP)、邻苯二甲酸丁基苄基酯(BBP)、邻苯二甲酸二(2-丁氧基)乙酯(DBEP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二苯酯(DPHP)、邻苯二甲酸二辛酯(DNOP)、邻苯二甲酸二壬酯(DNP),购自上海安普实验科技股份有限公司。4种内标物(IS)分别为 D4-DMP、D4-DBP、D4-DPP、D4-DEHP,购自上海安普实验科技股份有限公司。
色谱纯丙酮购于上海凌峰化学试剂有限公司,色谱纯甲醇与色谱纯正己烷购于德国Merck公司,色谱纯二氯甲烷,分析纯甲醇与无水乙醇购于天津富宇精细化工有限公司,色谱纯冰醋酸购于阿拉丁试剂上海有限公司,色谱纯异辛烷购于德国Merck公司,蒸馏水购于深圳屈臣氏饮用水,超纯水自制,氮气(纯度99.99%)购于广州科气达公司。
1.2 主要仪器
安捷伦7890B气相色谱仪和5977B质谱检测器(美国Agilent科技公司)、EFAA-DC24型24位氮吹仪(上海安普实验科技股份有限公司)、XW-80A涡旋混合器(上海驰唐电子有限公司)、945066多管式涡旋混合器(美国Talboys公司)、L550低速离心机(湖南湘仪实验室仪器开发有限公司)、KQ-500E超声波清洗器(昆山舒美超声仪器有限公司)、ME104分析天平(瑞士梅特勒-托利多集团)、FO810C马弗炉(日本雅马拓公司)、MPR-510立式冷藏冰箱(松下电器有限公司)、超纯水机(美国艾科浦国际有限公司)。
1.3 PAEs分析的样品前处理
将塑料餐盒洗净晾干,采用高速破碎机粉碎至粒径小于0.2 cm,准确称取0.5 g左右的塑料样品,置于50 mL玻璃离心管中,每种样品设置3个平行实验,每种样品中依次加入回收率指示物标准溶液和8 mL正己烷,置于超声仪中于30 ℃下超声15 min,然后转移上清液于50 mL比色管中,再加入正己烷重复提取2次并离心,合并上清液,补充正己烷定容至25 mL,混匀后取5 mL置于离心管中,用氮气吹至近干,加入100 μL内标物标准溶液,补充正己烷定容至1 mL后进样进行GC-MS分析。
1.4 餐盒中PAEs的浸出实验
1.4.1 浸出条件选择 主要探讨4种食品模拟液对PP塑料餐盒的浸出迁移量的影响。通过固定2个变量来考察另一个变量对PAEs迁移率的影响:
(1)实验温度、一次性塑料餐盒和实验时间相同,食品模拟物不同;
(2)实验温度、一次性塑料餐盒相同和食品模拟物相同,实验时间不同。
浸出实验参照《食品安全国家标准 食品接触材料及制品迁移试验预处理方法通则》(GB/T 5009.156—2016)中的规定流程,然后按照食品接触材料在实际使用过程中可预见的与食品接触的最长时间和最高使用温度进行浸泡。本实验使用的一次性餐盒通常在0~100 ℃温度范围内使用,与食品接触的时间最长为48 h,水性食品、酸性食品和酒精食品与一次性餐盒的接触最高温度为100 ℃。将塑料餐盒洗净晾干,选取25、40、55 ℃分别代表室温、常见接触温度和模拟加热温度(异辛烷最高使用温度)。在25、40、55 ℃温度下,取样时间分别为0.5、1、2、6、10、12、24、36 h。
本研究参照国家标准《食品接触材料 塑料中受限物质 塑料中物质向食品及食品模拟物特定迁移试验和质量分数测定方法以及食品模拟物暴露条件选择的指南》(GB/T 23296.1—2009)和欧盟指令(82/711/EEC),用不同的食品模拟物代替塑料餐盒接触不同类型的食物(表1)。

表1 食品模拟物的选择Table 1 The selection of food simulants
1.4.2 浸出实验样品处理 在塑料餐盒中分别加入4种食品模拟物(总体积约500 mL),用盖子密封,放入相应温度的恒温培养箱中浸泡,间隔不同时间取样。样品采集及前处理操作过程:准确吸取10 mL浸泡液移入30 mL离心管中,每种样品设置3个平行实验,根据样品性质采用不同前处理方法提取其中的PAEs。水性模拟物:向样品中加入4 mL正己烷并充分振荡5 min,3 000 r/min转速下离心5 min,将上层有机相转入玻璃离心管中,再加入正己烷萃取2次并离心,合并萃取液,用氮气吹至近干,加入100 μL内标标准溶液,将正己烷定容至1 mL后进样进行GC-MS分析。异辛烷模拟物:准确吸取10 mL浸泡液,用氮气吹至接近1 mL后转移至进样小瓶中,然后加入100 μL的PAEs内标标准溶液,补充正己烷定容至1.0 mL后进样GC-MS分析。上述浸泡实验均同时进行空白实验。
1.5 仪器分析
1.5.1 标准溶液配制 准确量取100 μL的100 μg/g混标储备液置于10 mL容量瓶中,用正己烷定容配成1 μg/g的标准储备液。PAEs标准曲线的绘制:分别取一定体积的PAEs标准储备液用正己烷进行梯度稀释,得到质量分数分别为1、5、10、100、500、1 000 μg/kg的标准工作液,-18 ℃恒温冰保存。
1.5.2 仪器条件 色谱条件:色谱柱型号为安捷伦DB-5MS毛细管柱(30 m×250 μm×0.25 μm);进样口温度为280 ℃,柱温80 ℃,升温程序为80 ℃保持1 min,以18 ℃/min升至160 ℃,再以9 ℃/min升至300 ℃,保持5 min;载气为氦气,纯度大于99.99%,流速为1.0 mL/min;1 μL不分流进样。
质谱条件:离子源温度为300 ℃,电子轰击源(EI)电离能量70 eV,溶剂延迟6 min,在选择性离子检测(SIM)模式下对化合物进行定量分析。该色谱分离条件下,16种PAEs能被有效分离,峰形较好且出峰稳定,PAEs在GC-MS中的分析时间为26 min。PAEs的标准品在SIM模式下的色谱及数据见图1、表1。

图1 PAEs标准品在SIM模式下的色谱图

表2 PAEs的保留时间和离子质荷比Table 2 The retention time and ion mass charge ratio of PAEs
1.6 质量保证和质量控制(QA/QC)
试验中所使用的全部玻璃器具在使用前必须洗净。洗涤流程:均使用碱液洗液浸泡24 h,用自来水冲洗干净,再用蒸馏水淋洗,于60 ℃烘箱烘干,最后在马弗炉内450 ℃下煅烧4.5 h再使用。对于不能煅烧的玻璃量器,待蒸馏水洗涤后用有机溶剂淋洗,在使用前需要依次用甲醇、丙酮、二氯甲烷、正己烷4种溶剂清洗。实验过程中避免使用普通移液枪,而替换为有机移液枪,防止普通塑料枪头带来的背景污染。为降低PAEs污染,实验过程中避免接触任何塑料制品。
样品在处理过程中,需同时做实验室空白和实验室控制样品。实验室空白样品中添加洁净的基质(本实验基质为正己烷)与实际样品按相同的步骤提取,用于分析人为操作、提取试剂等条件而引入的背景污染。实验室控制样品中需加入一定体积的标准品和基质,标准品一般为5 mg/L的混标样,与实际样品按相同的步骤提取,用于分析目标化合物提取条件的稳定性与重现性。
本研究分批进行了2次试验,每次试验均制定2个空白实验和2个加标回收实验。在16种PAEs中,大部分目标化合物所得回收率范围为57.3%~120.0%,精密度(RSD)范围为0.120%~9.949%,均小于10%,线性拟合结果的R2均在0.99以上,说明实验方法符合分析的要求。
1.7 PAEs浸出的健康风险评估
1.7.1 暴露评估模型 采用美国食品药品管理局(FDA)[21]推荐模型对PAEs的暴露量进行计算,即
(1)
其中,EDI为每日每公斤体重暴露量;CF为各种类型包装材料的消费因子;faq、fac、fal、ff为各种类型食品的分布因子,依次分别为水类、酸类、醇类和脂类食品;Maq、Mac、Mal、Mf为相应类型食品模拟物中PAEs迁移量;mf为每日食品消耗量;M为人均体重。根据FDA的推荐值,塑料包装材料的CF为0.4,faq、fac、fal、ff分别为0.49、0.16、0.01、0.34。每日食品消费量取3 kg,人均体重取60 kg。
根据日累积暴露量(EDI)的不同,FDA将其划分为4个水平[22]:①低于0.5 μg/kg;②0.5~50 μg/kg;③50~1 μg/kg;④高于1 μg/kg。日累积暴露量越大,危险性越大。
1.7.2 健康风险表征 美国环境保护署(U.S. EPA)将DEHP列为B2类致癌物质,将DBP和DIBP 列为非致癌化合物,某种PAEs潜在的非致癌风险(HQ)与致癌风险(CR)公式:
HQ=EDI/Rfd,
(2)
CR=EDI×SF,
(3)
其中,Rfd为某种PAEs在经口摄入途径下的参考剂量,DBP、DIBP、DEHP的Rfd分别为0.1、0.1、0.02 mg/(kg·d);SF为DEHP致癌风险的致癌强度系数,参考U.S. EPA的数据,取 0.014 (kg·d)/mg。
对于2种及以上非致癌物联合暴露的情况,总非致癌风险(HI)公式:
HI=ΣHQi,
(4)
其中,HQi为第i种PAEs对人体的非致癌风险。
2 结果与讨论
2.1 塑料餐盒样品中的PAEs
2.1.1 质量分数水平 14批次塑料餐盒样品中PAEs的质量分数见表3。对样品中的16种PAEs进行检测,仅检出DEP、DIBP、DBP、DEHP、DPhP和DNOP,检出率分别为100%、100%、78%、78%、92%、85%;质量分数范围分别为0.140~0.829、0.237~1.676、ND~0.995、ND~2.302、ND~1.714、ND~0.213 mg/kg。在这14批次塑料餐盒样品中,其余12种PAEs则均未检出。各样品中的PAEs总质量分数在1.589~6.141 mg/kg范围,平均值为3.144 mg/kg。

表3 塑料餐盒中PAEs的质量分数Table 3 The concentration of PAEs in plastic containers mg/kg
张磊等[23]检测广州市塑料食品包装材料中8种PAEs的残留情况,DBP、DEHP检出率分别为100%、44%,其中1份样品检出BBP,其他PAEs未被检出;DBP和DEHP残留量范围分别为 22.89~267.6和ND~899.8 mg/g。霍娇等[24]对成都市一次性餐具检测的16种PAEs中仅检出DEP、DIBP、DBP、DEHP,检出范围分别为ND~10.3、ND~6.4、ND~7.2、ND~65.6 mg/kg。祝惠惠等[15]从常州市PP快餐盒中仅检出DIBP、DBP、DEHP,其检出质量分数分别为ND~1.7、ND~4.7、ND~3.8 mg/kg。对比以上研究,本研究结果较低,但对塑料餐盒中能检出DEP、DIBP、DBP、DEHP的规律是一致的。这说明随着我国对塑料食品包装的法律法规的逐渐完善,我国各地塑料餐盒中仅存在轻微的PAEs污染。
我国GB/T 9685—2016禁止添加DMP、DIBP、DIOP,可添加的4种塑化剂(DEHP、DINP、DBP和邻苯二甲酸二烯丙酯(DAP))仅可用于PVC材料。本研究结果显示:DEP和DIBP在PP餐盒中的检出率达100%,最高残留量分别为0.829、1.676 mg/kg,这表明所检测的塑料餐盒均满足国家标准。
2.1.2 组成特征 将样品中各PAEs的质量分数进行归一化,计算其贡献率(质量百分比)。结果表明(图2),DIBP和DPhP是塑料餐盒中的优势PAEs污染物,其贡献率分别为8.6%~53.2%、0~60.1%,但不同样品中2种化合物的贡献率相差很大,如一些样品中DPhP贡献率高达60.1%,但DIBP仅占8.6%;有些样品中DPhP贡献率为0,而DIBP却占53.2%。这可能与本研究中的塑料餐盒材料种类、样品来源(不同省份、不同厂家)和生产工艺不同有关。这一现象在已有报道中也有发现,如江苏、安徽、浙江、陕西4个省份PVC餐盒中的PAEs以DBP和DEHP为主,贡献率均为0~100%;复合材料的检出则以DEHP和DIBP为主,贡献率均为0~100%[13]。成都一次性餐具中以DEHP为主,其贡献率为91.9%[24]。常州PP快餐盒PAEs中以DBP、DIBP、DEHP为主,其贡献率均为0~100%[15]。

图2 塑料餐盒中PAEs相关化合物的贡献率
2.2 浸出实验结果
根据塑料餐盒在4种食品模拟物浸出实验的分析数据可知,塑料餐盒的16种PAEs因浸出迁移而检出的只有DEP、DIBP、DBP、DEHP,其余12种PAEs均未被检出,所以本研究重点考察了这4种PAEs化合物的浸出规律和影响因素。
2.2.1 不同浸出液 对4种PAEs在不同食品模拟物中的浸出率进行比较(图3),结果发现:在相同温度下,各PAEs在4种食品模拟物中的浸出率从大到小顺序均为:异辛烷、10%乙醇、4%乙酸、水,且各PAEs样品在蒸馏水和4%乙酸中的浸出量在2 h内的变化最大,但随着浸泡时间延长各PAEs样品的浸出率变化不明显。这是因为上述4种PAEs均为亲脂性有机物,正辛醇-水分配系数lgKow的范围为2.42~7.60,在水中的溶解度低,在塑料-水体系中向水迁移较小。
在10%乙醇中,PAEs在各个时间段的浸出率明显高于蒸馏水和4%乙酸,这可能因为醇体系增大了有机相的萃取溶解能力,降低整体溶液的极性,使得浸出液相分配比例增加,浸出量增加。PAEs浸出率随时间增加而增大,至第2 h变化速度最快,此后缓慢增加并逐渐趋于分配平衡,这是因为实验前期浸出只发生在塑料餐盒表面,随后的溶胀作用加大了塑料与溶液的接触,从而加快了浸出速度,但随着浸泡时间延长,各PAEs在塑料-水相体系中的分配达到平衡。这与COLTRO等[25]发现塑化剂在酒精类食品模拟物中的迁移量显著高于酸性食品模拟物的迁移结果相一致。
异辛烷模拟液极性弱,PAEs具有较强的亲脂性,易溶解在异辛烷中,所以各物质的浸出率较其它3种食品模拟液均有显著增加。此外,异辛烷与酒精性质相似,会对塑料餐盒产生溶胀作用,从而促进小分子物质的迁移扩散[26]。

图3 不同食品模拟物中PAEs的迁移率
在55 ℃下,DEP、DIBP、DBP和DEHP在异辛烷中36 h时浸出率分别达到5.24%、21.32%、72.76%和7.34%,是相同时间水浸出液数据的3.8、24.4、58.8、64.7倍,是4%乙酸浸出液数据的4.0、18.6、48.4、88.5倍以及10%乙醇浸出液数据的3.7、22.6、36.4、60.3倍;且浸泡时间越长,浸出率越大。这与BOUSSOUM等[27]发现PVC材料中的增塑剂更易迁移至橄榄油等脂溶性物质中的结果一致。楼珏等[28]也发现食品包装PVC塑料薄膜中的PAEs(DBP、BBP、DEHP、DNOP、DINP、DIDP)在水、3%乙酸、20%乙醇中基本无浸出,但是极易迁移至异辛烷中。王君[29]测得聚乙烯(PE)保鲜膜中的DIBP和DBP在异辛烷和正己烷中的浸出量比在水、3%乙酸和10%乙醇中的浸出量显著增大。
2.2.2 不同温度 对4种PAEs化合物在不同温度中的浸出率进行比较(图4),结果发现:在相同食品模拟物中,DEP、DIBP和DBP在不同温度下的浸出率均随温度升高而增大,其中DEHP在异辛烷中的浸出率变化趋势与其它化合物的一致,但在水相模拟物中3种温度下浸出率从大到小顺序:40 ℃、55 ℃、25 ℃。在55 ℃下,DEP、DIBP、DBP和DEHP在水中36 h的浸出率分别达到1.39%、0.87%、1.29%和0.11%,是相同时间在25 ℃水中浸出率的10.5、11.6、2.2、1.8倍,是相同时间在40 ℃水中浸出率的3.4、1.1、1.0、0.4倍。4%乙酸和10%乙醇中各PAEs在不同温度下的变化趋势与水中的一致。在55 ℃下,DEP、DIBP、DBP和DEHP在异辛烷中36 h的浸出率分别达到5.24%、21.32%、72.76%和7.34%,是相同时间在25 ℃的4%乙酸和10%乙醇中浸出率的14.6、191.3、13.8、77.5倍,是相同时间在40 ℃的4%乙酸和10%乙醇中浸出率的2.8、5.8、6.4、21.3倍。这与何泽[30]的研究中PAEs的迁移量随温度升高而增大的结果一致。O’BRIEN等[31]研究温度对PP中5种常用增塑剂向橄榄油中的浸出规律,发现在121 ℃下PAEs浸出率是70 ℃下的10倍,在70 ℃下2 h的浸出量相当于40 ℃下10 d的浸出量。XU等[32]发现塑料制品在60 ℃的储存温度下,DBP的浸出量比40 ℃下的浸出量增加25%,比20 ℃下的浸出量增加50%,说明温度升高能显著提高浸出量。杜珍妮等[16]发现在相同食品模拟物中,随着温度升高,PAEs的扩散系数增大、分散系数变小,浸出量增大,例如3%乙酸溶液中DIBP在25、40 ℃下的扩散系数分别为4.00×10-14、6.00×10-14,分散系数分别为 51 442、26 535。因为室温下PAEs与聚合物是以范德华力、氢键等紧密结合,随温度升高,PP中高能分子链段获得的自由能足以使其活动能力增强,链段可自由旋转,构象数变多,使分子链形态发生变化,最终餐盒内部形成空穴。同时,小分子PAEs物质由于温度升高获得更多额外的自由能,使其摆脱PP分子间的相互作用力,最终从聚合物中浸出[16];另一方面,温度的升高会增强食品模拟物对PAEs的溶解能力,降低PAEs在塑料-食品模拟物体系界面处的分配系数,使PAEs更易被浸出。此外,迁移活化能Arrhenius经验公式[33]指出,小分子活化能随着温度的升高而升高,越容易从聚合物中迁移。
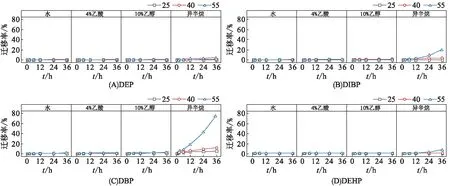
图4 不同温度下PAEs的迁移率
2.2.3 不同化合物的浸出 对比不同温度下4种PAEs化合物在同一食品模拟物中36 h时的浸出率(表4),结果表明:相同温度下,各PAEs在异辛烷中的浸出率从大到小顺序均为:DBP、DIBP、DEP、DEHP,浸出率随Kow增加表现为先增大后减小的趋势。Kow越大,化合物在有机相中的分配系数越大,浸出量也越大。后期降低的原因可能是因为分子体积大小和分子空间构象影响其浸出速度。一方面,在PP材料中,迁移物质的相对分子质量越小,在PP聚合物内部的扩散就越容易,越易迁移,即扩散系数随着迁移物尺寸的增大而减小。另一方面,迁移物的空间构象对迁移能力也有影响,分子空间构象越复杂,分子扩散和迁移能力越弱[13]。由DEP、DIBP、DBP和DEHP的结构式和相对分子质量可知,这4种PAEs都具有相似的对称结构,随着链长的增加,结构越稳定,迁移所需的能量越大,导致迁移能力逐渐减弱,因DEHP的相对分子质量(390.6)与DEP、DIBP、DBP的相对分子质量(194.2、278.3、278.3)相差较大,所以迁移能力比其它物质的弱。这与吴建文等[34]发现DIBP、DPP、DHXP、DEHP随分子链增长和相对分子质量增大时迁移至食品的能力依次降低的结论一致。

表4 不同温度下36 h时PAEs在不同食品模拟物中的浸出率Table 4 The migration rate of PAEs in different food simulators at different temperatures for 36 h %
不同化合物在25、55 ℃的水相溶剂中浸出率从大到小顺序为:DBP、DEP、DIBP、DEHP,即随Kow的增加而减小,但DBP的浸出率远高于其他3种化合物,这可能是由于PP餐盒中DBP质量分数高导致的。此外,各PAEs在40 ℃的水中浸出率从大到小顺序为:DBP、DIBP、DEP、DEHP,DIBP的浸出率变化趋势与25 ℃和55 ℃下的不一样,也说明了DIBP的浸出率受温度影响较大。
2.2.4 暴露健康风险结果 美国环境保护署(US EPA)评估6种优先控制PAEs的每日可耐受摄入量(Tolerable Daily Intake,TDI)[35-37]见表5。将一次性塑料餐盒中PAEs在不同食品模拟液的迁移量代入式(4)中计算可得PAEs的每日暴露量,结果见表6。鉴于DIBP、DBP、DEHP在总PAEs的占比高、日暴露量高,所以本研究仅对这3种PAEs进行健康风险表征,结果见表7。

表5 6种优先控制PAEs的TDITable 5 The TDI of 6 PAEs under priority control
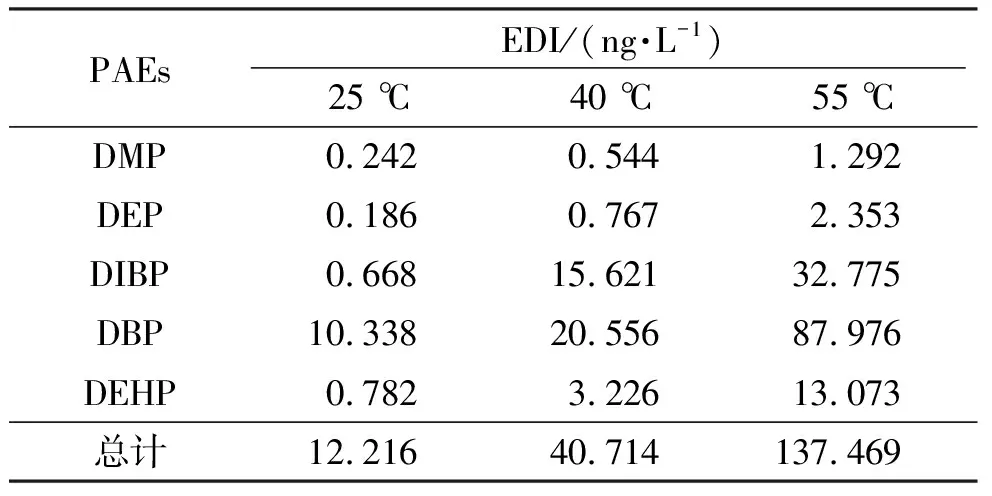
表6 塑料餐盒中PAEs的日暴露量Table 6 The daily exposure of PAEs in plastic containers

表7 塑料餐盒中PAEs的健康风险Table 7 The health risk of PAES in plastic containers
由PAEs的日暴露量可知:在25、40、55 ℃下,人体通过饮食从一次性塑料餐盒中摄入的PAEs总量分别为12.216、40.714、137.469 ng/(kg·d),远低于U.S. EPA规定的TDI;总非致癌风险分别为1.10×10-4、3.62×10-4、1.21×10-3;致癌风险为1.09×10-8、4.52×10-8、1.83×10-7,低于U.S. EPA推荐的人群可接受水平(10-6),表明该批次塑料餐盒在PAEs暴露方面对人体健康无已知的风险。但由于本实验关注的对象仅为PAEs,并未全面研究一次性塑料餐盒中其他有害化合物(如磷酸酯类、双酚类等)的迁移规律及其暴露风险,因此,后续研究还需对一次性塑料餐盒的使用安全性进行全面的风险评估。
3 结论
PAEs增塑剂在食品包装材料中使用广泛,易迁移至与之接触的食品中,从而造成食品污染安全问题。本研究测定了市售常用PP餐盒中PAEs的质量分数,发现所有批次均检出DEP、DIBP、DBP、DEHP、DPhP、DNOP,检出率分别为100%、100%、78%、78%、92%、85%;质量分数范围分别为0.140~0.829、0.237~1.676、ND~0.995、ND~2.302、ND~1.714、ND~0.213 mg/g。此外,16种PAEs仅有4种(DEP、DBP、DIBP、DEHP)在4种食品模拟物中均有不同程度的检出,其中模拟物种类对PAEs的迁移率影响很大,迁移率从大到小顺序为:异辛烷、10%乙醇、4%乙酸、水;温度越高、时间越长、迁移率越大。暴露评估健康风险结果显示:本研究中迁移的PAEs日暴露量致癌风险远低于U.S. EPA推荐的人群可接受水平,不会对人体造成明显损害。
本研究虽然证实了与食品接触的塑料餐盒中的PAEs暴露风险低,但不同使用环境下迁移量有很大差异,也可能会对人体造成健康危害,因此建议不能长期或在高温条件下使用塑料餐盒盛放食物。

