互花米草绿色合成ZnO纳米颗粒及其光催化和抑菌性能
景 花, 纪丽丽*, 周亚蕊, 郭 健, 孙佳星, 陆诗尧
(1. 浙江海洋大学/国家海洋设施养殖工程技术研究中心, 舟山 316022; 2. 浙江大学海洋学院, 舟山 316021; 3. 浙江海洋大学食品与医药学院, 舟山 316022)
随着科学技术的发展,纳米材料在材料、医学、生命科学等领域应用广泛[1-2],由于纳米粒子具有小尺寸效应、量子尺寸效应、表面效应以及介电限域效应等,纳米粒子比常规材料性能更加优良[3],ZnO是继TiO2以来第二代半导体光催化剂,具有和TiO2相似的禁带宽度和导带位置,并且具有更好的电子迁移率和稳定性[4]。此外,低剂量的ZnO即可对多种病原菌产生抗菌活性[5]。由于纳米ZnO具有更优越的光催化活性和抑菌性能,因此,近年来纳米ZnO的合成一直是国内外关注的热点。
目前合成纳米ZnO的方法主要分为物理法、化学法、生物法,其中生物法的原料来源十分广泛,包括植物、细菌、藻类等[6-7]。研究发现,植物中含有丰富的还原性小分子物质(如萜烯类、多酚类、生物碱、酚酸类、黄酮类、醌类等),可替代化学试剂,在合成ZnO纳米颗粒过程中发挥还原剂和分散剂的作用,并且制备的ZnO纳米颗粒比其他原料制备的纳米颗粒更加稳定[8]。此外,采用植物提取液为原料制备纳米ZnO还具有工艺温和、环保、高效、成本低等优点。
互花米草(Spartinaalterniflora)是多年生的根茎草,原产于北美大西洋沿岸,在1979年被引入江苏沿海,在保滩护岸发挥短暂的作用后,与当地植物竞争。近年来,互花米草作为我国滨海湿地最主要的外来入侵物种,不仅在黄河三角洲的潮汐地区迅速扩张,取代了本地物种,威胁了当地的生物多样性[9],进而对我国造成一定的经济损失,除了对互花米草治理,合理利用成为另一种生态途径。研究发现互花米草中黄酮类含量较高,尤其在叶片中的含量最高,黄酮总质量分数达到27.584 mg/g,并且发现互花米草中含有蛋白质、氨基酸、生物碱类等还原性成分[10],可作为前驱体绿色合成ZnO纳米颗粒,目前尚无利用互花米草制备Nano-ZnO纳米颗粒的研究报道。
本文提出Nano-ZnO的绿色化学法制备方法,即利用互花米草叶提取液,以聚乙烯吡咯烷酮为修饰剂,乙酸锌为原料,采用溶胶-凝胶法制备ZnO纳米颗粒;采用扫描电子显微镜 (SEM)、傅里叶红外光谱 (FTIR)、X射线衍射 (XRD)、紫外-可见漫反射光谱 (UV-Vis DRS)分析了绿色合成的纳米ZnO表面形貌、活性基团、晶型结构和光吸收特性;探讨了纳米ZnO对有机染料孔雀石绿(MG)的光催化降解活性以及对金黄色葡萄球菌的抑菌性能。
1 实验部分
1.1 材料制备
互花米草提取液的制备:将新鲜收集的互花米草叶用蒸馏水洗净后在烘箱中60 ℃下烘干5 h,粉碎至粉末。称取2 g粉末置于1 L容量瓶中,加入400 mL体积分数为95.0%的乙醇,置于恒温水浴锅中80 ℃下提取2 h,纱布过滤得到互花米草提取液。
ZnO纳米颗粒的制备:准确称取1.756 g(0.02 mol/L)二水合乙酸锌(Zn(Ac)2·2H2O),置于容积为500 mL锥形瓶中,加入200 mL蒸馏水,磁力搅拌1 min后加入0.1 g聚乙烯吡咯烷酮(PVP),继续搅拌5 min,缓慢添加100 mL互花米草提取液,然后搅拌1 h,最后加入100 mL浓度为0.4 mol/L的NaOH溶液,搅拌1 h后生成乳绿色络合物,即ZnO纳米颗粒前驱体。将前驱体在8 000 r/min转速下离心,放入烘箱60 ℃下干燥8 h,将干燥后的样品转移到管式炉中,在氮气保护下以5 ℃/min的速率由室温升温至400 ℃并在400 ℃下煅烧2 h,自然冷却到室温后得到ZnO纳米颗粒(Nano-ZnO)。
1.2 材料表征
采用粉末X射线衍射(XRD)表征样品的晶型结构,通过Debye Sherrer方程确定晶粒粒径;利用傅里叶变换红外光谱(FTIR)在400~4 000 cm-1波数范围分析绿色合成ZnO和ZnO标样的组成及活性基团。通过紫外-可见漫反射吸收光谱(UV-Vis DRS)测定样品的光吸收特性;通过扫描电子显微镜(SEM)表征样品的微观结构及形貌。
1.3 光催化活性测试
光催化降解有机染料实验在光化学反应器(XPA-7,中国江苏省徐江机电厂)中进行,称取40 mg样品加入到100 mL(50 mg/L)孔雀石绿溶液中,黑暗环境下磁力搅拌,每隔10 min取样直至吸附平衡。将300 W氙气灯(FSX-300,波长范围为:180~700 nm,北京NBeT集团公司)置于距液面25 cm处,每隔10 min取出20 mL溶液,以8 000 r/min转速下离心2 min取上清液,采用UV-Vis分光光度计在617 nm波长处测量吸光度,以ZnO光催化剂降解MG作为对照空白实验。
光催化降解率:
(1)
其中,A0为MG的初始吸光度,At为在某个反应时间点测得的吸光度。
1.4 活性物种测试
进行光催化降解实验时,分别向反应体系中加入2 mL二甲基亚砜(DMSO,0.1 moL/L)、甲酸(FA,0.1 moL/L)和对苯醌(BQ,0.05 moL/L)分别作为·OH、h+和·O2-的自由基捕获剂。
1.5 抗菌分析
采用滤纸片法,测定绿色合成Nano-ZnO的抗菌性能。将6 mm圆形滤片浸泡在10 mg/mL的Nano-ZnO溶液中,超声5 min。将100 μL金黄色葡萄球菌悬液接种至50 mL LB液体肉汤培养基中,放置在摇床37 ℃下培养8 h,测定光密度OD并计算菌群密度为5.6×107mL-1(CFU),然后滴加在LB固体肉汤培养基上并均匀涂布。取滤纸片放置于培养基表面,然后置于培养箱中37 ℃下培养12 h,测其抑菌圈的直径,平行做3次实验,并以ZnO的抑菌实验作为对照。
2 结果与讨论
2.1 材料表征
分析绿色合成Nano-ZnO和ZnO的XRD图谱(图1)可知,Nano-ZnO和ZnO的衍射峰基本一致,在2θ=31.76°、34.42°、36.24°、47.51°、56.57°、62.80°和 67.93°处的衍射峰与ZnO的六方纤锌矿结构(JCPDS:36-1451)的(100)、(002)、(101)、(102)、(110)、(103)和(200)衍射晶面一致[11]。然而Nano-ZnO的衍射峰更加尖锐,表明其结晶性更好,粒子尺寸更小,预示着互花米草提取液绿色合成的纳米ZnO具有更优秀的尺寸效应[12]。

图1 Nano-ZnO和ZnO的XRD图谱
Nano-ZnO微晶的平均粒径采用Scherrer方程计算[13]。
(2)
其中,D为晶粒平均粒径,λ为波长,β为衍射峰半峰宽,k为Scherrer常数(0.89)。计算出Nano-ZnO的晶粒平均粒径为36.8 nm,表明绿色合成Nano-ZnO颗粒尺寸已达到纳米级别,有利于提高其光催化活性和抑菌活性[14]。
样品的FTIR光谱如图2所示,与ZnO相比,Nano-ZnO红外光谱中出现多个吸收峰,表明其表面存在多种官能团。在波数480 cm-1处的伸缩振动为ZnO的特征吸收峰。在3 407 cm-1处的宽峰归因于O—H的振动[15]。在波数1 590 cm-1处的吸收峰属于CC键,而927 cm-1处的吸收峰归因于CO的伸缩振动[16]。此外,互花米草制备的Nano-ZnO在波数2 429~2 291 cm-1范围出现吸收峰,可能与残留的生物碎片有关。在776~634 cm-1范围的吸收峰表明存在烷基和C—H键[17],1 446 cm-1处的峰蓝移到1 449 cm-1,这归因于酚环类化合物(如多元醇、黄酮醇和氨基酸等)与Nano-ZnO表面的相互作用[18]。KARNAN等[19]认为,这些小分子在制备Nano-ZnO的过程中起连接剂和稳定剂的作用,不易洗脱,在绿色合成ZnO的过程中起重要作用。
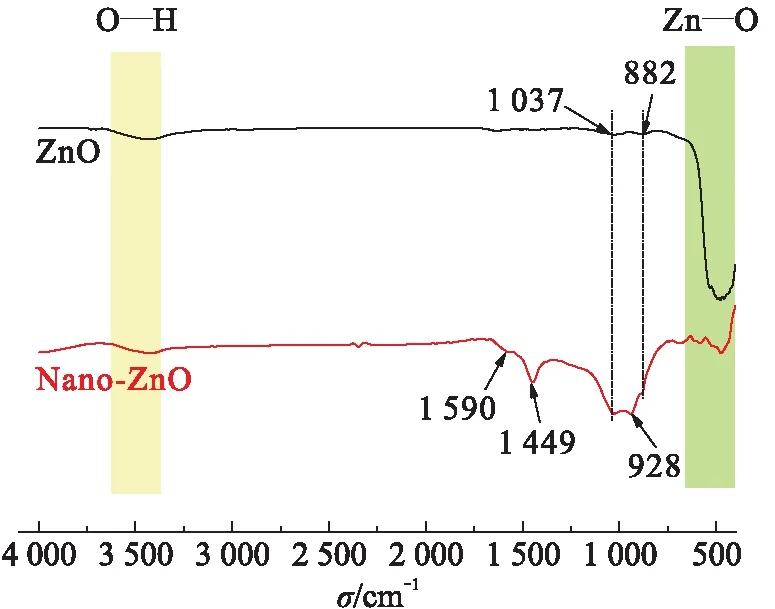
图2 Nano-ZnO和ZnO的FTIR谱
图3A为ZnO和Nano-ZnO的紫外吸收光谱,ZnO和Nano-ZnO在紫外光区表现出较强的光吸收性能,Nano-ZnO的吸收带边出现红移现象,扩展了光催化剂对可见光的响应范围。与ZnO相比,Nano-ZnO在可见光区的光吸收利用效率得到提高。
根据图3B,计算带隙能(Eg):
(3)
其中,Eg为带隙能,h为普朗克斯常数,c为光速,λ为样品特征波长。
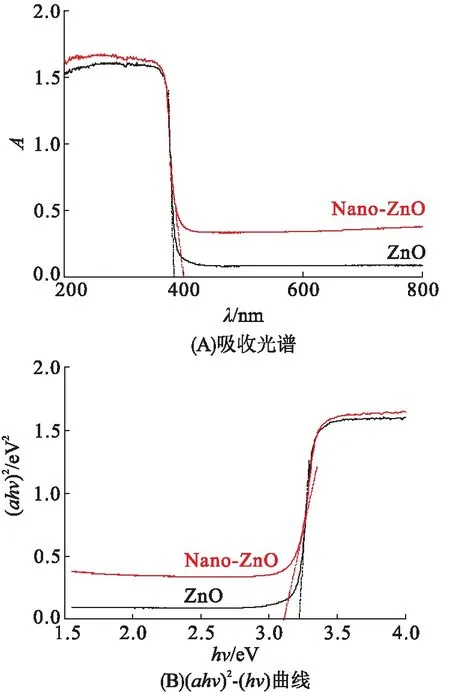
图3 Nano-ZnO和ZnO的UV-Vis DRS谱
计算结果显示,ZnO带隙能为3.21 eV,而Nano-ZnO的带隙能减小到3.09 eV,带隙能减小即电子从价带转移至导带(O 2p→Zn 3d)基带吸收能降低,有利于光催化时的电子转移[20],通过费米能级原理进一步证明绿色合成的Nano-ZnO在可见光区域的光响应显著改善。
Nano-ZnO颗粒呈球形、椭圆形、棒状等不规则形状(图4),颗粒分散性好,团聚现象较少,这与互花米草中类黄酮、生物碱类、氨基酸、蛋白质等生物小分子有关,这些小分子在ZnO的氧化锌合成过程中起分散剂的作用[21]。小的粒径有利于产生较多的光催化活性位点,同时团聚程度小有助于提高Nano-ZnO光催化及抑菌性能。

图4 Nano-ZnO和ZnO的SEM图
2.2 材料对孔雀石绿的光催化降解性能
Nano-ZnO与ZnO对孔雀石绿溶液的光催化降解性能测试结果(图5)表明,Nano-ZnO光催化性能明显优于ZnO,在达到吸附平衡后计时(t=0)并光照60 min,Nano-ZnO对孔雀石绿的去除率可达98.2%。与ZnO相比,较高的光催化活性与Nano-ZnO的禁带宽度减小有关,禁带宽度减小使得光催化剂在相同光照条件下可以产生更多的电子空穴对,同时通过XRD和SEM表征发现Nano-ZnO粒径较小,颗粒团聚程度降低,这有利于阻止电子和空穴的复合以及光生载流子的转移,从而使Nano-ZnO光催化性能得到显著提高。

图5 Nano-ZnO和ZnO对孔雀石绿的去除率
Nano-ZnO光催化降解MG溶液的吸收光谱(图6)显示,随着光照时间增加,MG在波长617 nm处的特征吸收峰强度逐渐降低,表明MG溶液中主要的发色基团逐渐被破坏,降解液在光照60 min后几乎观察不到特征峰,表明降解过程已基本完成。
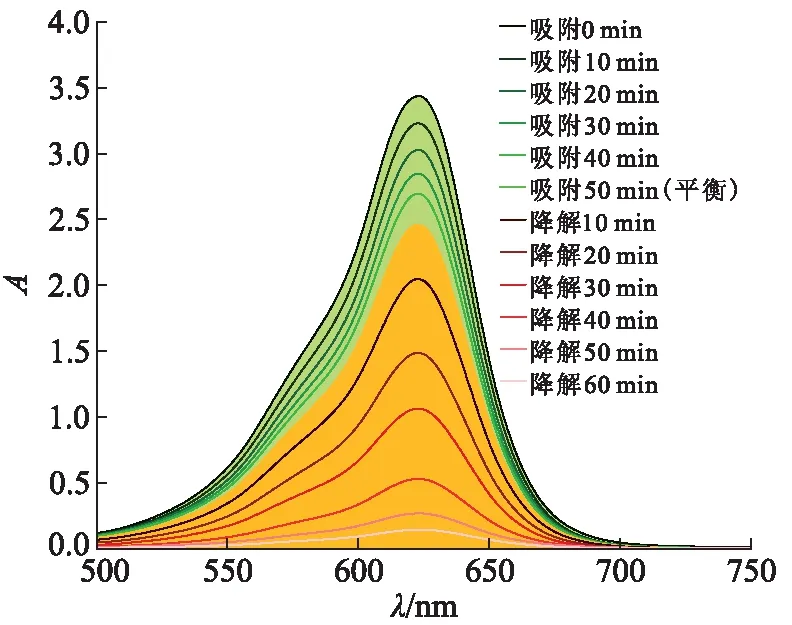
图6 孔雀石绿溶液的吸收光谱
2.3 活性物种分析
通过自由基捕获实验,分别添加二甲基亚砜、甲酸和对苯醌测试Nano-ZnO在光催化降解MG溶液时产生的活性氧自由基种类(图7)。结果表明:在Nano-ZnO对MG染料光催化降解过程中,h+和·O2-是Nano-ZnO发挥作用的主要活性物种。
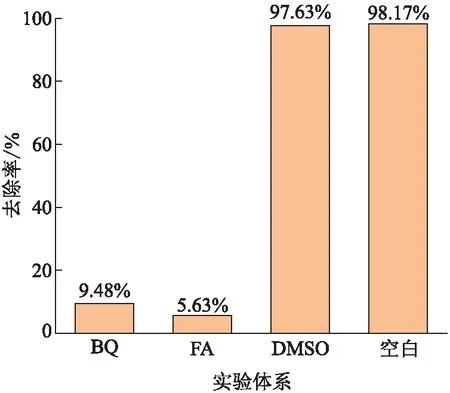
图7 BQ、FA和DMSO对可见光照射下Nano-ZnO对孔雀石绿去除率的影响
2.4 抗菌分析
通过抑菌圈法对Nano-ZnO的抑菌活性进行测试(图8),绿色合成ZnO对金黄色葡萄球菌的抑菌圈平均直径为16.75 mm,作为对照,ZnO对金黄色葡萄球菌的抑菌圈平均直径为8 mm,表明使用植物提取液绿色制备的Nano-ZnO抗菌性能更好。目前,对抗生素的广泛使用导致一些耐药菌株的出现,而使用抗菌药物或会对身体造成不同程度损伤,ZnO纳米颗粒的抗菌机制与传统抗菌剂不同,其光催化活性、生物相容性以及选择性使其成为目前抑菌材料的研究热点。据报道,ZnO纳米粒子接触细菌可以产生活性氧(ROS)和锌离子,进而攻击细菌细胞壁达到抑菌效果[22-23]。本实验使用互花米草提取液绿色制备的Nano-ZnO具有小尺寸和良好的分散性,能够有效破坏细菌的细胞膜以及产生活性氧从而提高其抑菌性能。
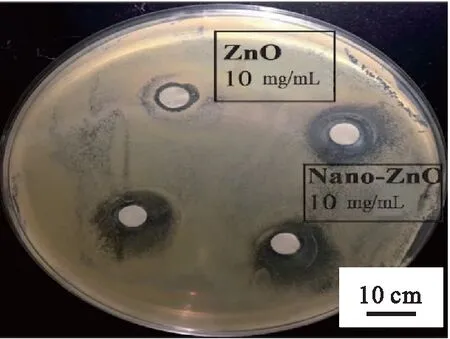
图8 Nano-ZnO和ZnO的抑菌性能
3 结论
利用互花米草提取液,采用溶胶-凝胶法成功制备Nano-ZnO纳米颗粒,该纳米颗粒具有较好的光催化降解性能,对有机染料孔雀石绿的降解率达到98.2%。Nano-ZnO所具有的较小粒径、良好的分散性、较多的官能团以及禁带宽度的减小是光催化活性增强的因素。活性物种测试实验表明:在降解MG染料时Nano-ZnO中发挥作用的主要活性物种为h+和·O2-。抗菌实验表明:互花米草提取液绿色化学法制备的Nano-ZnO具有更高的抑菌性能,对金黄色葡萄球菌的抑菌率是ZnO的2倍。
本研究使用植物提取液绿色化学法制备氧化锌纳米颗粒,不仅有效避免ZnO在化学合成过程中产生次级代谢废物以及二次污染,而且在制备过程中体现快速、低成本、环保的理念,将其应用于光催化降解有机染料的处理工艺,实现从植物合成到太阳能驱动的光催化理念,同时也为外来入侵物种互花米草提供一种高值化利用的新途径。

