基于咪唑并吡啶的双极性绿色磷光主体材料合成及其性能
黄科文, 陈嘉雄*, 戴 雷, 白科研, 周 路, 霍延平*
(1. 广东工业大学 轻工化工学院, 广东 广州 510006; 2. 广东阿格蕾雅光电材料有限公司, 广东 佛山 528300)
1 引 言
有机电致发光器件(OLED)因具有高分辨率、宽视角、更快响应速度以及可弯曲等优点[1-6],在智能手机、电视屏幕显示器和照明应用面板方面得到广泛的应用。根据自旋统计规则,OLED中电荷复合产生的单线态和三线态激子的比例为1∶3[7]。三线态激子通常是非发射性的,且与单态激子相比其能量更低、寿命更长。因此,传统荧光OLED的内量子效率(IQE)被限制在25%。对于磷光OLED而言,由于磷光材料中过渡金属的存在,使得单线态激子很容易通过快速系间窜越(ISC)转换为三线态激子,然后所有三线态激子以磷光的形式辐射衰减,从而捕获所有激子,进而实现100%的理论最大IQE,因而磷光OLED引起了人们的广泛关注[8-9]。迄今为止,磷光OLED的外量子效率(EQE)已超过20%。
为了防止三线态-三线态湮灭(TTA)和三线态极化子猝灭(TPQ)效应,磷光材料大多需要掺杂在合适的主体材料中,从而获得高性能的器件。因此,主体材料对于决定器件的整体性能具有十分重要的作用[10-11]。为了防止客体向主体的反向能量转移,主体需要具有比客体更高的三线态能级(T1)[12-13]。然而,主体材料三线态能级过高,不仅容易导致较深的最高占据分子轨道(HOMO)能级,使驱动电压升高,还容易引起客体诱导捕获激子,从而产生严重的效率滚降[14]。另外,为了提高器件的发光效率,加快载流子迁移率和平衡载流子的通量也是必不可少的。相比于传统的主体材料,双极性主体材料不仅可以更高效地平衡空穴和电子,还能改善载流子迁移率,更加有利于激子在发光层的复合,从而提高器件的发光效率[15-20]。因此,开发合适的双极性主体材料在有机电致发光材料的研究中至关重要。
本文选用咔唑衍生物为给体基团,其具有刚性的结构和高三线态能级,且其强给电子特性赋予了其良好的空穴传输性能;采用咪唑并吡啶衍生物作为受体基团以提高电子传输性能[21];引入刚性结构基团二苯并呋喃可以很好地平衡空穴和电子[8]。采用咪唑并吡啶、9-苯基咔唑和二苯并呋喃之间连接有和无苯环,我们设计合成了两种D-A型双极性绿光主体材料即9-苯基-3-(9-(4-(3-苯基咪唑并[1,2-a]吡啶-2-基)苯基)二苯并[b,d]呋喃-2-基)-9H-咔唑(CzDFDp)和9-苯基-3-(3-(9-(4-(3-苯基咪唑并 [1,2-a] 吡啶-2-基)苯基)二苯并 [b,d] 呋喃-2-基)苯基)-9H-咔唑(CzPDFDp)。与现有常用的绿光磷光主体材料4,4′-双(N-咔唑)-1,1′-联苯(CBP)进行了性能比较。实验结果显示,使用CzDFDp和CzPDFDp作为绿光磷光主体材料制作的OLED器件发光性能更高。
2 实 验
2.1 化合物合成
2-(4- (8-氯二苯并[b,d]呋喃-1-基)苯基)-3-苯基咪唑并[1,2-a]吡啶和三(4-甲基-2,5-二苯基吡啶)合铱(GD-Ir)由广东阿格蕾雅光电材料有限公司提供,纯度均为99%;1-溴-8氯二苯并呋喃、(9-苯基-9H-咔唑-3-基)硼酸和9-苯基-3-(3-(4,4,5,5-四甲基-1,3,2-二氧硼烷-2-基)苯基)-9H-咔唑均从上海阿拉丁生化科技股份有限公司购买,纯度为99%;其他试剂为工业级。
两个分子的结构和合成路线如图1所示,它们都可以通过两步合成得到,合成方法较为简单,易于合成。首先,选用1,1′-双二苯基膦二茂铁二氯化钯作为催化剂,在碳酸钾的作用下,原料1和原料2通过Suzuki偶联反应得到中间产物3,然后将3分别与4a和4b进行Suzuki偶联反应,得到两个目标产物。合成的中间产物和目标产物的结构已通过质谱和核磁共振谱进行了确认,具体合成步骤如下。
2-(4-(8-氯二苯并[b,d]呋喃-1-基)苯基)-3-苯基咪唑并[1,2-a]吡啶的合成:将8 g(20.19 mmol) 3-苯基-2-(4-(4,4,5,5-四甲基-1,3,2-二氧硼烷-2-基)苯基)咪唑并[1,2-a]吡啶、6.25 g(22.21 mmol) 1-溴-8氯二苯并呋喃、1.17 g(1.01 mmol) 1,1′-双二苯基膦二茂铁二氯化钯、5.58 g(40.37 mmol)碳酸钾加入到50 mL单口烧瓶中,缓慢加入160 mL二氧六环和40 mL水进行溶解,在氮气条件保护下加热80 ℃回流3 h。反应完毕后,将反应液进行浓缩,之后用500 mL水和1 L乙酸乙酯进行萃取,萃取后的有机液旋干后用乙酸乙酯/正己烷 (1∶3)为洗涤剂进行柱层析分离得到8.2 g产物,纯度:99.70%,收率:86.23%。1H NMR(400 MHz,CDCl3)δ8.02(d,J=7.0 Hz,1H),7.86(d,J=8.3 Hz,2H),7.73(d,J=9.0 Hz,1H),7.67~7.39(m,12H),7.34(d,J=8.7 Hz,1H),7.28(s,1H),7.23(d,J=9.3 Hz,1H)。
9-苯基-3-(9-(4-(3-苯基咪唑并[1,2-a]吡啶-2-基)苯基)二苯并[b,d]呋喃-2-基)-9H-咔唑(CzDFDp)的合成:将8.2 g(17.41 mmol) 2-(4-(8-氯二苯并[b,d]呋喃-1-基)苯基)-3-苯基咪唑并[1,2-a]吡啶、6 g(20.89 mmol)(9-苯基-9H-咔唑-3-基)硼酸、1.59 g (1.74 mmol) 三(二亚苄基丙酮)二钯、0.976 g (3.48 mmol) 三环己基膦、11.59 g (43.53 mmol) 三水磷酸钾加入到500 mL单口烧瓶中,缓慢加入246 mL二氧六环和41 mL水进行溶解。在氮气条件保护下,反应完毕后,将反应液进行浓缩,之后用500 mL水和1 L乙酸乙酯进行萃取,萃取后的有机液旋干后用乙酸乙酯/正己烷 (1∶3) 为洗涤剂进行柱层析分离得到8.4 g产物,纯度:99.97%,收率:71.29%。1H NMR (400 MHz,CDCl3)δ8.22(d,J=1.4 Hz,1H), 8.04(d,J=7.8 Hz,1H),7.90(t,J=6.2 Hz,4H),7.76(dd,J=8.5,1.8 Hz,1H),7.71(d,J=9.0 Hz,1H),7.64(dd,J=8.4,2.4 Hz,3H),7.61~7.48(m,7H),7.47~7.27(m,10H),7.25~7.20(m,1H),7.08(t,J=6.6 Hz,1H),6.74(t,J=6.6 Hz, 1H).13C NMR(101 MHz,CDCl3)δ156.97,155.63,144.79,143.24,141.30,140.13,139.01,137.84,137.72,136.56,135.80,133.51,130.72,129.89,129.72,129.56,129.05,129.00,128.10,127.44,127.07,126.64, 125.99,125.55,124.91,124.43,123.98,123.91,123.48,123.37,121.90,121.37,121.01,120.42,119.84,118.80,117.54,112.40,111.56,110.55,110.09,109.76,77.37,77.05,76.73。ESI-MSm/z: calcd for C49-H31N3O,677.246 7;found:678.252 9 [M+H]+。
9-苯基-3-(3-(9-(4-(3-苯基咪唑并[1,2-a]吡啶-2-基)苯基)二苯并[b,d]呋喃-2-基)苯基)-9H-咔唑(CzPDFDp)的合成:将1 g(2.12 mmol) 2-(4-(8-氯二苯并[b,d]呋喃-1-基)苯基)-3-苯基咪唑并[1,2-a] 吡啶、1.13 g(2.55 mmol) 9-苯基-3-(3-(4,4,5,5-四甲基-1,3,2-二氧硼烷-2-基)苯基)-9H-咔唑、0.194 g(212.34 μmol)三(二亚苄基丙酮)二钯、0.202 g (424.68 μmol) 2-二环己基磷- 2’4′,6′三异丙基联苯、1.41 g(5.31 mmol) 三水合磷酸钾,加入到100 mL单口烧瓶中,缓慢加入20 mL二氧六环和5 mL水进行溶解。在氮气条件保护下,反应完毕后,将反应液进行浓缩,之后用300 mL水和200 mL乙酸乙酯进行萃取,萃取后的有机液旋干,之后用乙酸乙酯∶正己烷=1∶5进行柱层析得到1 g 产物,纯度:99.98%,收率:80.2%。1H NMR(400 MHz,CDCl3)δ8.35(d,J=1.2 Hz,1H),8.15(d,J=7.7 Hz,1H),7.91~ 7.80(m,5H),7.72(dd,J=8.5,1.8 Hz,1H),7.57(dtt,J=12.4, 4.7,3.6 Hz,14H),7.45~7.38(m,6H),7.32(tdd,J=11.9, 7.4,4.5 Hz,5H),7.15~7.09(m,1H),6.64(t,J=6.8 Hz, 1H).13C NMR(101 MHz,CDCl3)δ156.94,156.03, 144.87,142.60,142.17,141.93,141.34,140.37,138.87,137.95,137.71,136.26,134.02,133.45,130.68,129.96,129.79,129.56,129.30,128.96,128.16,127.52,127.18,127.12, 126.80,126.69,126.12,126.00,125.67,125.57,124.68,124.49,123.97,123.87,123.48,123.22,121.88,121.31,121.24,120.40,120.10,118.97,117.50,112.23,111.64,110.56,110.06,109.89。HRMS-ESIm/z:calcd for C55-H35N3O,753.278 0;found:754.284 3 [M+H]+.

图1 化合物CzDFDp和CzPDFDp的合成路线
2.2 理论模拟
我们首先采用B3LYP/6-31G*基组下密度泛函理论 (DFT)对CzDFDp和CzPDFDp进行研究模拟,图2中显示出两个分子的最高占据分子轨道(HOMO)电子云主要分布在苯基咔唑基团上,最低未占据分子轨道(LUMO)电子云主要分布在咪唑并吡啶基团上,两个分子的HOMO和LUMO的分离是由咔唑的强给电子特性和咪唑并吡啶的吸电子特性造成的。这意味着HOMO由咔唑决定,而LUMO由咪唑并吡啶决定。因此,这两种主体材料在OLED中表现出双极传输特性。

图2 CzDFDp(a)、CzPDFDp(b)的HOMO和LUMO轨道分布图。
2.3 电化学和热学性质
为了进一步得到双极性主体材料的能级,我们采用循环伏安法(CV)对两个材料进行了测定,采用四丁基六氟磷酸铵(Bu4NPF6)为电解质,在二氯甲烷(DCM)溶液中对两种材料的氧化电位进行了扫描。图3是CzDFDp和CzPDFDp的氧化电位曲线,从它们氧化电位的起始位置计算可得CzDFDp和CzPDFDp的HOMO能级分别为-5.53 eV和-5.5 eV,利用光学带隙计算LUMO能级分别为-2.21 eV和-2.22 eV,与电子传输材料TPBi相匹配,说明具有良好的电子传输性质。因此,CzDFDp和CzPDFDp不仅可以传输空穴而且还可以传输电子,具有双极性传输性质。

图3 CzDFDp 和CzPDFDp的氧化曲线
利用热重分析(TGA)和差示扫描量热法技术(DSC)测定了CzDFDp和CzPDFDp的分解温度(Td,在5%损失下分解温度)和玻璃转换温度(Tg),由图4、5中可以看出,化合物CzDFDp和CzPDFDp的分解温度分别是509 ℃和529 ℃,玻璃转换温度分别是130 ℃和138 ℃,较高的分解温度和玻璃化转换温度表明了该系列材料具有较好的热稳定性和形貌稳定性,有利于器件蒸镀成膜,对于器件的稳定运行具有重要意义。
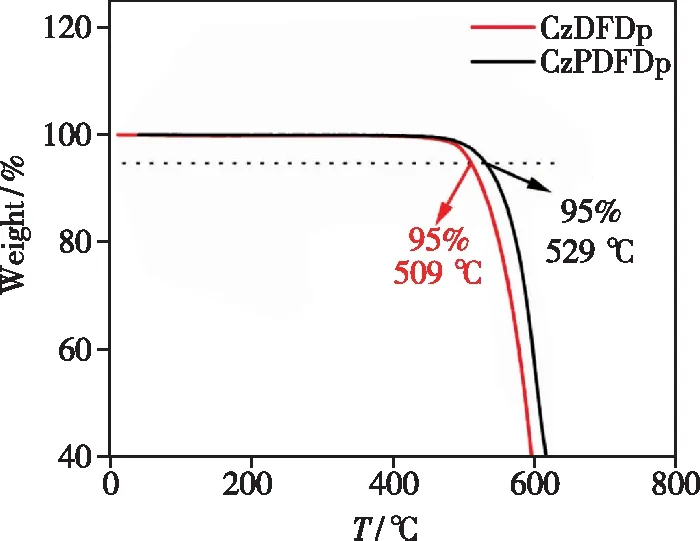
图4 CzDFDp和CzPDFDp的TGA曲线

图5 CzDFDp和CzPDFDp的DSC曲线
2.4 光谱性质
CzDFDp和CzPDFDp的紫外-可见吸收光谱(UV-Vis)采用TU-1810PC紫外-可见光谱仪、荧光光谱采用F-2700荧光光谱仪、低温77 K磷光采用爱丁堡FLS980稳态/瞬态荧光光谱仪测试。
由图6可以看出,CzDFDp和CzPDFDp的紫外-可见吸收光谱相似,在280 nm和250 nm附近有两个特征吸收峰。这两个特征吸收峰可归于分子的π-π*跃迁。两个材料最大吸收分别在374 nm和370 nm,其光学能隙(Eg)可通过(Eg=1240/λabs)计算得到(见表1),分别为3.32 eV和3.35 eV。测得CzDFDp和CzPDFDp室温荧光分别是403 nm和404 nm,呈现蓝光发射。在77 K温度下测量了薄膜状态下的磷光发射光谱,三线态能级(ET)由低温磷光第一发射峰和起始峰分别计算,为2.80 eV和2.49 eV。CzPDFDp分子中苯环链接二苯并呋喃和苯并咔唑,增强了局域共轭,分子轨道简并程度更强,使得CzPDFDp低温荧光发生红移,所以CzPDFDp具有降低的三线态能级;同时,苯环的引入增强了苯并咔唑、苯和二苯并呋喃的旋转和振动,使其非辐射跃迁增强并伴随减色效应。CzDFDp和CzPDFDp高于绿光磷光发光材料GD-Ir (T1<2.4 eV) 的三线态能级,因此,能够很好地阻止能量进行回传。

图6 CzDFDp(a)和CzPDFDp(b)的紫外-可见光吸收、荧光和低温(77 K)磷光光谱。

表1 CzDFDp、CzPDFDp的光谱学、电化学和热稳定性质
3 器件性能
3.1 单载流子测试
为进一步研究三种化合物的电子和空穴传输能力,制备了单空穴(HOD)和单电子器件(EOD),HOD器件结构为:HATCN(10 nm)/TAPC(50 nm)/host(40 nm)/HATCN(10 nm)/Yb(1 nm)/Ag(100 nm),纯电子器件结构为:Ag(100 nm)/BCP(10 nm)/host(40 nm)/TPBi∶LiQ(50 nm,1∶1)/Yb(1 nm)/Ag(100 nm)。图7显示了HOD和EOD器件的J-V图,由图中可知,CzDFDp和CzPDFDp的空穴传输性能均略高于CBP,主要是引入了具有较高空穴传输能力的苯并咔唑基团。而EOD中,CzDFDp和CzPDFDp电子电流密度远远高于CBP,且在2.2 V时即注入到器件中,明显低于CBP的4.0 V,说明CzDFDp和CzPDFDp中的咪唑并吡啶缺电子基团极大地改善了主体材料的电子传输和注入性能,证明CzDFDp和CzPDFDp具有双极性特性,有利于平衡空穴和电子。
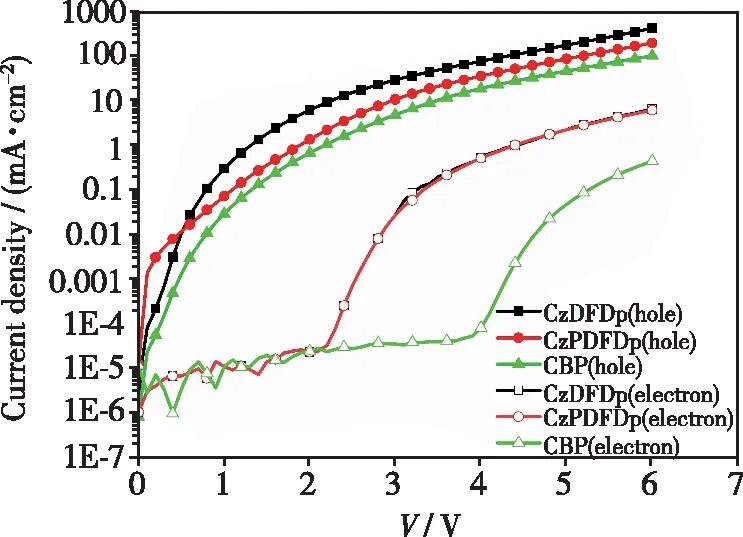
图7 CzDFDp 、CzPDFDp和CBP单载流子器件的电流密度-电压。
3.2 器件制备
由于两个材料具有高的热稳定性、合适的能级、双极电荷传输能力以及优异的光物理性质等优点,我们将两种双极性化合物用作磷光主体材料,并设计了器件结构为:ITO/HATCN(10 nm)/TAPC(50 nm)/Host∶GD-Ir(30 nm∶6%)/TPBi∶LiQ(50 nm,1∶1)/Yb(1 nm)/Ag(100 nm) 的器件。其中,ITO是铟锡氧化物,HATCN(二吡嗪[2,3-f∶2′,3′-h]喹啉-2,3,6,7,10,11-六碳腈)是空穴注入层,TAPC(4-[1-[4-[二(4-甲基苯基)氨基]苯基]环己基]-N-(3-甲基苯基)-N-(4-甲基苯基)苯胺)是空穴传输层,器件Ⅰ和器件Ⅱ的Host分别是CzDFDp(器件Ⅰ)和CzPDFDp(器件Ⅱ)。我们同时也制备了与两个器件做对比的基于4,4′-双(N-咔唑)-1,1′-联苯(CBP)的器件Ⅲ,掺杂客体铱GD-Ir,TPBi(1,3,5-三(1-苯基-1H-苯并咪唑-2-基)苯)是电子传输层,基片选用10 Ω的ITO导电玻璃,进行阳极图案设计、刻蚀阳极、清洗基片及O2plasma预处理。制备过程中系统的真空度应高于3×10-4Pa。器件的测试采用美国Photo Research公司生产的PR655分光扫描式亮度色度计和美国Keithley公司生产的K2400数字源表组成的测试系统。器件中的分子结构[9]如图8和图9所示。
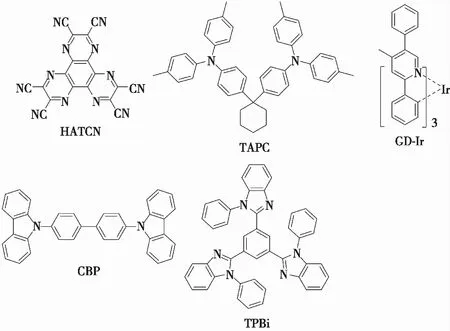
图8 器件中所用材料的化学结构

图9 器件Ⅰ、Ⅱ和Ⅲ各功能层能级结构。
3.3 器件对比
三个器件的电致发光性质如图10~11和表2所示。从图10可知,器件Ⅰ和Ⅱ具有较低的启亮电压,约为2.6 V,相比于CBP作为主体的器件Ⅲ的启亮电压降低了约1.0 V。启亮电压的大幅度降低主要原因是主体材料的LUMO能级与TPBi的LUMO能级相匹配,电子能够很好地从TPBi注入到CzDFDp和CzPDFDp两个主体材料中,且在主体中能快速复合产生激子。其中相同电压下,CzDFDp的电流密度略高于CzPDFDp,这可能是由于CzDFDp的平面性较好,分子堆积更加紧密,更有利于载流子的传导[22]。

图10 器件Ⅰ、Ⅱ和Ⅲ的亮度-电压-电流密度曲线。
图11(a)中,器件Ⅰ和Ⅱ都展现了较好的效率,最大电流效率分别是44.9,47.2 cd·A-1,最大功率效率分别是50.4,57.0 lm·W-1,远远高于器件Ⅲ(14.4 cd·A-1,5.8 lm·W-1)。较好的器件效率主要归因于主体材料良好的双极传输性质,电子和空穴都能够较好地注入到主体中,且在主体中有效地传输和复合,可显著增加激子复合区域宽度,从而降低三线态激子浓度,抑制三线态激子自湮灭,因而提升了电致发光效率,降低了效率滚降;而CBP作为主体材料,其电子无法在主体中得到很好的传输,因此激子复合发生在CBP和TPBi界面上,复合区域较窄,图中其电流效率在高亮度下达到最大值也说明该器件中电子与空穴严重不平衡。即使在高亮度下,CzDFDp和CzPDFDp的器件仍能保持较高的电致发光效率,在100 cd·m-2和1 000 cd·m-2下,两个材料的电流效率分别为37.0,36.8,29.0,27.8 cd·A-1,效率滚降分别为17.6%、22.0%和35.4%、41.1%,前者较低的效率滚降说明其具有更好的电子和空穴平衡性能,是一种优异的双极传输材料。

图11 (a)器件Ⅰ~Ⅲ的电流效率-亮度-功率效率曲线;(b)器件Ⅰ~Ⅲ电致发光光谱。
三个器件的电致发光光谱如图11(b),在8 V电压下的色坐标分别是(0.34,0.62)、(0.34,0.62)和(0.34,0.60),说明器件的电致发光光谱均为绿光掺杂剂的发射光谱。而CBP器件的色坐标与前两者略有差异,归结于其电致发光光谱中出现一个480 nm的蓝光峰[23],与TPBi的发射光谱相匹配,再次证明该器件中CBP的激子复合发生在发光层与电子传输层界面处,激子被TPBi捕获而发光。而CzDFDp和CzPDFDp的器件在不同电压下都未出现TPBi的发光峰(图12),其电致发光光谱未发生改变,表现出良好的电致发光稳定性。

图12 (a)器件Ⅰ在不同电压下的电致发光光谱;(b)器件Ⅱ在不同电压下的电致发光光谱。

表2 器件的发光性能
4 结 论
综上所述,通过光物理性能研究表明,我们合成的CzDFDp和CzPDFDp两种新型双极性绿光主体材料具有较高的T1、较好的热稳定性和形貌稳定性,有利于器件蒸镀和成膜。在器件中,采用的CzDFDp和CzPDFDp作主体绿光器件的启动电压均为2.6 V,最大电流效率分别达到44.9 cd·A-1和47.2 cd·A-1,最大功率效率达到50.4 lm·W-1和57 lm·W-1,相比CBP作为主体器件(3.6 V,14.4 cd·A-1,5.8 lm·W-1),两个主体材料的启亮电压降低了1 V,最大电流效率提高3倍以上,且功率效率提高了8倍以上,表明本文两个主体材料具有良好的双极性传输性质,能够有效地平衡载流子通量,是优异的绿光主体材料。
本文专家审稿意见及作者回复内容的下载地址:http://cjl.lightpublishing.cn/thesisDetails#10.37188/CJL.20210415.

