SCR脱硝氨转化、吸附及飞灰氨脱除技术研究现状
唐 潇,徐仁博,张发捷,马云龙,赵 宏,王乐乐,孙路石,于 洁
(1.华中科技大学 煤燃烧国家重点实验室,湖北 武汉 430074;2.华能大连电厂,辽宁 大连 116033;3.西安热工研究院有限公司苏州分公司,江苏 苏州 215153)
0 引 言
据生态环境部发布的《2020年全国大、中城市固体废物污染环境防治年报》显示,2019年重点调查工业企业的粉煤灰产生量为5.4亿t,其中4.7亿t来自电力、热力生产和供应业,占粉煤灰总量的86.1%[1]。粉煤灰产量巨大,随意填埋或堆放会消耗大量土地资源,还会破坏环境。将粉煤灰作为二次资源进行综合利用,能有效减轻环境污染、实现循环经济,产生可观的环境与社会效益[2-3]。
由于粉煤灰具有比表面积大、细度小、渗透性良好、火山活性高等特性,作为矿物掺合料时可延缓水泥水化热峰值出现的时间、改善混凝土物理力学性能、抑制混凝土碱骨料反应、提高混凝土长期稳定性、减少泛浆和早期开裂等现象[4-5]。此外,粉煤灰还可用来制作陶瓷材料、改良土壤品质、提取金属铝、作吸附剂等。目前我国粉煤灰综合利用率已近75%[1],其中用于制作水泥、混凝土以及墙体材料的粉煤灰占80%以上。粉煤灰提铝能在一定程度上缓解我国铝供求矛盾,主要包括烧结法、水化学法和酸浸取法等方法[2]。
近年来,随着烟气脱硝技术普及,粉煤灰在实际工程应用中暴露一些问题。为保证选择性催化还原技术(Selective Catalytic Reduction,SCR)和非选择催化还原技术(Selective Non Catalytic Reduction,SNCR)的脱硝效率,会向系统中喷入过量氨,若设备中流场分布不均,脱硝过程中不可避免有部分氨未与烟气中NOx反应而逃逸出来,70%~80%的逃逸氨最终会吸附在粉煤灰上[6],使粉煤灰氨质量分数达200~2 500 mg/kg[7]。戴会生等[8]发现使用含氨粉煤灰作掺和料时,混凝土浇筑后会冒出大量气泡,且硬化后表面会形成空鼓,整体体积增大甚至开裂,测试发现混凝土含气量增加10%,抗压强度降低30%,粉煤灰在碱性环境下会释放刺鼻气味,经检测为氨气。莫卫民等[9]发现与使用未脱硝粉煤灰相比,在相同制作条件下,含氨粉煤灰的加入会降低3 d和7 d水泥抗折和抗压强度。罗斌[10]发现含氨粉煤灰会导致混凝土含气量增大,强度降低10%以上,建议制作高标号和高性能混凝土时避免使用含氨粉煤灰。
通常认为氨质量分数≥300 mg/kg的粉煤灰释放的氨气足以危害人体健康[11]。经检测,在空气流通环境中使用氨质量分数200 mg/kg以下的粉煤灰,释放的气味可接受,但BITTNER等[12]建议粉煤灰氨质量分数应在100 mg/kg以下。美国普遍认为资源化利用的粉煤灰氨质量分数不应超过100 mg/kg,而德国为50 mg/kg[13]。
为保证含氨粉煤灰正常销售,促进粉煤灰综合利用,学者积极研究粉煤灰对氨的吸附特性及含氨粉煤灰脱氨方法。笔者主要论述了国内外粉煤灰氨含量的主要影响因素,总结现有粉煤灰脱氨技术,以期为相关研究提供参考。
1 NH4HSO4的生成
1.1 选择性催化还原技术
SCR技术脱硝效率高(80%~90%)[14]、运行可靠、便于操作与维护,成为燃煤电厂烟气脱硝的首选技术。SCR烟气脱硝技术是在含氧氛围下,向烟气中喷入适量还原剂(NH3、尿素或其他氮氢化合物),在催化剂作用下,于300~420 ℃温度窗口内选择性地与烟气中NOx反应。以NH3作还原剂为例,发生的反应如下:

(1)

(2)

(3)

(4)
在理想条件下NH3与NOx完全反应,生成无害的N2与H2O,如图1所示。
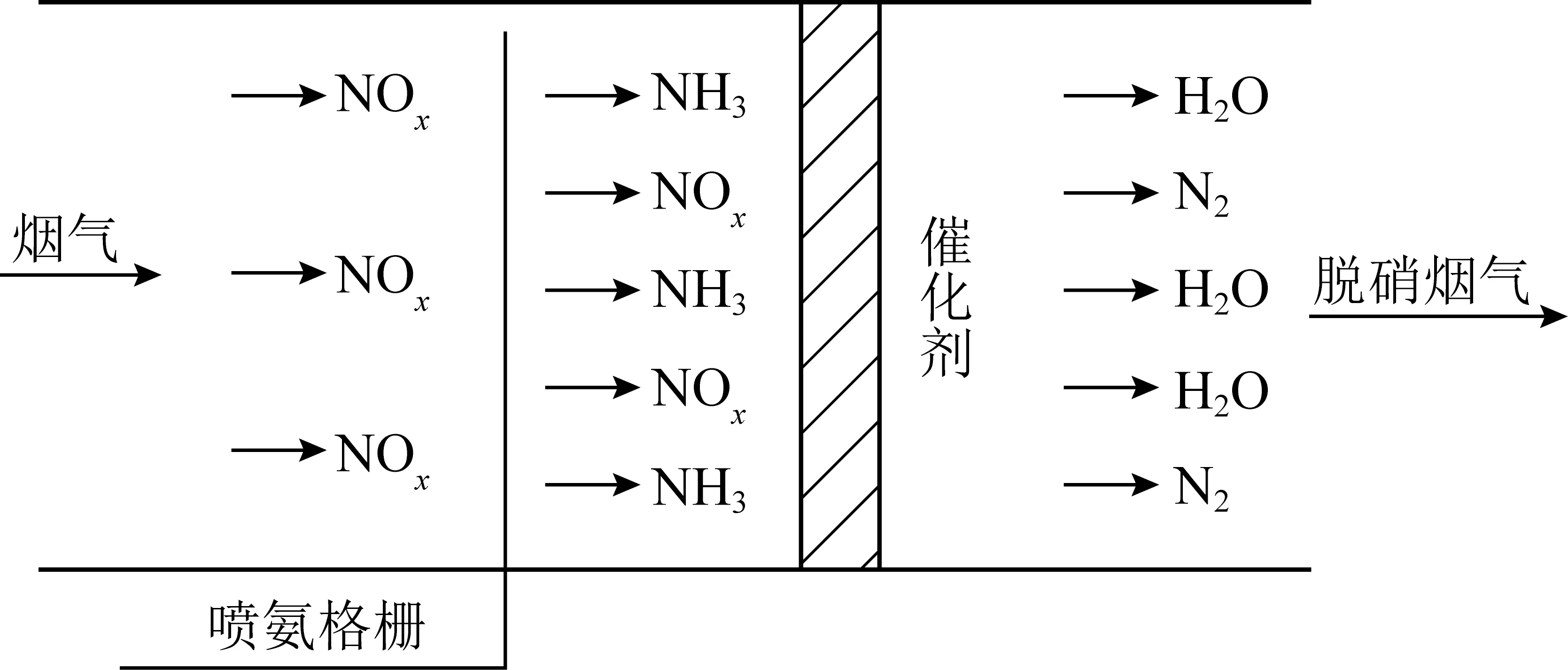
图1 SCR脱硝原理Fig.1 Principle of SCR denitrification
我国SCR烟气脱硝装置一般采用高尘布置,即布置在省煤器后,烟气先脱硝处理,随后进入空预器,经过除尘系统,最后脱硫处理。这种布置方式使得烟气有足够温度保证反应正常进行,但烟气未经处理,成分复杂,催化剂易中毒失活。目前燃煤电厂使用最多的是V2O5-WO3(或MoO3)/TiO2类催化剂[15]。V2O5催化剂活性组分表面呈酸性,易捕捉烟气中NH3使之与烟气中NOx反应;硫酸盐在TiO2载体上的稳定性较低,故TiO2具有较好的抗SO2性;WO3有助于抑制V2O5过强的氧化能力,减少SO2氧化;MoO3可提高催化剂活性,并在一定程度上减轻催化剂砷中毒[16]。但钒系催化剂存在温度窗口较高较窄、V2O5极易升华等缺点,所以开发低温高效且对环境污染小的非钒类催化剂十分必要[17]。
1.2 前体物
1.2.1逃逸氨
为保证脱硝效率,SCR烟气脱硝装置一般会喷入过量NH3,设有喷氨格栅及导流板等装置,使烟气中NOx与喷入的NH3充分接触并反应。但SCR烟气脱硝系统中还原反应受运行条件影响,如氨氮物质的量比、催化剂成分与结构、NH3与NOx在烟气中分布情况、温度等[18],不可避免有一部分NH3未与NOx反应而逃逸出来,且逃逸量随SCR烟气脱硝系统运行,催化剂中毒、失活、堵塞等因素而加剧。HJ 562—2010《火电厂烟气脱硝工程技术规范——选择性催化还原法》规定,SCR烟气脱硝的NH3逃逸量应小于2.5 mg/m3[19]。
1.2.2SO3
燃煤中可燃硫(有机硫、单质硫、硫化亚铁等)在炉膛高温下被氧化为SO2,而部分SO2会在炉膛中进一步反应生成SO3,主要反应如下:

(5)

(6)

(7)
SO3生成量主要取决于燃煤含硫量及过量空气系数,与煤种关系不大[20],0.5%~2.5%的SO2会在炉膛处被氧化为SO3。
高温换热段(如过热器、省煤器等)换热面以及粉煤灰中含有的V2O5、Al2O3、Fe2O3、SiO2等氧化物均可促使SO2与O2发生反应生成SO3,反应式为

(8)
式(8)转换程度受烟气中O2浓度、SO2浓度、温度、氧化物催化效果影响。烟气离开省煤器,温度低于400 ℃后,氧化物的催化效果不再明显[21]。
目前在SCR烟气脱硝装置中使用最广泛的催化剂是V2O5-WO3(或MoO3)/TiO2类催化剂,V2O5质量分数在1.4%~4.5%,具有很强的氧化能力,是最重要的活性物质。SVACHULA等[22]发现催化剂的活性组分会催化SO2氧化反应;束航[23]分析了SO2在催化剂中V2O5作用下被氧化为SO3的过程。SCR烟气脱硝装置在300~420 ℃下将NOx催化还原为N2的同时,不可避免促进一部分SO2转换为SO3。SO2向SO3转化的转化率受温度、NH3/NOx以及O2浓度等因素影响:温度越高,催化剂表面活性点位越易在SO2作用下失活[24];NH3与NOx会优先SO2占据催化剂活性点位,从而减少SO2吸附氧化;O2能促进SO2的吸附行为[23]。张萼松[25]研究了V2O5-WO3/TiO2、V2O5-MoO3/TiO2、V2O5-Sb2O5/TiO2和V2O5-Nb2O5/TiO2四种催化剂对SO2的吸附效果,结果表明V2O5-WO3/TiO2、V2O5-MoO3/TiO2两种催化剂具有酸性,SO2吸附能大且不易被氧化;V2O5-Sb2O5/TiO2无法形成B酸,还会直接与SO2反应生成SO3;V2O5-Nb2O5/TiO2的L酸对电子的吸引能力很弱,同时其SO2吸附构型与钒钛催化剂相近,SO2氧化率较高。SCR烟气脱硝装置中SO2氧化率在0.5%~1.5%,实施超低排放后该数值应控制在1%以内[26]。
1.3 NH4HSO4生成影响因素

除催化剂表面,SCR烟气脱硝装置中逃逸的NH3与烟气中SO3接触时也能生成NH4HSO4与(NH4)2SO4,反应如下:

(9)

(10)

(11)

(12)
上述反应生成的物质种类主要取决于烟气中NH3与SO3的物质的量比。理论上,烟气中NH3与SO3物质的量比小于1时,上述反应趋向生成NH4HSO4;烟气中NH3与SO3物质的量比大于2时,上述反应趋向生成(NH4)2SO4;当2者物质的量比在1~2时,2者均有生成[29]。实际燃煤发电厂中,正常运行的SCR烟气脱硝装置逃逸NH3体积分数在2~3 mL/m3,而烟气中SO3体积分数主要取决于煤炭含硫量,对于低硫煤,烟气中SO3体积分数约12 mL/m3,对于中高硫煤,SO3体积分数达35~55 mL/m3[30]。可见烟气中SO3体积分数远高于NH3,故实际电厂运行中,更倾向于生成NH4HSO4。
张玉华[31]研究发现SCR烟气脱硝装置出口处存在大量亚微米级颗粒,经检测为NH4HSO4与(NH4)2SO4,认为由SO2氧化与氨逃逸引起,且颗粒物生成量与烟气中氨氮物质的量比、SO2、H2O、O2有关。BURKE等[32]也认为温度与气体反应物浓度是影响NH4HSO4与(NH4)2SO4生成的重要因素。
(NH4)2SO4熔点为230~280 ℃,280 ℃以上分解,而空预器冷端温度在150~200 ℃,故(NH4)2SO4在空预器中以干燥固体粉末形式存在,粒径小于10 μm,几乎无法在空预器处沉积,大部分以气溶胶形式随烟气输送至除尘器,但除尘器不会捕获(NH4)2SO4,最终(NH4)2SO4随烟气排入大气,参与PM10的排放[33-34]。
NH4HSO4露点约147 ℃,低于其初始生成温度,故NH4HSO4的生成反应为气相反应,MENASHA等[35]研究证实了这个观点。空预器中生成的NH4HSO4起初以气态形式存在,与烟气向空预器后部流动,随烟气温度降低逐渐液化。在实际电厂运行中,空预器冷端150~200 ℃有液态NH4HSO4沉积。液态NH4HSO4具有黏性,沉积在空预器表面后会吸附大量烟气中的粉煤灰。
MENASHA等[36]使用N2、CO2、H2O、O2、SO2、NH3和SO3模拟烟气,探究NH3与SO3浓度对NH4HSO4生成的影响。装置示意如图2所示,模拟烟气组成见表1。
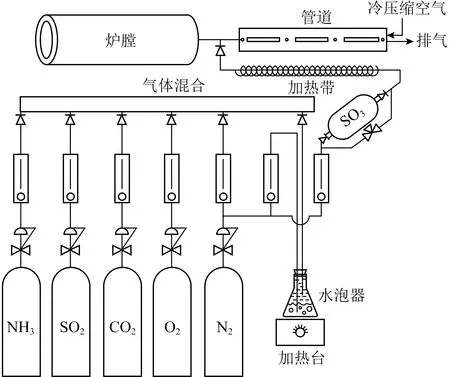
图2 NH4HSO4生成装置示意Fig.2 Schematic diagram of NH4HSO4 generating device
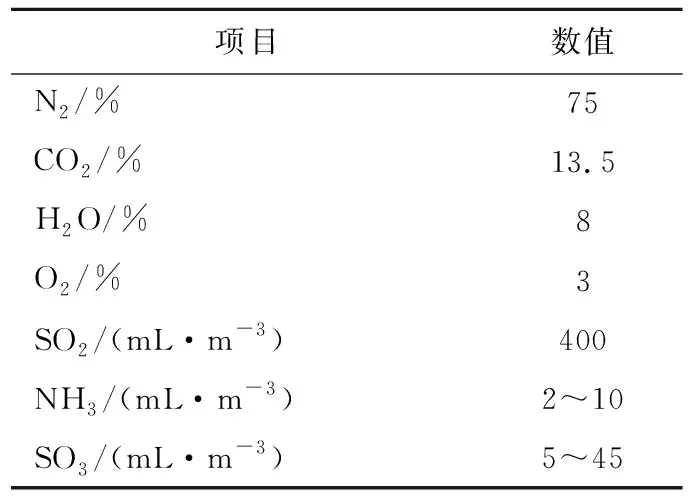
表1 模拟烟气体积分数Table 1 Components of simulated flue gas
NH4HSO4生成装置管道设有玻璃窗以确定NH4HSO4生成位置,并通过光学散射技术判断NH4HSO4是否以气溶胶形式生成,在管道内壁安装表面电极确定管壁上是否有NH4HSO生成,并使用热电偶监测烟气温度。结果表明,NH4HSO4在管道上游形成气溶胶,在温度较低区域表面沉积。NH4HSO4生成温度与NH3、SO3关系见表2。

表2 不同NH3、SO3浓度下NH4HSO4生成温度Table 2 Formation temperature of NH4HSO4 under different NH3 and SO3 concentrations
郑方栋[37]发现SO3和NH3反应先生成大量NH4HSO4,然后生成少量(NH4)2SO4。在NH3/SO3物质的量比相同时,随反应物体积分数增加,NH4HSO4和(NH4)2SO4生成速率逐渐增加,其中NH4HSO4生成速率上升幅度大于(NH4)2SO4。浓度积Φ[NH3]·Φ[SO3]在20~1 000 (μL/L)2时,NH4HSO4初始沉积烟温和沉积温度与反应物浓度积的对数呈线性正相关关系,沉积温度在225~251 ℃,初始沉积烟温在230~260 ℃。
杨建国等[38]用SO3、H2O、NH3三种气体混合模拟电厂的脱硝烟气,探究NH4HSO4初始生成温度,结果表明,在试验环境下,NH4HSO4初始生成温度在230~270 ℃。
卿梦霞等[39]向不同温度的玻璃反应管中通入一定比例的SO3、NH3,发现高温段223~390 ℃产物均为NH4HSO4,SO3浓度越低、沉积温度段越低,沉积物越易分解。低温段131~223 ℃,SO3、NH3物质的量比为2∶1时,生成物为H2O、H2SO4与NH4HSO4的混合物,SO3浓度与沉积温度越低,沉积物含水量越高,NH4HSO4含量越低,越易分解;SO3、NH3物质的量比为1∶1与1∶2时,沉积物分解特性与纯(NH4)2SO4基本一致。
由此可见,烟气中NH3与SO3浓度对NH4HSO4生成有决定性影响,NH3与SO3物质的量比小于1时,反应趋向生成NH4HSO4。而由于机组实际运行中粉煤灰中的氨主要以NH4HSO4形式存在。NH4HSO4生成为气相反应,初始生成温度刚好处于空预器温度范围内,烟气到达空预器冷端,温度下降,NH4HSO4变为液态,因其黏性高,极易吸附在粉煤灰表面致使氨含量升高并堵塞空预器。
2 粉煤灰对氨的吸附特性

TURNER等[41]探究了无SO3存在时,粉煤灰对NH3的吸附能力。向粉煤灰中通入不同浓度NH3,粉煤灰对NH3的单层吸附能力约为350 mg/kg。通入NH3体积分数500×10-6的气体、温度为350 ℃时,粉煤灰吸附NH3最少,该温度恰为SCR烟气脱硝装置催化剂处温度。在低温(<120 ℃)下发现,粉煤灰中水分能促进粉煤灰对NH3的吸附。常温下,通入NH3体积分数为500×10-6的气体,粉煤灰吸附NH3最大达600 mg/kg。
GOLDEN[42]采用含有SO2与NH3的合成气进行粉煤灰中氨的吸附试验,结果表明,不同煤种、不同燃烧条件下生成的粉煤灰对氨的吸附能力差异巨大。
O′CONNOR[43]以CO、CO2、H2O、O2、N2、HCl、NH3、NO、SO2、SO3和Hg(g)混合气来模拟电厂烟气,将模拟烟气通入加热的石英管中研究粉煤灰对NH3吸附特性。结果表明煤灰种类是影响NH3吸附的最关键因素,烟煤灰的NH3吸附能力是PRB(Powder River Basin,PRB煤是一种次烟煤,其S、Na、N和灰分含量低,Ca含量高)煤灰的数十倍;烟气中SO3的存在对NH3吸附影响仅次于粉煤灰种类,对于PRB煤灰,烟气中SO3的存在能使粉煤灰中吸附NH3翻倍,而对于烟煤灰,约增加30%。
MUZIO等[44]认为灰的烧失量、BET比表面积以及pH对NH3的吸附影响不大。IAOTS等[45]认为在SCR正常的氨逃逸浓度下,粉煤灰中残炭对NH3吸附影响不大,水蒸气与酸性气体的存在能促进粉煤灰对NH3吸附,粉煤灰对NH3吸附基本可逆,但也存在不可逆的化学吸附。
赵云龙[46]探究了2种煤炭在不同条件下制成的粉煤灰对NH3吸附能力,不同煤种粉煤灰对NH3吸附能力影响很大,这可能是由灰中铝含量以及硅铝比不同引起。此外,灰中残炭增多能提供更多酸性官能团,玻璃体、低温共熔体含量升高都能促进灰对NH3吸附。
综上,粉煤灰对单质氨的吸附有限,而由于火电机组烟气中存在SO3、H2O等物质,极大提高了灰对氨的吸附量。烟气成分与煤种是影响粉煤灰对氨吸附量的主要因素。这可能是由于在SO3和H2O存在时,NH3易与上述2种物质反应生成NH4HSO4,极易附着在飞灰颗粒表面,从而促进对氨的吸附。
3 含氨粉煤灰脱氨方法
粉煤灰中的氨主要以NH4HSO4形式存在,还有少量(NH4)2SO4、NH4Cl与NH3。粉煤灰氨含量主要取决于烟气中SO3、NH3浓度以及烟气温度等因素,脱硝粉煤灰氨质量分数可达200~2 500 mg/kg。为保证含氨粉煤灰正常销售,促进粉煤灰综合利用,研究人员积极研发含氨粉煤灰脱氨方法。美国电力研究协会(Electric Power Research Institute,EPRI)对粉煤灰氨去除工艺的评估标准[47]为:① 粉煤灰脱氨过程须在不影响其火山灰特性的条件下进行;② 对粉煤灰的机械加工须最小化,避免产生额外成本;③ 工艺须简单有效,不需大量测试或过程监督;④ 成本很低,能保证粉煤灰销售后的经济收益。
目前已有多种含氨粉煤灰脱氨工艺,主要脱氨方法有加热法、加碱法、氧化法、水洗法等。为保证脱氨效果,大多数工艺同时采用多种方法。
3.1 加热法
早在20世纪70年代,KIYOURA等[48]就提出(NH4)2SO4的热解分3步进行(式(13)~式(15))。(NH4)2SO4先发生脱氨反应生成NH4HSO4,NH4HSO4再脱水生成(NH4)2S2O7(焦硫酸铵),(NH4)2S2O7分解生成NH3、N2、SO2以及H2O。刘科伟等[49]在(NH4)2SO4恒温失重研究中通过红外光谱检测出了NH4HSO4和(NH4)2S2O7等中间产物,进一步证实了上述反应的正确性。这一系列反应并不是依次进行,而是各反应间互有交叉。普遍认为纯NH4HSO4的热解机理为式(14)和(15):

(13)

(14)

(15)
总反应:

(16)
李靖华等[50]认为NH4HSO4分解温度在345 ℃以上,其热分解反应式为式(17)。但该反应只在理论上可行,在无催化剂或其他物质存在的情况下,NH4HSO4很难直接分解生成SO3。

(17)
ZHU等[28]发现在无催化剂存在的情况下,390 ℃ 时NH4HSO4开始分解,490 ℃下NH4HSO4分解速率达到最大值。张立男[51]研究了NH4HSO4的挥发特性。通过热重分析得出,206 ℃时NH4HSO4开始挥发,297~390 ℃为NH4HSO4快速挥发阶段,378 ℃时NH4HSO4挥发最快,颗粒细度减小、接触面积变大都能加快NH4HSO4挥发速率。粉煤灰中掺杂的NH4HSO4越多,NH4HSO4的挥发速率越慢,但掺杂后NH4HSO4挥发速率均高于纯NH4HSO4样品。
BRENDEL等[6]研究了粉煤灰中铵盐的挥发规律。通过TG-MS分析发现,在惰性气氛中NH4HSO4起始挥发温度为214 ℃,(NH4)2SO4起始挥发温度为356 ℃,NH4Cl起始挥发温度为330 ℃。而在氧化气氛下这3种铵盐起始挥发温度比在惰性气氛下高出5~57 ℃。对含氨粉煤灰样品加热后发现,氨的释放一般存在2个峰值,分别位于低温区间(低于400 ℃)和高温区间。在惰性气氛中,高温区间内氨的释放常伴随相对分子质量44的物质释放,猜测氨可能会被粉煤灰中残炭吸附。而在氧化气氛中,高温区间内大部分氨转化为NOx释放出来,并伴随相对分子质量44的物质释放,这说明碳在氨转化过程中可能起催化作用。
粉煤灰中氨对高温十分敏感,因此将粉煤灰置于高温环境加热是一种有效去除氨的途径。HINTON等[52]研究了温度及加热时间对灰中氨脱除的影响,结果见表3。在204 ℃,粉煤灰中氨的脱除十分缓慢,在该温度下处理80 min,氨脱除率不到50%。随温度升高,氨脱除速率逐渐增大,在260 ℃ 处理20 min,氨脱除率约为50%,但仍不太适用于商业粉煤灰氨脱除工艺。温度≥371 ℃时,5 min内氨脱除率达到50%甚至更高。而在427 ℃ 或更高温度下,短时间内即可明显去除粉煤灰中氨。
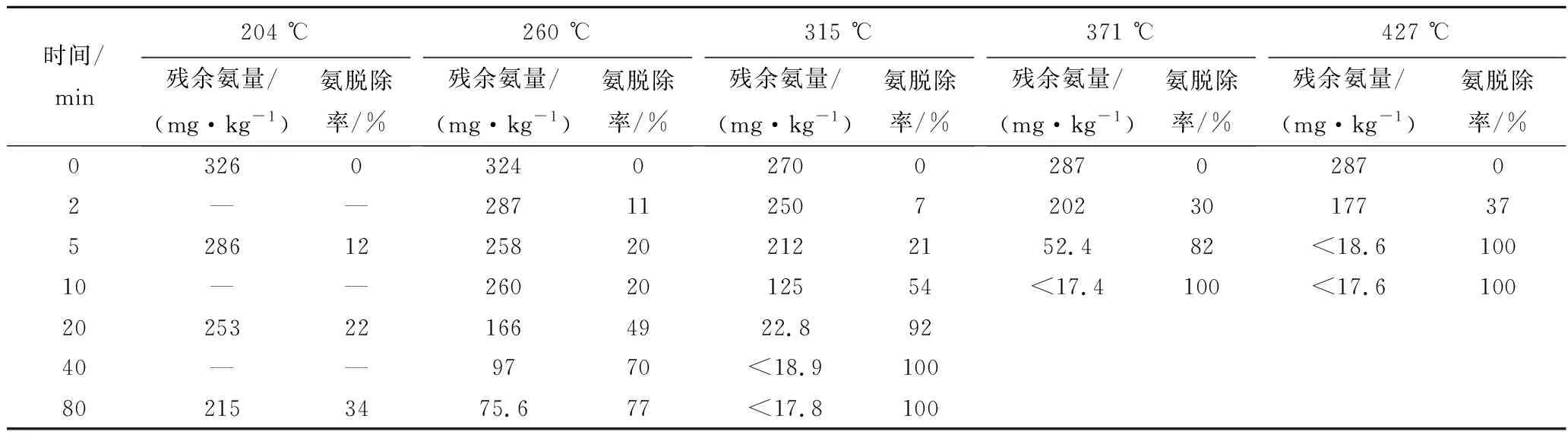
表3 温度及处理时间对粉煤灰氨含量的影响[52]Table 3 Effect of temperature and treatment time on the ammonia content of fly ash[52]
美国Progress Materials公司研发了碳燃尽技术(Carbon Burn-Out,CBO),将粉煤灰置于700 ℃流化床反应器中约45 min,粉煤灰中铵盐迅速分解释放,最终氨质量分数降至5 mg/kg以下。此外,粉煤灰中残炭也会因高温燃烧而减少从而改善其在建筑业中的使用,已在美国大规模应用[13]。对于残炭含量不高,难以再次燃烧的粉煤灰,SEFA集团开发了微波碳燃尽技术(Microwave Carbon Burn-out,MCB),与CBO技术不同,该技术将粉煤灰置于760 ℃左右的流化床反应器中并用微波补充碳燃烧释放的能量,从而脱除粉煤灰中氨以及残炭[53]。美国能源研究中心(Energy Research Center,ERC)提出将粉煤灰置入流化床反应器中,连续通入加热后空气,并在反应器上方安装声波发生器,用声波将可能聚成团的粉煤灰震散。以氨质量分数500~1 000 mg/kg的粉煤灰为试验材料,使用该方法加热到150 ℃时氨开始释放,343~398 ℃时氨释放趋于稳定,最终氨脱除率达90%以上,装置示意如图3所示。
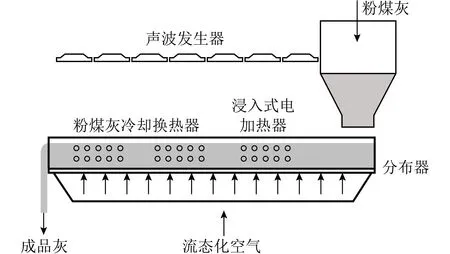
图3 ERC粉煤灰氨去除装置[54]Fig.3 Fly ash ammonia removal device of ERC[54]
3.2 水洗法
BAN[55]研究表明粉煤灰与水混合后,灰中氨易释放到水中,70%~90%的氨会在5~30 min释放出来。搅拌混合液能在一定程度上改变其pH,但不会促进氨释放;使用双蒸水或酸性溶液差别不大,说明粉煤灰pH对氨从灰中释放到水中的影响有限。
有学者使用超声波雾化器将水雾化后快速通入粉煤灰中以探究水雾对灰中氨的脱除效果,通入不等时间(1.5~8.0 min)水雾后在空气中干燥30 min,粉煤灰氨质量分数变化情况如图4所示(标记点为向粉煤灰中通入水雾结束后开始干燥前灰的含水量),通入雾气试验中灰含水量、含氨量随时间的变化如图5所示,3 min处多个点代表重复试验。

图4 向灰中通入不同量水对除氨效果的影响[11]Fig.4 Effect of different amounts of water into the ash on the effect of ammonia removal[11]
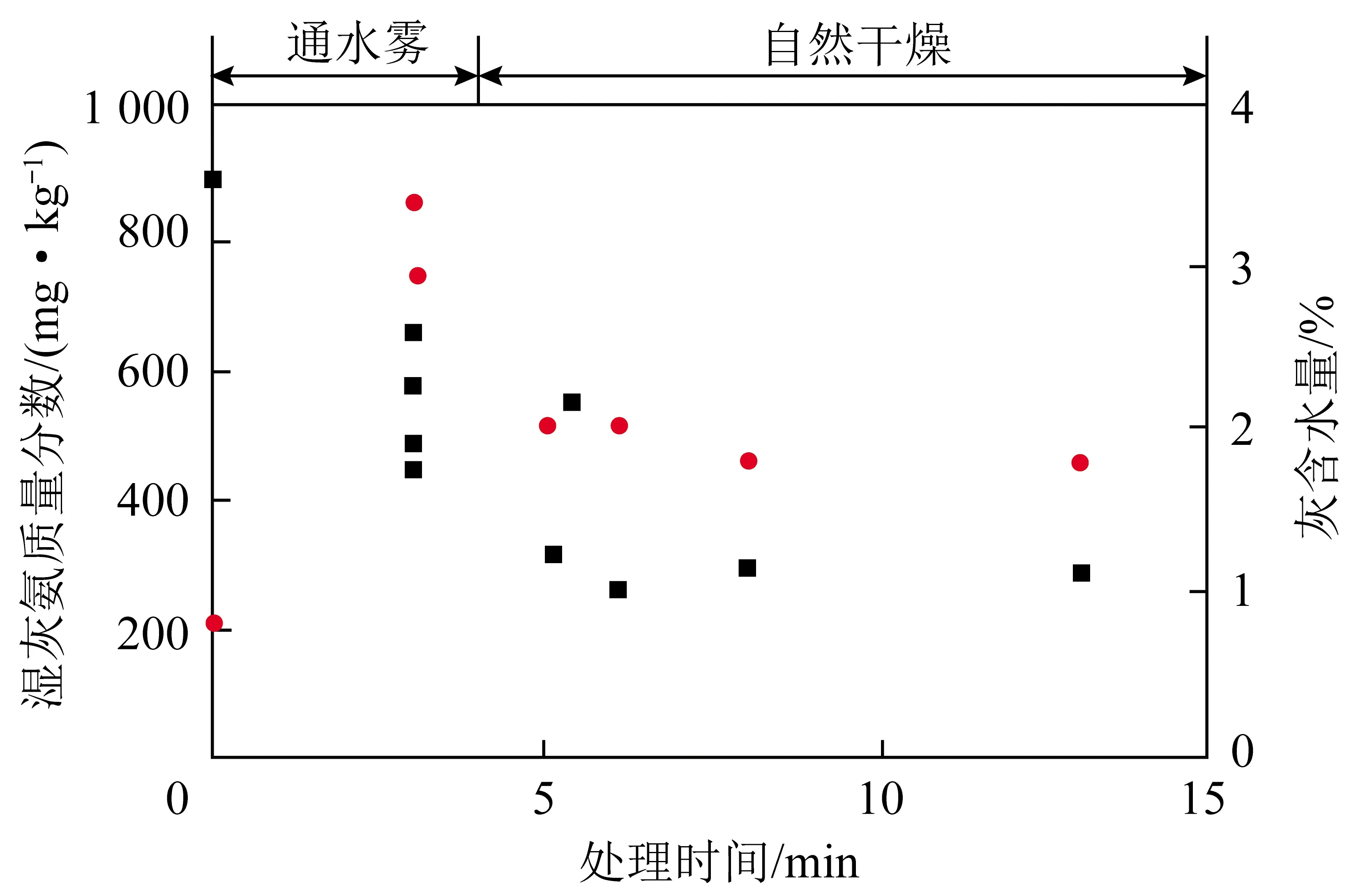
图5 灰中含水量、含氨量随时间变化[11]Fig.5 Changes of water content and ammonia content in ash with time[11]
由图4可知,向灰中通入水量高于2%(以质量分数计,下同)时,氨脱除速度很高。在2.5 min内向灰中加入3.3%水,即使不干燥也可脱除灰中近50%的氨,灰干燥后,氨质量分数还会进一步下降。由图5可知,灰中含水量高于3%时,氨脱除速率很高,但在随后的干燥阶段,灰中含水量降至2%以下后,氨脱除速率迅速下降[11]。
水洗法脱除灰中氨效果较好,但粉煤灰中还有其他重金属物质,水洗法除氨后,废水处理是一大难题。且湿润后的粉煤灰资源化利用需额外干燥步骤,增加了处理成本。
3.3 氧化法
选取合适的催化剂安装在SCR烟气脱硝装置后、空预器前,选择性将烟气中NH3催化氧化成N2能够有效除去烟气中的逃逸NH3,从而减少NH4HSO4生成,降低粉煤灰氨含量,主要反应为

(18)
学者提出包含Mg6Al2(CO3)(OH)16·4(H2O)的Mg-Cu-Fe系催化剂,该催化剂在试验气氛下(0.5% NH3、2.5% O2、97%惰性气体),450 ℃时,对NH3的选择性超过97%,NH3向N2的转化率为60%。Cu/TiO2型催化剂能在更低温度下选择性地将NH3氧化为N2,在250 ℃时转化率为95%,350 ℃ 时对NH3的选择性在93%以上。CHMIELARZ等[56]和SHRESTHA等[57]分别研究了Cu-SSZ-13型催化剂的效果,结果显示300 ℃时NH3转化率达到最大值94%。但该方法烟气与粉煤灰成分复杂,包含SO2、(NH4)2SO4、Hg、Pb等物质,还需要考虑催化剂中毒失活的情况。
将粉煤灰中氨氧化后释放也是一种有效的除氨方法。有学者研究了O3对粉煤灰中氨的脱除效果,向灰中添加Ca(OH)2以保证灰的pH大于10,通入潮湿空气使灰中含水量在1%~5%(以质量分数计),向所得半干灰中通入不同气体(O2、O2与O3混合气体、O3与空气混合气体),灰的初始氨质量分数为1 200 mg/kg,试验结果见表4。可知在常温下O3可将灰中氨部分脱除,最终产物含NO2,且不排除有N2存在[58]。

表4 O3除去粉煤灰中氨的效果[58]Table 4 Effect of O3 on removing ammonia in fly ash[58]
ASM(Ammonia Slip Mitigation)技术采用Ca(ClO)2作为氧化剂脱除灰中氨。将Ca(ClO)2融于水,按照一定Cl、N物质的量比将溶液以喷雾形式喷射到粉煤灰上使2者混合,主要反应为

(19)
文献[59]中提供了该方法的粉煤灰脱氨数据,见表5。
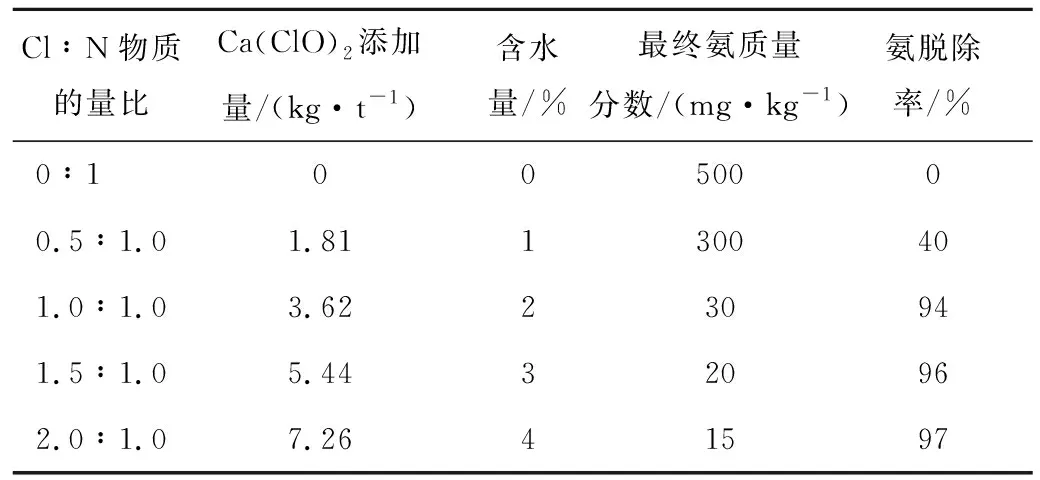
表5 ASM技术脱氨数据[59]Table 5 Deamination data of ASM technology[59]
由表5可知,该方法氨脱除率达到97%。但Cl与N物质的量比超过2,Ca(ClO)2会将NH3氧化为硝酸盐。实际生产中,Cl与N物质的量比在1.0~1.5。处理氨质量分数75~300 mg/kg的粉煤灰时,添加1.0~1.4 kg/t的Ca(ClO)2,氨脱除率达95%。
3.4 加碱法
BRENDEL等[6]研究表明在高pH铵盐水溶液中,氨主要以NH3形式存在,溶液pH>9时,NH3极易从溶液中逸出。向粉煤灰中加入水、碱性化合物后会使得粉煤灰pH升高,中和粉煤灰吸附NH3的酸性点位,使NH3释放出来[34],导致水泥混凝土加工使用含氨粉煤灰有刺鼻性气味。
STI(Separation Technologies,Inc)技术是利用该原理,向粉煤灰中加入少量碱(一般是CaO)和水来达到脱除氨的目的,主要反应如下:
(20)

(21)

(22)
(23)
(24)
其中,反应式(24)进行程度由系统pH确定。
不同量碱和H2O对不同pH粉煤灰中氨脱除的影响如图6所示。可知添加1% CaO与1% H2O(均以质量分数计,下同)对氨的脱除效果很不理想,但将H2O量增加到2%后氨脱除率大大增加。H2O添加量为4%时,加入0.66% Ca(OH)2的脱氨效果明显优于添加0.33% Ca(OH)2。0.5% CaO等同于0.66% Ca(OH)2,添加Ca(OH)2的效果更好。相较于pH=8.8的粉煤灰,pH=4.0需加入更多碱才能够达到较好的氨脱除效果。
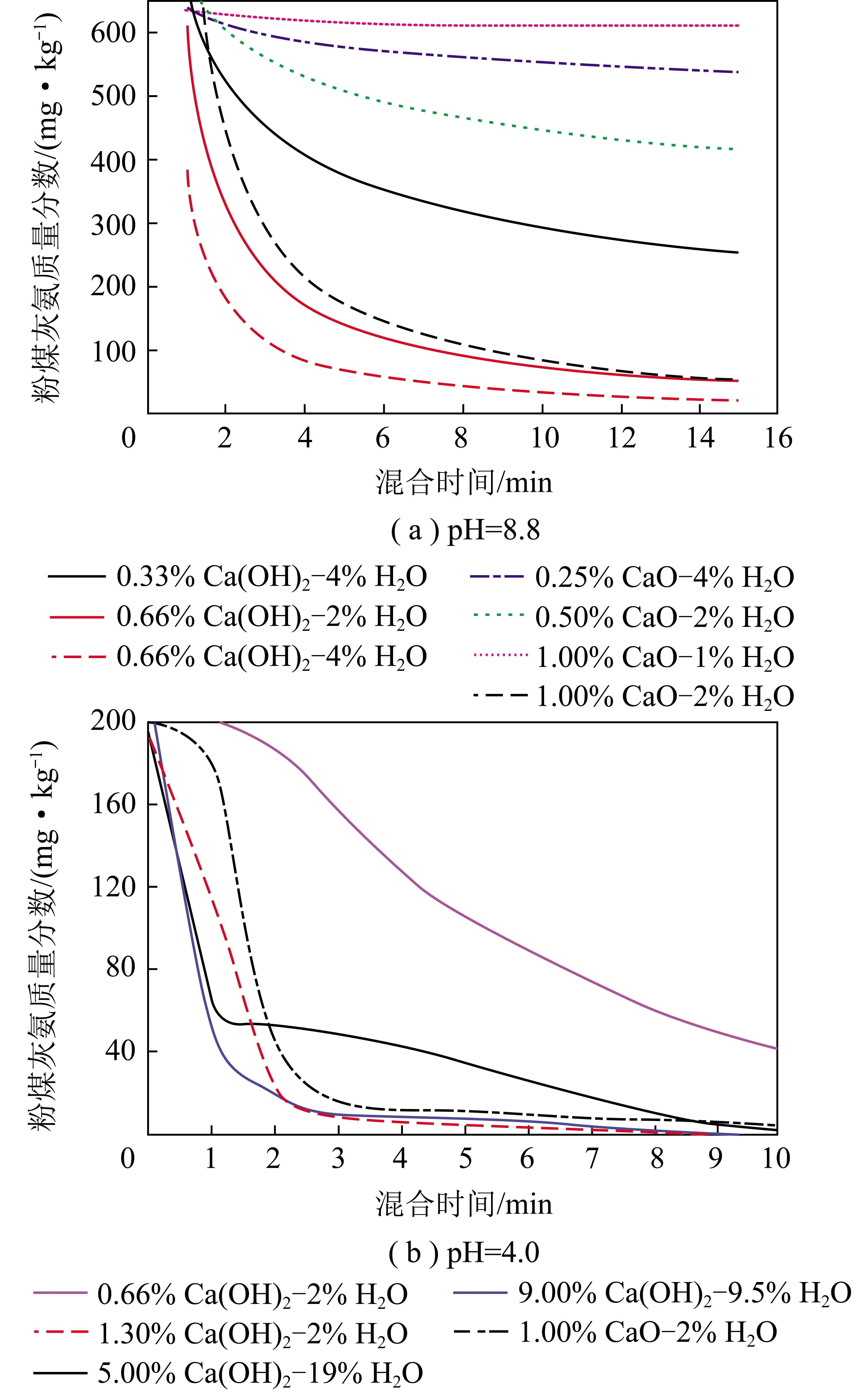
图6 pH为8.8和4.0的粉煤灰氨脱除情况[34]Fig.6 Removal of ammonia from fly ash at pH 8.8 and 4.0[34]
STI只需向粉煤灰中加入少量水(1%~4%,通常为2%)和少量碱(≤2%),加入水过多反而会降低反应速度,减缓氨的释放,且后续需额外步骤除去灰中多余水分。为达到理想的除氨效果,向粉煤灰中加入水和碱后,pH应≥10,否则需加入更多碱来保证pH。在实际生产中,该技术成功将粉煤灰氨质量分数从2 500 mg/kg降至75 mg/kg[60]。
上述4种方法中,水洗法产生的废水含重金属等物质处理是一大难题;而向灰中加入氧化剂后,灰中残余氧化剂易影响其资源化利用,如用掺和粉煤灰的混凝土搭建房屋,其中的氧化剂会腐蚀钢筋;加热法对粉煤灰本身特性的影响最小,但260 ℃ 及以下温度对灰中氨脱除效果不明显,对热源要求较高,应充分考虑成本;加碱法只需向粉煤灰中加入少量水和碱,粉煤灰中本身含有CaO、CaCO3等物质,加入钙基碱对粉煤灰本身特性影响小,且成本低、氨脱除率高,是一种优良的粉煤灰中氨脱除技术。
3.5 脱附氨处理
水洗法脱氨会产生液相二次污染物,需对水进一步处理;氧化法同样会产生二次污染。相比于加热法,加碱法对飞灰中氨的脱附可以较低运行成本达到较高脱除效率。但加碱法脱氨是将飞灰中氨释放至气相中,而氨直接排放至大气中会产生严重的二次污染,但目前对于气相中微量氨的脱除缺乏相关研究。从运行成本和投资成本角度出发,将处理后的气体通过引风机引至SCR入口实现对氨二次利用可防止二次污染。
4 结语及展望
1)SCR脱硝装置在脱除烟气中NOx的同时,也导致粉煤灰氨含量升高,极大影响了粉煤灰品质及资源化利用。由于火电机组烟气中NH3与SO3物质的量比小于1,2者反应趋向生成NH4HSO4,所以粉煤灰中氨主要以NH4HSO4形式存在。粉煤灰中氨质量分数受烟气中SO3浓度、NH3浓度、粉煤灰种类等因素影响。
2)目前国外已有多种含氨粉煤灰脱氨工艺,按照脱氨方法可分为加热法、加碱法、氧化法、水洗法等。选取粉煤灰氨脱除方法时需以下2点:① 粉煤灰本身售价低,需考虑脱氨工艺成本;② 尽量不改变粉煤灰本身特性,经脱氨处理后能更好地实现资源化利用。
3)加热法虽对粉煤灰特性影响最小,但260 ℃及以下温度脱氨效果差,对热源要求较高,需充分考虑加热成本。水洗法产生的废水中含有重金属等物质,需额外处理才能排放,后续还需干燥粉煤灰,经济性差。氧化法无法保证向粉煤灰中添加的氧化剂完全与氨反应,残余的氧化剂可能对粉煤灰利用产生不良影响。向粉煤灰中加入钙基碱和水并搅拌后氨脱除效果很好,且加入的水很少,后续干燥简单,处理过程中产生的NH3可重新喷入SCR烟气脱硝装置或制氨水。加碱法成本低、效率高,是脱除粉煤灰中氨的优良方法。

