乳腺乳头腺瘤7例临床病理分析及文献复习
郑丽媛,王秀红,钟定荣
(中日友好医院 病理科,北京 100029)
乳头腺瘤(nipple adenoma)是发生于乳腺乳头部的一种罕见良性肿瘤, 起源于乳头导管或输乳管。 其临床表现主要为乳头溢液、糜烂、湿疹样改变、 破溃结痂或乳头下结节形成, 临床易与Paget 病、导管内乳头状瘤、导管内癌或浸润性癌相混淆。许多临床医师对该疾病缺乏认识,容易过诊断,从而导致临床过度治疗。本文收集7 例乳头腺瘤,并复习相关文献,进一步探讨其临床病理学及免疫组化特点, 希望进一步提高对乳头腺瘤的认识。
1 资料与方法
1.1 临床资料
收集2012年1月~2021年6月在中日友好医院经病理明确诊断的乳头腺瘤7 例, 总结相关临床和病理资料。7 例乳头腺瘤患者均为女性,发病年龄34~51 岁,中位年龄37 岁。 其中4 例发生于右乳,3 例发生于左乳。4 例有乳头表面的改变,例如糜烂、湿疹、破溃等;1 例有乳头溢液(见表1)。

表1 乳头腺瘤7 例的临床病理资料
1.2 病理学检测方法
标本经4%中性福尔马林固定,常规脱水,石蜡包埋,切片厚4~5μm,行HE 染色,光镜观察。免疫组化采用EnVision 法,抗体包括P63、Calponin,CK5/6,ER,PR,Ki-67 等,均购自北京中杉金桥生物技术有限公司。 操作步骤严格按照试剂盒说明书进行。免疫组化结果判定以细胞核、细胞质和细胞膜出现明显棕黄色颗粒为阳性。
2 结果
2.1 巨检所见
肿瘤直径0.3~1.5cm,平均0.8cm。 肿物多呈结节状,切面灰白色,实性,质中,界限较清。
2.2 镜检所见
病变主要位于乳头部,肿块相对局限,没有包膜。其中病例1 导管上皮以旺炽型增生为主,呈实性团巢、不规则长条或拉网状生长,增生的上皮伴有轻度不典型增生,核分裂象少见,实性细胞巢中央偶有腺样的分化,腺腔内可见粉染的分泌物,个别团巢中央可见极少许坏死, 周边肌上皮部分增生伴有鳞化,增生的上皮伴有轻度不典型增生,核分裂象少见,有成熟现象(即近导管周边的细胞体积大,胞质丰富淡染,核大空淡,中央细胞较小,排列紧密),累及输乳管,并在输乳管开口处与乳头表面的鳞状上皮相连, 乳头鳞状上皮下间质疏松水肿,伴有较多慢性炎细胞浸润。病例2 部分导管上皮以旺炽型增生为主, 部分导管呈复杂乳头状增生,局灶紧邻乳头表面鳞状上皮基底层,乳头鳞状上皮下可见较多慢性炎细胞浸润。 病例3 主要呈乳头状瘤样生长, 乳头中央区部分呈腺病样改变,乳头表面被覆腺上皮呈柱状细胞样增生,肌上皮未见明显增生,未累及乳头表面鳞状上皮。病例4 和病例1 非常类似, 都表现为导管上皮以旺炽型增生为主, 不同的是病例4 中腺上皮部分呈微乳头状增生,而肌上皮增生不明显。病例5 和病例2 很类似,可见导管上皮旺炽型增生,部分呈乳头状增生,未累及乳头表面鳞状上皮。病例6 呈腺病样改变,部分腺上皮呈乳头状增生,中央区域呈硬化性腺病样改变,腺上皮呈立方柱状,病变累及输乳管,部分表面鳞状上皮糜烂,可见炎性肉芽组织形成。病例7 部分呈腺病改变,部分呈复杂的导管内乳头状瘤样改变(图1~4,见封二)。
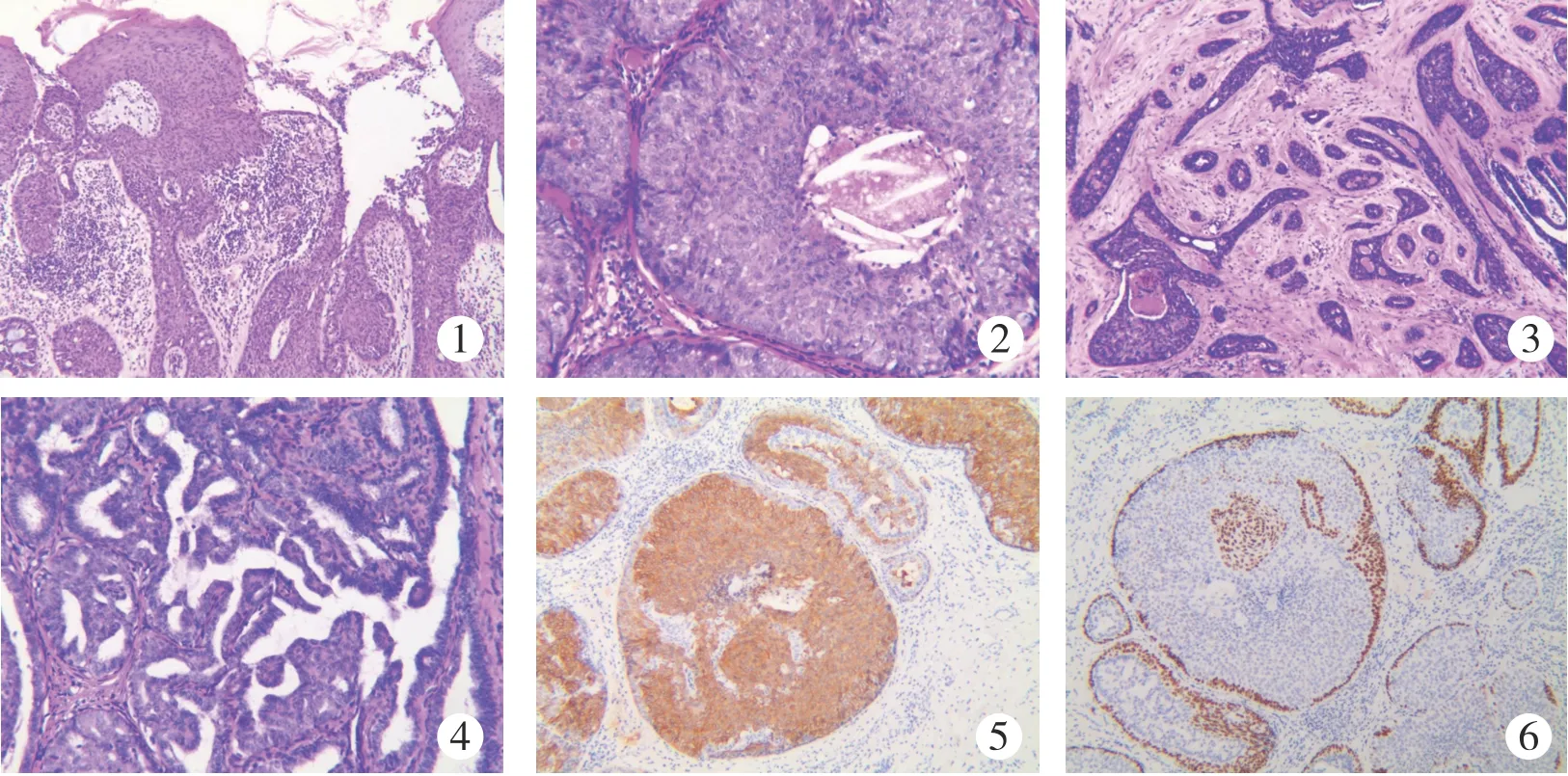
图1 病例1:导管上皮旺炽型增生,累及乳头表面皮肤,伴皮肤破溃,乳头鳞状上皮下间质疏松水肿,伴有较多慢性炎细胞浸润(HE×100)。图2 病例1:导管上皮旺炽型增生,呈实性团巢状,中央可见少量坏死(HE×200)。图3 病例6:硬化的纤维间质内见变形扭曲的腺管呈硬化性腺病样改变(HE×100)。图4 病例3:部分导管上皮呈导管内乳头状瘤样生长(HE×100)。图5 病例1:增生的导管上皮CK5/6阳性(×100),EnVision二步法。图6 病例1:导管周围肌上皮P63阳性(×100),EnVision二步法。
2.3 免疫组化染色结果
增生的导管上皮CK5/6 斑驳阳性,上皮巢周围肌上皮标记物P63、Calponin 阳性,雌激素受体(ER)、孕激素受体(PR)均呈强弱不等的阳性,Ki-67 增殖指数<15%,P53、Her-2 均阴性(图5~6,见封二)。
3 讨论
乳头腺瘤是发生于乳头部位的一种罕见的良性肿瘤,起源于乳头大导管及输乳管,又称乳头导管腺瘤、乳头状腺瘤、侵袭性腺病瘤、旺炽性乳头状瘤病及乳头部乳头状瘤病等[1]。 最早于1955年由Jones[2]报道,描述为“乳头导管的乳头状瘤病”,1965年Taylor 等提出用“乳头腺瘤”来形容这种不局限于导管腔内生长、 而是经常进入乳头基质的病变[3]。 WHO(2019 版)将其定义为一种良性的导管上皮增生性病变, 可以累及乳头表面的导管开口、周围的基质及邻近的表皮[4]。 强调了乳头腺瘤主要累及导管周围的基质, 也可以沿着乳头大导管开口累及到乳头表面鳞状上皮。 这也是导致乳头表面出现溢液、 糜烂以及结痂等临床表现的原因。
3.1 临床特点
乳头腺瘤发病率很低, 不足良性乳腺肿瘤的1%,大部分发生于青春期后的女性,罕见发生于男性乳头,偶尔可见发生于幼儿[5],平均患病年龄43 岁(20~87 岁)。 该肿瘤一般单发,生长缓慢,体积较小,直径一般<2cm。 因为肿瘤经常累及乳头部鳞状上皮, 所以临床约有1/3 以上患者出现乳头表面的病变,例如乳头糜烂、结痂,其余患者可出现乳头溢液或者乳头下可触及的结节。 这些表现易与乳头的Paget 病混淆。
在影像学方面, 乳腺疾病诊断中常用的检查方法有超声、X 线、MRI 等。 乳头腺瘤一般体积小且位于乳头内,超声难以发现,采用高频彩色超声可以显示肿瘤为边界较清的低回声结节[6];在乳腺X 摄影片上, 由于乳头腺瘤组织与正常乳头组织密度相似,肿物一般很难显示;动态增强磁共振成像(DCE-MRI)[7]由于较高的分辨率,近些年常被用于对乳腺疾病的诊断,效果相对好一些。我们的病例中,2 例超声可见低回声结节,3 例超声未见显著异常,但后续MRI 检查2 例提示有病变。
3.2 病理学特点
乳头腺瘤病变一般局限于乳头内或乳晕下,常无包膜, 镜下病理形态复杂多变, 生长方式多样,可以呈旺炽型增生样、乳头状瘤样、腺病样、硬化性腺病样或假浸润样, 边界可呈浸润样生长[8]。乳头腺瘤增生的腺管是位于乳头间质内的, 不像导管内乳头状瘤那样局限于导管内生长, 形态上类似普通型导管上皮增生, 具有上皮和肌上皮双层结构。腺上皮不同程度的增生,可出现旺炽型增生,扩张的导管可形成实性、筛状、乳头状等复杂结构。 但是这些腺上皮具有普通型导管上皮增生的特点,细胞拥挤、界限不清、相互重叠,可以呈流水样排列,出现成熟现象,细胞核大小不一、核仁不明显、核分裂象罕见,并可以伴随大汗腺化生或者鳞状细胞化生[10]。 随着腺上皮增生程度的增加,核分裂象也会增多, 部分病例还可以伴有小灶的坏死, 甚至出现不典型增生。 导管周围存在肌上皮,有时也可以伴有肌上皮的增生及化生。间质可有黏液样变性、水肿及胶原纤维增生等改变,增生的纤维组织挤压腺体可形成假浸润, 可伴有混合性炎细胞浸润,特别是在靠近乳头表面的一侧[9]。
常见的组织学类型一般分为3 种, 且通常混合存在[11]:①腺病型:与周围界限相对清楚,增生的腺管由腺上皮和肌上皮细胞组成, 可以呈囊性变,间质纤维化严重时可呈硬化性腺病改变,仅有腺病类型的乳头腺瘤病变通常不累及乳头表皮;②上皮增生型: 上皮常呈旺炽型增生, 可以呈实性、筛状或复杂的乳头状,这一类型可伴有核分裂象增多、坏死及不典型增生,增生的腺上皮常沿输乳管延伸至乳头表面,累及周围鳞状上皮,导致乳头出现糜烂、溃疡及结痂等改变,表面鳞状上皮下经常可见急慢性炎细胞浸润并形成肉芽肿。 ③假浸润型:主要是由于病变部位及周围的间质增生,纤维化硬化的间质挤压增生的腺体, 特别是一些小的腺管受压形成不规则条索状或单个细胞样,非常类似浸润的形态。
对于诊断困难的病例, 可以借助免疫组化进一步明确诊断,虽然乳头腺瘤的形态多样,但是腺管周围均存在完整的肌上皮, 因此肌上皮标志物p63、SMA、CD10、Calponin 等均可协助诊断。 腺上皮细胞不同程度的表达ER,高分子量CK(例如CK5/6)呈镶嵌状的表达,也可以证实增生腺上皮的异质性。
本组病例中,例1~5 均以上皮增生型为主,其中例1 和例4 旺炽型增生明显, 例2 和例3 以乳头状瘤样增生为主, 只有例1 在旺炽增生的团巢中央见极少许坏死;例6 和例7 以腺病型为主,局灶可见少量硬化性腺病及乳头状瘤样增生, 其他形态学改变在7 例中也偶有见到。 7 例中有6 例进行了免疫组化的染色,均证实肌上皮的存在。
3.3 鉴别诊断
在日常工作中遇到发生于乳头或乳晕部的病变,特别是当临床出现乳头糜烂或溢液,不仅要想到乳腺Paget 病等恶性疾病的诊断, 也要考虑到乳头腺瘤的诊断可能。 旺炽型增生的乳头腺瘤由于生长方式复杂多变,导管上皮增生显著,甚至出现坏死,易造成过度诊断。 间质纤维化严重时,增生的导管被挤压变形, 易形成假性浸润图像。 所以,乳头腺瘤虽然是一种良性肿瘤,但在临床工作中却很容易落入诊断的陷阱之中, 因此需要把握病变特点与以下疾病相鉴别。 ①Paget 病:两者临床均表现类似,Paget 细胞多位于鳞状上皮内,单个或成簇分布,细胞异型性明显,细胞核大、核仁明显,而且多数Paget 病均伴有导管内癌,特别是高级别导管内癌甚至是浸润癌, 所以常有HER2蛋白的过表达, 免疫组化还可以表达CK7、EMA等; 而乳头腺瘤是由于良性增生的腺上皮累及鳞状上皮,细胞没有明确的异型性。乳头腺瘤常伴有表皮内Toker 细胞的增生,也需要与Paget 细胞鉴别,Toker 细胞小,胞质透明,可含有黑色素,细胞核圆形,形态温和,免疫组化CK7 阳性,但是EMA 和HER2 阴性。②导管原位癌(DCIS):乳头腺瘤上皮旺炽型增生显著时可以伴有坏死, 此时要和DCIS 进行鉴别, 低级别DCIS 细胞形态单一,分布均匀,有极性;高级别DCIS 细胞异型显著,经常伴有坏死;纯粹的低级别或者高级别的DCIS和乳头腺瘤在形态学上鉴别比较容易, 但是有些中级别的DCIS 有时会出现细胞大小的混杂,排列的极性不明显,伴有小灶的坏死等。乳头腺瘤是良性上皮的异源性增生, 细胞大小混杂, 缺乏极性,免疫组化CK5/6 斑驳阳性,而DCIS 一般是阴性的。 ③浸润性癌:乳头腺瘤间质纤维化显著时,增生的导管被挤压变形,易造成浸润假象,在冰冻诊断时要尤其慎重。 这种假浸润的间质类似硬化性腺病的间质,主要为玻变的胶原纤维,其间的腺体形态温和, 免疫组化可以证实周围有肌上皮存在。真正发生于乳头部的浸润癌是非常少见的,浸润癌细胞异型性明显,腺体排列不规则,弥漫性浸润,周围缺乏肌上皮。 ④导管内乳头状肿瘤:乳头部的导管内乳头状肿瘤常局限于单一扩张的输乳管或近乳头的大导管内, 增生的上皮具有纤维血管轴心,形成复杂的分支乳头状结构,不累及导管周围间质。 乳头腺瘤增生的腺管是位于乳头间质内的, 不像导管内乳头状瘤那样局限于导管内生长,可以累及多个输乳管。 ⑤汗管瘤样腺瘤:汗管瘤样腺瘤也是发生于乳头及乳晕区的良性肿瘤,也可形成结节,形态类似皮肤的汗管瘤,小腺管呈拉长的逗点或蝌蚪状,由2 层或以上细胞组成,外层细胞P63 阳性,呈浸润性生长,分布稀疏,周围有丰富的纤维间质或平滑肌组织。
3.4 治疗及预后
乳头腺瘤虽然是良性肿瘤, 但是少数情况下可以合并或继发癌,包括DCIS、浸润性导管癌或小叶癌。乳头腺瘤一般只需要行局部手术切除,肿瘤体积小可行乳头部分切除术及乳头成形术,在保持乳头、 乳房外观的前提下尽量完整地切除肿瘤[12]。 手术完整切除后一般不会复发,单切除不彻底可复发,因此乳头腺瘤患者术后需要定期随访。

