岩藻黄质关键前体新黄质的代谢工程合成
张桂林,张亚亭,姜 宏,刘 振,毛相朝,
1. 中国海洋大学 食品科学与工程学院,山东 青岛 266003
2. 青岛海洋科学与技术国家实验室海洋药物与生物制品功能实验室,山东 青岛 266237
岩藻黄质是一种类胡萝卜素,在自然界中分布广泛,主要存在于藻类、贝类中,尤其在褐藻、硅藻中含量较高。岩藻黄质可以与叶绿素、蛋白质形成捕光复合体,是硅藻中发挥捕光作用的重要化合物[1]。目前有关岩藻黄质活性的报道较多,研究表明岩藻黄质具有抑菌、抗炎、抗肥胖、抗糖尿病、抗肿瘤、调节肠道菌群和抗器官纤维化等生理活性[2-6]。
目前岩藻黄质的最主要来源依旧是海藻[7],例如海带 (Laminaria japonica)、三角褐指藻 (Phaeodactylum tricornutum)[8]。岩藻黄质是一种优质的海洋来源功能因子,但由于其合成途径目前尚未得到完全解析,其生产及产量调控尚缺乏理论依据[9-12],合成生物学是发掘未知合成途径的重要手段,通常需要首先在微生物中异源构建目标化合物的上游已知中间物的合成途径,然后利用合成该中间物的工程菌株探索下游未知途径[13]。目前已知合成途径且结构上最接近岩藻黄质的中间物是新黄质[14]。作为岩藻黄质的可能前体物质,新黄质的结构与岩藻黄质很相似 (图1),两者均含有1条多烯链,2个六元环和1个累积双键,但存在着双键、羟基和羰基、乙酰氧基的区别。

图1 新黄质与岩藻黄质的结构式Fig. 1 Structural formula of neoxanthin and fucoxanthin
新黄质的合成途径见图2。甲羟戊酸 (MVA)途径主要存在于真核生物、古生菌和植物的细胞质中,甲基赤藓糖醇-4-磷酸 (MEP) 途径主要存在于细菌和植物叶绿体中,丙酮酸、甘油醛-3-磷酸和乙酰辅酶A分别通过MEP途径和MVA途径生成MEP和MVA,再经由其他酶催化生成异戊烯焦磷酸 (IPP) 和二甲基烯丙基焦磷酸 (DMAPP)[15-17]。大肠杆菌中含有MEP途径,并有法尼基焦磷酸 (FPP)可以作为岩藻黄质的底物[15,18]。

图2 新黄质合成途径Fig. 2 Synthetic pathway of neoxanthin
目前尚未见以微生物宿主生产新黄质的报道,因此构建合成新黄质的微生物细胞工厂成为发掘岩藻黄质的未知途径,并进一步成为海藻高效生产岩藻黄质提供理论依据的关键环节。本研究以大肠杆菌 (Escherichia coli ) 为宿主,按照代谢途径逐步构建番茄红素、β-胡萝卜素、玉米黄质、紫黄质的合成途径,最终实现了新黄质的代谢工程合成,为进一步发掘岩藻黄质合成的未知途径奠定基础。
1 材料与方法
1.1 试剂材料
1.1.1 菌株及质粒
本文所用菌株的基因型、功能及来源见表1,质粒的基因型、功能及来源见表2。

表1 本文所用菌株Table 1 Strains in this study

表2 本文所用质粒Table 2 Plasmids in this study
1.1.2 生化试剂及药品
番茄红素标准品、β-胡萝卜素标准品、玉米黄质标准品、紫黄质标准品和新黄质标准品购于Sigma-Aldrich公司。高保真DNA聚合酶试剂Phanta Max Super-Fidelity DNA Polymerase、DNA聚合酶试剂2×Taq Master Mix (Dye Plus)、重组克隆试剂ClonExpress Ultra One Step Cloning Kit购于诺唯赞生物公司。凝胶萃取试剂盒E.Z.N.A®Gel Extraction Kit购于Omega Bio-Tek公司。细菌基因组DNA提取试剂盒、快速质粒小提试剂盒购于天根生化科技公司。酵母粉、蛋白胨、琼脂粉、氨苄青霉素、氯霉素购于索莱宝科技公司。SSCS Solution感受态制备液购于上海捷瑞生物公司。其他试剂及药品未作特殊说明均为国药化试分析纯。PCR引物合成及测序由青岛擎科公司提供。
1.1.3 试剂及培养基配方
LB培养基:0.5%酵母粉,1%蛋白胨,1%的氯化钠(NaCl,固体培养基中加入2%琼脂粉),115 ℃ 灭菌 30 min。
ZYP-5052培养基:0.5%酵母粉,1%蛋白胨,8.1 g·L-1磷酸氢钠 (Na2HPO4),6.8 g·L-1磷酸二氢钾(KH2PO4),3.3 g·L-1磷酸铵 [(NH4)2SO4],0.2% 的0.5 mol·L-1硫酸镁 (MgSO4),2% 的 50×5052母液(50×5052母液:25%甘油,2.5%葡萄糖,10%的α-乳糖),115 ℃ 灭菌 30 min。
氨苄青霉素溶液:溶剂为水,在培养基中使用的终质量浓度为 100 μg·mL-1。
氯霉素溶液:溶剂为乙醇,在培养基中使用的终质量浓度为 25 μg·mL-1。
1.2 方法
1.2.1 DNA 目的片段 PCR 扩增
考虑到一个质粒上需要加入多个目的片段,为了保证每个片段能够正确表达,本研究在构建质粒的过程中会在2个目的片段的中间加入一段核糖体结合位点 (RBS)。在NCBI查找了菠萝泛菌中crtE、crtB、crtI、crtY、crtZ目的片段的CDS序列[19]。设计引物见表3,从菠萝泛菌基因组中通过PCR扩增得到了这5个基因。ZEP3基因来自三角褐指藻[20],NSY基因来源于番茄[21],由华大基因全基因合成。

表3 引物序列Table 3 Primer sequence
1.2.2 质粒的构建
同源重组法构建质粒:利用高保真DNA聚合酶PCR扩增目的基因片段与质粒片段,使得各片段连接处留有15~20 bp同源序列,使用重组克隆试剂进行重组连接,将重组产物转入E. coliTrelief™5α感受态中,涂布至对应抗生素的LB固体培养基上。12 h后对固体培养基上生长的转化子进行菌落PCR验证并选取样品进行测序。LB培养基培养测序正确的菌株,使用快速质粒小提试剂盒提取质粒。
1.2.3 工程菌的构建
单质粒工程菌的构建:将pTrc99a-crtEBI、pTrc99a-crtEBIY和pTrc99a-crtEBIYZ质粒分别利用热激法直接转入E. coliBL21感受态细胞中。
双质粒工程菌的构建:将E. coliBL21 pTrc99acrtEBIYZ工程菌制备成感受态细胞,再利用热激法将pACYCDuet-1-QZEP3、pACYCDuet-1-QZEP3-NSY质粒转入。感受态制备方法为:将需制成感受态的菌株在LB培养基中培养4~5 h (OD600达到0.6左右),取菌液在 4 000 r·min-1、4 ℃ 条件下离心5 min,弃上清后加入10%原菌液体积的10%无菌甘油洗涤菌体,再次离心弃上清,再重复一次甘油洗涤和离心弃上清,加入2%原菌液体积的SSCS Solution感受态制备液,即得到感受态细胞。
1.2.4 工程菌株的发酵培养
将工程菌在含有对应抗生素的LB固体培养基上培养,再挑取菌落在含有抗生素的LB培养基中培养12 h,得到种子液。按2%接菌量将种子液接入50 mL ZYP-5052培养基,20 ℃发酵48 h。
1.2.5 产物提取
大肠杆菌类胡萝卜素提取[22]:取2.0 mL的菌液,8 000 r·min-1离心10 min留菌体,加入1 mL丙酮,在40 ℃条件下,萃取至菌体颜色全部变成白色,12 000 r·min-1离心2 min留丙酮上清。萃取液采用氮吹法进行吹干,获得类胡萝卜素产物,用200 μL丙酮复溶,0.22 μm尼龙滤膜去除杂质,得到待检测样品。
1.2.6 高效液相色谱 (HPLC) 和质谱法 (MS) 对产物的鉴定及定量分析
C30检测方法[23]:使用YMC Carotenoid类胡萝卜素分析色谱柱 (250×4.6 mm) 对提取产物进行分析,进样量20 μL,吸光值476 nm,柱温35 ℃,流速1.0 mL·min-1。具体的液相检测条件见表4。用该方法绘制标准曲线 [y为峰面积,x为质量浓度(mg·L-1)]。番茄红素:y=52.505x-1.670 7,R2=0.999;β-胡萝卜素:y=1 312.9x-12.668,R2=0.999;玉米黄质:y=129.92x-39.204,R2=0.999;紫黄质:y=130.76x-33.414,R2=0.999。

表4 YMC Carotenoid流动相条件Table 4 YMC Carotenoid mobile phase conditions
上述C30色谱柱检测方法无法分离紫黄质和新黄质,所以我们采用了另一种C18检测方法来达到分离目的。C18检测方法[24]:使用C18 (250×4.6 mm, 5 μm)色谱柱检测,流动相是V(乙腈)∶V(乙酸乙酯)∶V(水)=74∶16∶10,采用等度洗脱,进样量20 μL,吸光值440 nm,柱温42 ℃,流速1.0 mL·min-1。用该方法绘制标准曲线 [y为峰面积,x为质量浓度 (μg·L-1)]。紫黄质:y=76.889x-140.93,R2=0.997;新黄质:y=357.07x+2.392,R2=0.991。
四极杆飞行时间质谱条件:离子源为电喷雾电离源 (ESI);电离化方式为ESI+;毛细管温度为350 ℃;雾化器压力为276 kPa;干燥气流速为10 L·min-1;扫描范围为 m/z 20~1 000。
1.2.7 细胞干质量的测量方法
取2 mL发酵后的菌液,12 000 r·min-1离心3 min,置于85 ℃烘箱烘干24 h,测量细胞干质量[25]。根据产物浓度与细胞干质量,计算出产量单位 (细胞干质量,下同) 为 mg·g-1或 μg·g-1。
2 结果与分析
2.1 番茄红素、 β-胡萝卜素和玉米黄质工程菌的构建
质粒pTrc99a-crtEBI、pTrc99a-crtEBIY和pTrc99a-crtEBIYZ成功转入E. coliBL21后,对应的工程菌E. coliBL21 pTrc99a-crtEBI、E. coliBL21 pTrc99a-crtEBIY和E. coliBL21 pTrc99a-crtEBIYZ发酵后菌体发生了颜色变化,对菌体内物质进行HPLC分析 (图3),结果表明成功产出了番茄红素、β-胡萝卜素和玉米黄质。根据标准曲线及细胞干质量计算出各产物浓度,其中E. coliBL21 pTrc99a-crtEBI的番茄红素产量为3.20 mg·g-1;E.coliBL21 pTrc99a-crtEBIY的β-胡萝卜素产量为1.35 mg·g-1;E. coliBL21 pTrc99a-crtEBIYZ 的玉米黄质产量为 0.70 mg·g-1。
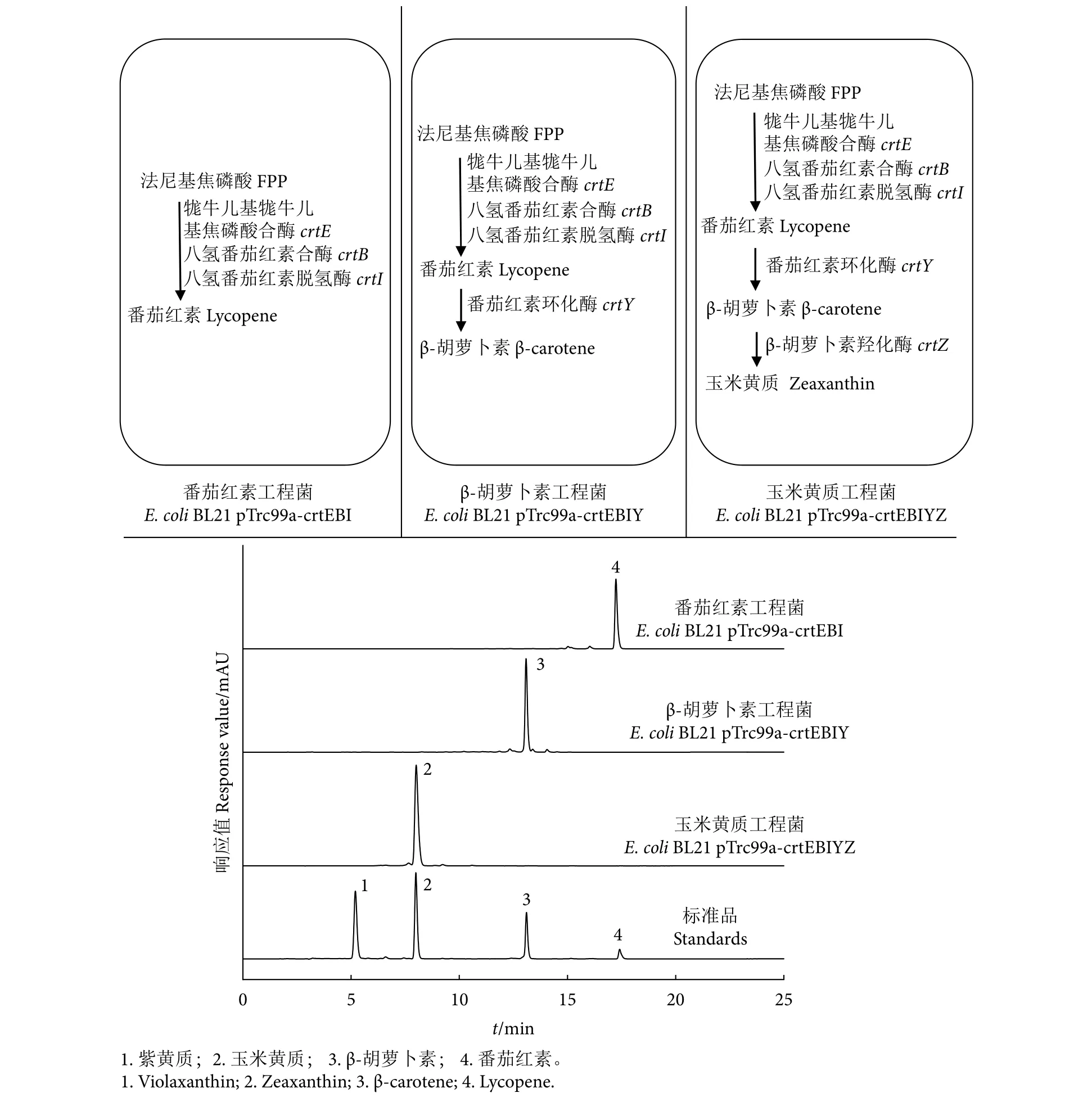
图3 番茄红素、β-胡萝卜素和玉米黄质工程菌的构建Fig. 3 Construction of lycopene, β-carotene and zeaxanthin engineered bacteria
在T7启动子的作用下,基因crtE、crtB、crtI、crtY和crtZ成功表达,产出目标产物。根据HPLC结果,E. coliBL21 pTrc99a-crtEBIY和E. coliBL21 pTrc99a-crtEBIYZ中并没有发现中间产物的积累,可能原因是产物浓度较低,CRTI、CRTY和CRTZ蛋白水平相较于低浓度产物来说催化能力较强,导致没有中间产物的积累,也可能与菌株本身以及生长状况有关,不同菌株在不同生长状况下产物积累量存在差异。
2.2 紫黄质和新黄质工程菌株的构建
以产玉米黄质的菌株E. coli BL21 pTrc99a-crtEBIYZ为宿主菌株,转入pACYCDuet-1-ZEP3质粒,构建产紫黄质菌株E. coli BL21 pTrc99a-crtEBIYZ pACYCDuet-1-ZEP3。但HPLC检测结果显示并无紫黄质产生。分析原因可能为ZEP3基因来源于三角褐指藻,是真核生物来源的基因,可能存在信号肽或叶绿体转运肽的编码区,但原核生物无法实现真核生物对蛋白的加工,导致蛋白折叠错误,使活性减弱甚至消失。
因此利用网站http://www.cbs.dtu.dk/services/ChloroP/预测叶绿体转运肽,预测前54个氨基酸为cTP区域。去除ZEP3基因的cTP后得到QZEP3,重新构建pACYCDuet-1-QZEP3质粒再转入产玉米黄质的工程菌中,HPLC分析菌体内产物有紫黄质存在 (图4),进一步证实了以上猜想。

图4 E. coli BL21 pTrc99a-crtEBIYZ pACYCDuet-1-QZEP3工程菌发酵产物HPLC结果Fig. 4 HPLC results of fermentation products of E. coli BL21 pTrc99a-crtEBIYZ pACYCDuet-1-QZEP3
根据标准曲线及细胞干质量计算出产物浓度,E. coli BL21 pTrc99a-crtEBIYZ pACYCDuet-1-QZEP3的紫黄质的产量为114.70 μg·g-1, 玉米黄质产量为289.45 μg·g-1。该工程菌中不仅有紫黄质生成,还有β-胡萝卜素和玉米黄质中间产物的积累,但并未检测到番茄红素的积累,可能原因是QZEP3的蛋白水平并不高,使得玉米黄质有较多积累,而番茄红素和β-胡萝卜素的积累可能与菌株生长状况相关,在不同生长状况下产物积累量存在差异,致使菌体内存在中间产物的积累。进一步分析HPLC结果,该工程菌不仅产出预期的β-胡萝卜素、玉米黄质和紫黄质,还有未知的产物 (保留时间6.2和10.6 min) 被检测到,猜测可能是QZEP3催化玉米黄质生成紫黄质时还生成了中间体产物。
以产紫黄质的菌株E. coli BL21 pTrc99a-crtEBIYZ pACYCDuet-1-QZEP3为宿主菌株,转入pACYCDuet-1-QZEP3-NSY质粒,构建产新黄质菌株E. coli BL21 NEO。用C30和C18色谱柱的方法对E. coli BL21 NEO菌体内产物进行检测 (图5)。紫黄质与新黄质是同分异构体,分子式为C40H56O4,分子量为600.417 9。E. coli BL21 NEO中的新黄质和紫黄质质谱结果 (图6) 显示,新黄质对应分子离子峰的m/z为600.414 6,紫黄质对应分子离子峰的m/z为600.413 8,这与紫黄质和新黄质分子量基本相当。HPLC与MS结果表明E. coli BL21 NEO成功产出新黄质。根据标准曲线及细胞干质量计算出各产物浓度,其中新黄质的产量为99.27 μg·g-1,紫黄质的产量为150.30 μg·g-1,玉米黄质的产量为119.77 μg·g-1。E. coli BL21 NEO 不仅产出预期的新黄质,还有β-胡萝卜素、玉米黄质和紫黄质的积累,也有未知的中间体产物生成。

图5 E. coli BL21 NEO工程菌HPLC检测结果Fig. 5 Detection of E. coli BL21 NEO by HPLC

图6 E. coli BL21 NEO工程菌新黄质 (a) 和紫黄质 (b) 的质谱检测结果Fig. 6 Detection results of neoxanthin (a) and violaxanthin (b) in E. coli BL21 NEO by MS
本文以产玉米黄质的工程菌为宿主,并将QZEP3和NSY导入,实现了新黄质的合成,但是QZEP3和NSY基因导入后的紫黄质和新黄质产量浓度不高,可能是上游途径的底物含量少,酶的催化效果不高,后续可以通过理性设计或定向进化对QZEP3和NSY进行改造,提高QZEP3和NSY在大肠杆菌中的活性来提高紫黄质和新黄质的产量,或者通过更换启动子,调节MEP上游通路途径,基因的过表达等方法[26-29],进一步提升紫黄质和新黄质的产量。
3 结论
本文以大肠杆菌为表达菌株,进行了新黄质合成途径的构建。以含有crtEBIYZ基因的产玉米黄质的E. coli BL21为宿主,引入了QZEP3和NSY基因,成功在大肠杆菌中建立了新黄质合成途径。有关新黄质本身的生理活性研究并不多[30-32],以微生物生产新黄质可提供新的生产途径,为研究新黄质的生理活性等提供便利,也为进一步探究岩藻黄质的合成途径奠定了基础。岩藻黄质的合成途径可以指导褐藻等海藻中岩藻黄质等物质的高值化利用,如通过理性设计改造获得高产岩藻黄质的藻类。
——一道江苏高考题的奥秘解读和拓展

