家蚕BiP基因的克隆及其对家蚕核型多角体病毒感染的影响
樊峰秀,李陈亚,Charles Amanze,郝碧芳
(江苏科技大学 生物技术学院,镇江 212100)
内质网(endoplasmic reticulum, ER)是蛋白质折叠和成熟的场所,分子伴侣在此过程中发挥重要作用[1].在细胞合成新生蛋白过程中,分子伴侣通过引导蛋白质在内质网正确的折叠及新生蛋白质在胞内的转运来发挥作用.分子伴侣在病毒感染、加热、重金属或缺氧等应激情况下,其表达会发生变化,以增强细胞在应激情况下的生存能力[2-8].结合免疫球蛋白(Binding immunoglobulin protein, BiP),又称葡萄糖调节蛋白78(Glucose-regulated protein 78, GRP78),是热休克蛋白70(Heat shock 70 kDa protein, Hsp70)家族成员之一,具有内质网分子伴侣的功能.
杆状病毒是一类主要感染节肢动物的病原微生物[9],杆状病毒在感染循环过程中产生两种不同表型的病毒粒子:芽生病毒粒子(budded virus, BV)和包涵体来源的病毒粒子(occlusion derived virus, ODV).ODV介导病毒入侵虫体的口服感染过程[10-11],BV介导病毒在虫体组织间的传播[12-14].家蚕核型多角体病毒(Bombyx mori nucleopolyhedrovirus, BmNPV)和苜蓿银纹夜蛾核型多角体病毒(Autographa californica multiple nucleopolyhedrovirus, AcMNPV)是研究较多的两种杆状病毒,基因组同源性达到90 %[15],但是两种病毒的宿主域差异显著,AcMNPV可以感染多种昆虫,而BmNPV主要感染家蚕,具体机理仍不是特别清楚.已有研究发现两种病毒的入侵方式有显著差别,AcMNPV主要采用Clathrin介导的内吞途径入侵宿主细胞,而且人工诱导的直接膜融合方式也可以使其有效感染细胞[16];与AcMNPV不同,BmNPV BV以巨胞饮的内吞方式入侵宿主细胞,人工诱导的直接膜融合方式则导致病毒丧失感染性[17].为了进一步探索BmNPV的感染机制,应用高通量测序技术对BmNPV BV以巨胞饮的内吞方式及人工诱导的直接膜融合方式感染的BmN细胞进行差异表达基因筛选,发现家蚕BiP(BmBiP)是表达显著差异基因之一[18].到目前为止,有关BmBiP在BmNPV感染家蚕过程中的作用还鲜有报道,因此,文中克隆了BmBiP基因,并分析了家蚕和其他6种昆虫BiP基因的相似性及亲缘关系,检测了病毒感染后其表达量的变化,最后利用RNA干涉技术探索了敲低BmBiP对病毒感染的影响,研究结果为深入阐释BmBiP参与病毒感染过程提供借鉴.
1 材料与方法
1.1 细胞与病毒
细胞系:BmN细胞(农业农村部蚕桑遗传改良重点实验室保存)用标准方法在含10%胎牛血清(Gibco)的TC-100培养基(Applichem)昆虫培养基中培养,培养温度为27 ℃.
病毒:BmBacJS13-egfp(农业农村部蚕桑遗传改良重点实验室保存)是一株与BmNPV 具有相同感染特性重组病毒[19],将增强型绿色荧光蛋白基因(egfp)通过转座的方式重组到BmNPV基因组上,病毒感染细胞后即可在感染的细胞中表达绿色荧光蛋白,方便观察和统计感染细胞的数量.
1.2 总RNA的提取及cDNA制备
将处于对数生长期的25 cm2的 BmN细胞用PBS洗两遍后,3 000 r·min-1离心10 min收集细胞沉淀,根据TRIzol© Reagent(Invitogen)说明书,加入500 μL TRIzol裂解细胞,提取BmN细胞总RNA.电泳检测总RNA的完整性,而后按照PrimescriptTMRT reagent Master Mix(TaKaRa公司)反转录试剂盒说明书反转录合成cDNA,并置于-20 ℃保存备用.
1.3 BmBiP基因的克隆与测序
根据Genebank上登陆的BmBiP序列(Genebank accession No.ACL36370.1)设计一对引物:BiP-F: 5’-ATAAGAATGCGGCCGCATGGTCAAGATGCGGTGG-3’和BiP-R: 5’-CCGCTCGAGTTACAACTCGTCCTTGAAGTCG-3’,两条引物包含NotI和XhoI酶切位点.以上述获得的cDNA为模板,利用rTaq(TaKaRa)PCR扩增BmBiP基因,电泳检测扩增的目的片段并进行回收,连接到pMD18-T载体(TaKaRa),由生物公司进行测序(尚亚生物技术有限公司),鉴定正确后用于后续序列比对分析.
1.4 生物信息学分析
利用Bioedit软件对家蚕和NCBI数据库中检索的小菜蛾(Plutellaxylostella)、黑脉金斑蝶(Danausplexippus)、草地贪夜蛾(Spodopterafrugiperda)、粉纹夜蛾(Trichoplusiani)、范式摇蚊(Polypedilumvanderplanki)和嗜卷书虱(Liposcelisbostrychophila)进行多序列比对,并用软件MEGA6.0的生物进化距离法构建系统进化树,校正参数Bootstrap设置为100次重复.
1.5 蛋白质印迹检测病毒感染后BiP表达变化
将处于对数生长期的5×105个BmN细胞接种到直径35 mm的细胞培养皿中,以10个感染复数的BmBacJS13-egfp感染BmN细胞,孵育1 h后,去除含病毒的培养基,用无血清TC-100培养基轻轻清洗细胞两次,添加含10 % 胎牛血清的新鲜培养基标准培养.分别在感染后24、48和72 h收集细胞,PBS洗两遍后,离心收取细胞样品,用50 μL 1×SDS-PAGE上样缓冲液裂解细胞,95℃煮沸5 min,样品12 000 r·min-1离心5 min备用.
取10 μL上清样品经12 % SDS-PAGE胶分离后,将蛋白转移至PVDF膜上.将PVDF膜置于5%脱脂牛奶中4 ℃封闭过夜;加入稀释1 000倍的GRP78多克隆抗体(Thermo Fisher Scientific)孵育2 h,用TBS-T缓冲液洗膜3次,每次10 min;二抗为碱性磷酸酶标记的羊抗兔的IgG(Promega),用0.5 % 脱脂牛奶稀释5 000倍,将膜浸入二抗中,孵育1 h,TBS-T缓冲液洗膜3次,每次10 min,用NBT与BCIP(上海生工生物工程股份有限公司)显色,检测目的蛋白表达变化.
1.6 BmN细胞中BmBiP RNA干扰及病毒感染分析
为了进一步分析BiP在病毒感染中的作用,利用RNA干扰技术敲低BmN细胞中的BiP表达水平,而后用病毒感染BmN细胞,并通过流式细胞仪分析感染效果.将1×105个处于对数生长期的细胞接种到24孔的细胞培养皿过夜培养,分别取2 ng的siRNA-BiP(序列为:5’-CCACUUACUCAUGUGUCGGUGUCUA-3’及5’-UAGACACCGACACAUGAGUAAGUG G-3’)和siRNA-NC(序列为5’-CCAUCAUGUACCUGUGUGGUUCCUA-3’及 5’-UAGGAA CCACACAGGUACAUGAUGG-3’)稀释液与1 μL的EnteransterTM-R4000(英格恩生物公司)的转染液混合,室温静置15 min,将转染复合物添加到细胞培养皿中,6 h后更换新的培养基,常规培养24 h后,以10个感染复数(multiplicity of infection, MOI)的BmBacJS13-egfp感染BmN细胞,孵育2 h后,去除含病毒的培养基,用无血清培养基轻轻清洗细胞两次,添加新鲜培养基,常规培养48 h,而后用PBS洗细胞两次,利用流式细胞仪(FACSCalibur, BD)测定表达绿色荧光蛋白的细胞比率.
2 结果与分析
2.1 BmBiP基因序列分析
利用TRIzol提取BmN细胞的总RNA,通过完整性分析,确定较好的RNA样品用于cDNA合成,通过两步法PCR扩增BmBiP基因,琼脂糖凝胶电泳分析发现一条大小约2 000 bp的特异性扩增条带(图1),而对照则无扩增产物,表明该条带是BmBiP的扩增产物.将扩增产物连接在pMD18-T载体后进行测序分析,结果表明BmBiP基因全长为1977 nt,与Genebank(ACL36270.1)中的家蚕BiP基因同源性很高,氨基酸序列分析发现仅有4个氨基酸的差异(16A/P, 275R/K, 320F/S, 479H/Y).
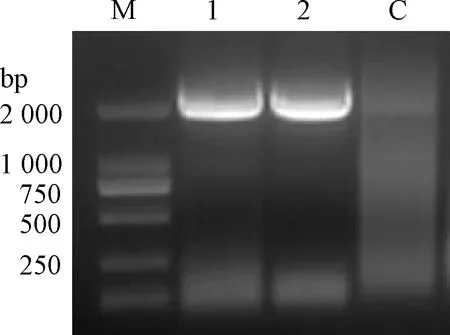
M: DL2000 Marker;1-2: PCR 扩增产物; C: 阴性对照
根据BmBiP的cDNA序列演绎的氨基酸序列,从NCBI数据库搜索选取了6种昆虫BiP的氨基酸序列,进行同源比对分析.结果显示,家蚕的BiP与小菜蛾、黑脉金斑蝶、草地贪夜蛾、粉纹夜蛾、范式摇蚊的BiP同源性比较高,其同源性分别为94.97 %、94.97 %、94.69 %、93.78 %、93.78 %,而与嗜卷书虱的BiP同源性较低,达到88.7%(图2),主要的差异存在于其N端和C端序列,而且在所有的物种BiP的C端都检测到典型内质网定位信号KDEL序列,同源比对分析结果表明BiP在物种进化过程中保守性较强.

图2 家蚕和其他6种昆虫的BiP氨基酸序列比对分析
利用生物进化距离法构建了家蚕与其他6种昆虫的BiP系统进化树(图3),校正参数Bootstrap设置为100次重复.结果表明家蚕与小菜蛾亲缘关系最近,而粉纹夜蛾和草地贪夜蛾关系较近,黑脉金斑蝶与草地贪夜蛾、粉纹夜蛾聚在同一个大的分支上,范式摇蚊与以上物种关系较远,而嗜卷书虱与其他昆虫物种亲缘关系最远(图3).

图3 基于MEGA6.0软件的家蚕和其他6种昆虫BiP氨基酸序列的进化树
2.2 BmNPV感染上调BmN细胞中BiP的表达
以10个MOI的BmBacJS13-egfp感染BmN细胞,分别在感染后24、48和72 h收获细胞,通过SDS-PAGE分离蛋白,并将蛋白转移到PVDF膜上,利用BiP特异抗体蛋白质检查BmBiP不同时间的表达变化,以未感染的细胞样品为对照.结果表明,在感染细胞和健康细胞中都检测到一条特异性条带,其中病毒感染后不同时间细胞中BiP的表达水平明显高于健康细胞(图4,箭头所示),而在感染后不同时间则无明显差异,这表明病毒感染显著上调BmN细胞内BiP的表达水平.

M:蛋白质标记;1-3:病毒感染后24,36,72 h细胞样品;C:健康细胞,箭头所示BiP蛋白
2.3 敲低BmBiP表达降低了病毒感染效率
已有研究表明小RNA参与BmNPV感染[20],为了进一步确定BiP对BmNPV感染的影响,分别用siRNA-BiP和siRNA-NC转染BmN细胞,转染后24 h,用携带绿色荧光蛋白报告基因的重组病毒BmBacJS13-egfp感染细胞,感染后48 h,收集细胞,用PBS洗涤BmN细胞两次,并用1 mL PBS悬浮细胞,用流式细胞仪统计表达绿色荧光蛋白细胞的比例.结果如图5,siRNA敲低细胞内的BmBiP表达后,其被BmNPV病毒感染的比率仅为对照(BiP-NC)的68.37%(P<0.001),这表明BiP参与BmNPV的入侵过程,BiP表达的下调极显著影响病毒的入侵效率.

图5 siRNA-BiP干扰BmN细胞后病毒感染率变化
3 结论
最新的研究表明BmNPV以巨胞饮的内吞方式入侵宿主细胞,人为诱导的病毒在早期内吞体内的膜融合方式可以使BmNPV进入宿主细胞质[17],但是病毒不能有效地进入细胞核导致感染失败,而正常的內吞途径可以使BmNPV病毒粒子进入细胞核起始感染,机理不清楚.研究发现AcMNPV病毒粒子从核孔进入细胞核内,而细胞核周围是被内质网紧密包被的,所以内质网与病毒入核可能有关[21].腺病毒是一种无囊膜的DNA病毒,2型腺病毒感染BHK-21和HeLa 细胞后,其核衣壳穿刺细胞膜后,分子伴侣蛋白HSP70 和 HSC70(heat shock cognate protein 70)会和核衣壳结合,通过免疫荧光共定位与细胞组分分离证实HSP70蛋白进入细胞核,并且与病毒粒子共定位于细胞核;进一步分离HSP70蛋白发现,它以一种复合体存在,并且和病毒颗粒交联在一起;免疫共沉淀发现HSP70及 HSC70和病毒衣壳蛋白Hexon有相互作用[22],这些研究表明宿主BiP参与腺病毒入侵宿主过程.
在探索BmNPV的感染机制过程中,研究团队分别用BmNPV的BV以巨胞饮的内吞方式和人工诱导的直接膜融合方式感染BmN细胞,高通量测序筛选BmN差异表达基因,发现BmBiP是表达显著差异基因之一.本研究克隆了BmBip基因,序列比对和进化分析表明BiP基因是一个保守性较强的基因,免疫印迹检测证明在BmNPV感染BmN细胞后BmBiP的表达量增加;而敲低BmBiP表达后,BmNPV的感染率显著降低,表明BmBiP参与BmNPV感染细胞的过程,BmBiP与腺病毒BiP有类似的功能.
而文献[23]研究发现人巨细胞病毒能精确的控制感染的人包皮成纤维细胞中BiP/GRP78的表达,以有利于病毒的复制;分别在病毒感后不同时间去除细胞内的BiP/GRP78,发现对病毒蛋白的合成影响很小,但是明显抑制了子代病毒的合成,暗示BiP/GRP78参与子代病毒的形成;电子显微镜观察发现,当去除细胞的BiP/GRP78后,导致感染病毒核衣壳无法释放或者导致大量核衣壳聚集在核膜外,表明BiP主要参与病毒粒子组装形成.
病毒入侵及释放是一个较为复杂的病毒与宿主相互作用的一个过程,已有研究表明BiP在不同病毒的感染过程中作用有所差异.本研究首次分析BiP在BmNPV的感染过程的作用,通过敲低BiP的表达,确定病毒对细胞感染率显著下降,这表明BiP参与BmNPV的入侵过程,但BiP是否参与病毒粒子在细胞内的运输,以及是否介导病毒粒子入核需要深入研究.

