加味升降散辅助治疗Ⅳ期糖尿病肾病患者的临床疗效观察*
程丽颖 ,张翥 ,马继伟 ,王琴 ,刘浩飞 ,罗伟贤
(1.河南中医药大学,郑州 450064;2.阜外华中心血管病医院肾内科,郑州 451464;3.河南中医药大学第一附属医院肾内科,郑州 450003;4.郑州市第一人民医院中医科,郑州 450000)
糖尿病肾病(DKD)是中国乃至世界范围内导致终末期肾病(ESRD)最常见的原因之一[1],进入ERSD后,患者将面临多种并发症甚至替代治疗。过度的炎症反应及肾纤维化是导致DKD进展为ESRD的关键环节,但目前以控糖、降压、调血脂为主的常规西医治疗并不能有效降低尿蛋白及抗肾脏纤维化。对于DKD患者来说,如何有效降低尿蛋白、抗肾脏纤维化,降低其进展为ERSD的风险,是临床上十分棘手的难题。
中医范畴内DKD归属于“水肿”“尿浊”“关格”等,气虚血瘀为其基本病机[2]。DKD病程较长,在其Ⅳ期阶段除“气虚血瘀”外,湿热互结也是其重要病理因素[3]。因此本团队总结“益气活血、除热祛湿”的治法,化裁“加味升降散”以辅助治疗Ⅳ期DKD患者。先期的小样本临床非随机对照试验提示加味升降散辅助治疗Ⅳ期DKD患者可进一步降低尿蛋白,改善肾功能。鉴于此,本团队严格按照随机对照原则,对加味升降散辅助治疗Ⅳ期DKD患者的临床疗效进行多中心的观察与评价。
1 对象与方法
1.1 研究对象 选取2018年9月—2020年6月期间就诊于本院泌尿内科、阜外华中心血管病医院肾内科及郑州市第一人民医院中医科门诊或住院的中医辨证为气虚血瘀,湿热互接的Ⅳ期DKD患者80例。依照随机数字表法把将其分成观察组40例,对照组40例。本研究经过伦理委员会审批(伦理编号:2019HL-050-01)。
1.2 中西医诊断标准及分期
1.2.1 西医诊断标准 诊断要点符合《糖尿病肾病防治专家共识》[4](2014年版);分期标准符合1998年Mogensen[5]分期的Ⅳ期即Ⅳ期糖尿病,尿白蛋白排泄率持续>200 μg/min,或尿蛋白>0.5 g/24 h,血肌酐(Scr)<178 μmol/L。
1.2.2 中医辨证标准 基于《2型糖尿病病症结合诊疗指南》[6]中关于气虚血瘀、湿热互结证中的一项及以上的主症加次症。主症:形体肥胖,腹部胀大,口干口渴,喜冷饮,饮水量多,脘腹胀满,易饥多食,心烦口苦,大便干结,小便色黄,舌质淡红,苔黄腻,脉弦滑。或见五心烦热,盗汗,腰膝酸软,倦怠乏力,舌质红,苔少,脉弦细数。次症:肢体麻木或疼痛,下肢紫暗,胸闷刺痛,中风偏瘫,或语言謇涩,眼底出血,唇舌紫暗,舌有瘀斑或舌下青筋显露,苔薄白,脉弦涩。
1.3 纳入标准 1)符合西医诊断标准和中医的证型标准,DKD的Mogensen临床分期为Ⅳ期,经常规综合治化疗后血压≤140/90mmHg(1mmHg≈0.133kPa),年老者(>65岁)收缩压可放宽至≤150 mm Hg。2)临床资料齐全,积极参加本课题研究。3)自愿配合至疗程结束并签订知情同意书。
1.4 排除标准 1)妊娠期或哺乳期妇女。2)3月内服用过肾毒性药物。3)存在其它可使尿蛋白增多的因素:发热、运动、感染等。4)合并严重的血液、脑、心、肺、肝等系统疾病或合并肿瘤、精神疾病、免疫功能低下。5)合并糖尿病酮症酸中毒、乳酸酸中毒等糖尿病急性并发症。6)合并其他可继发肾损伤的疾病。
1.5 剔除标准 1)用药疗程中出现过敏或严重不良反应。2)病情进行速度较快,需要替代治疗。3)过程中临床资料丢失。
1.6 干预措施 对照组:以DKD健康教育、控糖、降压、调脂、减少尿蛋白(贝那普利)为主的常规综合治疗[7]。观察组:在对照组基础上辨证联用加味升降散(主方为生黄芪30 g,蝉蜕9 g,僵蚕9 g,姜黄12 g,大黄 6 g,水蛭 6 g,虻虫 6 g,桃仁 9 g,积雪草15 g,翻白草30 g)。药材来自江阴天江药业有限公司提供的混合盒装颗粒剂,每日2次,每次1格,60℃温开水150 mL冲服,以12周为1个疗程,在治疗开始前及疗程结束时对疗效进行评价。
1.7 观察指标
1.7.1 疗效指标 采用酶联免疫吸附法测定:24 h尿蛋白定量(24 h UP)、白细胞介素-6(IL-6)、白细胞介素-1β(IL-1β)、肿瘤坏死因子-α(TNF-α);采用全自动生化分析仪测定:Scr、血尿素氮(BUN);临床总有效率[8](显效:24 h UP的减少量>50%;有效:30%<24 h UP的减少量<50%;无效:24 h UP的减少量<30%)。
1.7.2 安全性指标 丙氨酸氨基转氨酶(ALT)和门冬酸氨基转氨酶(AST),指标采用全自动生化分析仪测定。
1.7.3 不良反应 记录两组患者出现的头晕、呕吐、腹痛、腹泻等不良反应。
1.8 统计学方法 使用SPSS 24.0处理资料数据,计量资料用(±s)来表示,采用Shapiro-Wilk检验评估数据正态性,符合正态分布,组间对比选用独立样本t检验,组内对比选用配对样本t检验,反之选用 Mann-Whitney U 检验,用 M(Q1,Q2)表示;计数资料采用%表示,采用χ2检验,P<0.05差异具有统计学意义,P<0.001差异具有显著统计学意义。
2 结果
2.1 两组患者基线资料对比 经比较,两组患者在性别、年龄、糖尿病(DM)病程、DKD病程和治疗开始前的空腹血糖、糖化血红蛋白、体重指数、总胆固醇、三酰甘油、舒张压、收缩压等基线资料的差异无统计学意义(P>0.05),见表 1。
表1 两组患者的基线资料对比(±s)
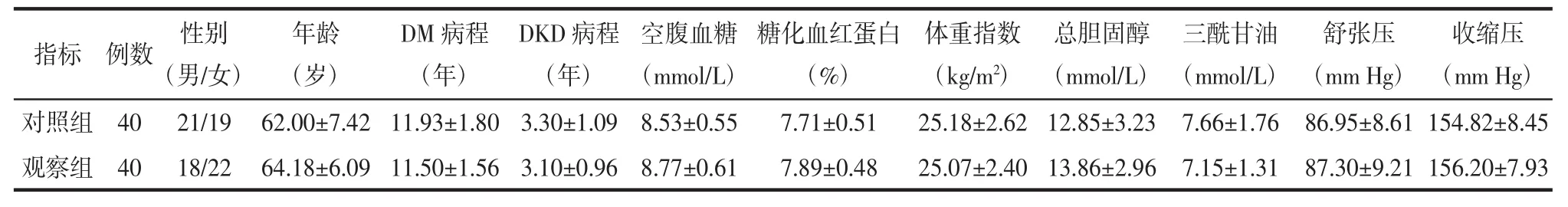
表1 两组患者的基线资料对比(±s)
DKD病程(年)指标 例数 性别(男/女)年龄(岁)DM病程(年)空腹血糖(mmol/L)糖化血红蛋白(%)体重指数(kg/m2)总胆固醇(mmol/L)三酰甘油(mmol/L)舒张压(mm Hg)收缩压(mm Hg)对照组 40观察组 40 18/22 64.18±6.09 11.50±1.56 3.10±0.96 8.77±0.61 7.89±0.48 25.07±2.40 13.86±2.96 7.15±1.31 87.30±9.21 156.20±7.93 21/19 62.00±7.42 11.93±1.80 3.30±1.09 8.53±0.55 7.71±0.51 25.18±2.62 12.85±3.23 7.66±1.76 86.95±8.61 154.82±8.45
2.2 临床总有效率对比 疗程结束后,对两组的临床总有效率进行比较,结果显示:观察组的总有效率高于对照组,差异存在统计学意义(P<0.05),见表2。提示在常规治疗的基础上联用加味升降散可以提高Ⅳ期DKD患者的总有效率。
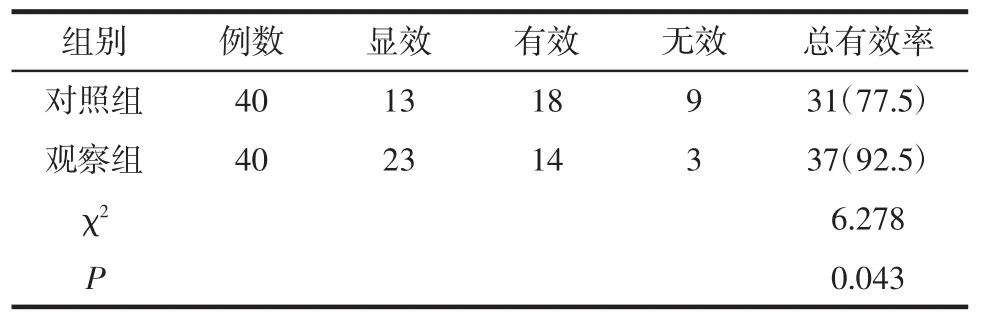
表2 两组临床总有效率对比 例(%)
2.3 肾功能相关指标对比 对两组患者治疗前后的肾功能相关指标进行比较,结果显示:治疗前两组患者的24 h UP及Scr、BUN差异无统计学意义(P>0.05),具有可比性;疗程结束后,观察组的24 h UP、Scr、BUN低于对照组,存在显著统计学差异(P<0.001),见表3。提示在常规治疗的基础上联用加味升降散可进一步减少Ⅳ期DKD患者的24hUP,降低患者的Scr与BUN。
表3 两组治疗前后肾功能相关指标比较(±s)

表3 两组治疗前后肾功能相关指标比较(±s)
注:与本组治疗前比较,*P<0.05。
0.139 -7.968 -0.255 -4.636 0.486 -5.502 0.890 <0.001 0.799 <0.001 0.629 <0.001组别 例数24 h UP(g) Scr(μmol/L) BUN(mmol/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 40观察组 40 1.22±0.45 0.31±0.16* 99.55±4.39 92.18±4.45* 8.02±0.64 6.38±0.36*1.21±0.36 0.63±0.20* 99.78±3.44 96.25±3.33* 7.96±0.47 6.81±0.35*t P
2.4 相关炎症因子对比 对两组患者治疗前后体内相关炎症因子水平进行比较,结果显示:治疗前,两组患者在IL-1β、IL-6及TNF-α表达水平上的差异无统计学意义,具有可比性(P>0.05);疗程结束后,观察组的IL-1β、IL-6、及TNF-α低于对照组,差异具有显著统计学意义(P<0.001),见表4。提示在常规治疗的基础上联用加味升降散可进一步降低Ⅳ期DKD患者体内IL-1β、IL-6及TNF-α的表达。
表4 两组治疗前后 IL-1β、IL-6、TNF-α 比较(±s)
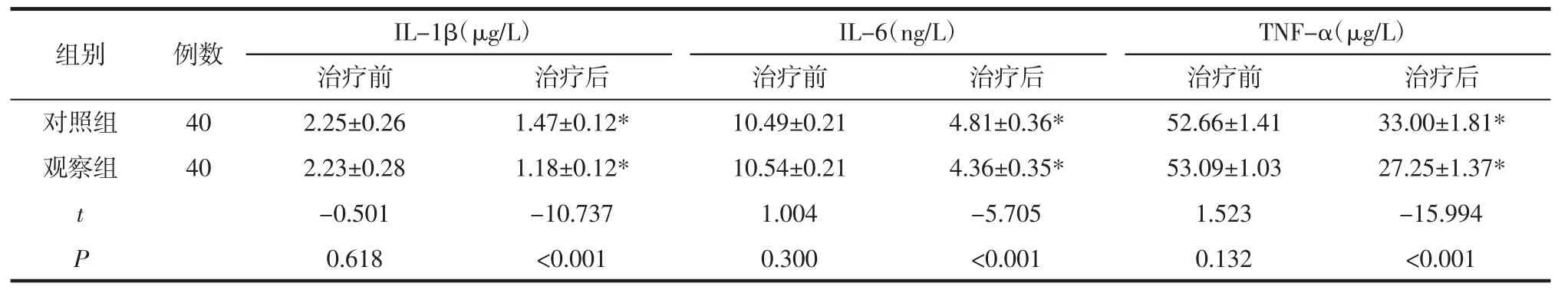
表4 两组治疗前后 IL-1β、IL-6、TNF-α 比较(±s)
注:与本组治疗前比较,*P<0.05。
IL-1β(μg/L) IL-6(ng/L) TNF-α(μg/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后组别 例数对照组 40观察组 40 2.23±0.28 1.18±0.12* 10.54±0.21 4.36±0.35* 53.09±1.03 27.25±1.37*2.25±0.26 1.47±0.12* 10.49±0.21 4.81±0.36* 52.66±1.41 33.00±1.81*t P-0.501 -10.737 1.004 -5.705 1.523 -15.994 0.618 <0.001 0.300 <0.001 0.132 <0.001
2.5 安全性指标及不良反应 如表5所示,治疗前后,两组患者的ALT、AST无明显变化,无统计学差异(P>0.05)。治疗期间,观察组患者出现恶心2例,对照组出现头晕1例、恶心1例,但症状均较轻,经对症治疗后好转,不影响研究进展。
表5 两组治疗前后ALT、AST比较(±s)U/L
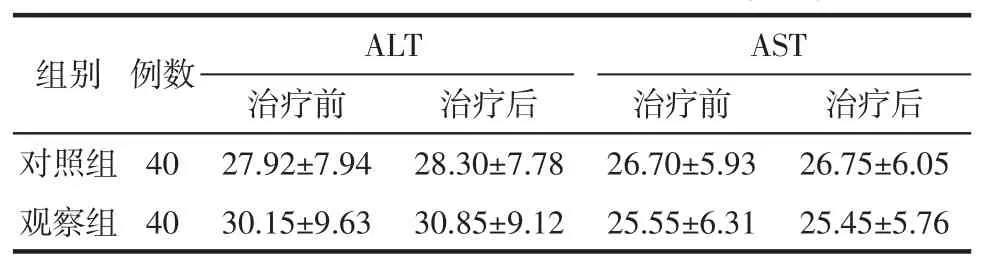
表5 两组治疗前后ALT、AST比较(±s)U/L
组别 例数ALT AST治疗前 治疗后 治疗前 治疗后对照组 40观察组 40 30.15±9.63 30.85±9.12 25.55±6.31 25.45±5.76 27.92±7.94 28.30±7.78 26.70±5.93 26.75±6.05
3 讨论
DKD是DM最常见且危害最大的微血管并发症,其可使预期寿命减少16.9年[4],给患者家庭以及整个社会带来沉重的医疗负担,防控情况不容乐观。
DKD的病理改变主要是肾小球高滤过、氧化应激损伤和炎症导致的足细胞损伤、肾小球基底膜、细胞外基质(ECM)增生、肾小球硬化、小管间质炎症和纤维化等[9]。有效抑制DKD患者机体的氧化应激损伤和炎症反应是抑制肾纤维化、改善肾功能关键。
研究表明DKD患者肾损伤的程度与尿蛋白的量呈正相关[10],因此,减少尿蛋白对于延缓DKD患者的肾损伤进展至关重要。目前,DKD患者尿蛋白增多的原因主要是肾小球滤过压的增高和足细胞损伤、肾小球基底膜、ECM增生导致肾小球滤过膜孔径硬化、变大等。西医常规防治主要是使用ARB或ACEI等药物作用于RAAS系统,抑制血管紧张素Ⅱ受体,降低肾小球的滤过压。虽然上述药物也具有一定的抗炎、抗氧化应激的作用,但是降低尿蛋白、延缓肾功能恶化的效果仍差强人意。多项研究表明中医药在降低DKD患者尿蛋白、延缓肾功能恶化方面具有一定优势[11-12]。因此,本课题组致力于研究在西医常规治疗的基础上联合中医药辅助治疗DKD。
虽然中医无糖尿病肾病一词,但早在《诸病源候论》中就已认识到DKD的发病过程,原文中提到:“消渴其久病变,或发痈疽,或成水疾”,故DKD归属“水肿”“尿浊”等范畴。DKD病程迁延,气虚为其根本病因。《医林改错》云:“元气既虚,必不能达于血管,血管无气,必停留而瘀。”气虚则无力行血,血行缓慢可阻滞成瘀,且气虚时津液无力运化、布散,故而凝结成痰湿,病程日久,痰湿凝结,郁而生热,故气虚血瘀、湿热互结为本病的基本病机。
基于DKD的基本病机,本团队总结“益气活血、除热祛湿”的治法,化裁“加味升降散”。方中黄芪乃补气要药,“气为血之帅”“气顺则一身之津液亦随气而顺矣”,故以黄芪补气既可行血又可化痰湿。僵蚕与蝉蜕着重作用于气分,在黄芪补气的基础上调理气机,助力津液的运化、布散,避免痰湿凝结、久而郁热。大黄和姜黄作用于血分,以行气活血、清解热毒。水蛭、虻虫、桃仁进一步活络祛瘀。翻白草、积雪草,入肝肾经以清郁热利痰湿。全方共达益气活血、除热祛湿之效。
现代中药药理中,黄芪主要成分为黄芪多糖、黄芪皂苷等,能有效抑制氧化应激损伤,提高机体抗炎的能力[13]。蝉蜕、僵蚕可减轻肾小球基底膜通透性、改善肾小球高滤过[14]。姜黄、大黄可抑制氧化应激损伤,阻碍ECM增生,抑制肾小球滤过屏障的进行性损伤和抑制纤维化[14-15]。水蛭、桃仁可既可抑制肾小球的炎性损伤,又可改善肾小球灌注压[15-16]。翻白草中的三萜类成分可减轻的ECM增殖,抑制肾小管细胞的肥大和纤维化[17]。积雪草可通过下调TGF-β1、Smad7 的表达,抑制 ECM 过度积聚[18-19]。总的来说,肾小球走向硬化的直接因素是ECM的过度积聚,这也是肾脏走向纤维化的首要病变因素,更是加速DKD向ESRD进展的关键环节。以上论述均表明加味升降散可抗炎症反应、抑制肾脏进一步纤维化、进而延缓DKD向ESRD进展。
本研究中,疗程结束后,观察组的临床总有效率显著高于对照组,24 h UP、Scr、BUN水平显著低于对照组,且两组患者的不良反应无明显差异。提示在常规治疗基础上联用加味升降散可进一步提高Ⅳ期DKD患者的临床总有效率,降低尿蛋白、改善肾功能,且不增加患者的不良反应。
TNF-α和白介素是DKD的疾病进展中重要的炎性因子[20]。TNF-α既可直接引起炎症反应,又可通过活化其它炎症因子导致肾小球硬化和肾小管的纤维化的促炎性介质[21]。IL-1β和IL-6在介导炎症的同时也可上调前列腺素E2的表达引起肾小球系膜增殖和ECM沉积,导致肾功能恶化[22]。体内TNF-α、IL-1β、IL-6等炎症因子的水平,一定程度上可反应DKD患者的疾病进展。本研究中,观察组TNF-α和IL-1β、IL-6水平显著低于对照组,提示在常规治疗的基础上联用加味升降散可进一步达到抗炎、抗肾脏纤维化的作用,进而延缓DKD患者进展为ERSD的速度。
综上,加味升降散辅助治疗Ⅳ期DKD患者可进一步提高患者的临床总有效率,降低尿蛋白,改善肾功能,减轻炎症状态且具有较好的安全性,值得临床推广应用。同时本研究尚存在以下不足:首先,加味升降散为中药颗粒剂,对于研究者和观察组患者来说未采用盲法;其次,虽然加味升降散组具有一定的抗炎、抗氧化的作用,但其具体作用靶点和机制仍需在进一步的动物及细胞实验中进行研究。

