卵巢无性细胞瘤的超声表现
贺宇凡 涂艳萍 欧阳春艳 曾思惠
卵巢无性细胞瘤是一种少见的生殖细胞恶性肿瘤,好发于年轻女性,经综合治疗预后较好,因此早期正确诊断尤为重要[1-2]。由于该肿瘤发病率低,临床症状、体征及超声表现缺乏特异性,容易被误诊。本研究回顾性分析经手术病理证实的10例卵巢无性细胞瘤的临床及超声资料,探讨其超声表现,以提高对该病的超声诊断水平。
方 法
1. 一般资料
收集2013年1月至2021年6月本院收治的经手术病理证实的10例卵巢无性细胞瘤患者资料。患者8例为女性,2例为染色体异常。年龄16~44岁,平均年龄(26.7±8.17)岁。临床表现:腹痛2例,原发闭经2例(其中1例患高促性腺激素性性腺功能减退症),排卵期出血1例,3例合并妊娠(分别于孕7+周、孕5周、孕15周时发现),2例无明显症状者为体检时发现。7例行阴道超声检查,1例经直肠超声检查,2例经腹部妇科超声检查。
2. 检查方法
有性生活者采用经阴道超声,无性生活者采用经腹部盆腔超声检查/经直肠超声检查,标本均行光镜及免疫组化染色检查。观察肿瘤的部位、大小、形态、边缘、回声、血流信号、有无盆腹腔积液。
3. 统计学分析
采用SPASS16.0统计软件进行统计学处理,呈正态分布的计量资料以xˉ±s表示。
结 果
1. 一般表现
本组10例患者共11个病灶,位于左侧3例,右侧6例,双侧1例。肿瘤最大者为214 mm×163 mm,最小者为37 mm×23 mm,最大径(100±55.35)mm,5例病灶最大径>10 cm。肿瘤大多巨大,呈类圆形。1例双侧附件未探及明显包块,仅在手术病理发现。4例血清人绒毛膜促性腺激素(HCG)升高(3例合并妊娠),10例糖类抗原(CA)-125均升高,所有病例甲胎蛋白(AFP)、癌胚抗原(CEA)、CA19-9、CA15-3均阴性。
2. 超声表现
10例患者均接受超声检查,8例子宫大小未见异常,1例为始基子宫,1例为幼稚子宫。子宫附件未见明显异常1例,实性软组织肿块5例,实性部分为主的囊实性肿块4例。3例伴有少许散在不规则液性区,2例病灶内可伴小斑点状、小条状、大片状钙化(其中1例为混合型合并畸胎瘤)。形态均较规则,边界清。
彩色多普勒血流成像(CDFI):6例肿块内血流丰富,血流频谱呈高速低阻型,阻力指数(RI)为0.51~0.65,2例合并蒂扭转(其中1例血流信号稀少,1例未见明显血流信号),1例混合型(畸胎瘤成分为主)未见明显血流信号。不合并直肠窝积液4例(3例ⅠA期,1例ⅢC期),合并单纯子宫直肠窝积液1例(转移至右髂内及右闭孔淋巴结),盆腹腔积液2例,均为无性细胞瘤合并蒂扭转,1例(腹膜组织活检)纤维结缔组织中可见肿瘤细胞浸润,1例未见转移。
术前超声诊断:阴道下段或处女膜闭锁、宫外孕、畸胎瘤子宫肌瘤各1例(后病理证实均为误诊),盆腔包块性质待查5例,双侧附件未探及明显包块1例。典型病例超声表现如图1所示。
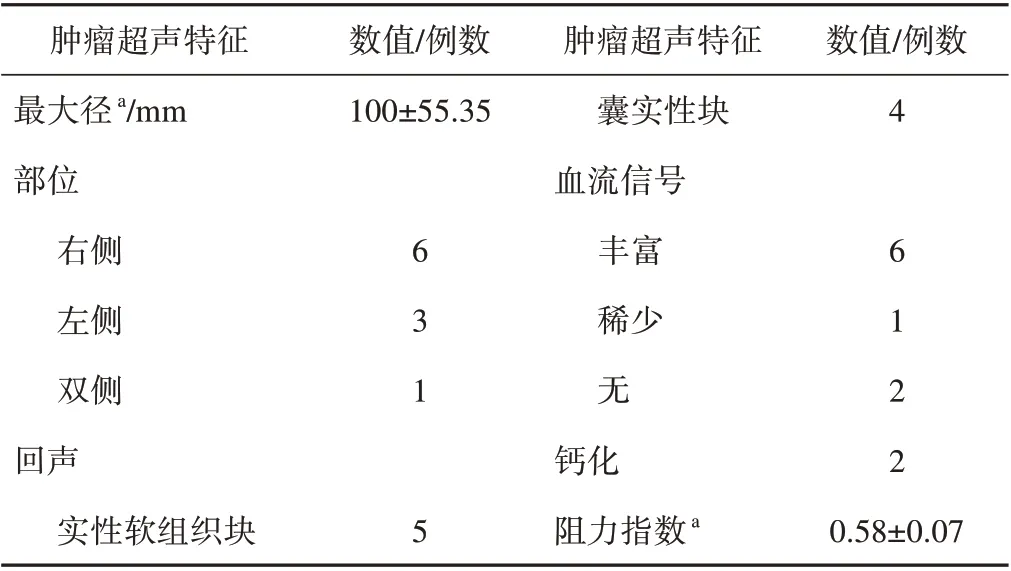
表1 10例无性细胞瘤患者超声表现
3. 病理学分析
10例无性细胞瘤中,7例行患侧卵巢切除术,1例46岁患者腹腔镜下右侧附件切除术后10 d再行腹腔镜下全子宫切除术+左侧卵巢输卵管切除术+盆腔淋巴结清扫术,2例行双侧性腺切除术。
大体病理:大部分肿块边界清楚,有完整包膜,。切面呈灰白或灰红色,部分呈分叶状,部分伴囊变、病灶出血和坏死。
镜下表现:7例为单纯型,肿瘤由大小一致的细胞构组成,瘤细胞呈多角形或圆形,呈团状及片状排列,细胞间境界清晰,胞质淡染或透亮,核大而圆,核仁明显,瘤细胞团被富含血管的纤维组织分隔,间隔内见较多淋巴细胞浸润。3例为混合型,其中1例为畸胎瘤合并恶性生殖细胞成分(无性细胞瘤,范围约1 cm),2例含性腺母细胞瘤成分。
讨 论
1. 临床表现
早期诊断困难,缺乏典型临床症状,多数患者因后期肿物较大出现腹痛、腹部肿物就诊。极少数合成HCG的无性细胞瘤可引起月经紊乱、不规则阴道流血,临床表现类似异位妊娠。本组病例中因腹痛就诊2例,原发闭经就诊2例,排卵期出血就诊1例,体检发现2例,产检时发现3例。
2. 超声表现
单纯型卵巢无性细胞瘤多表现为巨大实性肿块,呈不均质等或低回声,无声衰减,瘤体中部可见树枝状稍高回声分隔,将实性肿瘤组织分隔成小叶状低回声区,无或仅有少许散在不规则液性区,病灶内可伴小斑点状、小条状、大片状钙化,形态较规则,边界清。彩色多普勒血流成像:肿块内血流多丰富,合并蒂扭转时血流信号稀少或未见明显血流信号。有研究指出[3]50%病例出现子宫直肠窝积液,本组3/7有直肠窝积液,另有研究[4]转移病例合并大量盆腹腔积液,其他病例未发现明确积液,然而本研究中1例ⅢC期不合并积液,1例ⅠC期合并盆腹腔积液,考虑无性细胞瘤与盆腔积液没有必然联系,合并盆腔积液与是否合并转移亦无必然联系。
混合型超声表现缺乏特异性,本组3例混合型(1例合并畸胎瘤,2例合并性腺母细胞瘤):1例因无性细胞瘤范围小(约1 cm)且合并畸胎瘤而误诊为畸胎瘤。2例合并性腺母细胞瘤者均存在染色体异常和子宫畸形,其一合并幼稚子宫,超声表现为双侧附件未见明显占位灶,仅术后病理发现;另一合并始基子宫,右侧盆腔占位表现为实性回声包块,内回声不均,可见散在强回声光斑,后方未见声影,CDFI示包块内可见丰富条状彩色血流信号,RI为0.65,可见来源右侧髂内动脉血供。少量盆腔积液声像。
无性细胞瘤可因体积过大而发生蒂扭转,本组病例中2例合并蒂扭转,均因腹痛来我院急诊超声,其中1例误诊为宫外孕,误诊原因在于患者急性起病,有停经史,β-HCG升高,达39.58μg/L(正常值0~5 μg/L),超声声像图把扭转的蒂部当成右侧卵巢,从而把肿物当成卵巢以外的包块。同时,蒂扭转导致无性细胞瘤血流信号稀少。
无性细胞瘤可能与性腺发育不良、Turner综合征、睾丸女性化、3X综合征有关[5],本研究中2例染色体异常:其一为46XY,病理双侧卵巢性腺母细胞瘤并(右侧)卵巢无性细胞瘤,盆腔内有始基子宫及输卵管;另一为45X/46XY嵌合型发育异常,超声提示幼稚子宫,双侧附件未见明显异常,因患者要求切除性腺行性腺切除术,病理:混合性生殖细胞合并性索肿瘤。
3. 鉴别诊断
本研究中有超声检查并且得到病理确诊的无性细胞瘤10例,其中误诊4例,1例初次经直肠超声检查误诊为阴道下段或处女膜闭锁,三维经直肠超声复查时得以明确诊断;1例误诊为子宫肌瘤;1例误诊为宫外孕;1例因无性细胞瘤体积小且合并畸胎瘤被误诊为畸胎瘤。当合并始基子宫时应仔细寻找子宫的轮廓,辨别包块的位置是位于宫腔及阴道上段还是附件区,避免误认为积血,而考虑为阴道下段或处女膜闭锁。子宫浆膜下/阔韧带肌瘤:好发于孕龄期女性,浆膜下肌瘤常有“蒂”与子宫相连,阔韧带肌瘤沿阔韧带走行,不侵犯邻近结构,肿瘤标志物正常[6]。本组1例无性细胞瘤表现为一个巨大低回声团,而检查者未对双侧附件进行认真扫查,误以为双侧附件因子宫过大及肠气回声遮挡显示不清,而把无性细胞瘤误认为子宫肌瘤,分清肿块与子宫的关系及对正常一侧卵巢的寻找是避免误诊的关键;无性细胞瘤HCG可升高,合并蒂扭转且瘤体内血流稀少时易误诊为宫外孕。
卵巢无性细胞瘤还需与以腹、盆腔实性肿块为主要表现的以下肿瘤相鉴别:
(1)卵巢卵泡膜-纤维瘤类肿瘤:好发于50~60岁女性,属于间质肿瘤,典型超声表现:肿块多呈实性低回声,形态规则,边界清,后方多伴回声衰减,彩色多普勒血流成像:肿瘤内部无或少许血流,常伴有雌激素升高及子宫内膜增厚[6]。本组7例发生在育龄女性,3例为青春期,发病年龄可作为鉴别点之一。
(2)卵巢内胚窦瘤:也是好发于年轻女性,发病平均年龄18岁,且瘤体较大,但实性部分内见大小不一、边界清晰的小囊腔散在分布,血清AFP浓度增高。恶性程度高,进展快,易出现转移和复发,预后较差。
综上所述,由于无性细胞瘤发病率低,超声医生对其认识不足,诊断多局限于常见的妇科疾病,因而容易误诊,但通过总结其超声声像图表现,发现其具有一定特异性,如果对其有一定的认识,结合患者年龄,临床特点及实验室检查,可与其他腹盆腔实性肿块相鉴别。此外,对青少年患者,尤其无月经来潮的青春期患者,应除外染色体异常。

