超声内镜与CT对上消化道黏膜下肿瘤诊断价值比较研究
上消化道黏膜下肿瘤(submucosal tumors,SMTs)为上消化道被覆正常上皮的一类肿瘤,根据其生物学特性可分为良性肿瘤(如平滑肌瘤、囊肿、脂肪瘤等)和恶性肿瘤,两者具有不同的治疗策略及预后
。胃肠道间质瘤(gastrointestinal stromals,GISTs)为最常见具有恶性潜能的SMTs,目前诊断仍依靠病理及免疫组化,其影像学研究仍较贫乏,尤其对长径<20 mm的微小GISTs的影像学诊断仍较困难
,本文旨在探讨超声内镜(endoscopic ultrasonography,EUS)和CT对不同大小SMTs的影像学特点及诊断价值。
1 资料与方法
回顾性分析2018年8月至2020年10月因上消化道SMTs就诊我院并行手术治疗患者的病例资料,纳入标准:(1)具有完整的EUS及CT检查资料;(2)EUS及CT检查前未接受穿刺、化疗、新辅助治疗等;(3)均行手术治疗且具有术后完整病理诊断资料。排除标准:(1)合并其他恶性肿瘤者;(2)临床资料不完整或病理诊断不明确者。
综上所述,在临床护理教学中采用CPBL教学模式,力求提高临床护理教学质量,为CPBL教学法在临床护理学中广泛应用提供参考。
1.2.1 EUS检查:术前禁食水8 h,术前半小时内予消泡剂、咽喉局部麻醉剂,解痉剂等药物,根据病变大小及位置选在超声微探头或纵轴超声,观察并记录结果。
但银隆内部人士说,孙国华根本坐不稳这个位置。由于孙国华与魏银仓关系私密,离任的魏银仓经常对公司运作发出指令。而董明珠则要求加强公司制度建设,通过股东会和董事会来加强对公司的控制,双方矛盾再度加深。
死体可燃物含水率(Y)与气温(X2)、相对湿度(X3)、连旱天数(X4)、风速(X5)、蒸发量(X6)之间的数学模型为:
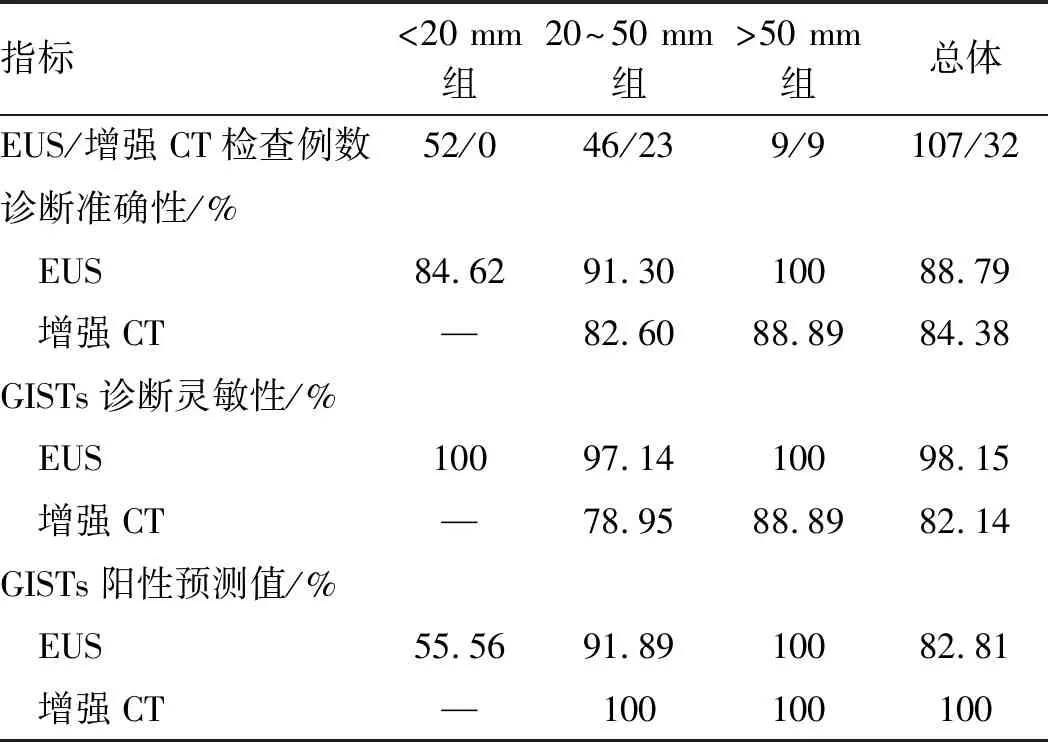
本研究根据肿瘤长径分为三组,EUS扫查均能发现病灶,阳性率为100%,且与手术病理对比102例肿瘤起源层判断准确,诊断符合率为95.33%。长径<20 mm组52例,CT仅发现胃部病灶5例,阳性率仅9.62%,而食管内病灶阳性率为0,且均未获得明确诊断;长径20~50 mm组46例,CT发现31例,阳性率为67.39%;长径>50 mm组9例,阳性率为100%。以手术病理为金标准,EUS和增强CT对各组的诊断价值如表2所示,可见EUS对长径<20 mm阳性预测值较低,余均具有较高灵敏性及准确性,增强CT对长径>20 mm组具有较高的准确性,且与EUS差异无统计学意义(
<0.05)。
2 结果
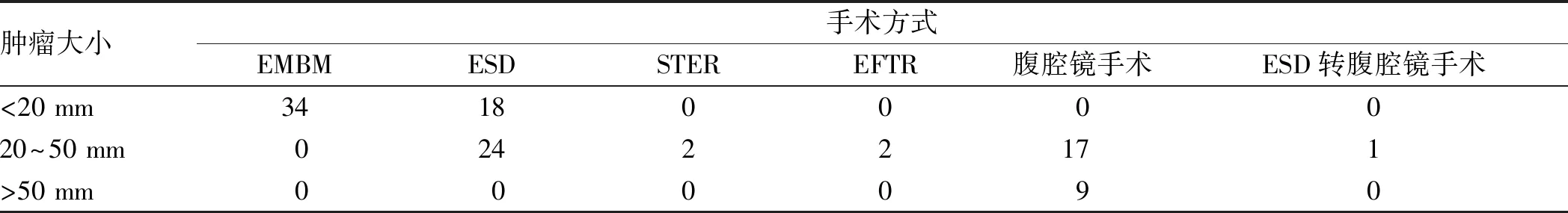
本研究中所有长径<20 mm及部分20~50 mm者进行内镜下手术,包括内镜下多环黏膜套扎切除术(endoscopic multi-band mucosectomy,EMBM)、内镜下黏膜剥离术(endoscopic submucosal dissection,ESD)、内镜黏膜下隧道肿瘤切除术(submucosal tunneling endoscopic resection,STER)、内镜全层切除术(endoscopic full-thickness resection,EFTR)(见表3),其中1例ESD出现穿孔进而转为腹腔镜手术,其余均接受腹腔镜下肿瘤切除术。
石西岳不笑,也不讲话,一时间冷了场。就在这时,外面传来一阵吵闹声,众多粗嗓门中夹杂着一个尖细的声音。刘雁衡侧耳听了听,快步走出室外。
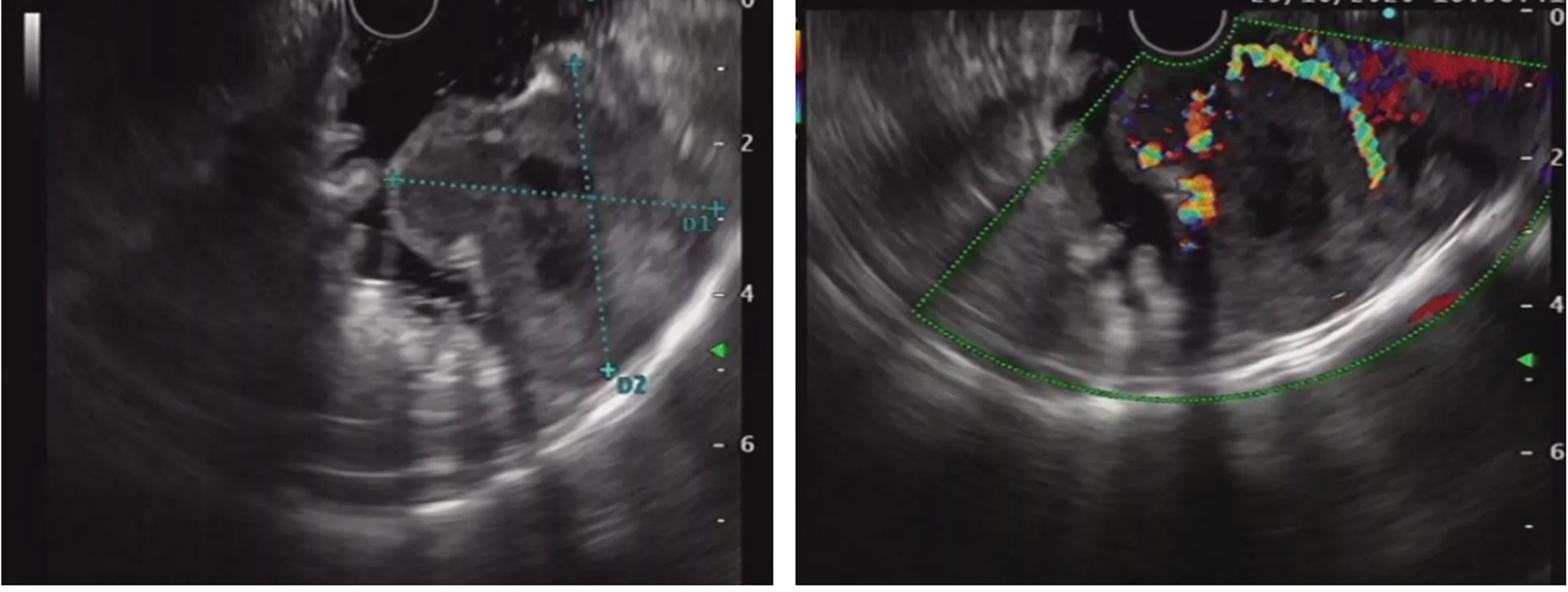
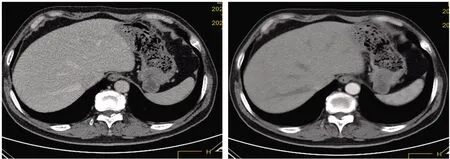
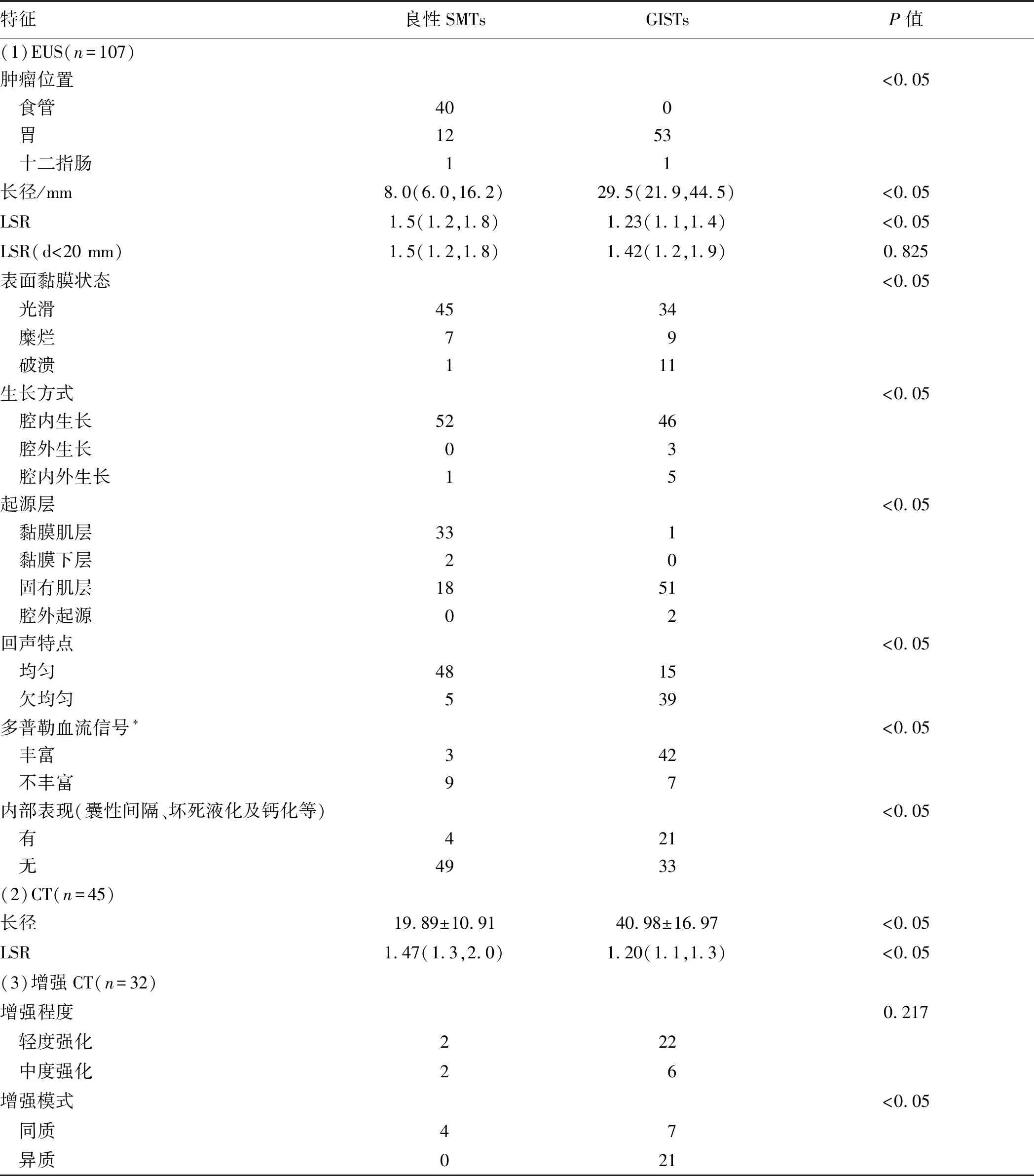
本研究中良性SMTs和GISTs影像学表现如图1~2所示。EUS下可见良性肿瘤及GISTs在肿瘤位置、长径、长短径比值(long-to-short ratio,LSR)、生长方式、表面黏膜状态、起源层、回声特点、多普勒血流信号、内部表现等方面差异有统计学意义(
<0.05)。107例患者均接受CT检查,其中45例发现病灶,阳性率42.06%,良性SMTs和GISTs在长径、LSR方面比较,差异有统计学意义(
<0.05),CT平扫下肿瘤均表现为软组织密度影,其中有32例平扫发现病灶后进一步接受增强CT检查,良性SMTs与GISTs均多表现轻度强化,但差异无统计学意义(
>0.05),而GISTs内部密度多不均匀呈现异质强化,与良性SMTs比较,差异有统计学意义(
<0.05)(见表1),此外CT发现1例肿瘤伴有腹腔淋巴结转移,行腹腔镜手术切除后病理证实为高风险间质瘤,术后辅以伊马替尼治疗。
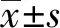
共收集126例SMTs患者相关资料,根据相关标准排除部分资料不全或合并其他肿瘤者,最终107例患者纳入本研究,男49例,女58例,年龄(56.31±9.50)岁,病灶长径为2.5~83.2 mm,中位长径为20.2 mm,经病理确诊GISTs共54例,良性SMTs共53例(其中平滑肌瘤45例、炎性纤维性肿瘤4例、囊肿2例、布氏腺瘤2例),良性SMTs年龄(52.79±9.24)岁,GISTs年龄(59.76±8.51)岁,两组年龄比较,差异有统计学意义(
<0.05)。
收集患者基本资料,EUS下所见(包括病灶位置、大小、起源层、回声、血流信号、病灶内部表现等),CT表现(包括位置、大小、边缘轮廓、生长模式、增强模式、淋巴结、远处转移等),手术方式及病理结果。该研究已通过医院伦理委员会审核(伦理号:SL-LC2019019)
1.2.2 CT检查:所有患者采用多排螺旋CT机,检查前口服纯净水600~800 ml充盈胃腔,增强扫描前经肘静脉高压注射碘对比剂,扫描范围从膈顶至双肾下级,分别记录动脉期、静脉期、延迟期图像。
3 讨论
随着内镜技术的普及和发展,上消化道SMTs的发现率不断升高,其中,GISTs为最常见的具有恶性潜能的肿瘤,目前临床上对上消化道SMTs的诊断重点依旧是对良恶性肿瘤的鉴别及对GISTs恶性潜能评估,常用检查手段包括EUS、CT等。本研究选取患者均接受EUS和CT检查,经最终病理诊断,GISTs 54例,良性SMTs 53例,与彭春艳等
研究结论相符,间质瘤主要发生于胃(53/54)且源于固有肌层(51/54),腔内、腔外及腔内外生长,表面黏膜可见糜烂或破溃,瘤体更大,LSR比值更低,EUS见肿瘤内部呈不均匀低回声且可存在囊性间隔、液化坏死、钙化等特异性表现,彩色多普勒可见较丰富的微细血流,与良性肿瘤比较,差异均有统计学意义(
<0.05),以术后病理为金标准,本研究中EUS诊断的总体准确性可达88.79%。
既往研究中CT结合肿瘤位置、长径、LSR、肿瘤CT值及增强模式进行鉴别诊断
,本研究发现CT诊断性能较EUS差,尤其对长径<20 mm者CT阳性率仅9.62%,食管病变的检出率甚至为0,这部分患者选择CT进行诊断及随访是不可靠的,而EUS诊断准确性为84.62%,对GISTs诊断灵敏性及阳性预测值为100%、55.56%,且詹翔等
研究超声联合内镜下治疗具有较高的安全性,该组52例中34例行EMBM手术,另18例行ESD,均成功切除并未出现并发症,EUS为长径<20 mm肿瘤不可替代的术前检查或随访手段。
在20~50 mm组CT的检出率仍偏低,为67.39%,增强CT诊断准确性为82.60%,EUS为91.30%,差异无统计学意义(
>0.05)。Huh等
指出增强CT与EUS鉴别平滑肌瘤和GISTs同样有效,增强CT表现病灶内坏死区和低LSR为GISTs的独立预测因素,但本研究中增强CT对GISTs诊断的灵敏性78.95%远不如EUS为97.14%,且体积越小肿瘤内部特异性表现越少见。此外术前明确肿瘤位置、大小、起源层,初步判断良恶性及进行恶性风险预评估等对不同手术方式选择具有指导作用,该组46例患者中24行ESD,2例行STER,2例行EFTR,1例ESD术中转腹腔镜,17例腹腔镜手术,从手术方式选择上EUS诊断性能明显优于CT,EUS通过结合白光内镜及超声成像,清楚显示消化道并动态观察肿瘤的来源层次,明确肿瘤生长方式及与邻近组织器官的关系,本研究中对病变的起源与病理符合率高,为95%以上,与丁艳乐等
97.73%相仿。CT作为横断面扫描手段对周围组织侵犯,淋巴结及远处转移具有优势,本研究中有1例经CT发现周围淋巴结肿大,最终行腹腔镜手术且术后病理提示为间质瘤,辅以伊马替尼治疗,且Chu等
研究表明,与单纯EUS相比,术前同时联合CT还具有更短的手术时间及更少丙泊酚使用剂量,因此,EUS表现高风险特征联合CT检查可获得更全面的评价及制定更合适的治疗策略,同时减少对一些良性肿瘤(如脂肪瘤、囊肿等)或较小肿瘤不必要的放射性检查。对长径>50 mm组本研究EUS与CT诊断价值间差异无统计学意义,在最新胃肠间质瘤内镜下诊治专家共识
里指出,对肿瘤长径>50 mm者均需行外科手术治疗,术前接受EUS及CT双重检查能够获得更全面的术前评价,本研究中9例接受腹腔镜手术,术后均无并发症发生。
调查项目包括株高、穗高、播种至抽丝期、播种至散粉期、鲜穗重,室内考查穗长、穗行数、行粒数、穗粒重和品质得分。授粉后第28天在各小区取中间2行果穗,测定鲜穗重、穗长、穗行数及行粒数,晒干后脱粒测定每穗粒重。在小区中间1行随机选取10株进行穗套袋自交,用于测定参试组合的品质得分,品质得分参照四川省区域试验品质评价方法。
既往研究
EUS下GISTs高风险特性包括不完整包膜、不规则边界、异质性回声、内部特异性表现等,且NCCN指南指出对缺乏高风险特征的微小GISTs(<20 mm)能够选择定期随访
,但本研究发现这些特点在中小型肿瘤(尤其<20 mm)中并不常见,在GISTs之间差异无统计学意义(
>0.05)。近些年研究发现肿瘤内血管密度对诊断具有重要作用
,多普勒超声往往只能对较粗或血流速度较快血管进行成像,而一种新技术对比谐波超声造影(contrast-enhanced harmonic endoscopic ultrasonography,CEH-EUS)将谐波成像和第二代造影剂(常用的有SonoVue、Sonazoid)相结合,对肿瘤内部微血管进行灌注成像,结合不同强化模式、肿瘤内不规则血管及时间强度曲线等进行鉴别诊断及对GISTs进行评估
,有望成为上消化道SMTs一种无创、安全、有效的检查方法。
综上所述,EUS对不同长径肿瘤均具有较高的诊断价值,尤其对<50 mm的肿瘤明显优于CT,并对不同大小的间质瘤的鉴别诊断具有其独特的优势,且随着EUS-FNA等技术的发展,EUS已成为首选的检查方式。恰当联合CT检查可提高诊断的准确性及制定更优治疗策略。本研究因样本量问题存在一定的局限性,有待扩充样本量进一步研究。
[1] Koo DH, Ryu MH, Kim KM, et al. Asian consensus guidelines for the diagnosis and management of gastrointestinal stromal tumor [J]. Cancer Res Treat, 2016, 48(4): 1155-1166. DOI: 10.4143/crt.2016.187.
[2] Iorio N, Sawaya RA, Friedenberg FK. Review article: the biology, diagnosis and management of gastrointestinal stromal tumours [J]. Aliment Pharmacol Ther, 2014, 39(12): 1376-1386. DOI: 10.1111/apt.12761.
[3] Nishida T, Goto O, Raut CP, et al. Diagnostic and treatment strategy for small gastrointestinal stromal tumors [J]. Cancer, 2016, 122(20): 3110-3118. DOI: 10.1002/cncr.30239.
[4] 彭春艳, 吕瑛, 徐桂芳, 等. 术前超声内镜对胃间质瘤的诊断及侵袭危险性评估价值研究[J]. 中华消化内镜杂志, 2015, 32(6): 361-366. DOI: 10.3760/cma.j.issn.1007-5232.2015.06.002.
Peng CY, Lyu Y, Xu GF, et al. Evaluation of preoperative endoscopic ultrasonography for diagnosis and invasive risk assessment of gastric gastrointestinal stromal tumors: a single-center retrospective study [J]. Chin J Dig Endosc, 2015, 32(6): 361-366. DOI: 10.3760/cma.j.issn.1007-5232.2015.06.002.
[5] Choi YR, Kim SH, Kim SA, et al. Differentiation of large (≥5 cm) gastrointestinal stromal tumors from benign subepithelial tumors in the stomach: radiologists’ performance using CT [J]. Eur J Radiol, 2014, 83(2): 250-260. DOI: 10.1016/j.ejrad.2013.10.028.
[6] Choi JW, Choi D, Kim KM, et al. Small submucosal tumors of the stomach: differentiation of gastric schwannoma from gastrointestinal stromal tumor with CT [J]. Korean J Radiol, 2012, 13(4): 425-433. DOI: 10.3348/kjr.2012.13.4.425.
[7] 詹翔, 周玉保, 张道权, 等. 超声微探头联合多环黏膜套扎切除术治疗食管黏膜下肿瘤的临床研究[J]. 中国内镜杂志, 2020, 26(9): 29-34. DOI: 10.3969/j.issn.1007-1989.2020.09.006.
Zhan X, Zhou YB, Zhang DQ, et al. Clinical study of ultrasound microprobe combined with endoscopic multi-band mucosectomy in the treatment of esophageal submucosal tumors [J]. China Journal of Endoscopy, 2020, 26(9): 29-34. DOI: 10.3969/j.issn.1007-1989.2020.09.006.
[8] Huh CW, Jung DH, Kim JS, et al. CT versus endoscopic ultrasound for differentiating small (2-5 cm) gastrointestinal stromal tumors from leiomyomas [J]. AJR Am J Roentgenol, 2019, 213(3): 586-591. DOI: 10.2214/AJR.18.20877.
[9] 丁艳乐, 丰义宽, 周新玲, 等. 超声内镜对上消化道黏膜下肿瘤的诊断价值[J]. 胃肠病学和肝病学杂志, 2017, 26(10): 1146-1149. DOI: 10.3969/j.issn.1006-5709.2017.10.020.
Ding YL, Feng YK, Zhou XL, et al. The value of endoscopic ultrasonography in diagnosis of submucosal tumor of upper gastrointestinal tract [J]. Chin J Gastroenterol Hepatol, 2017, 26(10): 1146-1149. DOI: 10.3969/j.issn.1006-5709.2017.10.020.
[10] Chu Y, Qiao X, Gao X, et al. Combined EUS and CT for evaluating gastrointestinal submucosal tumors before endoscopic resection [J]. Eur J Gastroenterol Hepatol, 2014, 26(8): 933-936. DOI: 10.1097/MEG.0000000000000136.
[11] 中华医学会消化内镜学分会消化内镜隧道技术协作组, 中国医师协会内镜医师分会, 北京医学会消化内镜学分会. 中国胃肠间质瘤内镜下诊治专家共识意见(2020,北京)[J]. 中华胃肠内镜电子杂志, 2020, 7(4): 176-185. DOI: 10.3877/cma.j.issn.2095-7157.2020.04.002.
[12] Nishida T, Kawai N, Yamaguchi S, et al. Submucosal tumors: comprehensive guide for the diagnosis and therapy of gastrointestinal submucosal tumors [J]. Dig Endosc, 2013, 25(5): 479-489. DOI: 10.1111/den.12149.
[13] Palazzo L, Landi B, Cellier C, et al. Endosonographic features predictive of benign and malignant gastrointestinal stromal cell tumours [J]. Gut, 2000, 46(1): 88-92. DOI: 10.1136/gut.46.1.88.
[14] von Mehren M, Randall RL, Benjamin RS, et al. Soft Tissue Sarcoma, Version 2.2016, NCCN Clinical Practice Guidelines in Oncology [J]. J Natl Compr Canc Netw, 2016, 14(6): 758-786. DOI: 10.6004/jnccn.2016.0078.
[15] Chhoda A, Jain D, Surabhi VR, et al. Contrast enhanced harmonic endoscopic ultrasound: a novel approach for diagnosis and management of gastrointestinal stromal tumors [J]. Clin Endosc, 2018, 51(3): 215-221. DOI: 10.5946/ce.2017.170.
[16] Masayuki K, Yasunobu Y. New imaging techniques for endoscopic ultrasonography: contrast-enhanced endoscopic ultrasonography [J]. Gastrointestinal Endosc Clin N Am, 2017, 27(4): 569-583. DOI: 10.1016/j.giec.2017.06.002.

