g-C3N4复合Ge锂离子电池负极材料的制备及其性能
殷立雄, 李书航, 宋佳琪, 黄剑锋, 赵 津, 白培杰
(陕西科技大学 材料科学与工程学院 陕西省无机材料绿色制备与功能化重点实验室, 陕西 西安 710021)
0 引言
科技时代与时俱进的今天,无线电子设备普及广,而这些设备都需要电源[1].锂离子电池(LIBs)由于具有较高能量密度、无记忆效应、长循环寿命、低自放电、环保等优点,正逐步成为应用广泛的主流电池[2].相应的,锂电池成为研究大热.目前商用的石墨电极理论容量较低(372 mAh/g),很难满足当前时代的要求[3,4].锗作负极材料有较优越的理论容量(Ge为1 600 mAh/g,GeO2为2 152 mAh/g)和优异的电化学性能[5-8]被认为是石墨的良好替代品,当然这主要归因于其小的带隙(0.6 eV)、高的电子电导率和快的锂离子扩散速率[9,10].但锗作负极材料同样面临严重问题:在充放电过程中发生合金/去合金化反应发生巨大体积膨胀(完全锂化形成的Li4.4Ge体积膨胀高达370%),带来材料的结构粉化和坍塌,造成电极容量快速衰减的不良后果.阻碍了锗基负极材料在锂离子电池上的应用发展[11].
为了克服这个障碍,提高电池的循环寿命.科研工作者已经进行了许多的相关工作,构造不会引起或可以缓解巨大的体积变化的Ge基材料[12-14]:锗合金负极材料(如二元电极材料Ge/Sn、Ge/Se和Ge/Si等[15,16],三元电极材料Zn2GeO4、CuGeO3和Ca2Ge7O16等[17,18])和复合材料(如Ge/C复合材料、Ge/石墨烯复合材料和核壳结构纳米复合材料等[19]).Wang等[20]通过射频溅射方法在预合成的Cu纳米线阵列的表面上直接沉积Ge,合成了具有三维结构的Cu-Ge核壳纳米线阵列电极材料.Cu-Ge纳米线阵列在0.5 C电流密度下,循环40圈后,显示出1 419 mAh/g的高容量,甚至在60 C高电流密度下,80次循环后,仍保持较高的比容量(734 mAh/g);Li等[21]通过碳热反应,使用NH4H3Ge2O6/间苯二酚-甲醛作为前驱体,成功制得了Ge纳米颗粒被中空碳盒均匀封装的Ge/C复合材料.拥有此特殊微观结构的Ge/C,在0.2 A/g电流密度下,初始的库仑效率高达85.1%,同时有1 336 mAh/g的优异可逆容量.此外该电极在4 A/g的电流密度下仍有825 mAh/g的倍率容量,这等优秀的电化学性能归根到底是因为此法所致的Ge/C独特微结构.
目前,报道较多的方法是使用类碳缓冲材料来减缓Ge体积变化.缓冲矩阵能减缓体积膨胀是因为与锂发生反应的材料分散在电化学不活跃(或不太活跃)的矩阵中,以此达到缓解体积膨胀的目的.碳基体可起阻止活性材料团聚的作用,减轻电极中的粉化,使电极在电化学上有较好可逆性.
本研究中,使用管式炉煅烧制备Ge单质后,以聚乙烯吡咯烷酮作碳源制得氮化碳(g-C3N4),通过水热反应制备出具层级结构和丰富孔道结构的Ge/g-C3N4复合材料.研究发现,当反应温度为180 ℃时所制备的复合电极初始容量高达1 275.7 mAh/g,经过100圈循环,电极的可逆容量仍保持在684.2 mAh/g,具有较高的比容量,就LIBs负极材料而言,该电极在电化学方面有良好性能,具备可观应用前景.
1 实验部分
1.1 实验材料
实验中采用的原材料有:二氧化锗(GeO2)、乙二胺(C2H8N2)、三聚氰胺(C3H6N6)、聚乙烯吡咯烷酮(PVP).
以上材料纯度都是分析纯,并且实验过程中没有再次提纯.
1.2 Ge/g-C3N4的制备
(1)Ge单质的制备:首先将1 g市售GeO2加入15 mL去离子水中,再将5 mL无水乙二胺逐滴加入烧杯,80 ℃下加热搅拌,直至溶液变成乳白色胶体,冷冻干燥12 h,得到白色颗粒.将颗粒研磨成粉末放入瓷舟后置于管式炉的石英玻璃管中,在氩气保护氛围下于800 ℃保温3 h,反应结束后得到黑色颗粒,研磨成粉末后即得Ge单质.
(2)g-C3N4的制备:称量5 g三聚氰胺放入瓷舟,瓷舟外层用铝箔包覆,置于马弗炉中于550 ℃条件下反应4 h,取出产物,用乙醇和蒸馏水反复离心几次后干燥,即得g-C3N4.
(3)Ge/g-C3N4的制备:称50 mg自制氮化碳于50 mL去离子水中,超声分散半小时,后加入0.5 g的PVP和100 mg的Ge单质,充分地搅拌.将溶液转移到100 mL聚四氟乙烯内衬,用不锈钢外釜密封后,置于烘箱内160 ℃、180 ℃、200 ℃温度下反应18 h,待反应结束,用C2H5OH及去离子水,对所得产物多次离心、洗涤,然后进行真空干燥(60 ℃、12 h),所得样品即为Ge/g-C3N4,按照温度高低,将160 ℃、180 ℃、200 ℃条件下制得的样品分别记为Ge/CN-1、Ge/CN-2、Ge/CN-3.
1.3 材料表征
采用型号为D/max-2200PC的衍射仪(日本Rigaku生产)对样品进行成分鉴定.通过场发射扫描电子显微镜(SEM,S4800)观察样品微观形貌,用透射电子显微镜(TEM,Tecnai G2 f20)分析样品地内部结构和分布.利用美国麦克仪器公司生产的ASAP2460比表面积分析仪(BET)测试氮气等温吸附-脱附曲线,来确定材料的比表面积.
1.4 电化学性能测试
1.4.1 电池的制备与组装
活性电极的制备通过70%活性物质、7.5%聚丙烯酸、7.5%羧甲基纤维素和15%乙炔黑混合并磨匀所得,后滴少量去离子水,磨到均匀浆料状.把浆料均匀得在铜箔上涂覆,放在烘箱中去除多余水分.使用切片机将干燥后的铜箔切成直径为10 mm的圆形电极片,最后称重并计算活性物质的质量,为后续性能测试准备.
在氩气充盈的手套箱(水、氧气含量<0.5 ppm)里装配CR-2032型纽扣电池,将装配好的电池静置48小时,让电解液完全浸润,最后进行电化学性能的相关测试.
1.4.2 恒流充放电测试
采用新威BST-5 V/50 mA二次电池测试系统对组装的纽扣电池进行恒流充放电测试,电流密度为0.1 A/g.测试所用电压范围:0~3 V(相对于Li/Li+).
1.4.3 循环伏安(CV)测试
采用电化学工作站(CHI 660E)测量循环伏安曲线(CV).扫描速率:0.1 mv/s,电压范围:0.01~3 V.
1.4.4 电化学阻抗谱(EIS)测试
采用上述电化学工作站进行电化学阻抗(EIS)测试,频率范围:0.01~10 000 Hz.
2 结果与讨论
2.1 XRD分析
图1为在不同水热温度下(160 ℃、180 ℃、200 ℃)所制备样品的XRD图.从图1的XRD谱中清楚地看到,所有样品的主衍射峰全部位于27.3 °、45.3 °、53.7 °、66.0 °四个位置,所有衍射峰都与锗标准卡片(PDF.65-0333)相对应,分别代表(111)、(220)、(311)、(400)晶面,并且在26.5 °有较为明显的峰,对应于C3N4标准卡片(PDF.87-1526)的(002)晶面.这证明该制备方法成功合成出Ge/g-C3N4材料.
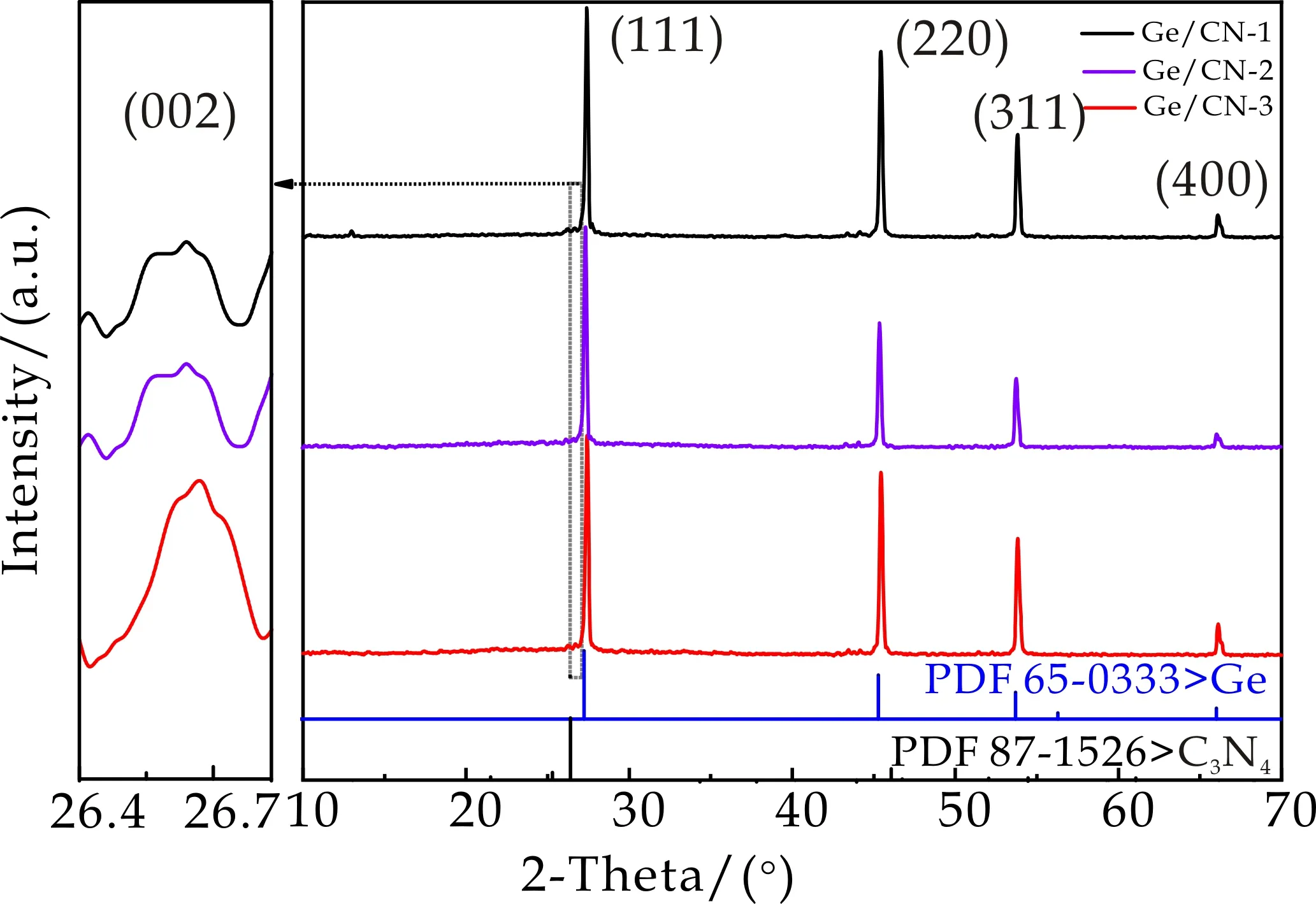
图1 不同温度所得样品的XRD图
2.2 SEM和TEM分析
图2是不同水热温度下所制样品的SEM图.当水热温度为160 ℃时,Ge/CN-1样品(如图2(a)所示)的微观形貌是团聚成块的层状结构,观察到有一定的孔隙.当温度调整到180 ℃时,图2(b)样品的孔道结构明显且很丰富,将倍数放大后,从图2(c)中能继续观察到材料存在孔隙,同时有较清晰的层级结构,对电极材料而言这种结构可以提供更多的活性位点,利于后续的电化学性能测试.当水热温度继续增至200 ℃时,Ge/CN-3样品(如图2(d)所示)的孔道结构坍塌的同时层级结构也遭到破坏,表现得不明显.

(a)Ge/CN-1 (b)、(c) Ge/CN-2 (d)Ge/CN-3图2 不同温度下所得Ge/CN的SEM图
为了研究Ge/CN-2的微观形貌,采用TEM表征,如图3所示.从图3(a)可以看出,Ge/CN-2拥有二维层级结构和孔隙结构,与上述SEM分析一致.进一步通过HRTEM图能看出Ge/CN-2复合物存在晶格条纹和非晶区域.通过测量,Ge/CN-2样品的晶格间距为0.197 nm,对应有序晶体纳米Ge单质的(200)晶面的晶面间距.而非晶区则代表氮化碳的存在[22].图3(c)~(f)为Ge/CN-2样品的EDS图,该图进一步显示Ge/CN复合材料中含有Ge、C、N和O元素.综上所述,通过安全简单的工艺成功制备出了氮化碳复合Ge的电极材料(Ge/CN-2).

(a)Ge/CN-2的TEM (b)Ge/CN-2的HRTEM (c)Ge (d)C (e)N (f)O图3 Ge/CN-2的TEM图、HRTEM图以及元素分布图
2.3 BET分析
图4为不同水热温度下(160 ℃、180 ℃、200 ℃)所制样品的N2等温吸附-脱附曲线.从图4可以看出,这是一种H4型滞后回线的IV型等温线,三个样品的比表面积分别为2.689 4 m2/g 、22.566 1 m2/g和12.256 6 m2/g.相比之下,180 ℃温度下制备的Ge/CN具有较大的比表面积.

图4 同温度Ge/CN的N2等温吸附-脱附曲线
2.4 电化学性能测试
为了进一步研究不同水热温度(160 ℃、180 ℃、200 ℃)条件下制备的Ge/CN电极材料的储锂性能,图5展示了包含纯相Ge电极材料和不同温度所制Ge/CN复合电极材料在0.1 A/g电流密度下的循环性能图.从图5中可以看出,在0.1 A/g电流密度下,Ge/CN-2电极的初始放电容量为1 275.7 mAh/g.从第二圈到第十二圈有上升趋势,这可能是活性物质与电解液充分发生反应,从第十三圈开始放电容量缓慢下降,直到第100圈容量仍能保持在684.2 mAh/g,远高于其他三个电极.而循环100圈后,纯相Ge的容量还剩370.9 mAh/g,Ge/CN-1和Ge/CN-3的容量仅维持在305 mAh/g和170.9 mAh/g.Ge/CN-2复合电极拥有较高容量与其二维层级结构和丰富的孔隙有直接关系,且孔道结构能和电解液接触更充分,同时富余的活性位点,提供通道便于离子和电子传输,缩短锂离子的扩散距离,对电化学的反应有益.
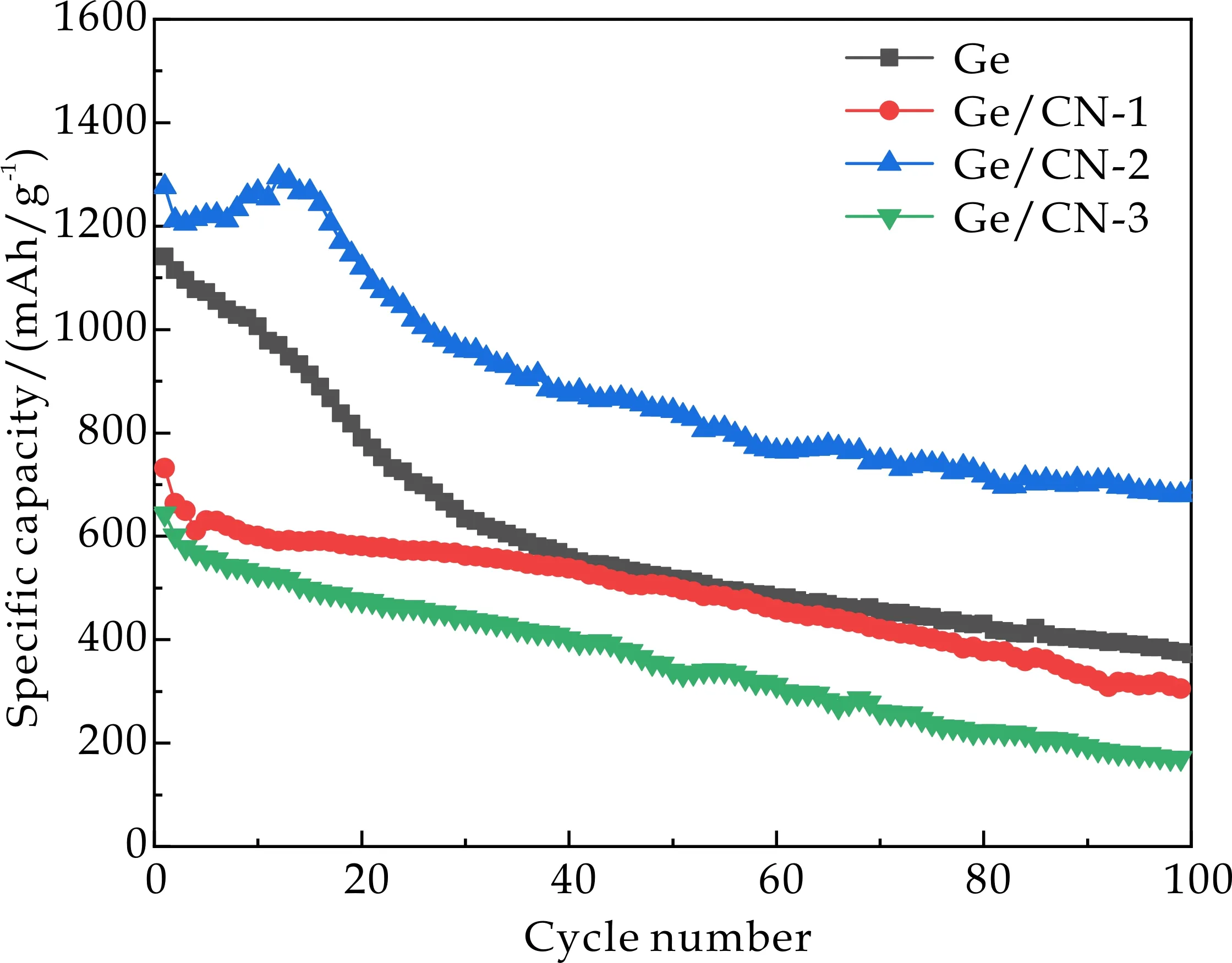
图5 纯相Ge和不同水热温度制备的Ge/CN复合电极材料的循环性能图
倍率性能是锂电池实际应用所需要考虑的另一个重要因素.图6所示为四个电极在0.05 A/g、0.1 A/g、0.2 A/g、0.5 A/g、0.8 A/g和1 A/g电流密度下的倍率性能图.从图6中能看出,Ge/CN-2电极在不同电流密度下的容量均高于其它电极,当电流密度为0.05 A/g、0.1 A/g、0.2 A/g、0.5 A/g、0.8 A/g和1 A/g时,该电极的倍率容量分别为1 273.1 mAh/g、950.5 mAh/g、674.0 mAh/g、529.4 mAh/g、 445.0 mAh/g和397.7 mAh/g.当电流密度恢复到0.1 A/g,Ge/CN-2电极的容量可以保持在563.7 mAh/g,同时Ge/CN-2电极在不同电流密度下容量相差较小,说明该电极拥有良好的倍率性能和电化学可逆性.这可能与其丰富的孔道结构和层级结构有关,BET测试结果显示这种结构拥有更大的比表面积,能提供更多的活性位点,益于电化学反应.
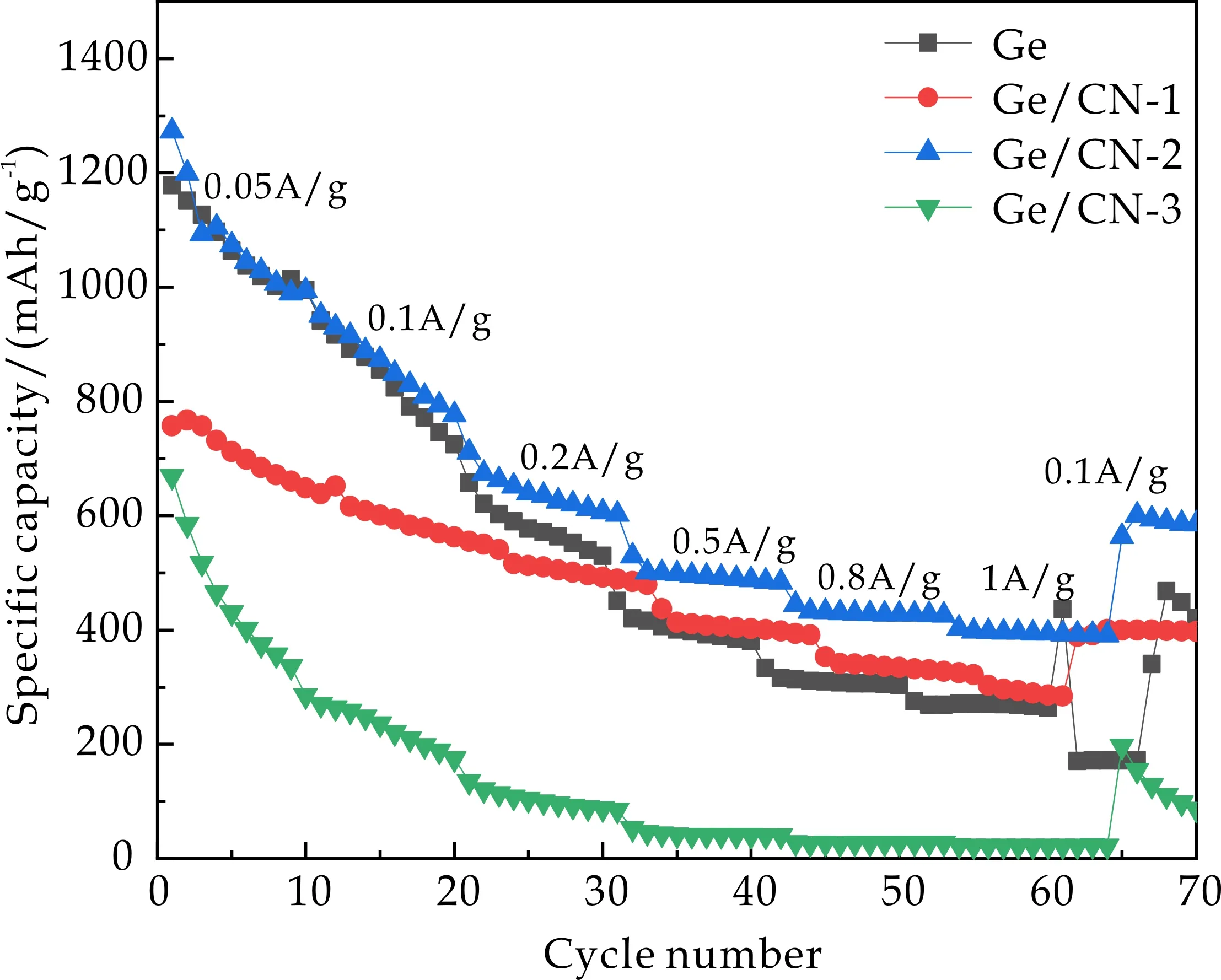
图6 纯相Ge和不同水热温度制备的Ge/CN复合电极材料的倍率性能图
为了进一步研究Ge/CN复合电极作锂离子电池负极材料时发生的电化学反应和储锂机理,将纯相Ge及Ge/CN-2复合电极进行CV测试,扫描电压范围:0.1~0.3 V,扫描速率:0.1 mv/s.如图7(a)所示,纯相Ge电极在第一圈放电过程中可以看到于初始电压处出现了一个还原峰,此峰对应于锗的合金化反应和锂锗合金的生成(Ge+xLi++xe-↔LixGe).而充电过程中位于0.5 V处的氧化峰则对应着去合金化反应,此外锗单质的氧化发生在第一圈中1.14 V处的氧化峰.和第一圈相比,在第二圈和第三圈的循环中,其增加了还原峰,除了在0.08 V对应的合金化反应外,位于0.3 V与0.5 V处的两个弱峰是由于SEI膜的生成和锗的转换反应(LixGeO2+Li→LiO2+Ge),其中SEI膜的形成无法避免,这也是不可逆容量损失多和初始库伦效率低的主要原因.与第一圈相比,在之后的第二圈和第三圈的循环中,还原峰的位置基本没有变化,只有转换反应峰的位置向高电位移动,这主要是由于电极材料结构的变化,也可能是由于固体电解质界面膜的生成.图7(b)为Ge/CN-2电极的CV曲线,由图7可知Ge/CN复合电极发生的电化学反应与纯相Ge类似,并且其氧化还原峰也有所重叠,且第二与第三圈所包围的面积没有较大变化,这表明Ge/CN复合电极有良好的电化学可逆性.
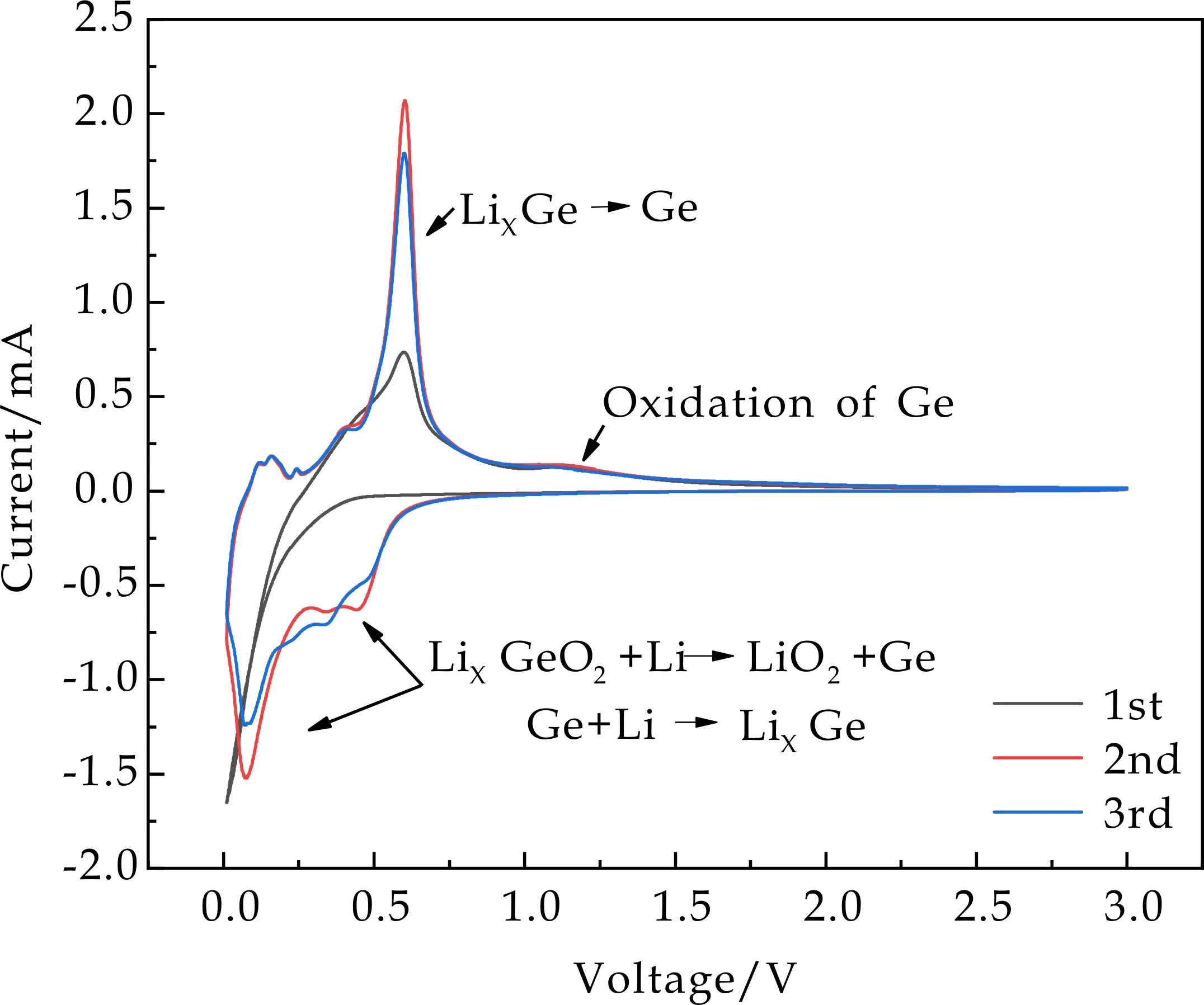
(a)纯相Ge电极的CV曲线
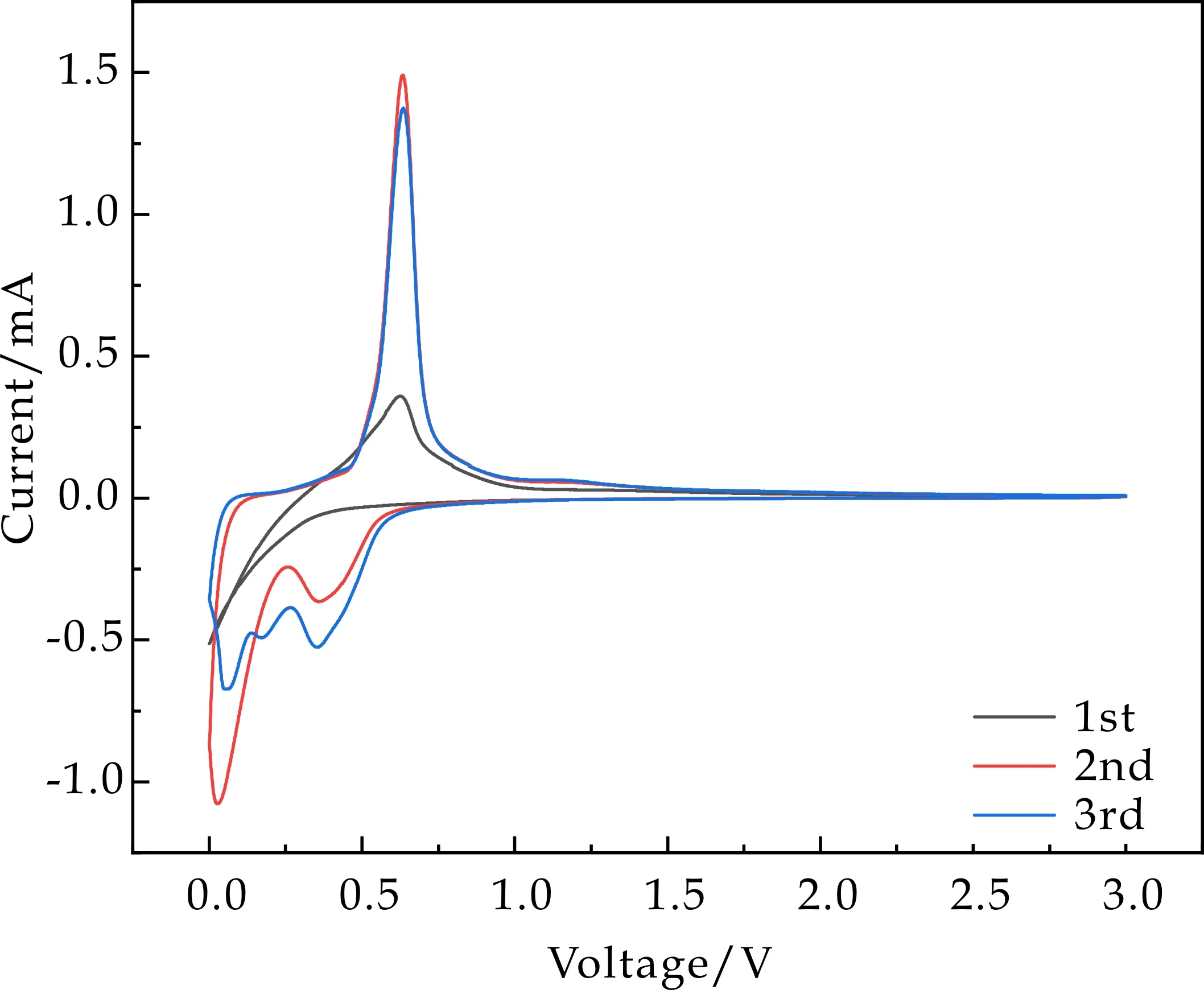
(b)Ge/CN-2复合电极的CV曲线图7 Ge和Ge/CN-2电极的CV曲线
图8展示的是Ge/CN-2电极材料循环3圈和100圈后,在频率范围:100 KHz~0.01 Hz内测试的阻抗谱图(EIS),主要目的是表征循环后的电池材料参与电化学反应的阻值.图8清晰地反映出,EIS曲线由两部分组成,一是低频区斜线,二是高频区半圆,半圆对应SEI膜电阻和电荷转移阻抗,斜线与锂离子在电极中的扩散行为有关.由图8可知,循环100圈后的半圆区直径明显大于循环3圈的半圆,因为Ge/CN-2电极在充放电过程中不可避免有体积膨胀,导致结构遭到一定程度的损坏,离子和电子迁移也因此受到影响,因此,循环100圈后的电荷转移阻抗增加.
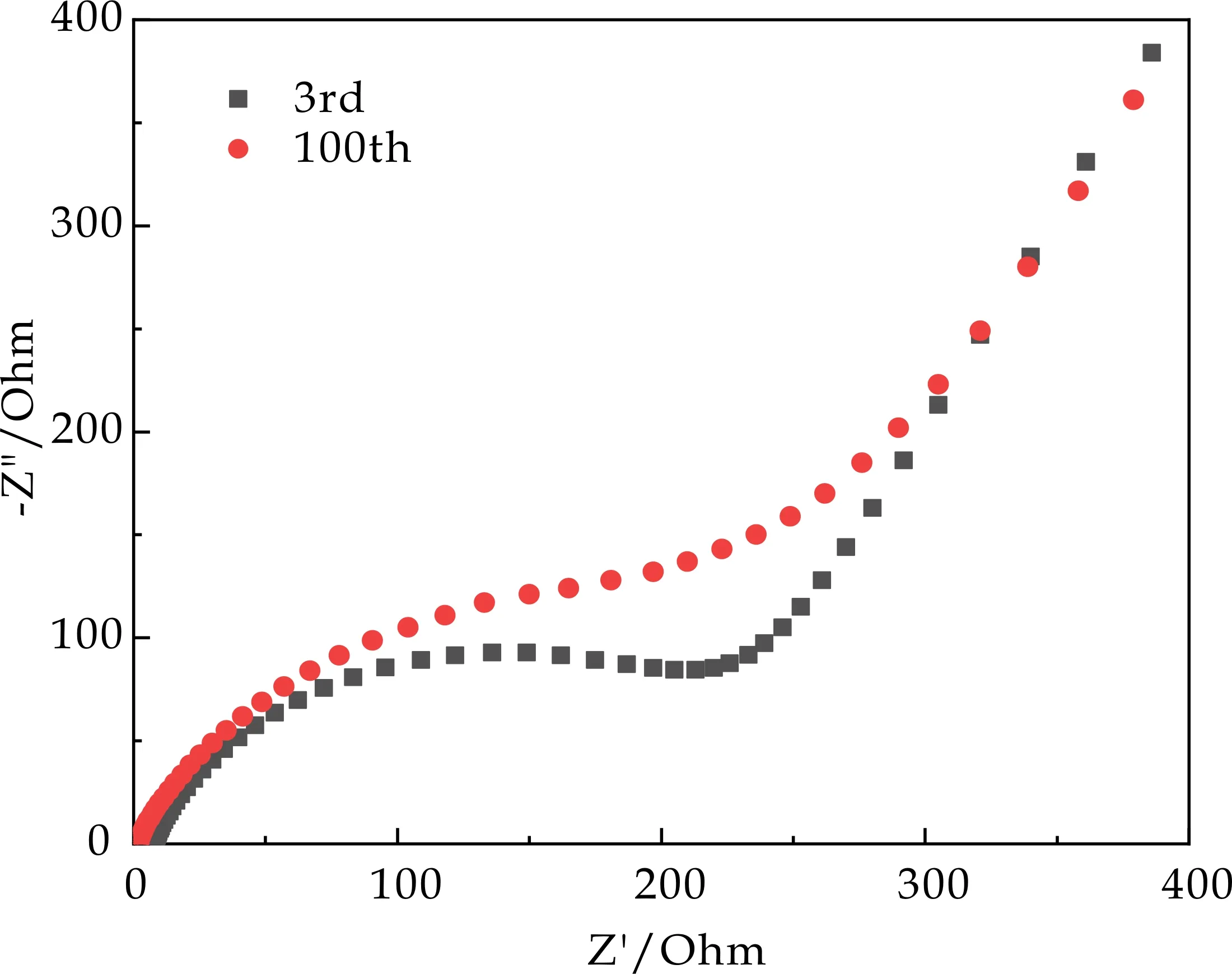
图8 Ge/CN-2电极分别循环3圈和100圈后的EIS曲线
3 结论
本文以三聚氰胺和氧化锗作原料,通过简单工艺制备了Ge/CN复合材料.研究发现,水热温度在180 ℃时,Ge/CN复合材料具有较明显的层级结构和孔隙结构.对比电化学测试发现,与纯Ge电极相比,Ge/CN-2电极拥有更好的性能.在0.1 A/g电流密度下,Ge/CN-2电极初始容量高达1 275.7 mAh/g.循环100圈后可逆容量维持在684.2 mAh/g,电化学性能良好.通过分析发现,与其他三个电极相比,Ge/CN-2电极拥有明显的层级结构且丰富的孔隙提供了活性位点和离子传输通道,能将离子扩散及电荷传输提速,进而提高反应动力学.

