老年吸入性肺炎的危险因素分析及风险预测模型构建
谢 恋 卢慧英 王瑞瑜 马 为 赵 俊 唐带君
广州市第一人民医院,华南理工大学附属第二医院( 广州 510180)
吸入性肺炎是指吸入食物、口咽分泌物、胃内容物及其他液体或固体物质引起的肺部化学性或合并细菌性炎症[1],这使吸入性肺炎具有发病隐匿且不易与其他肺炎区别的特点,因而吸入性肺炎对老年人的健康有很大的负面影响。随着我国人口老龄化逐步加快和地区医疗条件差异,老年吸入性肺炎的发病率和死亡率仍在上升[2]。为降低老年吸入性肺炎的发生率,改善老年吸入性肺炎患者的预后,本研究旨在通过临床观察对比老年吸入性肺炎与非吸入性肺炎患者的差异性临床指标,探讨影响老年吸入性肺炎的危险因素,构建风险预测模型。
1 资料与方法
1.1 研究对象
采用方便抽样法,抽取 2017年8月28日—2020年 10月30日在广州市第一人民医院老年病科住院治疗的205例老年肺炎患者作为研究对象。其中男性患者164例,女性患者41例,年龄范围为65~105岁,平均年龄(85.80±7.44)岁。依据吸入性肺炎的诊断标准,筛选出老年吸入性肺炎患者104例,归为吸入性肺炎组;老年非吸入性肺炎患者101例,归为非吸入性肺炎组。2组在性别及年龄上的差异无统计学意义(P>0.05),见表1。

表1 吸入性肺炎组与非吸入性肺炎组的一般资料比较
纳入标准:①年龄≥65岁;②符合《中国成人社区获得性肺炎诊断和治疗指南》或《医院获得性肺炎诊断和治疗指南》中的肺炎诊断标准;③吸入性肺炎的入选标准:存在与误吸相关(有明显误吸史;进食呛咳或呕吐后呛咳或痰中混有食物残渣;存在误吸的高危因素,如有吞咽功能障碍、食管癌、食道松弛症、脑卒中、长期卧床、鼻饲致胃食管反流等情况)的肺炎;④知情并同意参加者。
排除标准:①肺结核、肺部恶性肿瘤、服用免疫抑制剂或有严重免疫缺陷的患者;②严重肝肾功能不全的患者;③在研究开始前2个月内参加了其它临床研究。
1.2 研究方法
1.2.1 问卷调查法 通过查阅文献及专家咨询,设计病例报告表收集病人资料。该表已通过广州市第一人民医院伦理委员会审查(伦理批件号:K-2020- 623-01)。具体内容包括:(1)患者的一般资料:性别、年龄、生命体征、基础疾病(慢阻肺、哮喘、支气管扩张、脑梗塞、肺癌、高血压、冠心病、糖尿病、帕金森和痴呆)、预后情况。(2)患者的临床特征:意识障碍、吞咽功能障碍、胃食管反流、镇静药、气管插管、留置胃管、胃排空延迟、口腔不洁、高龄、长期卧床、吸烟史。其中,意识障碍评估的方法为格拉斯哥昏迷评分法;吞咽功能障碍的评估方法为洼田饮水试验。

2 结 果
2.1 老年吸入性肺炎预后分析
本研究中,吸入性肺炎组经治疗后好转率低于非吸入性肺炎组(P<0.05)。吸入性肺炎组复发率占42.31%,死亡率占18.27%,均高于非吸入性肺炎组(P<0.05),见表2。
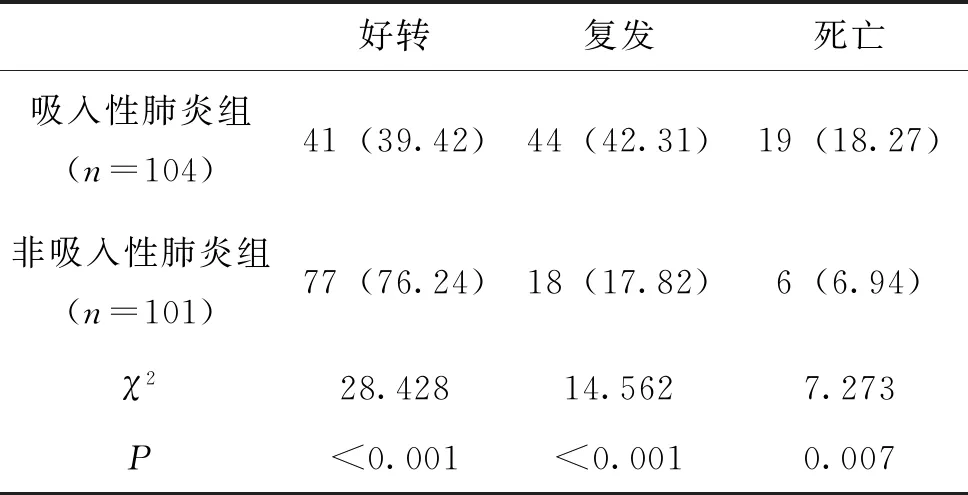
表2 吸入性肺炎组与非吸入性肺炎组的预后比较例(%)
2.2 老年吸入性肺炎的单因素分析
见表3,吸入性肺炎组与非吸入性肺炎组在慢阻肺、脑梗塞、帕金森和痴呆上的比较差异有统计学意义(P<0.05)。

表3 吸入性肺炎组与非吸入性肺炎组的基础疾病比较
由本研究结果可知,意识障碍、吞咽功能障碍、胃食管反流、留置胃管、胃排空延迟、长期卧床与老年吸入性肺炎的发生相关,差异有统计学意义(P<0.05),见表4。

表4 吸入性肺炎组与非吸入性肺炎组的临床特征比较
2.3 老年吸入性肺炎的多因素Logistic回归分析及风险预测模型建立
为进一步明确相关因素对老年吸入性肺炎的作用,以是否发生吸入性肺炎作为因变量,单因素分析结果中有统计学意义的变量作为自变量,进行Logistic回归分析,变量赋值方式见表5。最终筛选出脑梗塞、帕金森、留置胃管、长期卧床为老年吸入性肺炎的独立危险因素,结果见表6。由Logistic回归分析结果可得模型方程:Logit(P)=-2.952+1.221X2+2.417X3+2.388X8+1.683X10。经Hosmer-Lemeshow拟合优度检验风险预测模型的拟合效果,得P=0.926,即模型中老年吸入性肺炎预测值与实际值无明显差异。
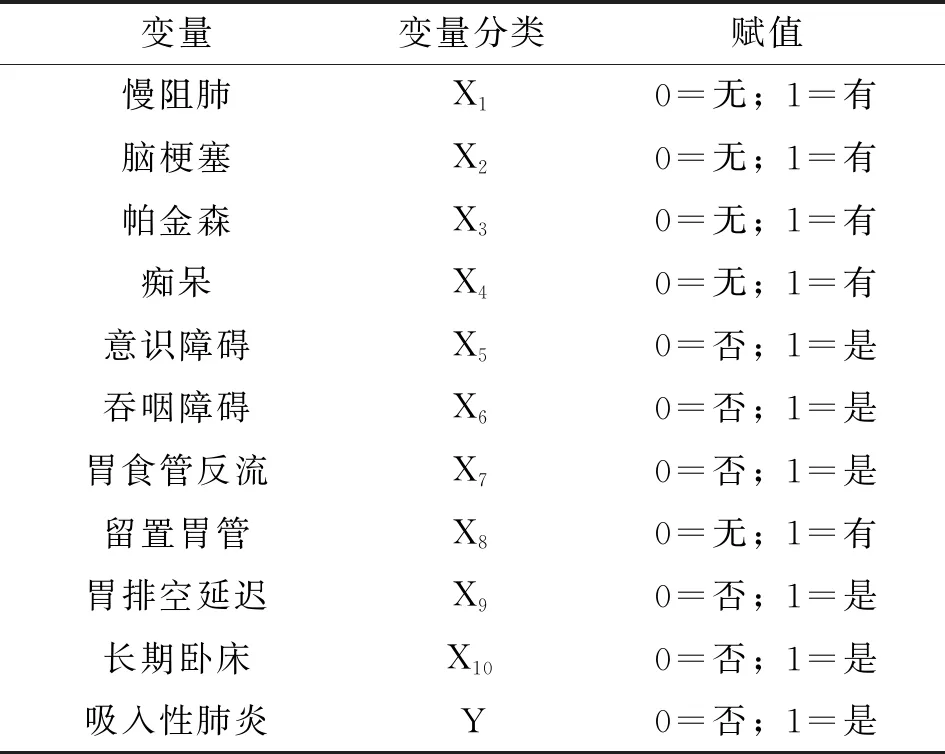
表5 变量赋值情况
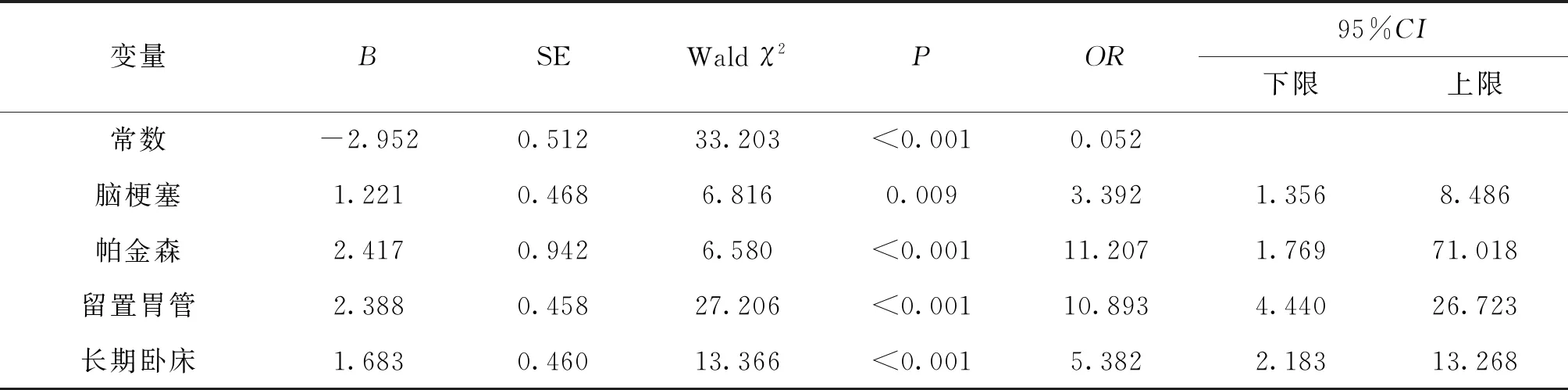
表6 老年患者发生吸入性肺炎的多因素Logistic回归分析
2.4 ROC曲线对老年吸入性肺炎风险预测模型的预测效果分析
根据前述Logistic回归方程可得本研究中老年患者发生吸入性肺炎的概率预测值,绘制ROC曲线,见图1。经计算得出约登指数为0.636,此时ROC曲线下面积为0.894,灵敏度为0.913,特异度为0.723。
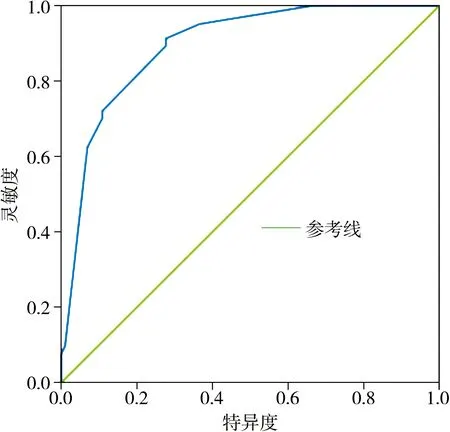
图1 预测老年患者发生吸入性肺炎的ROC曲线
3 讨 论
3.1 老年吸入性肺炎危险因素分析
随着年龄的增长,老年患者存在咳嗽反射不敏感、气道清洁能力减弱、由肌肉萎缩及结缔组织弹性的下降所致的吞咽强度及活动范围缩小等生理机能退行性改变,误吸风险明显增加,极易引发吸入性肺炎。本研究发现,患有吸入性肺炎的老年患者,复发率、死亡率均高于未患吸入性肺炎的老年患者。老年人免疫力下降,常合并一种或多种基础疾病,因而一旦出现吸入性肺炎易预后不良。
脑梗塞因脑部血液供应障碍使脑组织缺血、缺氧,出现不同程度的缺血性坏死或软化,加之患者患病后免疫功能降低,极易并发其他疾病。Kalra等[3]在其研究中报道,约有15%的脑梗塞患者合并吸入性肺炎。本研究结果显示,脑梗塞是老年吸入性肺炎的独立危险因素。研究表明,45%~65%的脑梗塞患者由于意识障碍、延髓性麻痹或咽部感觉神经损伤等因素出现吞咽困难[4]。正常的吞咽功能是避免发生误吸的重要保障。有吞咽困难的老年患者进食后可出现部分食物残留在口腔或咽部的情况,存在随时流入气管发生误吸的可能,引起吸入性肺炎。除此以外,老年脑梗塞患者常伴有意识障碍、留置胃管、长期卧床等吸入性肺炎的影响因素,增大了吸入性肺炎的发生风险。
吸入性肺炎是帕金森患者的主要死亡原因之一,而大部分帕金森患者都伴有不同程度的吞咽功能障碍[6]。目前帕金森病引起的吞咽困难病理生理机制尚未明确,可能与多种神经发生病理改变有关[8]。这一病变增加了误吸风险。此外,帕金森病还可能出现神经精神症状,包括轻度认知障碍和痴呆[9]。吞咽是最复杂的躯体反射之一,其生理过程包括认知期、口腔准备期、口腔期、咽期及食管期。当老年帕金森患者出现认知障碍时,其记忆力、定向力、精神行为异常甚至丧失生活自理能力均会影响吞咽过程的各个阶段,进而发生进食困难或呛咳,引发吸入性肺炎。
许多老年患者因吞咽困难或营养不足需要留置胃管。现有的研究证据表明,留置胃管并不能直接预防吸入性肺炎,反而容易增加感染吸入性肺炎的风险[10]。朱兆凤等[12]的研究结果指出,经鼻胃管进食的患者误吸率为61.11%,因误吸引发吸入性肺炎的患者高达38.89%。本研究结果也显示,留置胃管是吸入性肺炎的危险因素。对此可能的原因有以下两方面:其一,长期留置胃管会减弱吞咽反射,对咽部产生一定的刺激性,严重者可有咽部环状括约肌受损。此外,管径较粗的鼻胃管还可导致贲门关闭不全,出现胃食管反流、误吸的症状[13]。其二,传统方法按耳垂至鼻尖至剑突的长度插入胃管,约为55 cm。结合人体解剖学分析,胃管顶端仅至贲门下,且胃管侧孔并未完全进入胃内。因而在进行鼻饲时,营养液易从胃管侧孔溢出反流误吸,发生吸入性肺炎。
本研究还发现长期卧床是吸入性肺炎的独立危险因素。长期卧床的老年患者胃肠蠕动功能减弱,胃潴留情况增加,抗反流防御机制减弱,加之平卧位时气道处于开放状态,因而极易发生食物反流至气管,误吸入肺[14]。此外,长期卧床的老年患者碍于体位限制,痰液及分泌物不易咳出体外而发生呛咳,诱发吸入性肺炎。
3.2 老年吸入性肺炎风险预测模型构建意义
在老年肺炎住院患者中,吸入性肺炎发生率约占80%[15]。我国人口老龄化问题日益严峻,老年吸入性肺炎的患病率随之增加,这都将造成患者病程延长、再入院风险高、经济负担增加、治疗护理难度增大、社会资源利用率降低等影响。因此,如何预防老年患者发生吸入性肺炎具有重要意义。本研究中构建的老年吸入性肺炎风险预测模型将危险因素及各因素对吸入性肺炎的作用大小通过Logistic回归方程展示,有助于医护人员在老年患者入院时就对其是否存在吸入性肺炎风险、危险程度如何均有良好预判,并可于入院后依据现存的危险因素对其采取相应的预防措施,例如长期卧床的老年患者进食时应抬高床头[16],对需留置胃管的患者实行科学的鼻饲管理,注重老年脑梗塞、帕金森患者的吞咽功能评估等[17]。
本研究通过单因素及多因素Logistic回归分析发现脑梗塞、帕金森、留置胃管和长期卧床是老年吸入性肺炎的4个独立危险因素,并构建老年吸入性肺炎风险预测模型。该模型具有良好的预测能力,为临床工作提供有效的科学指导,对尽早采取干预措施、预防老年患者发生吸入性肺炎具有重要意义。

