亲缘HLA单倍体相合高剂量外周血造血干细胞移植后aGVHD与生物标志物表达的关系
徐建丽,袁海龙,王洪波,陈 刚,杨蕊雪,古力巴旦木·艾则孜,曲建华,江 明
(1新疆医科大学第一附属医院血液病中心,2新疆维吾尔自治区血液病研究所,乌鲁木齐 830054)
单倍体造血干细胞移植(Haplo-HSCT)因为其供者易获得性,被全世界接受并成为目前异基因造血干细胞移植的主流选择。与全相合造血干细胞移植相比,Haplo-HSCT 通常具有更强的移植物抗白血病(graft versus leukemia,GVL)效应,然而急性移植物抗宿主病(acute graft versus host disease,aGVHD)的发生率及植入失败率高于全相合移植[1-2],影响移植效果。aGVHD 关键在于宿主T 细胞的活化和功能异常,在一定程度上是由于人类白细胞抗原(HLA)不合造成,同时大量的细胞因子也参与aGVHD 的发生。因此,寻找能够及时诊断疾病,甚至在出现临床表现之前预测aGVHD的临床指标至关重要。
本研究自2002年设计并逐步完善了亲缘间HLA单倍体相合非体外去T 细胞高剂量外周血造血干细胞移植(related HLA-haploidentical non T cell-depleted in vitro high dose peripheral blood hematopoietic stem cell transplantation,Haplo-HDPSCT)模式,取得了较好的临床疗效[3-5]。本文收集了2004 年1 月-2017年12 月新疆医科大学第一附属医院血液科收治的154 例患者,回顾性分析移植后血清PD-L1、PD-1 水平,以探讨是否对Haplo-HDPSCT 患者发生aGVHD具有预测价值。
1 资料与方法
1.1 研究对象选取2004年1月-2017年12月在新疆医科大学第一附属医院行亲缘间HLA 单倍体相合非体外去T 细胞高剂量外周血造血干细胞移植(Haplo-HDPSCT)治疗的154 例患者,分析截止到2019 年6月的aGVHD 发病率、发生部位,以及发生aGVHD 后血清PD-L1、PD-1 水平。患者主要临床特征见表1。这项研究符合赫尔辛基宣言规定,并得到医院伦理委员会批准。所有移植受者均签署书面知情同意。

表1 亲缘HLA单倍体相合异基因外周血造血干细胞移植患者的临床特征
1.2 预处理方案201 例患者采用Ara-c+Bu/Cy 方案:阿糖胞苷(Ara-c)2~4 g/m2静脉滴注(-9 d~-8 d);白消安(Bu)4 mg·kg-1·d-1,分4 次口服,或3.2 mg·kg-1·d-1,分4 次静脉滴注(-7 d~-5 d);环磷酰胺(Cy)1.8 mg·m-2·d-1静脉滴注(-3 d~-2 d);4例受者用TBI/Cy 方案:全身照射(TBI)为单次照射,除1 例为9 Gy(-1 d),其余3 例剂量均为8.5 Gy,Cy 用法同上;2~3个位点不合者均应用兔抗人胸腺免疫球蛋白(rATG)2.5 mg·kg-1·d-1静脉滴注(-4 d~-1 d),1 个位点不合者则不用rATG。
1.3 干细胞的动员、采集应用粒细胞集落刺激因子(G-CSF)对供者进行外周血造血干细胞(PBSC)动员,剂量为7~10 μg·kg-1·d-1,于动员后第5和第6天用血液细胞分离机进行PBSC单采,如果供者体重明显低于受者体重,则在动员后第4天开始采集,共采集3 d已达到预期的PBSC数量。设定输注的采集物中有核细胞计数(MNC)≥12×108/kg或CD34+细胞≥6×106/kg。
1.4 GVHD 预防与治疗患者均予以的环孢素A(CsA)/他克莫司(Tac)+短程甲氨蝶呤(MTX)+吗替麦考酚酯(MMF)+糖皮质激素(GC)作为基础方案:起始量CsA 2.5 mg·kg-1·d-1静滴或Tac 0.02 mg·kg-1·d-1静滴,根据血药浓度进行剂量调整;MMF 1 000 mg/d分两次口服(-2 d~+100 d);MTX 15 mg/m2静滴(+1 d),10 mg/m2(+3 d,+6 d,+11 d),地塞米松3 mg·m-2·d-1静滴(+1 d~+30 d,分两次),白细胞恢复后改为强的松口服逐渐减量直至停用;2~3个抗原不合者常规加用抗CD25单克隆抗体20 mg/d静滴(01 d,+2 d)。aGVHD的诊断分度和器官分级标准参考Glucksberg等西雅图标准[6]。
1.5 血清中生物标志物的水平检测检测移植后30 d、60 d、90 d 采集患者外周血,血清样本采集后冻存于-80℃冰箱中,按照CBA 试剂盒说明检测血清中PD-L1、PD-1水平。
1.6 统计学处理应用SPSS23.0 软件进行统计分析,计算患者aGVHD 累积发生率、总生存率(OS)、无病生存率(DFS),采用Kapalan-Meier法绘制生存曲线,计量资料以均数±标准差()表示,通过受试者工作特征(ROC)评价生物标志物的诊断价值,以P<0.05为差异有统计学意义。
2 结果
2.1 移植后造血重建情况及生存情况154 例患者中除1例患者植入失败,其余患者均植入成功。所有患者连续3 d 检测中性粒细胞≥0.5×109/L 的中位时间为13 d(8~25 d);血小板≥20×109/L的中位时间为16 d(8~31 d);3 年的DFS 和OS 率分别为(64.62±3.93)%、(66.41±3.79)%。
2.2 aGVHD 的发生情况发生aGVHD 患者共94例,中位发生时间为45 d(6~95 d),其中发生I 度aGVHD 患者45例,Ⅱ~Ⅳ度aGVHD 患者49例,Ⅲ~Ⅳ度aGVHD 患者14 例。I~IV 度aGVHD 累积发生率为(61.04±3.92)%,其中II~IV 度aGVHD 累积发生率为(37.69±4.50)%,III~IV 度aGVHD发生率为(11.69±3.05)%,见图1。发生aGVHD94例患者中皮肤型aGVHD有66例,肠道型aGVHD有15例,肝脏型aGVHD有13 例。皮肤型aGVHD累积发生率为(48.51±4.36)%,肠道型aGVHD累积发生率为(16.09±3.49)%,肝脏aGVHD累积发生率为(14.47±3.05)%,见图2。
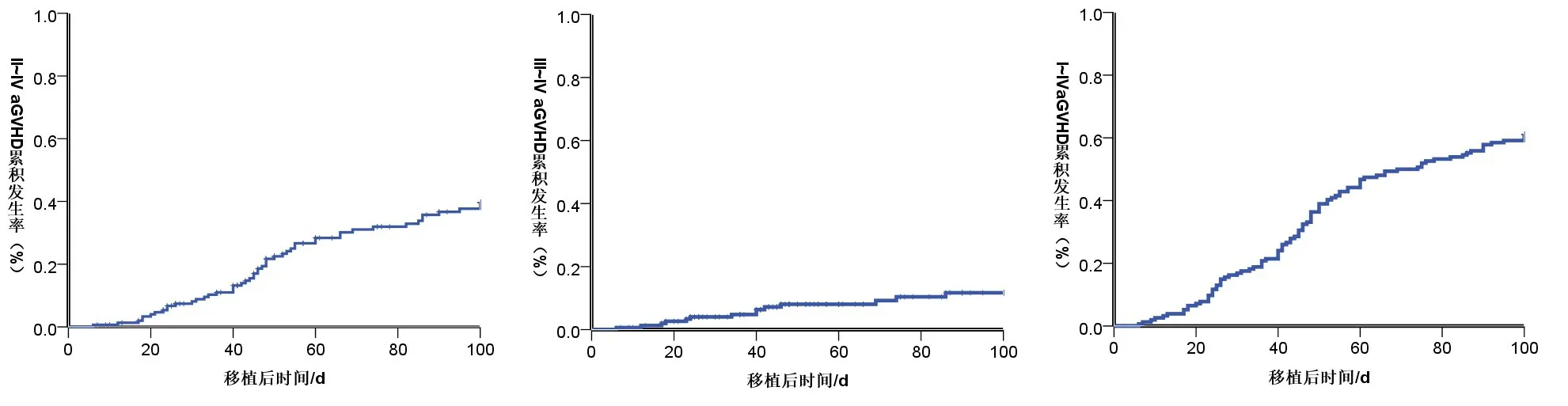
图1 移植后aGVHD的发生情况
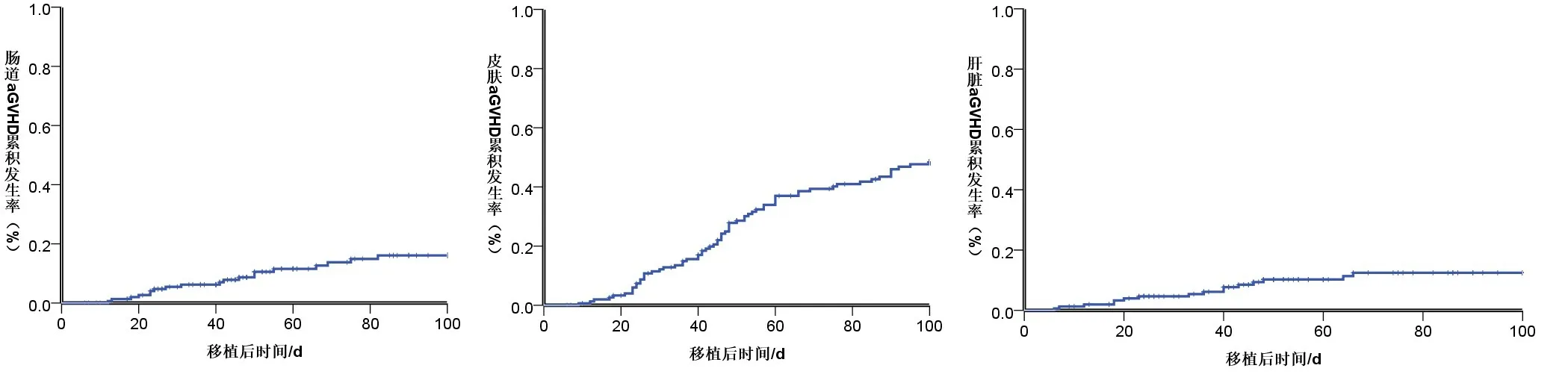
图2 移植后不同受累部位aGVHD发生情况
2.3 PD-1、PD-L1 水平与aGVHD 关系总共收集了68 例患者的血清样本,26 例患者发生aGVHD,其中4 例患者发生III~IV 级aGVHD。回顾性检测所有患者移植后30 d、60 d、90 d 的PD-L1、PD-1 血清水平,PD-L1 水平在发生aGVHD 及未发生aGVHD 患者中的差异无统计学意义。aGVHD 患者移植后30 d的PD-1 平均水平为(96.40±13.00) pg/mL,无aGVHD 患者的血清水平为(46.77±9.61)pg/mL,差异有统计学意义,见表2。此外,移植后60dPD-1血清水平在未发生aGVHD 与I~II 级aGVHD 患者中无明显差别,但III~IV级aGVHD患者的PD-1水平明显高于无aGVHD患者,差异有统计学意义,见表3。aGVHD 与未发生aGVHD 患者比较,PD-1 的曲线下面积(AUC)在移植后30 d 和移植后60 d 为0.857(P=0.048)和0.750(P=0.033),表明PD-1 血清水平可以用来预测aGVHD,见图3。
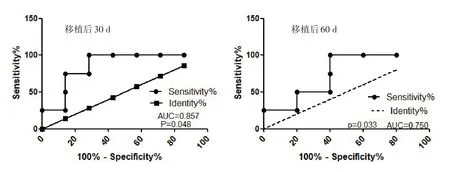
图3 血清PD-1水平预测aGVHD发生的ROC曲线图
表2 aGVHD发生后PD-1、PD-L1动态变化(pg/mL,)
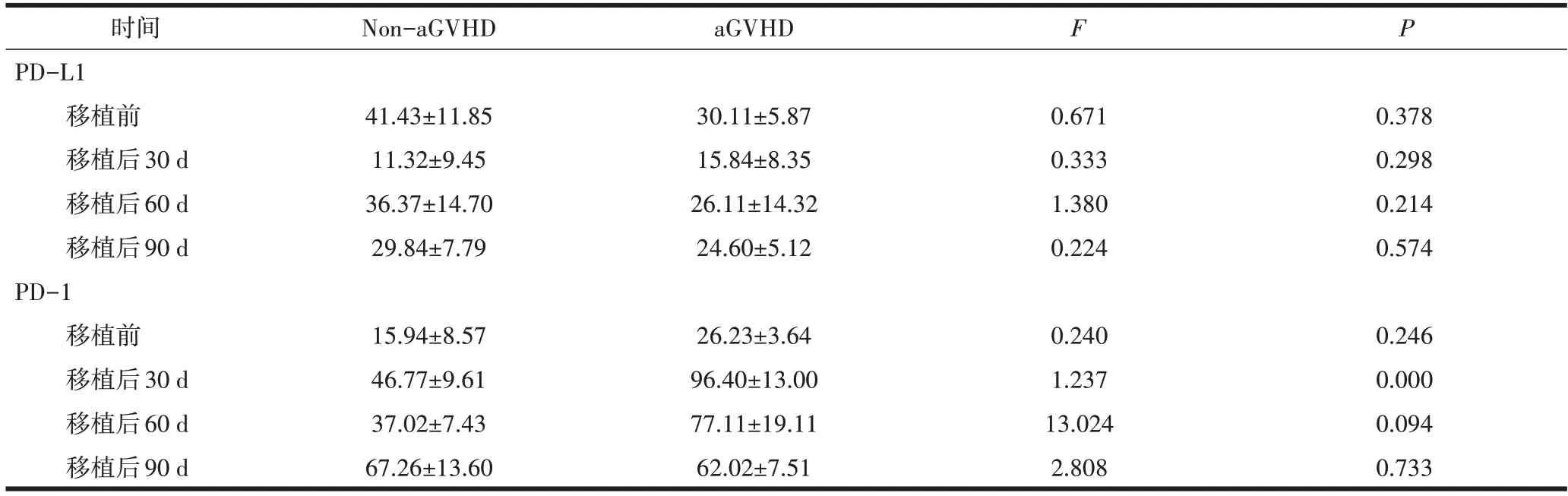
表2 aGVHD发生后PD-1、PD-L1动态变化(pg/mL,)
表3 分层分析发生aGVHD患者PD-1变化(pg/mL,)
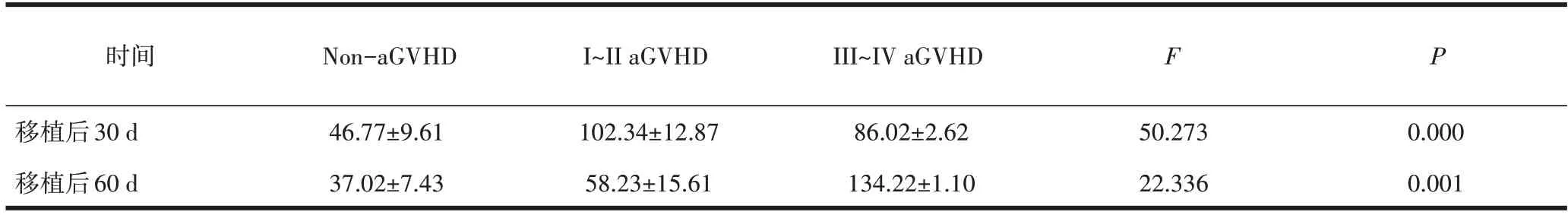
表3 分层分析发生aGVHD患者PD-1变化(pg/mL,)
3 讨论
单倍体相合外周血造血干细胞移植(Haplo-PBSCT)近年来得到了迅速的发展,GVHD 及植入失败仍是影响疗效的关键问题。新疆医科大学第一附属医院血液病中心独特的亲缘间HLA 单倍体相合非体外去T 细胞高剂量外周血造血干细胞移植(Haplo-HDPSCT)模式:(1)输注粒细胞集落刺激因子(G-CSF)动员高剂量供者非体外去T 细胞外周血造血干细胞;(2)2~3 个位点不合者采用TBI/Cy 或Ara-c+Bu/Cy+ATG,而1 个位点不合者不加ATG 作为清髓性预处理方案;(3)2~3个位点不合者采用CsA/Tac+短程MTX+MMF+抗CD25 单克隆抗体+GC 作为加强的GVHD 预防方案,而1 个位点不合者则不常规加用抗CD25 单克隆抗体作为GVHD 预防方案;(4)应用加强的细菌、真菌和病毒等感染防控措施,取得了较好的临床疗效,植入率好,重度aGVHD发生率不高。本研究的移植模式中使用高剂量的外周血造血干细胞作为移植物可以克服移植排斥导致的植入失败[7],但因含有大量供者T 淋巴细胞,从而也会增加aGVHD 发生率,而使用ATG 可以克服HLA 不合,使体内T 细胞耗竭。常规应用二次巴利昔单抗及短程的激素,有明确的抗GVHD 作用,并且可以持续较长的时间,方案中GCSF 也可以促进T 细胞向Th2 型转化,一定程度上降低aGVHD 的发生率。本研究中,虽然总的aGVHD 的累计发生率略高,为(61.04±3.92)%,但Ⅲ~Ⅳ度aGVHD 的累计发生率不高,且以皮肤型aGVHD 为主,临床上易于治疗,并发症少,表明此种移植模式是可行的。
由于GVHD 仍然是移植后非复发死亡的主要死亡原因,因此寻找能够预测GVHD发生的生物标记物显得尤为重要。据报道,大量的血浆生物标记物可以以不同的准确度预测aGVHD,如致癌抑制因子2(ST2)、TNF-α和人再生胰岛衍生蛋白3α(REG3α)、IL-10、IL-9[8-15]。程序性死亡受体-1(PD-1)与程序性死亡受体-配体1(PD-L1)是共刺激分子B7 家族重要成员,在同种异体造血干细胞移植后维持免疫耐受中起着重要作用[16-17],它们作为一对负性共刺激分子,促进IL-10 分泌的Th2 型细胞分化,进而抑制Th1 型细胞,诱导Th1型细胞向Th2型细胞极化[23],从而降低移植后GVHD 的发生率[18]。Zhou 等[19]报道Haplo-HSCT的北京移植方案在移植后第7天PD-L1血清水平可预测III~IV 级aGVHD。几项小鼠模型研究表明,PD-1 及PD-L1 在移植物抗白血病(GVL)效应和GVHD 中起双重作用[20-22]。然而,由于众多研究者报道了不同的观点,这一问题仍然存在争议。在本研究中,PD-L1 水平在发生aGVHD 与未发生aGVHD 患者中的差异无统计学意义,PD-1 水平在移植后30 d发生aGVHD 患者高于未发生aGVHD 患者,发生aGVHD 与未发生aGVHD 患者在移植后60 d PD-1 水平差异无统计学意义,然而对发生aGVHD 患者进行分层分析,结果显示III~IV 级aGVHD 患者在移植后60 d时血清PD-1水平高于未发生aGVHD 患者,提示移植后PD-1血清水平可预测aGVHD的发生。
本研究所采用的Haplo-HDPSCT 模式,重度aGVHD 发生率较低,以皮肤型aGVHD 为主,OS 率及DFS 率较高,证明该移植模式治疗恶性血液病有效、安全、可行,移植后PD-1 水平的升高对预测早期临床aGVHD可提供帮助。

