骨科手术中自体血回输的临床效果
王文秀,段声吉,杨晓茂,张 丽,梁永涛,廖常莉,周述芝
1.川北医学院麻醉学系(南充 637000);2.雅安市人民医院骨科(雅安 625000);3.雅安市人民医院麻醉科(雅安 625000);4.西南医科大学 麻醉学系(泸州 646000)
目前脊柱、骨折、关节置换等骨科手术日益增多,在手术分离组织、暴露术野的过程中常常会导致出血量增大,术中快速失血可能引起患者血压、脉搏等生命体征不稳定,需要进行输血治疗[1]。术中大量输注异体血可能会导致溶血反应、急性输血相关肺损伤、传播艾滋病、肝炎等输血相关不良反应发生,同时也会加重血源紧张、增加患者住院费用[2]。近年来,随着自体血输注(autologous blood transfusion,ABT)技术的进步,除了输入异体血外,ABT也是抢救生命的有效措施,并逐渐被应用于临床各个领域[3]。自体输血可通过减少大手术中的同种异体输血量来预防输血相关并发症的发生,也可以节约血液成本,缓解临床用血紧张的问题,带来一定临床和经济效益,特别是在一些大出血的危重患者中[4-5]。目前广泛应用的自体血液回输技术,是利用负压吸引将手术野失血及浸血纱布血回收,再经过离心洗涤处理,将激活的血浆蛋白成分、血小板、游离血红蛋白、肝素、组织碎屑等去除,最后制成红细胞的生理盐水悬浮液[6]。回输这种红细胞是否会对患者自身凝血功能产生影响,一直备受临床所关注。本文回顾性分析近年骨科手术中63 例自体血回输患者的临床资料,比较其术前、术后相关临床指标变化,以探讨自体血液回输在骨科手术中的应用效果。
1 资料与方法
1.1 一般资料
本研究选取2019 年1 月至2020 年12 月于雅安市人民医院行骨科手术并使用血液回输的患者63例,美国麻醉医师学会(American Society of Anesthesiologists,ASA)分级为Ⅱ~Ⅲ级,年龄33~66 岁,男性34 例,女性29 例,其中行脊柱骨折内固定术16 例,椎管扩大减压术18 例,腰椎滑脱内固定术15 例,股骨骨折内固定术8 例,髋关节置换术6 例。本研究通过雅安市人民医院伦理委员会批准,患者均知情同意。使用自体血回输的条件为:手术出血400 mL 以上;术前血红蛋白(Hb)>90g/L,血细胞比容(Hct)>30%;血小板功能及凝血指标正常;术前未合并恶性肿瘤、感染者。
1.2 自体血回收方法
术前常规禁食禁饮,入室后建立静脉通路,常规监测生命体征,术中采用气管插管静吸复合全身麻醉。使用北京京精3000 P 型自体血液回收机:采用100~150 mmHg负压吸引及收集术野失血,将肝素钠25 000 u加入500 mL 0.9%氯化钠注射液中制作成抗凝剂,血液回收前先将250 mL抗凝剂预充管道,抗凝剂的流速根据术中出血速度调整。当血液收集达500 mL即开始进入回收罐清洗,经过滤、洗涤、离心、净化,每罐可得到浓缩洗涤红细胞250 mL,收集血液于手术结束前回输。
1.3 观察指标
统计患者术中出血量、输血情况;术前、术后1 d患者血浆凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT)以及纤维蛋白原(fibrinogen,FIB);白细胞(white blood cell,WBC)计数、血小板(platelet,PLT)计数、红细胞压积(hematocrit,Hct)、血红蛋白(hemoglo⁃bin,Hb);血钾、血乳酸水平变化;记录患者输血时、术后1 d 至术后7 d 输血不良反应发生情况(凝血功能障碍、溶血反应、脂肪栓塞及肝肾功能损伤等)。
1.4 统计学分析
采用SPSS 21.0统计学软件,计量资料以均数±标准差()表示,采用配对t检验比较,P <0.05为差异有统计学意义。
2 结果
2.1 患者一般资料
本研究共纳入患者63 例,所有患者ASA 分级为Ⅱ~Ⅲ级,年龄为33~ 66(58.66 ± 12.91)岁,男性34例,女性29例,其中行脊柱骨折内固定术16例,椎管扩大减压术18 例,腰椎滑脱内固定术15 例,股骨骨折内固定术8例,髋关节置换术6例。
2.2 出血量及不良反应
患者术中出血量为400~ 1 500(621.76 ± 45.34)mL,输入自体血量为250~1 250(441.37±44.58)mL,无一例术中输入异体血。回输自体血过程中无一例发生皮疹、发热、过敏性休克等输血相关不良反应。术后7 d 内均未出现凝血功能障碍、溶血反应、脂肪栓塞及肝肾功能损伤等严重并发症。
2.3 血常规及电解质指标
患者术后1 d 的Hct、Hb 较术前下降,差异有统计学意义(P <0.05);术后1 d 血钾、血乳酸水平、PLT 水平与术前相比无明显变化,差异无统计学意义(P>0.05);术后WBC 计数较术前有所增加,差异有统计学意义(P <0.05),见表1。
表1 血常规及电解质指标比较()Table 1 Comparison of blood routine and electrolyte tests()
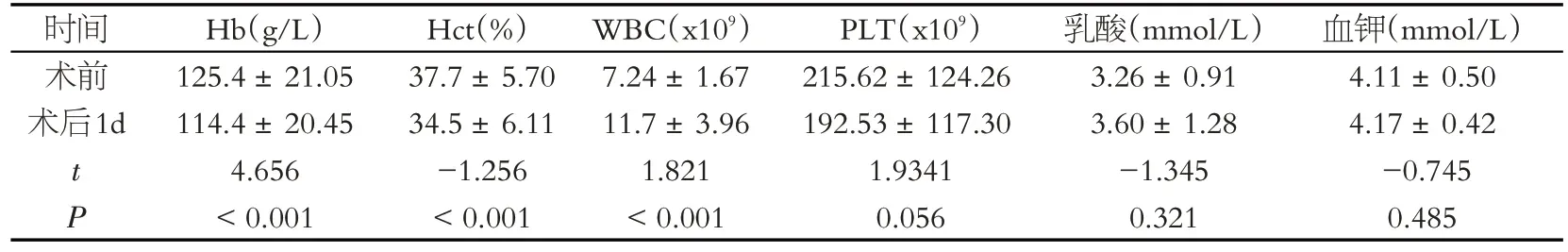
表1 血常规及电解质指标比较()Table 1 Comparison of blood routine and electrolyte tests()
2.4 凝血指标
与术前相比,患者术后1 d 血浆PT、APTT 较术前均有所上升,FIB较术前有所下降,但差异无统计学意义(P>0.05),见表2。
表2 凝血功能比较()Table 2 Comparisons of coagulation functions()
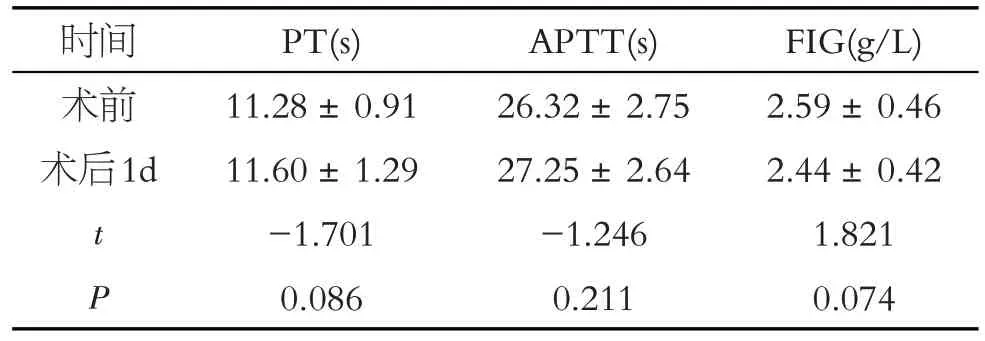
表2 凝血功能比较()Table 2 Comparisons of coagulation functions()
3 讨论
在骨科手术中,脊柱及股骨、髋关节等部位的手术往往渗血较多,随着手术复杂性及时间的增大,出血风险也随之增加,例如器械使用、多个脊柱节段(至少三个椎体水平)手术等因素往往导致术中大量出血[7]。但是输注大量同种异体血液制品可能带来输血错误、输血相关反应、传播输血相关传染性疾病等医疗问题[8]。随着加速康复外科(enhanced recovery after surgery,ERAS)理念的提出,微创手术的开展及选择合理的血液管理方法可以减少术中失血,而术中多模式、个体化血液管理方案以及血液回输技术的使用也可有效降低异体输血率及术后贫血发生率[9-11]。
本研究发现,患者术后1 d的Hct及Hb指标较术前有所下降,原因可能在于:①术野血液未完全回收,导致术中血液丢失[12];②部分血细胞在吸引、离心、过滤、洗涤过程中被破坏;③洗涤液稀释;④围术期间补充晶体、胶体液对血液成分有所稀释。与库存血液相比,回收血液中的红细胞没有储存,存在于机体外时间较短,其红细胞有两倍或更多的2,3-二磷酸甘油酸(2,3-bisphosphoglyceric acid,2,3-DPG)含量及完整变形能力,这些红细胞可能比库存血中的红细胞质量更高,对于术前患者一般状况可,患者机体内红细胞及血红蛋白数量在患者自身可代偿水平内时,术后稍低的血细胞水平不会导致机体器官、组织缺氧,无须额外输注血液制品[13-14]。本试验所有患者术后7 d 内未有额外输注异体血液成分者,进一步提示术后稍低的血细胞不会造成显著影响,不影响患者术后恢复。因此,自体血使用可以减少异体血制品的输注。
国外有研究表明:术中自体血回收的使用可以减少脊柱畸形手术患者约一个单位量的异体血输注[15]。同时,本研究表明患者在回输自体血时及术后7 d内均未发生输血反应、出凝血功能异常等不良反应,也证明自体血使用具有一定的安全性。但KELLY等[16]认为,手术中常规使用血液回收是有悖于成本效益的,可能在某些情况下并不会减少异体血输注量。据估计,只有在多个节段脊柱手术和预期失血超过500 mL时,自体血回收才具有成本效益。因此,在临床使用过程中,应严格把握自体血回收使用的适用证,对于一些手术创面大、止血相对困难、手术时间长、预计出血量大的患者来说,自体血回收是一项减少围术期输血、提高预后效果的必要措施[17-18]。
有学者认为,在自体血回输使用中,及在回收过程中,由于肝素钠的使用以及血小板、凝血因子、纤维蛋白等凝血成分的破坏,会影响患者术后的凝血功能。KAMURA 等[19]研究发现,由于手术本身因素及某些药物(如氨甲环酸)的影响,骨科患者术后较术前血液会呈现高凝状态。同时,自体血液回收过程中由于凝血相关因子及血小板破坏等因素影响,回输的血液会呈现低凝状态,正好可以逆转这种不良影响,因此,患者术后静脉血栓形成等不良并发症发生率将会有所下降。本研究发现,患者术后PT、APTT、FIB 较术前未有明显变化,提示自体血回输不会影响骨科病人凝血功能,本研究结果与宋江涛[20]、张理宾[21]以及陈姗[22]等的观点一致。本文凝血结果没有较大变化也可能与微创手术的开展,手术技术的改进,患者出血量不大、回收血量不多有关。当临床上出血及输入血量大时,也应该根据临床指标及患者临床表现指导输入其他血液成分,以保证患者围术期间安全[23-25]。本试验对于凝血功能指标只有常规凝血指标,用传统的实验室凝血检查结果来预测临床结局的准确率有限,常规凝血检测有时候不能反映机体凝血系统全貌[26]。目前,应用血栓弹力图(thromboelastogram,TEG)或快速血栓弹力图(rotation⁃al thromboelasto-metry,ROTEM)已被证明可以精准指导临床血液管理,减少术中出血,减少输血量及相关并发症及医疗保健费用[27-28]。因此可采用更准确的检测方法如TEG等。
4 结论
本研究结果显示,骨科手术患者术中应用自体血液回输未造成术后血常规、凝血常规等指标的明显改变,无不良反应发生,有很好的临床应用价值。
(利益冲突:无)

