听神经瘤的显微切除及对面神经保护的策略研究*
谢姗,邵志林2,姜之全,韩易,赵永轩,娄飞云
(1. 蚌埠医学院第一附属医院神经外科,安徽 蚌埠 233000;2. 蚌埠医学院第一附属医院急诊外科,安徽 蚌埠 233000)
听神经鞘瘤(acoustic neuroma,AN)是小脑桥脑角(cerebelopontine angle,CPA)的良性颅内占位性病变,约占颅内肿瘤的6%~8%,并超过所有小脑桥脑角肿瘤的80%[1]。听神经瘤的典型症状是由于压迫肿瘤周围邻近的颅神经引起的,可能表现为听力下降、耳鸣、头晕、面部麻木或无力。肿瘤体积越大,甚至可能导致脑干受压或引起脑积水。听神经瘤往往是单侧发病的,双侧发病通常与神经纤维瘤病2型有关[2]。目前对于听神经瘤的手术治疗方法,术中争取最大程度地切除肿瘤,同时面神经功能得到完整保留,使患者生活质量得到提高,是神经外科医师追求的最优手术效果。然而,在听神经瘤手术切除过程中,最大限度地做到面神经解剖及功能的保留仍然是手术的重点和难点[3]。 随着显微手术操作技术的进步及神经电生理监护技术的不断提高,完整切除听神经瘤、术中保护面神经功能的技术有了很大的改善[4]。因此,本研究通过对蚌埠医学院第一附属医院神经外科2018年5月—2020年5月收治的134例大型听神经瘤患者的临床资料进行回顾分析,以探讨听神经瘤显微手术操作技巧及术中神经电生理监测对于面神经功能保护的作用,现报告如下。
1 资料与方法
1.1一般资料 选择蚌埠医学院第一附属医院神经外科自2018年5月—2020年5月收治的134例听神经瘤患者,其中男性58例,女性76例,平均年龄(55.10±9.66)岁。肿瘤位于左侧者62例,位于右侧者72例,均为单侧发病病例。所有患者入院前均未予以任何治疗。两组一般资料对比差异无统计学意义(P>0.05),见表1。

表1 两组一般资料对比结果
1.2临床表现 ①耳蜗及前庭神经症状,听力下降89例,耳鸣10例,听力丧失25例,其中部分患者是耳鸣伴听力下降10例;②三叉神经功能障碍症状,面部麻木42例,三叉神经痛15例,面部感觉异常23 例;③面神经功能障碍症状,按照面神经功能状态House-Brackmann(H-B)分级[5]:Ⅰ~Ⅱ级 81例,Ⅲ~Ⅳ级35例,Ⅴ~Ⅵ级18例;④小脑及脑干功能受损症状,主要表现为共济失调 36例;⑤后组颅神经功能障碍症状,主要表现为声音嘶哑、吞咽困难、饮水呛咳者28例;⑥颅内压增高症状,主要表现为头痛、呕吐87例。
1.3影像学评估 所有患者术前均行头颅MRI检查,其中实性肿瘤107例,囊性肿瘤27例。根据Koos分级[6],即肿瘤大小与侵犯内听道及周围结构关系分为四级,1级:肿瘤直径≤1 cm,瘤体位于内听道内23例;2级:肿瘤直径≤2 cm,瘤体侵犯桥小脑角38例;3级:肿瘤直径≤3 cm,瘤体占据了桥小脑角池,不伴有脑干移位46例;4级:肿瘤直径>3 cm,伴有脑干移位27例。图1展示了右侧听神经瘤及左侧听神经瘤MRI增强图像。
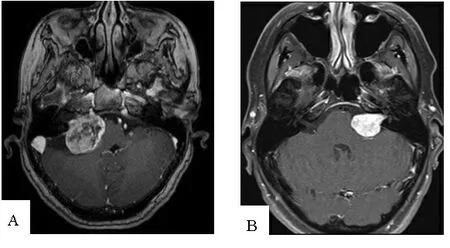
A为右侧听神经瘤,B为左侧听神经瘤。
1.4面神经功能评估 根据House-Brackmann分级[5],Ⅰ级42例,变现为各区面部运动正常;Ⅱ级39例,表现为轻度功能异常,仔细检查时有轻度的面肌无力,可有非常轻的联带运动;Ⅲ级20例,中度功能异常,表现为明显的面肌无力,但无面部变形,联带运动明显或伴面肌痉;Ⅳ级15例,中重度功能异常,表现为明显的面肌无力或面部变形;Ⅴ级10例,重度功能异常,表现为仅有几乎不能察觉的面部运动;Ⅵ级8例,变现为面部完全麻痹,无运动。分别观察术前1天、术后1周、术后3个月、术后1年两组患者面神经功能,院内直接观察患者面神经功能状态,出院后则采取门诊评估或者电话随访。
1.5手术情况 所有病例均采用显微镜下枕下乙状窦后入路切除肿瘤。全麻后,患者采取侧俯卧位,上半身抬高20°~30°,以降低静脉压,暴露星点位于最高点,头架固定。外耳发迹内侧约1 cm标记6~8 cm纵形切口,切开头皮后铣刀铣开骨窗大小约3~3.5 cm,充分显露横窦乙状窦交汇处。缓慢并充分释放小脑延髓池及枕大池蛛网膜下的脑脊液,脑组织充分塌陷后,切开硬膜,充分显露桥脑小脑角区。见肿瘤组织后,先用神经电生理监测刺激电极刺激肿瘤背侧,确认无可疑神经结构后再切开肿瘤的蛛网膜,先进行囊内切除。瘤体较大时,会使长期受压的面神经变得异常菲薄,需仔细辨别。待瘤内减压后,依次切除肿瘤上、下极,最后切除内侧近脑干部位的肿瘤。大多数情况下,肿瘤与脑干之间有较完整的蛛网膜间隙,仔细分离后绝大多数可以完全切除。切除内听道内肿瘤时,先用磨钻磨开内听道后壁,然后用剥离子将肿瘤小心剥离。切除肿瘤过程中,术中电生理监测持续应用,观察面神经是否受到牵拉,功能是否受损,配合术者在保护面神经的前提下,最大可能完整切除肿瘤。
1.6术中电生理监测技术应用 面神经功能监测采用美国Itake32导联神经监护仪,全麻后消毒电极置入点,将一次性使用针状电极分别插入面神经支配的患侧眼轮匝肌和口轮匝肌中,正负极间距1 cm,地线位于三角肌,进行连续自发肌电图间断电刺激诱发肌电图和连续自发肌电图监测。手术过程中对疑为面神经的组织以双极刺激器刺激探头刺激,刺激量在5 mA以内,由小到大,沿着神经走行由远及近准确定位。如神经收到牵拉或压迫及刺激时,监护仪都会发出报警声,并将异常波形实时显示在屏幕上,这样就能及时准确向术者反馈面神经波形信息,配合术者保留神经,提高肿瘤切除率。
2 结果
2.1术后两组肿瘤切除率及面神经解剖保留率比较
监测组与非监测组在肿瘤切除情况上两组差异无统计学意义(P>0.05),而监测组的面神经解剖保留情况明显优于非监测组,差异有统计学意义(P<0.05),见表2。
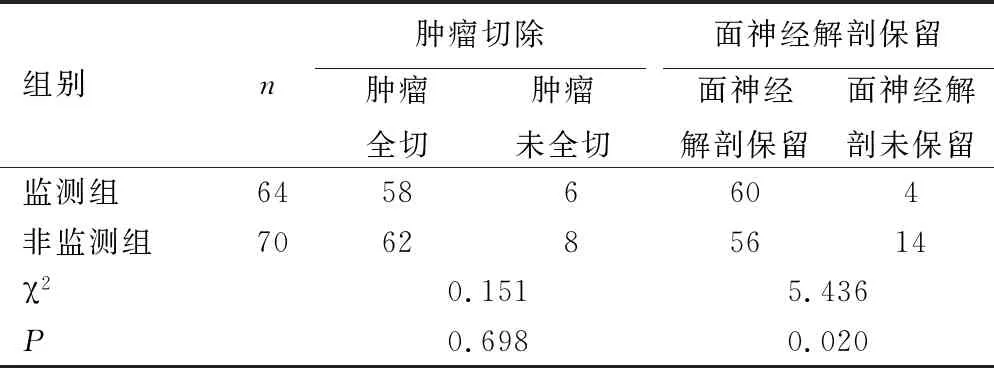
表2 术后两组肿瘤切除率及面神经保留率比较
2.2两组患者术前1天、术后1周、术后3个月、术后1年面神经功能比较 两组术前1天及术后1周面神经功能评估结果差异无统计学意义(P>0.05)。术后3个月、术后1年监测组面神经功能恢复情况明显优于非监测组,差异有统计学意义(P<0.05),见表3、表4。
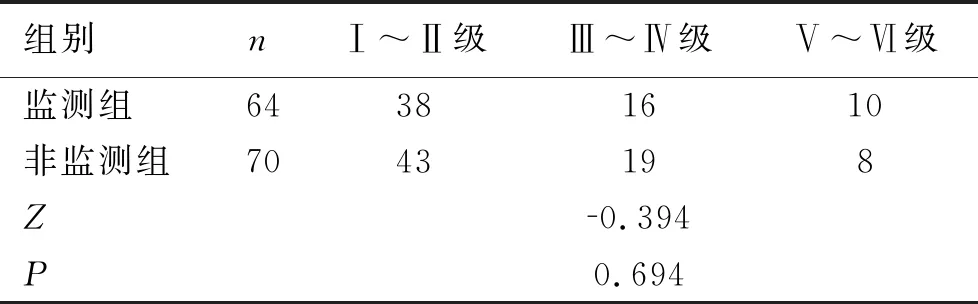
表3 术前1天两组面神经功能评估比较

表4 两组病人术后不同时间的面神经功能比较
3 讨论
听神经瘤是一种常见的颅内肿瘤,大多起源于前庭神经,瘤体所在部位为小脑脑桥角区[7]。随着肿瘤的生长,不仅会引起相应颅神经功能障碍,也可因瘤体挤压四脑室引起脑脊液循环通路不畅,从而引发相应的颅内压高的表现。同时肿瘤向内侧生长侵犯小脑和脑干,向外侧生长侵入内听道[8]。由于听神经瘤为良性肿瘤,首选的治疗方式便是手术切除[9]。但听神经瘤位置深在颅底与脑组织之间,术中显露肿瘤难度高;同时,瘤体位置与重要的神经血管结构毗邻,因此,在安全切除肿瘤的基础上,尽可能保留神经功能,是保证患者良好预后的重要原则[10]。为达到这一目标,神经外科医生需要选择合适的手术入路,不断提高术中显微操作技术,掌握肿瘤切除技巧,减少损伤,同时配合电生理监测为神经保护保驾护航。
3.1听神经瘤手术入路的选择 首先,对于手术入路的选择:听神经瘤的手术入路包括经乳突迷路入路、经中颅窝入路和枕下乙状窦后入路[11]。经乳突迷路入路通常基本是颅外入路,适用于直径<2.5 cm,无需顾及听力问题的肿瘤。术中早期可显露面神经,面神经保留率高,脑组织和后组颅神经损伤轻。但术中暴露范围有限,不宜于长入CPA池过多的肿瘤,手术时间相对长,术后易发生脑脊液漏,容易损伤听神经。颅中窝入路仅局限在内听道外侧较小的肿瘤,不易到后颅窝,面神经损伤率较高,但保留听力机会大。但如果肿瘤侵及岩骨,颅中窝入路则不适宜,因为需要对面神经进行更多的操作。乙状窦后入路适用于所有大小和位置的听神经瘤,特别是在切除直径>3 cm的肿瘤时应采用该入路。术中可根据需要显露乙状窦、横窦范围,有利于显露该区域内的重要血管及分支,同时手术视野好,面神经、耳蜗神经易于显露,有利于保留面听神经功能,此外,对脑干面的显露充分可减少相应风险[12-13]。因此,在听神经瘤手术中,本研究均采取乙状窦后入路切除肿瘤,为患者选择最佳的手术方式。
3.2听神经瘤的显微切除技巧 听神经瘤显微手术切除原则是首先予以瘤内切除,瘤体组织得到减压后,周围血管神经才能逐渐辨别,在肿瘤未切除之前就盲目寻找肿瘤旁边的神经和血管的做法是不可取的[14]。当切除肿瘤内部组织后,可以分离出舌咽、迷走、副神经、舌下神经以及肿瘤周边的小脑前下、后下动脉。小脑与瘤体的界限分离出来后,就能开始辨别面神经走行。面神经与肿瘤的病理解剖关系有以下几种:肿瘤腹侧面中部居多,其次是下极、上极、背侧,有时面神经被肿瘤挤压侵犯,不能判断其走行和位置[15]。明确肿瘤与面神经的解剖位置后,再将肿瘤下极、上极和肿瘤前方依次切除,最后处理靠近内听道及内听道内部的肿瘤。在切除这部分肿瘤前,需要恰当磨除部分内听道壁,同时予以生理盐水冲刺,避免热传导对面、听神经的损伤,以促进面、听神经的分离,达到尽量保留的作用。之后再次辨认肿瘤与神经、血管的关系,配合神经剥离子的作用,将肿瘤轻轻剥离。大多数情况下,当肿瘤体积较大时,瘤体会压迫推移面听神经,难以辨认,这时可以从脑干端、内听道端寻找与瘤体粘连不紧的面神经段,然后沿着面神经走行方向,向面神经与瘤壁粘紧密连处分离,分次逐块切除肿瘤壁。对于与脑干相连的肿瘤组织,肖烽[16]研究了听神经瘤的蛛网膜结构对于肿瘤切除的作用,认为大多数肿瘤与脑干之间是有蛛网膜间隙的,神经血管走行于肿瘤表面的两层蛛网膜之间。术中可沿蛛网膜间隙分离肿瘤,这样可减少脑干及神经血管的损伤。如脑干与瘤体之间的蛛网膜间隙不明显,就可借助显微器械将肿瘤包膜轻轻提起,用脑棉轻而均匀地将瘤体与脑干分离。如果肿瘤与脑干粘连紧密,不能强行切除,遗留的少部分肿瘤组织术后可行放疗[17]。此外,在切除肿瘤的过程中,双极电凝的使用功率不宜过大,应尽量减少双极电凝对于神经血管的电灼伤效应。
3.3重要血管的保护 就动脉而言,与听神经瘤的关系最为密切的是小脑前下动脉,术中如果对小脑前下动脉出血处理时过度压迫或电凝,都会引起血管痉挛甚至栓塞,可造成脑干缺血水肿,出现血压降低,呼吸及心跳停搏的风险[18]。尼莫地平稀释液浸泡的棉片可防止或减轻脑血管痉挛。迷路动脉是小脑前下动脉的分支,为面神经的供应血管,阻断后可导致不可恢复性的面瘫症状,另外,迷路动脉的保留是术后听力得以保留的解剖学基础,所以术中要避免损伤,尤其在处理内听道内的肿瘤时要格外注意[19]。小脑后下动脉的作用主要是延髓的供应血管,与后组颅神经位置较近,相对容易区别,在肿瘤体积较大时经常附壁生长或侵入瘤内生长。当瘤体巨大时,小脑上动脉、椎基底动脉可出现侵犯,必须仔细辨别,小心处理。此外,岩静脉及颈静脉球等静脉的处理同样重要[20]。一般情况下,上述血管的小分支切断不会引起严重后果,但如果是肿瘤的穿支血管,管壁附着的少量肿瘤不可强行剥离。
3.4神经电生理监测对于听神经瘤术中面神经的保护 神经电生理监测技术的出现给面神经保护带来一次革命性的进展,使得面神经解剖保留率和功能保留率都有了显著提高[21-23]。本研究中,对于面神经的保护我们进行了间断性术中电刺激和连续自发肌电图监测。术中电刺激可以指导术者辨别面神经与肿瘤、与听神经、三叉神经的位置关系,还能判别神经功能存在与否[24]。在切除大听神经瘤时,往往面神经已经被严重挤压成薄片状或细丝状,很难与瘤体薄膜或蛛网膜区分开来。这种情况下,面神经刺激可以帮助定位面神经走行,也提高了肿瘤切除率。连续自发肌电图监测可实时动态关注面神经有无牵拉或挤压情况。在切开肿瘤薄膜之前,我们先用双极刺激器刺激肿瘤背侧,距离由远及近,刺激强度由小到大,确认无神经组织后再予以瘤内减压,在分离瘤壁面神经收到牵拉时,连续自发肌电图可以出现波幅大小不一的收缩波形。一旦出现异常波形,随时报告术者,调整操作方式。虽然本研究的监测组与非监测组听神经切除率无明显差异,但是监测组面神经的解剖保留率明显高于非监测组。且在术后3个月、术后1年面神经功能改善情况明显优于非监测组。虽然术者娴熟的显微操作技术对于肿切切除至关重要,但是神经电生理监测对于面神经保护不可或缺。
综上所述,在未来听神经瘤的切除手术中,我们神经外科医生需要选择最佳的手术方案,掌握熟练的显微操作技巧,术中应用神经电生理技术提高神经保护,从而造福于广大患者。

