基于网络药理学和GEO数据研究三七、黄芪和丹参防治缺血性脑卒中作用机制 *
刘玥彤杨鎏鑫黄清欧阳扬刘蕾陈玉珍方子文蒙兰青
(1. 右江民族医学院研究生学院,广西 百色 533000;2. 右江民族医学院附属医院神经内科,广西 百色 533000;3. 广东省粤北人民医院,广东 韶关 512000)
卒中,中医又叫中风,是全球第二大致死和致残原因[1],是中国第三大死因,2018年中国卒中死亡人数为157万,给中国的医疗保健系统带来了巨大的负担[2]。缺血性脑卒中占卒中70%~80%,对缺血性脑卒中有效治疗的研究是目前卒中关注的热点之一。中药是祖国医学的瑰宝,几千年的医学实践发现中药在治疗中风方面具有独特疗效[3-5]。三七、黄芪、丹参为治疗淤血症著名的单味中药,是复方药血栓通胶囊和芪参益气方的重要组成成分,研究[6-8]表明其配伍使用对缺血性脑卒中的治疗有着重要影响,对于缺血性脑卒中具有神经保护作用[9-10],但作用机制目前尚未明确。网络药理学是运用系统生物学、网络分析对药物进行设计分析的一种方法,具有连通性、冗余性和多效性[11]。同时将药理学网络映射到人类疾病-基因网络上,不仅揭示了药物的作用靶点,而且可以对药物靶点涉及的多种疾病有所了解[12-13]。在目前国内外研究中,网络药理学已广泛应用于中药活性成分及靶点的预测、药物与疾病之间相互作用的预测等。本研究将通过网络药理学以及GEO数据,探索中药三七、黄芪、丹参防治缺血性脑卒中的作用机制,为中药在缺血性脑卒中的临床应用提供理论依据,流程图见图1。

图1 基于网络药理学和GEO数据研究三七、黄芪
1 资料与方法
研究中药活性成分相关靶点以及与缺血性脑卒中疾病靶点相互作用中需要用到的工具,见表1。

表1 常用数据库以及软件
1.1三七、黄芪和丹参化学成分的检索与筛选 在中药系统药理学TCMSP数据库(https://tcmsp-e.com/)分别检索三七、黄芪以及丹参获得所有化学成分,根据口服生物利用度(oral bioavailability,OB)≥30%,化合物类药性(drug-likeness,DL)≥0.18,将三七、黄芪以及丹参符合筛选标准的化学成分信息作为活性成分。并通过查阅相关文献获取有效活性成分作为补充。
1.2三七、黄芪和丹参活性成分靶点信息的获取 在TCMSP数据库获取与活性成分相关的作用靶点蛋白信息,通过Uniprot数据库(https://www.uniprot.org/)进行蛋白质ID转换。采用Cytoscape 3.8.0软件 (https://cytoscape.org/)构建三七、黄芪以及丹参与其作用靶点网络图。
1.3缺血性脑卒中疾病靶点信息的检索与收集 在OMIM数据库(https://omim.org/)和GeneCards综合数据库(https://www.genecards.org/)检索ischemic stroke获取缺血性脑卒中疾病的靶点。合并去重后通过在线工具Veen(http://bioinformatics.psb.ugent.be/webtools/Venn/)绘制维恩图获取药物活性成分在疾病中的作用靶点。
1.4中药-活性成分-作用靶点-疾病相关网络的构建 将筛选整合得到的三七、黄芪、丹参在缺血性脑卒中疾病中发挥潜在作用有效成分及相关靶点通过Cytoscape 3.8.0软件来构建“中药-活性成分-作用靶点-疾病”相关网络。
1.5蛋白相互作用(PPI)网络构建及核心蛋白筛选 将三七、黄芪和丹参有效成分靶点与疾病靶点交集后所得相关的靶点蛋白导入String数据库(http://string-db.org)。在String数据库中设定物种为“Homo sapiens”(人源),相关作用最低置信度为“Highest confidence=0.9”,导出蛋白质相互作用网络图,并运用Cytoscape 3.8.0软件中Anlyze Network工具和CytoNCA插件,筛选得到中药活性成分靶点-疾病网络中核心模块和核心蛋白。
1.6GO生物学过程以及KEGG通路富集分析 将核心基因导入DAVID数据库(https://david.ncifcrf.gov/)进行基因本体(gene ontology,GO)中的生物过程(biological process,BP)、分子功能(molecular function,MF)和细胞组成(cellular component,CC)分类富集分析和KEGG通路注释分析,设定阈值为P<0.05作为显著性标准。利用Bioinformatics在线工具(http://www.bioinformatics.com.cn/?p=4J)进行结果可视化分析。
1.7潜在核心靶点的验证 在GEO(http://www.ncbi.nlm.nih.gov/geo)数据库搜索关键词“Ischemic Stroke”获取得到基因微阵列数据集GSE22255,使用RStudio软件(https://www.rstudio.com/)进行质量以及数据可视化分析,以P<0.05且|log2FC|>0.6为标准筛选得到缺血性脑卒中具有差异表达基因(differential expressed genes,DEG),同时通过string数据库以及Cytoscape 3.8.0软件获取得到核心差异基因,将其结果与所获取的三七、黄芪、丹参在IS中作用的潜在核心靶点取交集,来进一步验证潜在核心靶点的表达。
2 结果
2.1三七、黄芪和丹参活性成分靶点信息 在TCMSP数据库中检索得到三七的化合物共119个,黄芪的化合物共89个,丹参的化合物202个。筛选后得到三七活性成分为13个,黄芪活性成分为21个,丹参活性成分为65个,其中需根据文献补充三七活性成分notoginsenoside R1、ginsenoside Re、ginsenoside Rb1、ginsenoside Rg1以及ginsenoside Rd,黄芪活性成分Astragaloside IV。在TCMSP数据库获取靶点蛋白信息以及Uniprot数据库蛋白质ID转换后收集得到具有潜在靶蛋白有效活性成分和靶蛋白,具有潜在靶蛋白有效活性成分如表2所示。其中三七有效活性成分相关作用靶点186个,黄芪作用靶点215个,丹参作用靶点137个。构建“中药-活性成分-相关靶点”网络,见图2。
2.2缺血性脑卒中相关靶点的获取以及三七、黄芪、丹参在其潜在靶点 在OMIM数据库和GeneCards综合数据库经检索分别获得337个和3937个缺血性脑卒中相关靶点。筛选合并去重后得到IS相关靶点2100个。将三七、黄芪和丹参活性成分相关靶点进行合并去重,通过绘制Veen收集中药活性成分在IS中的潜在作用靶点160个,见图3。

图2 “三七、黄芪和丹参-活性成分-靶点”网络图
图3 三七、黄芪、丹参在缺血性脑卒中潜在靶点Veen图
2.3“中药-活性成分-作用靶点-疾病”相关网络的构建 将三七、黄芪、丹参在缺血性脑卒中作用的有效成分及相关靶点导入Cytoscape 3.8.0软件,构建“中药-活性成分-作用靶点-疾病”相关网络,见图4。其中三七和黄芪活性成分含有共同靶点(如图4中A1所示)。蓝色部分为三七、黄芪、丹参在缺血性脑卒中作用靶点,橙色矩形部分为三七在缺血性脑卒中的有效作用成分,粉色三角形部分为黄芪在缺血性脑卒中的有效作用成分,绿色菱形部分为丹参在缺血性脑卒中的有效作用成分。
2.4蛋白相互作用(PPI)网络构建及核心蛋白筛选结果 将所获取的三七、黄芪、丹参在缺血性脑卒中潜在160个靶点导入String数据库中,将结果保存为TSV格式并导入Cytoscape 3.8.0软件,得到蛋白互作网络图,见图5。同时通过Cytoscape软件中cytoNCA插件对网络中靶点度值(Degree)、介度中心性(Betweenness Centrality,BC)和接近中心性(Closeness Centrality,CC)进行分析筛选得到“中药活性成分靶点-疾病”网络中核心蛋白及基本信息,如图6和表3,其中颜色越深代表靶点度值越大。
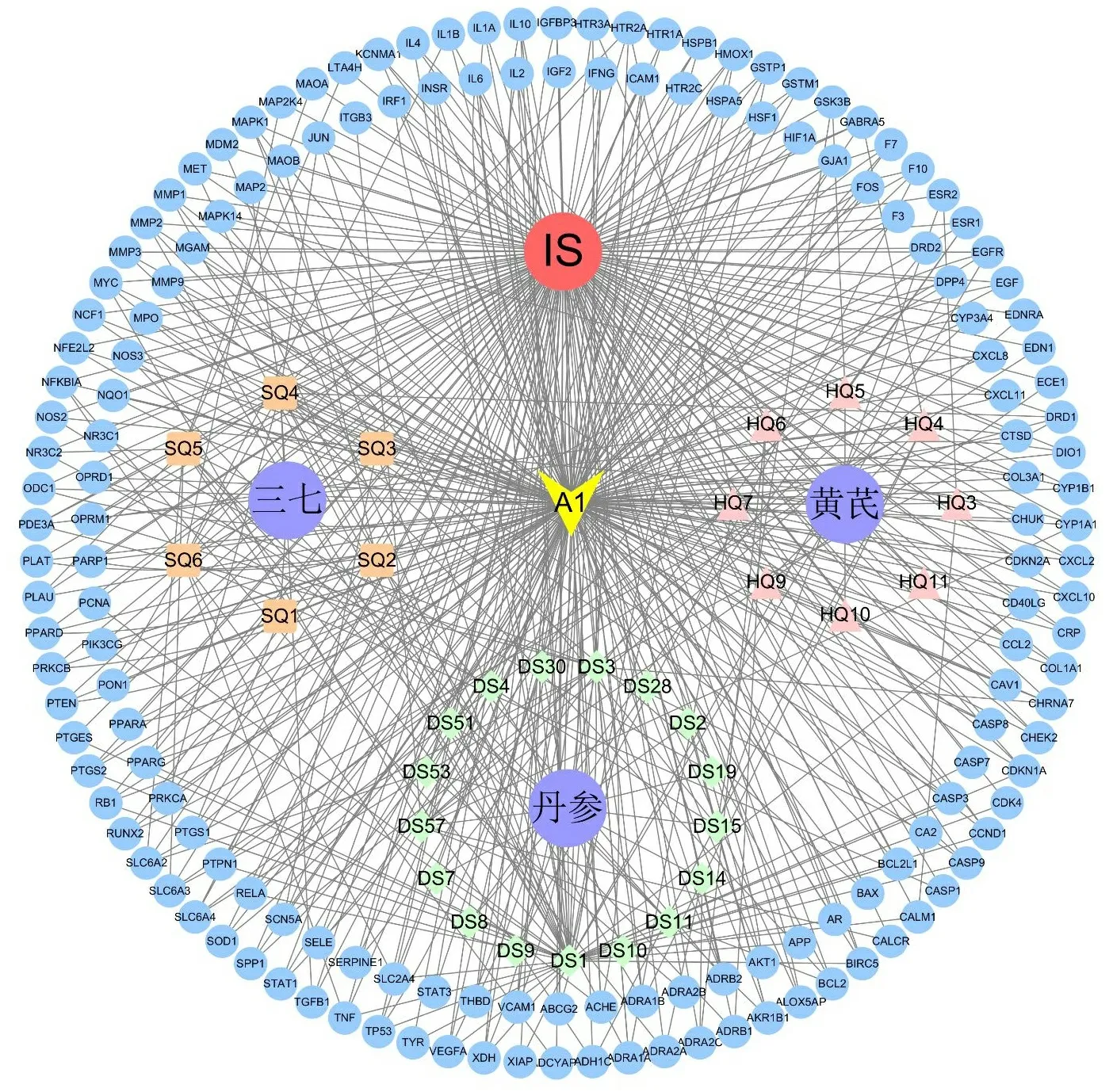
图4 “中药-活性成分-作用靶点-疾病”网络图

图5 三七、黄芪、丹参在缺血性脑卒中潜在靶点PPI网络图

图6 潜在靶点PPI网络图核心蛋白

表3 三七、黄芪、丹参在缺血性脑卒中潜在核心靶点蛋白基本信息
2.5核心靶蛋白GO以及KEGG通路富集 将核心基因导入DAVID数据库,进行GO以及KEGG通路富集。根据P-Value<0.05进行筛选后共获取GO富集条目共105条和KEGG通路70条。其中GO富集中包含生物过程条目80条,分子组分条目6条,分子功能条目19条。同时对GO各分类条目前10名以及KEGG通路前20进行注释分析,如图7、图8所示。在生物学过程中主要为脂多糖介导的信号通路(lipopolysaccharide-mediated signaling pathway)、RNA聚合酶Ⅱ启动子对转录的正调控(positive regulation of transcription from RNA polymerase Ⅱ promoter)、正向调控基因表达(positive regulation of gene expression)、调控一氧化氮生物合成过程(positive regulation of nitric oxide biosynthetic process)等,分子组分主要富集于核质、胞浆、胞核,分子功能主要是与相同蛋白、蛋白磷酸酶、转录调节区DNA等结合有关。在对三七、黄芪、丹参在缺血性脑卒中潜在核心靶点KEGG通路富集中包含MAPK信号通路、T细胞受体信号通路、Toll样受体(TLR)信号通路、肿瘤坏死因子(TNF)信号通路、鞘脂信号通路、神经营养因子(BDNF)信号通路、FOXO信号通路等。

图7 三七、黄芪、丹参在缺血性脑卒中潜在核心靶点GO富集(排名前10)

图8 三七、黄芪、丹参在缺血性脑卒中潜在核心靶点KEGG通路富集分析(排名前20)
2.6潜在核心靶点验证 GSE22255数据集中有40个样本,来自缺血性脑卒中组(n=20)和对照组(n=20)。使用GEO2R进行在线分析,将筛选得到差异基因在String数据库PPI网络导入Cytoscape 3.8.0软件中用cytoHubba插件,按照degree筛选得到排名前十的靶基因,如图9所示,颜色越深表明程度分值越大。与所获取的三七、黄芪、丹参在IS中作用的潜在核心靶点取交集后得到靶基因转录因子AP-1(JUN)、肿瘤坏死因子(TNF),在GSE22255数据集卒中组和对照组表达如图10所示。该结果进一步表明JUN、TNF在缺血性脑卒中发挥着相关作用,并可能为三七、黄芪、丹参的作用重要靶点。

图9 GSE22255数据集PPI网络中排名前十靶基因

图10 JUN、TNF分别在数据集GSE22255中表达
3 讨论
三七、黄芪、丹参是我国著名中药,广泛应用于缺血性脑卒中的临床治疗[14-16]。梁萍等[17-18]研究发现三七可以对急性脑缺血/再灌注损(I/R)伤大鼠神经血管单元的整体保护作用。王萍等[19]研究中发现三七中皂苷类成分能抑制大鼠缺血性脑卒中模型中巨噬细胞和小胶质细胞肿瘤坏死因子α(TNF-α)和白介素1β(IL-6)的表达,减轻炎症反应从而起到神经保护作用。黄芪甲苷和山萘酚是黄芪的活性成分,研究表明黄芪甲苷可以通过促进自噬抑制细胞凋亡在脑缺血/再灌注损伤中发挥神经保护作用[20],山萘酚通过降低TNF-α和 IL-1β减轻炎症反应,保护血脑屏障完整性,减少脑梗塞体积改善神经损伤。在Lee JC等[21]研究中发现丹参提取物丹参酮Ⅰ( tanshinone Ⅰ)通过减少缺氧缺血小鼠模型的脑组织梗死灶体积以及防止病灶侧神经元死亡从而发挥神经保护作用。而Hou S等[22]研究发现丹参提取物丹酚酸在缺血性脑卒中中可以减少皮层梗死体积,防止细胞凋亡和增加线粒体膜电位(mitochondrial membrane potential,MMP),减轻了对线粒体结构和功能的损害。
通过网络药理学分析,本研究发现中药三七、黄芪、丹参中豆甾醇(stigmasterol)、槲皮素(quercetin)、异鼠李素(isorhamnetin)、毛蕊异黄酮(calycosin)、丹酚酸(salvianolic acids)、隐丹参酮(cryptotanshinone)等活性成分在缺血性脑卒中疾病中发挥重要作用。在构建的蛋白相互作用网络中,信号转导和转录激活因子3(STAT3)、丝氨酸/苏氨酸蛋白激酶(AKT1)、转录因子AP-1(JUN)、细胞肿瘤抗原p53(TP53)、肿瘤坏死因子(TNF)、丝裂原活化蛋白激酶1(MAPK1)、丝裂原活化蛋白激酶14(MAPK14)、表皮生长因子受体(EGFR)为三七、黄芪、丹参在缺血性脑卒中疾病中的治疗作用中核心潜在靶蛋白。GO富集和KEGG通路富集在脂多糖介导的信号通路、RNA聚合酶Ⅱ启动子对转录的正调控、正向调控基因表达、NO生物合成过程、MAPK信号通路、T细胞受体信号通路、Toll样受体信号通路、TNF信号通路、鞘脂信号通路、BDNF信号通路、FOXO信号通路等。豆甾醇为三七的有效活性成分,Sun JD等[23]研究表明豆甾醇可以抑制缺血/再灌注损伤后的自噬作用,降低脑缺血/再灌注损伤后NO水平减轻氧化应激发应,减少由缺血/再灌注损伤引起的神经功能缺损和梗塞损害,同时能有效地保护损伤后的神经元细胞。在Liang QL等[24]研究中同样发现豆甾醇通过调控对脑缺血/再灌注损伤凋亡标志物Bcl-2相关X蛋白(Bax)、半胱天冬酶3(caspase3)、抗凋亡蛋白Bcl-XL的表达来发挥抗凋亡作用和NO水平调控发挥抗氧化作用,并且豆甾醇能在一定程度上缓解炎症,促进组织抗氧化能力的提高,保护神经元。研究表明黄芪提取物毛蕊异黄酮可以增加缺血性卒中大鼠脑内BDNF及其酪氨酸激酶受体B(TrkB)的表达,从而减少脑梗死体积、神经元变性和凋亡损伤以及含有TNF-α的小胶质细胞的聚集来改善缺血性脑卒卒中神经损伤症状[25]。Zhu WX等[26]研究发现丹参活性成分隐丹参酮可以通过升高缺血性脑卒中中大脑皮层和外周血中B细胞淋巴2(Bcl-2)和NO水平来发挥抗凋亡和血管保护作用,同时可以增加清除氧自由基的能力指标内源性抗氧化酶(SOD)活性和降低脂质过氧化的敏感指标丙二醛(malonaldehyde,MDA)来发挥抗氧化作用。除此之外,隐丹参酮可以降低缺血性脑卒中大鼠模型中的磷脂酰肌醇3-激酶(PI3K)和蛋白激酶B(AKT)水平的表达,抑制PI3K / AKT信号通路在缺血性脑卒中保护脑组织[26]。槲皮素为三七和黄芪共有的活性成分,Wang YY等[27]研究表明槲皮素可以减轻缺血/再灌注损伤所致的神经功能缺损、脑梗死、血脑屏障破坏、氧化应激、TNF-α和IL-1β的表达,以及凋亡的caspase3活性。在Yao R等[28]研究中发现槲皮素可能将通过BDNF-TrkB-PI3K/Akt信号通路来能减少大鼠局灶性脑缺血后的细胞凋亡保护脑组织。
通过与GEO数据库中缺血性脑卒中GSE22255数据集的结合,更进一步证明JUN、TNF为缺血性脑卒中关键核心靶蛋白,并可能成为三七、黄芪、丹参在缺血性作用的重要靶点。转录因子活化蛋白1(AP-1)家族蛋白是基本的亮氨酸拉链(bZIP)转录因子,涉及多种细胞过程的调控,包括增殖和存活、生长、分化、凋亡、细胞迁移和转化,Jun蛋白是其中的成员,包含c-jun、junB、junD[29]。Xiao P等[30]实验表明脑缺血再灌注过程中,神经细胞中c-Jun的表达是增加的,并且与抗凋亡蛋白Bcl-2/促凋亡蛋白Bax的变化同步。张路等[31]研究表明三七成分三七皂苷可通过抑制c-jun的表达来降低缺血再灌后脑细胞凋亡。而丹参、黄芪以及配伍使用均能够部分抑制FOS蛋自、JUN蛋白的高表达,对脑缺血再灌注损伤起到保护作用[32]。肿瘤坏死因子(TNF)超家族是由19个配体和29个受体组成,在炎症、细胞增殖、凋亡和形态发生中的作用,其中TNF-α与神经系统也有着密切的关联[33]。在神经系统常见疾病缺血性脑卒中中,TNF对再灌注损伤所引起的炎症反应具有一定的调节作用[34-35]。而三七、黄芪、丹参中的活性成分均能够通过调节缺血/再灌注损伤中TNF的表达来保护神经功能[25-27]。
综上所述,网路药理学为中药在缺血性脑卒中的研究提供了新的方法。本研究通过结合GEO数据进行生物信息学分析筛选得到三七、黄芪、丹参中潜在核心靶蛋白STAT3、AKT1、JUN、TP53、TNF、MAPK1、MAPK14、EGFR可通过MAPK、T细胞受体、TLR、TNF、FOXO等信号通路调控基因表达、转录等多途径在缺血性脑卒中发挥神经保护作用,其中JUN、TNF为缺血性脑卒中关键核心靶蛋白。由于网络药理学是根据在线数据库所获取的大数据进行分析,其数据的实时性和及时性存在局限性,后期的研究将通过实验进一步验证。

