凝胶渗透色谱-十八角激光光散射仪(GPC-MALLS)在聚丙烯酰胺合成中的应用
林朝阳, 郝小飞, 霍炳臣, 王冬梅, 李天仚, 赵献增
(河南省科学院高新技术研究中心,河南省精细化工重点实验室,郑州 450002)
聚丙烯酰胺(PAM)是由丙烯酰胺(AM)单体通过自由基聚合而成,是一种应用极广的水溶性高分子材料,其结构单元中CONH2结构特征决定了聚丙烯酰胺具有良好的吸附性、高黏性、交联性,被广泛应用于造纸、纺织、医药、建筑、石油、地质、农业、采矿采油和环保等诸多领域[1-3].聚丙烯酰胺及其相关降解物较为安全,但其残留的未聚合的丙烯酰胺是水溶性较好的神经性毒素,易通过消化系统、呼吸系统、皮肤被人体吸收,可引起神经损伤及DNA损伤从而致癌、致畸等,对人体及环境有一定的危害[4].因此,准确测定聚丙烯酰胺中残留单体对聚丙烯酰胺的质量控制具有重要的意义.
为有效评价聚丙酰胺相关产品的安全性,需准确测定其残留单体的含量,目前用于测定聚丙烯酰胺中丙烯酰胺含量的方法主要有化学分析法[5]、紫外分光光度法[6]、气相色谱法及气相色谱质谱联用法[7-9]、液相色谱法及液相色谱串联质谱法[10-12].但化学分析法使用指示剂确定滴定终点,终点颜色变化不宜观察,操作烦琐,耗时耗力.紫光分光光度法在测定聚丙烯酰胺单体残留时,聚合物在所选取的波长范围有一定的吸收,容易干扰测定的准确性,存在准确度不高、易受干扰等缺点.气相色谱法与液相色谱法需要提前将丙烯酰胺从聚合物中分离出来,且气相法需要进一步对单体进行衍生化,单体的提取率及衍生化率势必会对测定结果产生影响.上述方法缺点明显,难以广泛应用.本研究团队多年来致力于研究水溶液聚合法合成低分子量聚丙烯酰胺[13-16],已在纳米材料制造、特种陶瓷、耐火材料、水处理、数码印刷等领域使用,迫切需要建立一种快速、准确、稳定的方法检测产物中丙烯酰胺的含量来指导绿色合成工艺的开发.本文建立凝胶渗透色谱法(GPC)直接测定聚丙烯酰胺合成中残留单体的方法,尚未见报道,适用于丙烯酰胺聚合反应进程的监测及合成产物中残留单体的测定.
聚合物分子量和分子量分布是表征聚合物性能的重要指标,目前聚丙烯酰胺的相对分子量主要通过黏度法测定,但黏度法存在耗时长、操作烦琐等缺点,且不能测定其分子量分布.GPC凝胶渗透色谱被广泛应用于测定高聚物的相对分子质量和相对分子质量分布,但是GPC 方法需要结构与其相似的标准品作为对照,其测定结果受柱效、所选的标准品等多种因素影响.近年来发展起来的凝胶渗透色谱-十八角激光散射仪(GPC-MALLS)是测定高聚物相对分子质量及分散系数(PDI)的有效方法,该方法简便、准确、不需色谱柱的标定和对照品的参考,又能测定均方根半径等相关参数[17].目前,国内外几乎很少有文献报道利用GPC-MALLS系统来测聚丙烯酰胺的相对分子质量及分子质量分布[18].本文采用GPC-MALLS系统来测定聚丙烯酰胺分子量及分子量分布,进而来指导聚丙烯酰胺的合成工艺开发.
本文采用GPC-MALLS系统来测定聚丙烯酰胺分子质量及分子质量分布及其合成工艺中残留单体的含量,实现了一次进样即可同时测定单体的残留量和聚合物的分子量,具有高效、准确、稳定的特点,对聚丙烯酰胺的合成具有重要的意义.
1 实验部分
1.1 仪器与试剂
岛津LC-20AT高效液相色谱仪、岛津RID-10A 示差折光检测器、美国怀雅特公司十八角度激光光散射仪(DAWN HELEOS Ⅱ)、美国怀雅特公司示差折射率测定仪(Optilab T-rEX)、V7.3.2.19b型Astra数据采集及处理软件、水溶性SEC(GFC)色谱柱(OHpak SB-806 HQ、OHpak SB-804 HQ)、上海精天电子仪器有限公司电子天平FA2004A.
丙烯酰胺(纯度99.8%,aladdin公司,乙酸乙酯重结晶纯化)、超纯水(0.45 μm滤膜过滤)、标准品葡聚糖T40、过硫酸铵(AR)、甲醇(AR)、乙醇(AR)、乙酸乙酯(AR)、硝酸钠(AR).
1.2 标准溶液的配制
标准储备液(5 mg/mL):准确称取500 mg纯化后的丙烯酰胺,超纯水溶解并定容至100 mL容量瓶中.
分别准确吸取标准储备液1、2、4、8、16 mL 定容于100 mL 容量瓶中,配制质量浓度为0.05、0.10、0.20、0.40、0.80 mg/mL的丙烯酰胺标准溶液,水系针式过滤器过滤,以建立标准工作曲线.配制0.1 mol/L的NaNO3溶液,水系微孔过滤膜过滤,作为流动相使用.配制2 mg/mL分子量为4万的葡聚糖标准品溶液(水系微孔过滤膜过滤),以备十八角度激光光散射仪归一化用.
1.3 色谱条件
为达到较好的分离度,通过对柱温、流速、进样量、色谱柱等色谱条件进行优化,确定最优色谱条件为:色谱柱OHpak SB-806 HQ、OHpak SB-804 HQ串联,柱温:40 ℃;流动相:0.1 mol/L的NaNO3,流速:0.5 mL/min;进样体积:50 μL.
1.4 合成方法
将带有搅拌装置、回流冷凝管、温度计、蠕动泵接口的500 mL四口烧瓶置于可调节温度的油浴中,加入40 mL 水和一定量的有机溶剂,升温至回流状态,100 mL 质量分数为15%的AM 单体及20 mL 浓度为2 mmol/L 的过硫酸铵溶液的混合溶液通过蠕动泵滴加,1.5 h 内滴加完毕,保持回流状态,继续反应2 h,蒸馏去除有机溶剂,降温至常温,即得到聚丙烯酰胺的水溶液(图1).
图1 聚丙烯酰胺的合成Fig.1 Synthesis of polyacrylamide
1.5 dn/dc值的测定
dn/dc值即折光指数增量,是描述聚合物溶液折光指数相对于溶质浓度的变化的参数,在特定温度及特定溶液中可视为固定常数.取上述合成得到的30 g聚丙烯酰胺水溶液倒入恒压滴液漏斗中,逐滴滴加到400 mL甲醇中(边加边搅拌),进行第一次纯化,析出白色固体,布氏漏斗减压过滤得白色固体,用30 mL去离子水溶解,重复上述操作,进行第二次纯化,抽滤,放入真空干燥箱中干燥24 h,取出后用研钵研碎,即得聚丙烯酰胺粉末.取适量的纯化后的聚丙烯酰胺样品配制成2 mg/mL 的NaNO3的溶液,在上述色谱条件下,通过凝胶渗透色谱对其纯度进行分析,结果表明,纯化后的PAM较为纯净(图2).
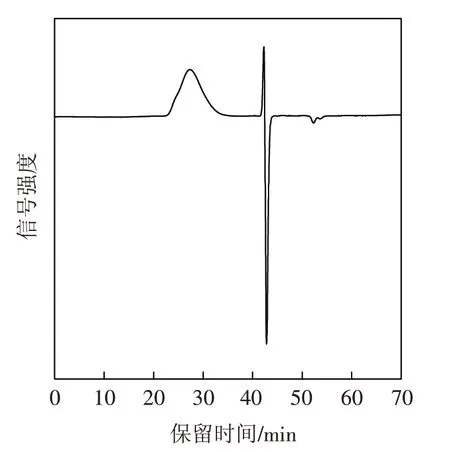
图2 纯化后PAM的色谱图Fig.2 Chromatogram of purified PAM
取适量的纯化后的聚丙烯酰胺粉末,用0.1 mol/L 的NaNO3的溶液依次配成质量浓度为0.25、0.50、0.75、1.00、1.25、1.50 mg/mL的供试品溶液.打开Astra软件下的dn/dc测试模块并设定有关参数,将样品按浓度从低到高顺序注入检测器并进行数据收集,最终通过软件处理(定基线,选峰,输入相关峰浓度依次进样),示差折射率测定仪(Optilab T-rEX)测定聚丙烯酰胺在0.1 mol/L 的NaNO3中的dn/dc.
1.6 实验方法
精密称取5.00 g样品(丙烯酰胺水溶液聚合产物),0.1 mol/L的NaNO3溶液定溶于100 mL容量瓶中,放置过夜使其充分溶解.首先打开液相系统、示差检测器、十八角度激光光散射仪实现GPC-MALLS-RI 的联用,待仪器达到测试状态后,首先取2 mg/mL分子量为4万葡聚糖标准品溶液对十八角度激光光散射仪进行归一化操作.然后注射器取2 mL配制好的样品溶液,通过0.45 μm 水系针式过滤器过滤,在上述色谱条件下上机测定.通过十八角度激光光散射仪相关软件处理(定基线,定峰,输入dn/dc值)直接测定分子量及分子量分布,根据示差检测器检测结果及建立的工作曲线测定单体含量.
2 结果与讨论
2.1 色谱条件的选择
在本合成工艺的条件下,自由基水溶液聚合法得到的聚丙烯酰胺中常含有自由基引发剂分解物(硫酸铵等)、残留单体、残留有机溶剂等多种成分,各成分的充分分离是实现准确测定分子量及单体残留的前提.首先对流动相、流速及柱温进行条件筛选,结果显示,上述条件对各组分的分离效果影响不大、为防止仪器系统压力过高而损坏仪器,因此选择柱温:40 ℃,流动相:0.1 mol/L的NaNO3,流速:0.5 mL/min为流动相条件为色谱条件.示差及激光检测器和色谱柱对进样量有一定的要求,既要满足检测的灵敏度,又要防止色谱柱超载,结合配制样品的浓度,选择进样体积为50 μL.选择分子量分析范围为500~2000万的OHpak SB-806 HQ色谱柱、和分子量分析范围为500~200万的OHpak SB-804 HQ色谱柱.当两根色谱柱单独使用时,部分组分叠加,不能很好地实现各组分分离(图3),因OHpak SB-804 HQ分离范围较窄,分离效果比OHpak SB-806 HQ色谱柱稍好.当色谱柱OHpak SB-806 HQ、OHpak SB-804 HQ串联使用时分离效果较好(图4),示差、激光检测器信号呈对称、正态分布图样,能实现聚合物、残留单体、引发剂残留物的充分分离.因此确定最优色谱条件如下:色谱柱OHpak SB-806 HQ、OHpak SB-804 HQ 串联;柱温:40 ℃;流动相:0.1 mol/L 的NaNO3;流速:0.5 mL/min;进样体积:50 μL.
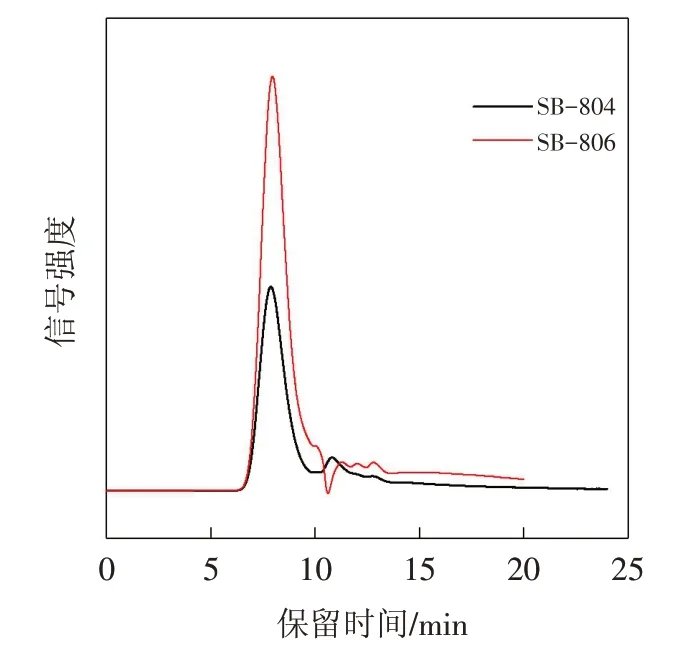
图3 SB-806和SB-804分离色谱图Fig.3 Chromatogram of PAM separated by SB-806 and SB-804
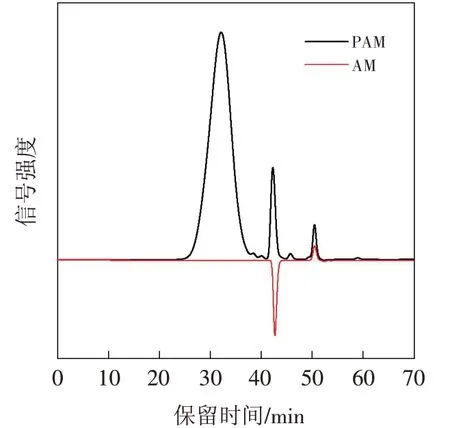
图4 聚丙烯酰胺及丙烯酰胺色谱图Fig.4 Chromatogram of polyacrylamide and acrylamide
2.2 线性范围与检出限
打开液相系统、示差检测器.将质量浓度为0.05、0.1、0.2、0.4、0.8 mg/mL的标准溶液在上述的色谱条件下浓度由低到高依次进样检测,每个浓度标准溶液测定三次,计算峰面积的平均值(表1),以浓度为横坐标、色谱峰面积为纵坐标,绘制标准曲线.标准工作曲线的线性方程为:y=897 156x-1577,R2=0.999 9,线性相关系数R2接近1,说明标准曲线的相关性良好(图5).以色谱峰3 倍信噪比(S/N=3)对应浓度为检出限(LOD),检出限为0.001 25 mg/mL,10 倍性噪比(S/N=10)对应浓度为定量限(LQD),定量限为0.006 25 mg/mL.
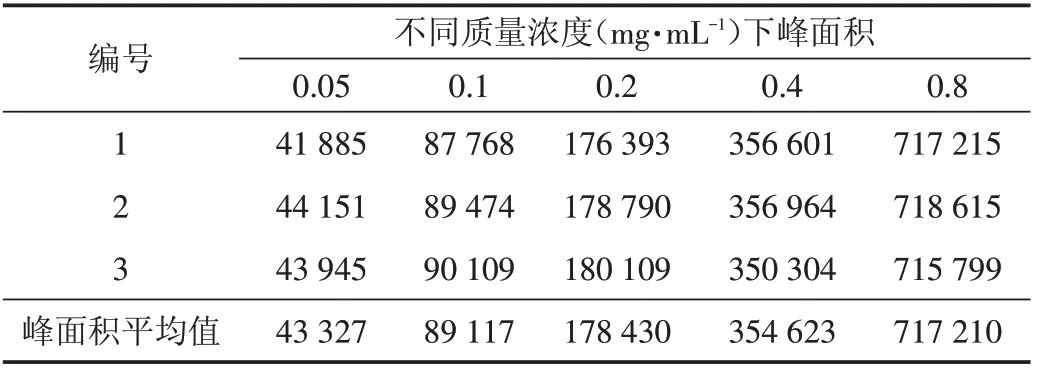
表1 标准溶液峰面积结果Tab.1 Peak area results of standard solutions
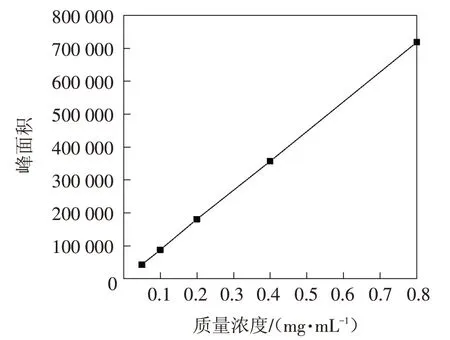
图5 丙烯酰胺标准曲线Fig.5 Standard curve of acrylamide
2.3 加标回收率与精密度
准确称取适量的丙烯酰胺标准品及纯化后的聚丙烯酰胺粉末,配制丙烯酰胺添加水平分别为0.10、0.150、0.200 mg/mL的加标聚丙烯酰胺溶液.按此方法测定聚合物样品中丙烯酰胺含量,每个水平进行6次重复实验,计算加标回收率及精密度(表2),结果显示平均回收率在99.3%~101%,相对标准偏差为0.55%~3.425%,表明该方法准确、可靠,均满足理化分析指标.
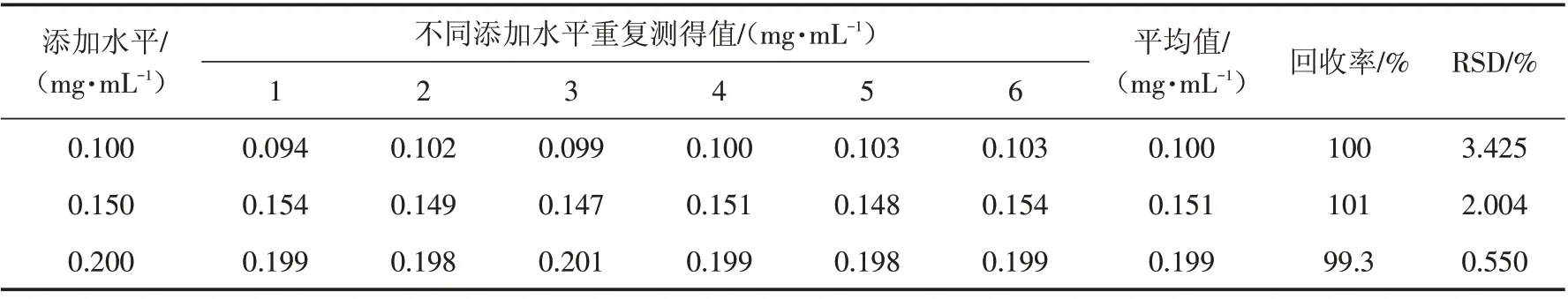
表2 方法加标回收率及精密度计算结果(n=6)Tab.2 Method recovery rates and precision calculation results(n=6)
2.4 在低分子量及中等分子量聚丙烯酰胺合成中的应用
按上述实验方法进行测定(图6),根据峰面积,结合标准工作曲线计算得到所配置的样品浓度,根据取样量,进一步计算得该合成工艺中聚丙烯酰胺残留单体含量.
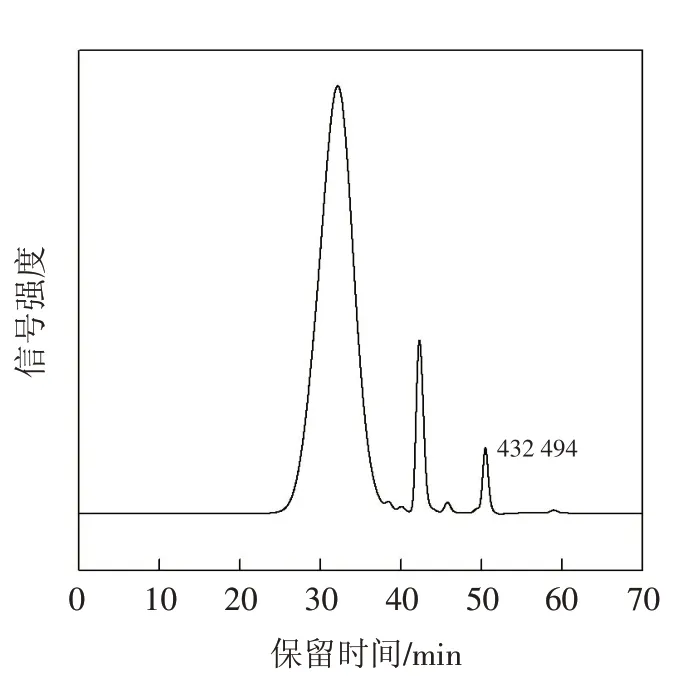
图6 所测样品PAM-1色谱图Fig.6 Chromatogram of the tested sample PAM-1
GPC-MALLS 方法测定相对分子质量,需要测定样品在溶液中折光指数增量(dn/dc),测得聚丙烯酰胺在0.1 mol/L的NaNO3的dn/dc值为0.150 0.对收集到的实验数据(激光检测器数据和示差检测器数据)进行处理,计算出相对分子质量大小及分子质量分布(图7).

图7 GPC-MALLS 法测定聚丙烯酰胺PAM-1分子质量的色谱图Fig.7 Chromatogram of polyacrylamide(PAM-1)molecular mass determined by GPC-MALLS
由于丙烯酰胺的自由聚合反应活性很高,其水溶液自由基聚合难以控制,易发生交联、爆聚等情况,需要加入相应的分子量调节剂来调控分子量及控制聚合反应的进程.有机溶剂易挥发且部分具有活性基团,在自由基水溶液聚合中起转移热量及链转移的作用.分别以乙醇、乙酸乙酯作为分子量调节剂来调控聚丙烯酰胺的聚合反应,调节乙醇或乙酸乙酯的量合成不同分子量的聚丙烯酰胺,合成的聚丙烯酰胺的分子量及单体残留结果见表3.乙醇含有活泼氢的羟基,较易与自由基发生链转移反应,因此选择乙醇作为分子量调节剂来合成低分子量聚丙烯酰胺,当加入1 g乙醇时,合成的目标产物分子量为78.68万,随着乙醇的量增加到3 g,得到了分子量为20.58万的低分子量聚丙烯酰胺,在此过程中,单体的残留量(即反应的转化率)变化不大,由此可以看出,乙醇是合成低分子量聚丙烯酰胺的良好分子量调节剂.乙酸乙酯具备不饱和的酯基,但不具备活性氢,而导致其链转移作用较弱,其难溶于水又较易挥发,在反应体系中可以起到很好的转移热量作用,避免反应体系热量聚集导致的反应不可控,因此选择乙酸乙酯调控中等分子量聚丙烯酰胺的合成.当20 g乙酸乙酯作为分子量调剂时,合成得到分子量为158.9万的中等分子量聚丙烯酰胺.当乙酸乙酯的量增加到40 g时,合成的聚丙烯酰胺分子量下降为120.9万,分子量有所降低,但不明显,进一步说明,乙酸乙酯在反应体系中主要起转移热量的作用.综上所述,凝胶渗透色谱-十八角激光光散射仪联用成功应用于低分子量及中等分子量聚丙烯酰胺的合成中,其准确、快速地测定了聚丙烯酰胺的分子量及单体残留,揭示了相关反应规律,为聚丙酰胺的合成提供了一种便利的检测方法.
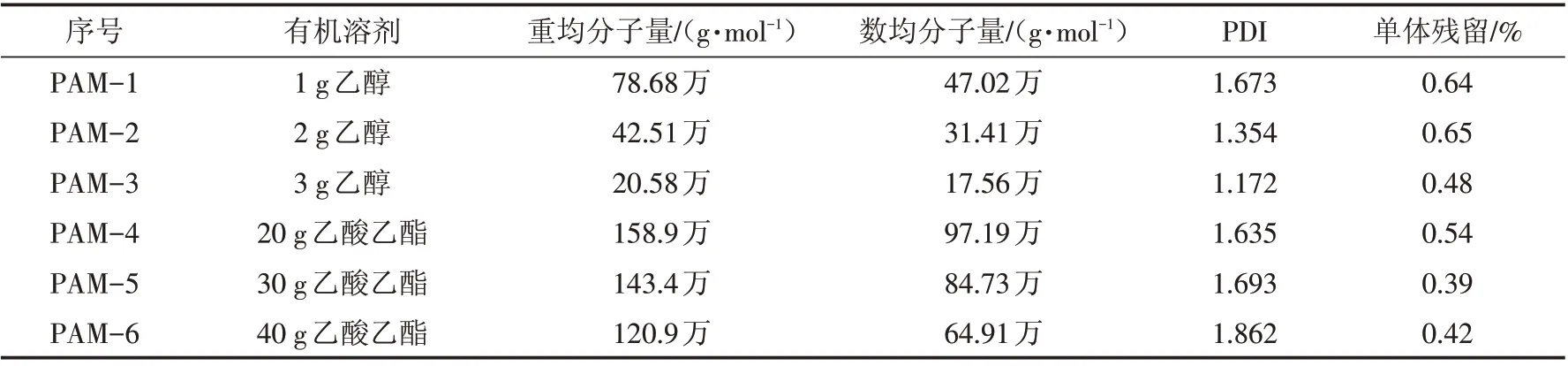
表3 聚丙烯酰胺的分子量及单体含量测试结果Tab.3 Test results of molecular weight and monomer content of polyacrylamide
3 结论
随着经济社会的发展,聚丙烯酰胺相关产品的种类及需求量仍在不断地增加,迫切需要一个快速、简便的检测方法助力聚丙烯酰胺的合成及开发.本文报道了不经任何前处理,凝胶渗透色谱-十八角激光散射仪(GPC-MALLS)直接测定聚丙烯酰胺合成工艺中单体残留、分子量及分子量分布的方法.通过合适的色谱条件,实现聚合物、单体及其他杂质的分离,外标定量法建立分析方法.一次进样即可实现单体含量及分子量的测定,并成功用于聚丙烯酰胺的合成中,该方法操作简便,测定结果准确,适合在聚丙烯酰胺合成工艺中应用.

