高温储能金属氧化物研究综述及其与 超临界二氧化碳循环耦合研究
杨天锋,向 铎,袁 鹏,聂 婧,林诚乾
(1.浙江大学能源清洁利用国家重点实验室,浙江 杭州 310027; 2.杭州明晟新能源科技有限公司,浙江 杭州 310023)
截至2020年底,中国风电和光伏累计装机约5.34亿kW(风电2.82亿kW,光伏2.52亿kW),占总装机的24%,占总发电量的9.5%,风电和光伏发电逐渐进入大规模平价时代[1]。可再生能源在未来能源消费中的比重将越来越大,以达成碳中和目标。高比例风电和光伏发电的强波动性与随机性对电网的安全可靠性造成了巨大威胁[2-3]。为进一步提高光伏、风电等新能源的消纳能力及保障电网安全稳定,可解决能源供给与需求在时空上的不匹配问题的储能成为新能源大规模应用的战略核心技术。
太阳能光热发电系统自带大规模储能,输出稳定,是一种对电网友好的调峰调频电源[4-6]。常见的太阳能热发电储能方式有显热、潜热和热化学储能。目前,商业化的太阳能热发电系统基本采用二元硝酸盐的显热储热,其最高储热温度为565 ℃[7-9]。为进一步提升太阳能热发电系统动力循环效率并降低成本,需提高系统最高工作温度。应用超临界二氧化碳(S-CO2)布雷顿循环、超临界水蒸气循环以及空气布雷顿循环等形式的高温太阳能热发电 (>600 ℃)被认为是下一代潜力技术[10-14]。
基于可逆反应的热化学储能温度高、能量密度大,主要包括碳酸盐、氢氧化物、金属氧化物、氨等反应体系[15-17]。对于金属氧化物反应体系,当反应温度高于平衡温度时,金属氧化物发生还原反应,吸收热能并释放氧气(MexOy+z→MexOy+z/2O2);当反应温度低于平衡温度时,金属氧化物发生氧化反应,释放还原反应所存储的热能并吸收氧气(MexOy+z/2O2→MexOy+z)。金属氧化物反应体系可以在开放环境中与空气反应,避免了碳酸盐体系以及氢氧化物体系中的CO2或水蒸气的存储,简化系统,提高可靠性,在高温太阳能热发电中具有广阔的应用前景。理想的金属氧化物储能物质需具备合适的反应温度、高反应焓值、循环稳定性以及低成本、低毒性等特点,本文对相关研究文献进行梳理,比较不同种类金属氧化物特性,分析储能性能提升方法、储能系统设计方案,并提出相应研究热点及建议。进一步地,构建了100 MW级S-CO2布雷顿循环与金属氧化物储能耦合系统,并进行了系统建模分析。
1 储能材料选择
金属氧化物储能材料主要分为单一金属氧化物(含有1种金属元素)以及混合金属氧化物(含有2种及以上金属元素)。钙钛矿型金属氧化物属于混合金属氧化物,但由于其具有特殊结构和特性,本文将其单独列为一类进行讨论。
1.1 单一金属氧化物
Wong等人[18]利用HSC化学反应与平衡计算软件得到了74种不同单一金属氧化物在常压空气氛围下的平衡热力学特性,并选出了16种潜在的金属氧化物储能材料。表1列出了相关金属氧化物的平衡温度、反应焓以及储能密度[18]。综合考虑上述材料的反应性能、安全以及成本等因素,本文从中优选钴氧化物、锰氧化物、铜氧化物、钡氧化物以及铁氧化物等反应体系作为太阳能高温热化学储能的潜在材料。

表1 基于计算热力学的金属氧化物反应特性Tab.1 Characteristics of metal oxide reactions based on thermodynamics calculation
原位XRD及TGA/DSC测试表明,钴氧化物反应体系内只存在Co3O4及CoO这2种物质的变化[19-20]。Co3O4/CoO的平衡温度约为890 ℃,反应焓为 844 kJ/kg。Hutchings等人[21]发现,经过100次循环测试后,Co3O4/CoO仍具有良好循环特性,无明显性能衰减。Wong等人[18]发现,经过500次循环测试后Co3O4/CoO氧化率仍可达90%以上,氧化物颗粒尺寸随着循环次数增加;比表面积对于反应性能具有重要影响,且可通过调节反应气氛实现体系的等温反应,以达到更高的效率。
在锰氧化物反应体系中,存在4种氧化物之间的变化(MnO2↔Mn2O3↔Mn3O4↔MnO)。在空气氛围中,温度约为500 ℃时,MnO2能够还原为Mn2O3,但未发现Mn2O3在空气氛围中的氧化过程[18]。上述氧化过程需要在纯氧以及300 MPa的压力下才能发生,条件苛刻[22]。Mn3O4/MnO的反应平衡温度为 1700 ℃,超过了材料的熔点(1567 ℃),将引起较严重的烧结现象,影响材料循环特性[22]。在空气氛围下,Mn2O3/Mn3O4的反应温度区间为600~ 1050 ℃[23],该温度较适合太阳能热发电储能系统。由于氧化过程受限,单一的Mn2O3/Mn3O4体系的可逆反应率较低。Karagiannakis等人[24]研究了Mn2O3/ Mn3O4颗粒堆积床反应器,最高转化率只有50%, 氧化放能密度约为110 kJ/kg。Mn2O3/Mn3O4的氧化特性与其形态特征密切相关,较细颗粒的材料能够降低氧化温度,但更容易导致循环性能衰减[25]。Mn2O3/Mn3O4体系由于其低成本及低毒性,仍被认为是一种潜力材料。
CuO/Cu2O体系的平衡温度约为1100 ℃,与其融化温度(1232 ℃)接近,因此需控制运行温度避免造成严重的晶粒粗化[18]。CuO/Cu2O经过 20次循环反应后,仍然可以保持较一致的热重反应特性,而在堆积床反应器中则出现了烧结的颗粒小球[26]。Alonso等人[27]设计搭建了一个旋转炉式CuO/Cu2O太阳能反应器,利用聚光太阳辐射加热使其发生还原吸热反应;结果表明,CuO/Cu2O在氩气氛围中还原率可达80%,在空气氛围中还原率为40%,氧化率仅为9%。
早在20世纪70年代,Bowrey和Jutsen[28]已经测试了BaO2/BaO体系,经过5次氧化还原反应之后,该体系无明显的衰减迹象,最大氧化还原率可达93%。Fahim和Ford[29]则发现经过20次循环测试后,BaO2/BaO体系出现了较严重的性能衰减;氧化过程中,在BaO表面形成的BaO2层阻碍了氧气扩散,从而减缓了氧化过程。
稳定的气体扩散通道是保证氧化还原可逆性的必要条件。样品的制备过程对反应具有重要影响。溶胶-凝胶法制备的样品相比水热法具有更好的循环稳定性[30]。Carrillo等人[31]通过预煅烧制备的BaO样品可以完成30次以上无明显衰减的氧化还原循环反应。
Fe的氧化物储量丰富,且反应特性研究较多,主要有Fe2O3/Fe3O4体系以及Fe3O4/FeO体系。Fe3O4/FeO的反应温度过高(>2000 ℃),难以工程化实施;Fe2O3/Fe3O4体系在空气氛围中的平衡温度为1361 ℃,在氩气氛围中的平衡温度为1145 ℃[32]。Fe2O3/Fe3O4体系的氧化温度区间为750~900 ℃,氧化过程分为2个阶段:初始阶段可以用成核及生长过程描述;随着氧化反应在表面持续进行,氧气通过产物表层进行扩散,进入速率控制阶段[33]。虽然铁氧化物反应温度高,但可作为低成本的掺杂材料。
综上,对于单一的金属氧化物,Co3O4/CoO具有良好的反应动力学及循环稳定性,是一种较理想的潜在热化学储能材料[34]。但钴的储量少、成本高,对其掺杂低成本其他金属元素是一种有效降低成本的方法[25]。单一的CuO/Cu2O、Mn2O3/Mn3O4、BaO2/BaO以及Fe2O3/Fe3O4仍需要进一步提高循环稳定性、反应速率,特别是氧化过程的性能。掺杂混合是提高反应性能的一种重要方法,通过引入另一种不同大小及氧化态的金属元素,造成晶格畸变以及电荷不平衡,增加晶体中空穴的密度,提高氧的扩散速率,从而提高氧化性能。
1.2 混合金属氧化物
Co3O4/CoO经过Fe掺杂之后,反应温度与单一Co3O4/CoO相近,但其反应焓明显降低,微观结构稳定性和循环可逆性有较大提升。当Fe的摩尔分数为10%时,可在反应焓的降低及稳定性的提高方面取得合理的折中[35]。Pagkoura等人[36]利用混合Co3O4/CoO制成颗粒小球,经过10次循环测试后,Al或者Fe掺杂后的样品能够保持小球结构;用单一Co3O4/CoO制成的蜂窝状模块在多次循环后发生了严重的变形开裂,而掺杂Al之后,膨胀度大幅减小,储能模块的循环稳定性提高。然而当Co3O4和Mn2O3混合后,其反应性能比单一的氧化物差,同时Ni、Mg及Cu的掺杂对Co3O4/CoO体系的氧化还原性能无明显影响[19]。
Mn2O3/Mn3O4体系安全、储量丰富,但其反应性能较差。Fe掺杂能够提高Mn2O3/Mn3O4体系的氧化速率及循环稳定性。当Fe/Mn的摩尔比为1:4时,测得该混合物的还原起始温度为995 ℃,反应焓为219 kJ/kg[37];当Fe/Mn的摩尔比为1:3时,通过STA测得其反应焓为271 kJ/kg[38];当Fe/Mn的摩尔比为1:2时,还原反应起始温度为999 ℃,反应焓为233 kJ/kg[39]。Wokon等人[40]利用混合物(Mn0.33Fe0.67)2O3制成直径0.5~1.0 mm的颗粒球,利用堆积床测得其反应焓为200 kJ/kg。经模型计算得,反应的前80%受制于内部气体扩散,后20%则受限于外部气体扩散。Mn2O3/Mn3O4的还原温度以及反应焓随着Fe掺杂量并没有明显改变,表明Fe在混合物中参与了氧化还原反应,而并非惰性材料(Fe2O3的还原温度在1300 ℃以上,远高于该混合物的还原温度)。立方尖晶石的形成很可能提高了混合物的氧化性能[41]。
肖刚等[42]对掺杂CuO/Cu2O进行了实验研究,结果表明:单一CuO/Cu2O粉末的循环反应再氧化(放热)速率缓慢;Al掺杂后能使样品在保持稳定循环性能的情况下显著提高Cu2O氧化生成CuO的反应速率;当Al2O3的掺杂质量分数为10%时,样品反应效果最佳,其氧化反应活化能从1052 kJ/mol减小至563 kJ/mol。
1.3 钙钛矿型金属氧化物
钙钛矿型金属氧化物属于混合型金属氧化物,但具有相似的特殊结构ABO3-δ,其可逆反应可表示为ABO3-δ↔ABO3-δ-Δδ+Δδ/2O2。其中非化学计量比δ与反应温度以及氧分压有关,具有较宽的反应区间,在该区间内可连续发生反应,这与单一金属氧化物具有1个明显的平衡温度点不同。因此,钙钛矿型金属氧化物具有灵活的温度区间,与不同温区的太阳能集热相匹配。在B位上的多价阳离子主要为Mn、Co、Cu或Fe。在晶相不发生不可逆变化的条件下,非化学计量比变化Δδ可达0.5。此外,还可以在A位和B位上进行掺杂,对反应特性进行调控。钙钛矿型金属氧化物作为载氧体在化学链燃烧以及化学链重整领域已有较多研究,其反应特性要求与热化学储能类似[43-45]。
在A位进行Sr掺杂的CaMnO3-δ能够完成循环1000次以上(500~1000 ℃),比无掺杂样品有很大提高,其反应焓可达320~555 kJ/kg[46]。Jackson等人[47]比较了Sr掺杂的CaMnO3-δ以及硅铝基的惰性颗粒在太阳能储能中的应用,结果表明钙钛矿型金属氧化物在太阳能高温热发电储能中具有较大优势。表2总结了钙钛矿型金属氧化物的相关研究。
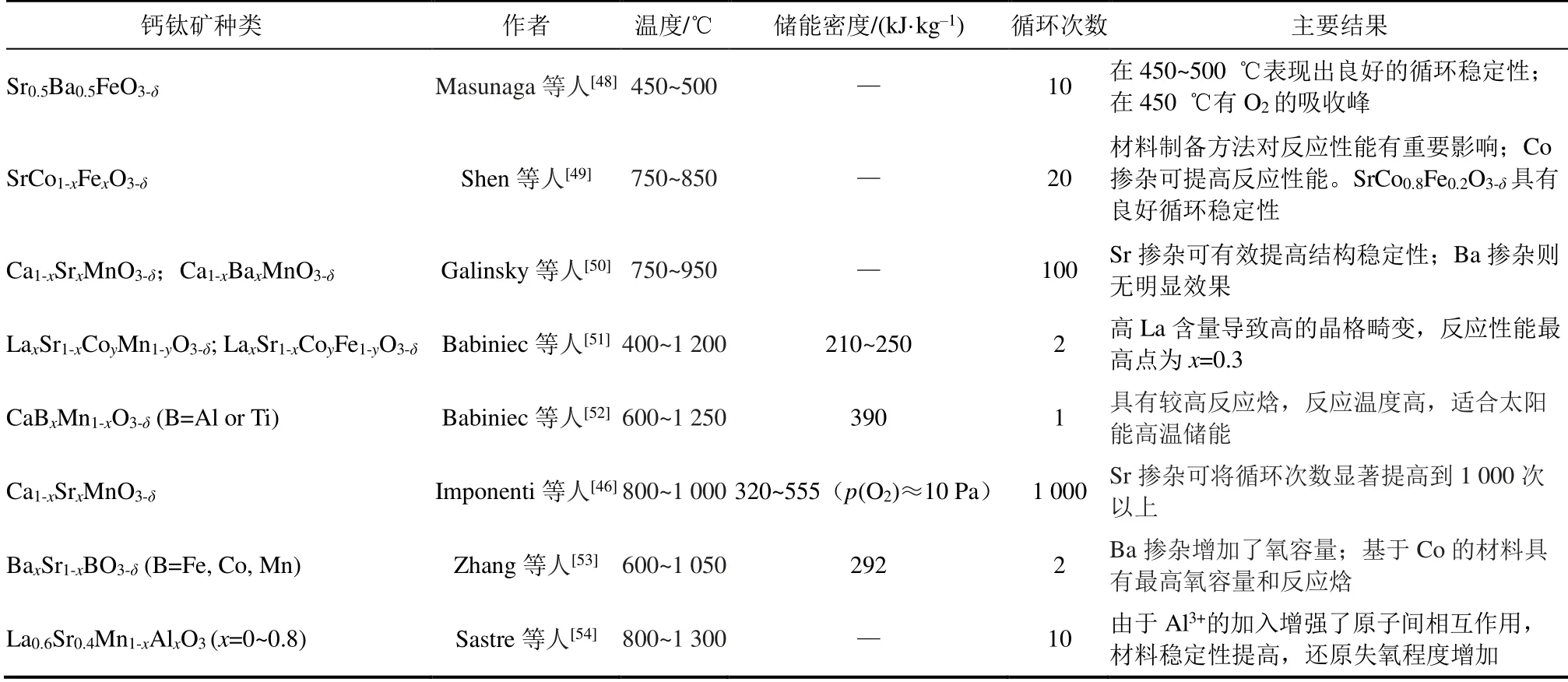
表2 钙钛矿型金属氧化物研究总结Tab.2 A summary of researches on perovskite metal oxides
2 反应模型
储能金属氧化物的氧化还原反应属于气固两相反应,过程复杂,影响因素较多。为进一步提高金属氧化物反应性能,还需从微观层面对材料结构进行研究,从理论上指导材料的改性,提高试验试错效率。
2.1 动力学模型
金属氧化物的反应动力学可以从热重实验数据得出,根据阿伦尼乌斯方程计算反应常数k:
式中:A为指前系数;EA为反应活化能;R为气体常数;T为反应温度。反应速率与反应常数及反应机理函数f(α)有关:
式中:t为时间;α为反应转化率。
式中:M0、Mt、和M∞分别为样品的初始质量、在t时刻的质量以及反应终了时的质量。表3总结了不同反应机理函数[55]。
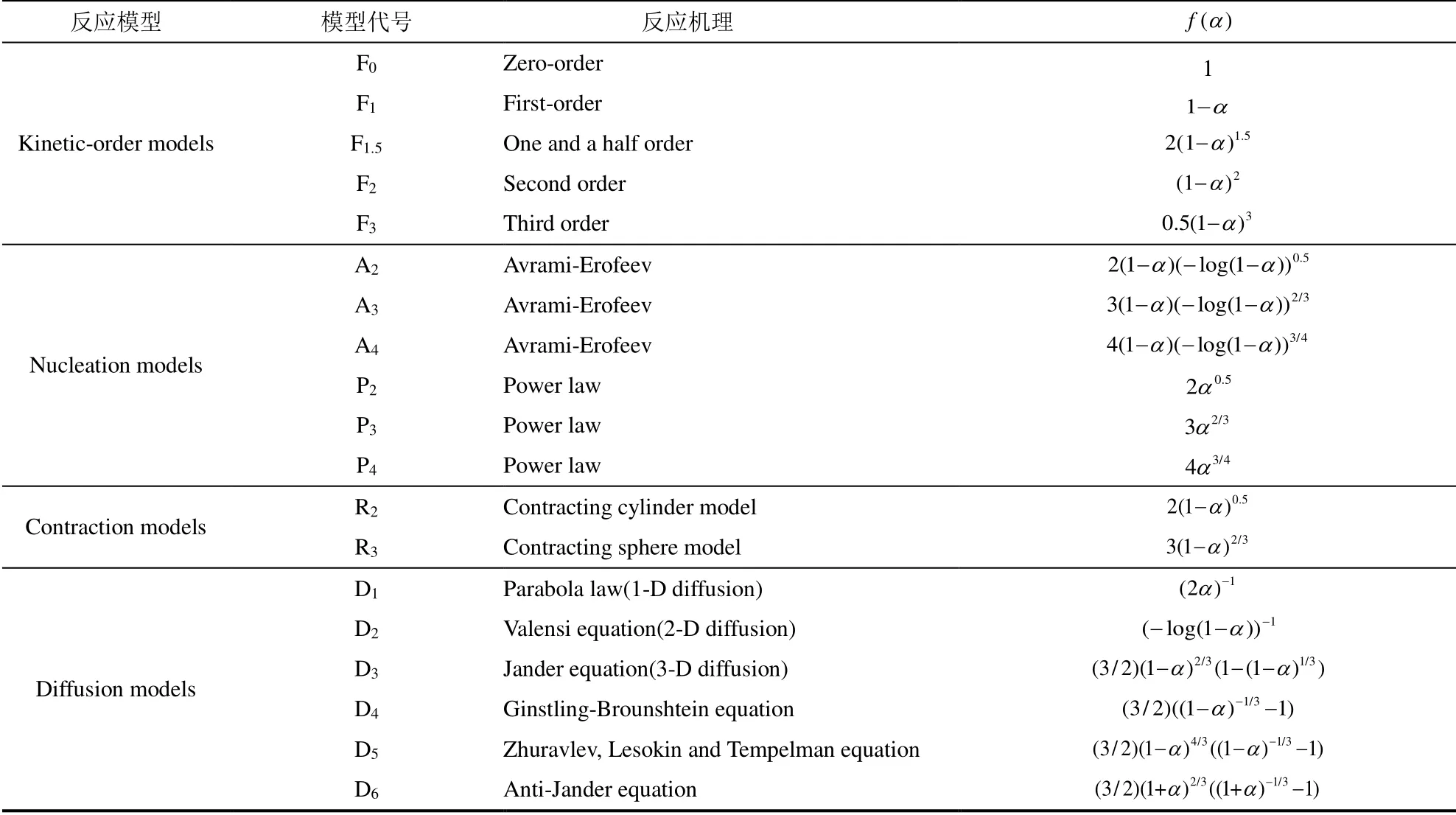
表3 适用于气固反应的机理函数Tab.3 Mechanism functions for gas-solid reactions
反应气氛对反应过程具有重要影响,如果气体产物不及时分离,反应将趋于平衡[56]。氧分压peq与平衡温度Teq间的关系从吉布斯方程导出[38]:
式中:Keq为平衡常数;下标0表示标准状况;ΔH为反应焓;ΔS为反应熵。从式(4)可以看出,氧分压的对数与平衡温度的倒数呈线性关系。考虑氧分压的影响,式(2)可表示为[56]:
式中h(p)是压力影响因子。推荐的压力影响因子可表示为[56]:
基于阿伦尼乌斯方程的反应速率计算方法没有考虑反应过程中的传热传质现象,而反应速率与反应器尺寸等具体设计参数密切相关。Pagkoura等人[36]提出了一种简化的动力学模型,与实际试验结果相吻合:
式中:kred和koxi分别为还原过程和氧化过程的反应常数,可用阿伦尼乌斯方程表示。
2.2 第一性原理研究
第一性原理研究能够获得体系的薛定谔方程的基本参数,比如电子质量和原子数等。广义第一性原理研究可分为从头算方法和密度泛函理论(DFT)。第一性原理已经广泛应用于能带结构模拟、电荷分布等微观结构分析。
对钙钛矿型金属氧化物La0.5Sr0.5MnO3的DFT计算表明,由于吸附能差异,O2优先吸附在Mn位而不是La位,说明对于还原过程,B位的阳离子比A位的阳离子更具有活性[57]。Kotomin等人[58]利用第一性原理计算了Ba1-xSrxCo1-yFeyO3-δ中氧空位的形成与迁移能,可用电子结构解释越低的氧空位形成能对应越低的迁移能现象。Curnan等人[59]基于DFT方法研究了钙钛矿型金属氧化物中氧空位形成能,当晶胞尺寸大时,氧空位更易形成,而在菱形和正交畸变钙钛矿中氧空位不易形成。Vieten等人[60]基于DFT方法提出了一种钙钛矿型材料的设 计方法,计算了超过240种复杂钙钛矿材料的反应焓,归纳了基于反应焓的经验公式,并用实验进行了验证,结果表明该种计算方法可有效应用于设计性能优良的钙钛矿材料。
3 反应器及储能系统
金属氧化物作为储热介质的同时,又可以作为传热介质。基于金属氧化物的储能系统可分为直接储能系统与间接储能系统。在间接储能系统中,空气作为传热介质在太阳能吸热器中被加热,再进入堆积床中,加热其中由金属氧化物制成的多孔储能介质。在直接储能系统中,金属氧化物颗粒在吸热/反应器中直接吸收高倍聚光,发生还原反应,吸收存储热量,还原后的金属氧化物颗粒进入储罐中存储。
蜂窝状或者泡沫状的多孔结构金属氧化物模块适合于堆积床储能系统。多孔储能模块可通过金属氧化物整块压制以及在惰性基底涂层2种方法制 成。Agrafiotis等人[61]使用在惰性蜂窝陶瓷以及泡沫陶瓷基底涂层的方法制成储能模块,当负载质量分数达到200%,经过100次循环时,仍能保持稳定的动力学特性。Karagiannakis等人[62]在电加热炉中测试了整体挤压成型的蜂窝陶瓷储能模块,发现单一Co3O4/CoO样品经过反应循环后发生明显膨胀,导致结构开裂;而掺杂了Al之后的样品可将循环次数提高到100次以上而不发生明显的结构破坏。
Tescari等人[63]建立了小型金属氧化物储能示范系统,利用88 kg的CoO在惰性堇青石蜂窝陶瓷上涂覆制成储能模块,其系统示意如图1所示。试验经历了22次储放能过程,其热化学储能密度相比惰性蜂窝陶瓷显热储能提高1倍。
上述堆积床中的储能模块需通过空气间接加热,而在太阳能颗粒吸热器中,金属氧化物颗粒可以被太阳光直接加热发生还原吸热反应。Neises等人[64]利用回转炉式颗粒吸热器直接加热CoO颗粒,利用石英玻璃密封入射光孔,通过监测氧浓度间接测量反应速率(图2),经过聚焦太阳光加热至900 ℃,约50%的储能材料被还原(95 kW·h/m3),移除聚焦太阳能后被氧化放热,且经过30次以上循环后,没有发现明显的衰减迹象。
Albrecht等人[65]提出了利用钙钛矿型金属氧化物颗粒(Ca0.9Sr0.1MnO3-δ)吸热的储热系统,用于提高太阳能储能密度和温度(700~1100 ℃),但需在吸热器中保持低氧环境(氧分压10~1000 Pa),设计并比较了真空泵系统和惰性气体扫气系统,两者的太阳能光电转化效率都能达到30%以上。Gorman等人[66]提出了基于钙钛矿型金属氧化物储能的空气布雷顿循环系统,建立了一维准稳态模型,包括吸热/反应器、热罐、冷罐、动力循环装置、氧化放热器等,由于透平温度较低,该动力循环的热效率约为30%。Schrader等人[67]分析了利用Co3O4/CoO进行高温储能的空气布雷顿循环系统,如图3所示,当热化学反应温度为1050 K、压比为30时,该系统最大循环热效率可达44%。
4 S-CO2与储能耦合系统
S-CO2布雷顿循环热效率高、系统紧凑、无需水冷,有望替代传统太阳能热发电系统中的水蒸气朗肯循环[68-69]。本文提出了100 MW太阳能S-CO2布雷顿循环与金属氧化物储能耦合系统(图4),包括热化学 颗粒储放热子系统及S-CO2布雷顿循环子系统。
图5总结了多种金属氧化物反应温度和反应焓的特性分布及对于布雷顿循环及联合循环的储能适用情况。对于S-CO2循环,Mn2O3/Mn3O4具有合适的反应温度(700~1000 ℃)以及较低的成本,本文将其作为潜在储能材料。
利用热重分析仪(Hitachi STA 7200),在合成空气(体积分数为20%O2+80%N2)流速为50 mL/min、升降温速率为20 ℃/min时,测试了单一Mn2O3/ Mn3O4以及Fe掺杂样品(摩尔分数为20%,通过柠檬酸溶胶-凝胶法制成)的循环反应性能,结果如 图6所示。结果表明:单一样品在还原过程中质量减少3.38%,与理论值相符,但其难以完成氧化放能过程;掺杂样品的氧化还原率为3.33%,与理论值接近,表明Fe掺杂能够大幅提高氧化过程的反应性能。
本文基于再压缩S-CO2循环进行改进。将循环中S-CO2回热分为高温回热和低温回热2部分。经过低温回热器冷却后的S-CO2一部分进入预冷器冷却后进入压缩机,另一部分直接进入再压缩机。通过再压缩技术降低了低温回热器中由于S-CO2物性剧烈变化导致的窄点温差,大幅提高了回热效率。进一步利用再热提高透平做功能力,利用间接冷却降低压缩机耗功。建立了基于Aspen Plus的系统稳态模型,主要参数见表4。系统热效率随着透平进口温度(TIT)以及进口压力的提高而提高,但边际效果逐渐降低,如图7所示。考虑系统材料性能以及成本因素,选择透平进口最高温度为700 ℃,透平进口压力为26 MPa,此时系统的热效率为51.2%。
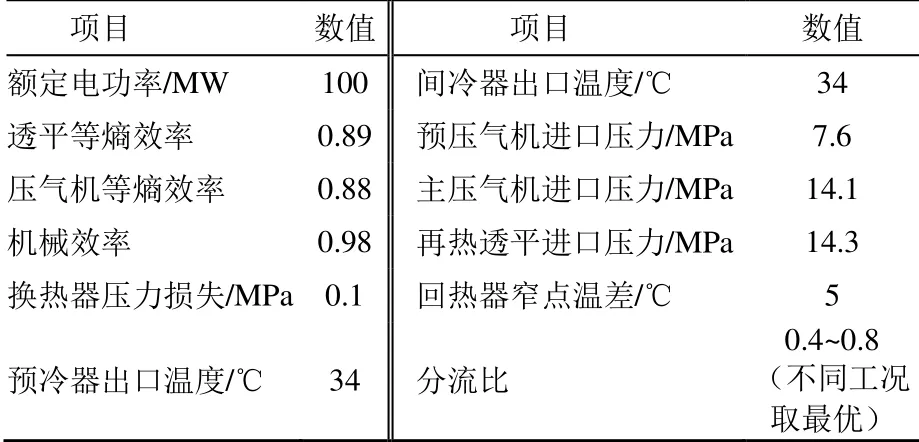
表4 S-CO2循环系统主要参数Tab.4 Main parameters of S-CO2 cycle system
系统中加热器和再热器采用流化床形式的氧化反应器,具有高的传热系数和操作温度区间,同时流化空气可作为氧化剂。本文设计了4级流化床系统,其中3级作为加热器,另外1级作为再热器(图8)。经过模拟计算,当流化数为1.5时,该流化床的换热系数可达590~860 W/(m2·K)。利用空气回热器收回流化气体的热量,可将流化床的热效率提高到98%以上。
该太阳能热发电系统的设计地理位置为甘肃玉门,模拟时间为春分日,主要参数见表5。根据蒙特卡洛光线跟踪方法,编制了MATLAB定日镜场聚光模拟软件。经过定日镜场优化排布及聚光模拟,春分日中午定日镜场光学效率分布如图9所示,典型晴朗春分日逐小时系统性能如图10所示。最大储能材料为20340 t,满足1天24 h稳定发电,系统平均光电转换效率为25.2%,比目前熔盐储热系统高约10百分点。
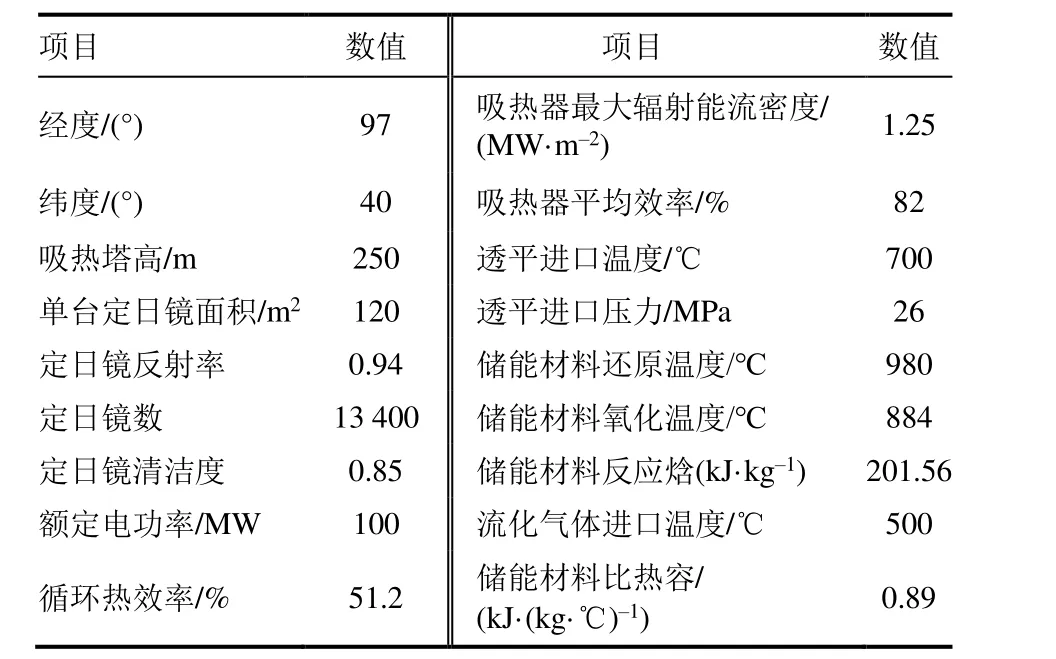
表5 太阳能S-CO2循环电站主要参数Tab.5 Main parameters of the solar S-CO2 cycle power plant
5 结 语
基于金属氧化物可逆氧化还原的高温热化学储放能,在下一代太阳能高温热发电系统中具有重要应用价值。本文对单一金属氧化物以及混合氧化物进行了详细的分析总结。单一金属氧化物反应性能受制于反应动力学和循环稳定性,而对其进行掺杂改性可以大幅提高材料的储放能特性。本文基于Fe掺杂Mn2O3/Mn3O4储能颗粒构建了100 MW太阳能S-CO2布雷顿循环系统,并建立了其稳态模型,得到典型晴朗春分日系统最大热效率可达51.2%,平均太阳能光电转换效率可达25.2%。由于储能系统的加入,该系统可实现24 h不间断运行。
需要指出的是,金属氧化物热化学储能与实际推广应用仍有不小差距,需要进一步提高其反应性能,进行实验室以及中试规模的验证;应重点关注通过原子层面的微观改性研究,提高设计预测材料反应温度、反应焓、循环稳定性等反应特性能力,有效指导试验研究。

