前列环素联合神经肽Y对糖尿病肾病心血管不良事件的预测价值
董小伟,齐 琳,房勃龙,郝 玉,贾慧彦,朱永栋,顾红兰,刘红梅
糖尿病肾病是一种由长期高血糖引起的肾脏微血管病变,为终末期肾病的主要病因之一,亦是动脉粥样硬化的独立危险因素[1]。既往研究显示,糖尿病肾病患者发生以动脉粥样硬化为基础的心血管疾病风险明显增高,与钙磷代谢紊乱、血管中膜钙化、动脉僵硬度增大有关[2]。鉴于糖尿病肾病患者的早期动脉粥样硬化病情较隐匿,且目前临床尚缺乏特异、敏感的检测手段。因此,在糖尿病肾病患者中寻找能筛查动脉粥样硬化并预测心血管不良事件的血液学指标,对于指导临床诊治极其重要。内皮细胞功能障碍可能是动脉粥样硬化的始动机制之一[3]。前列环素(PGI2)是外周循环中最强的舒张血管因子之一,神经肽Y(NPY)是促进血管收缩的长效物质,二者比例失衡,可能预示着内皮功能障碍,存在动脉粥样硬化,对于预测心血管不良事件具有一定价值[4-5]。本研究分析PGI2联合NPY对糖尿病肾病患者发生心血管不良事件的预测价值。
1 资料与方法
1.1临床资料 选择我院2017年1月—2018年5月收治的糖尿病肾病196例作为研究对象。纳入标准:均符合糖尿病肾病的临床诊断标准[6];年龄40~75岁;按照《糖尿病肾病防治专家共识(2014年版)》[7]的要求规范治疗,严格控制血糖及其他危险因素;病情稳定,生命体征基本正常;知悉研究内容,配合治疗和随访。排除标准:合并严重的心、肝功能损伤,肾炎综合征,恶性肿瘤者;糖尿病相关急性并发症者;有急性心血管事件病史者;终末期肾病阶段者;临床资料不全者。根据心血管不良事件发生情况分为发生心血管不良事件组34例和未发生心血管不良事件组162例。
1.2方法
1.2.1血浆PGI2、NPY检测:所有患者入组24 h内,收集清晨空腹静脉血5 ml,3000 r/min离心10 min,分离血浆,使用酶联免疫吸附试验检测血浆PGI2水平,检测试剂盒来源于北京拜尔迪生物技术有限公司;使用放射免疫分析法检测血浆NPY水平,检测试剂盒来源于上海信裕生物技术有限公司。检测方法严格按照试剂盒说明书进行操作。
1.2.2动脉粥样硬化指标检测:使用美国GE Voluson S8彩色多普勒超声诊断仪对颈动脉和下肢动脉进行超声检查,检测颈动脉内-中膜厚度(CIMT)、颈-股动脉脉搏波速度(CFPWV)和股动脉内-中膜厚度(FIMT),其中CIMT指动脉腔-内膜界面与中层-外膜界面间的距离,CFPWV=颈动脉和腹股沟动脉搏动最明显处体表距离/脉搏波传导时间。
1.2.3临床资料:收集两组性别、年龄、体质量指数、吸烟史、饮酒史、高血压病、冠心病、心率、陈旧性心肌梗死、既往行经皮冠状动脉介入(PCI)术、总胆固醇、三酰甘油、血钙、血磷、PGI2、NPY、CIMT、FIMT、CFPWV。
1.3观察指标 所有患者均随访36个月,观察心源性死亡、休克、恶性心律失常、心肌梗死等心血管不良事件发生情况,比较两组血浆PGI2、NPY水平及动脉粥样硬化指标,分析血浆PGI2、NPY水平与动脉粥样硬化指标的关系及影响糖尿病肾病患者发生心血管不良事件的独立危险因素,同时评价血浆PGI2联合NPY对心血管不良事件的预测效能。
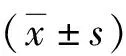
2 结果
2.1临床资料比较 发生心血管不良事件组与未发生心血管不良事件组在冠心病、三酰甘油、PGI2、NPY、CIMT、FIMT、CFPWV方面比较差异均有统计学意义(P<0.05,P<0.01)。见表1。
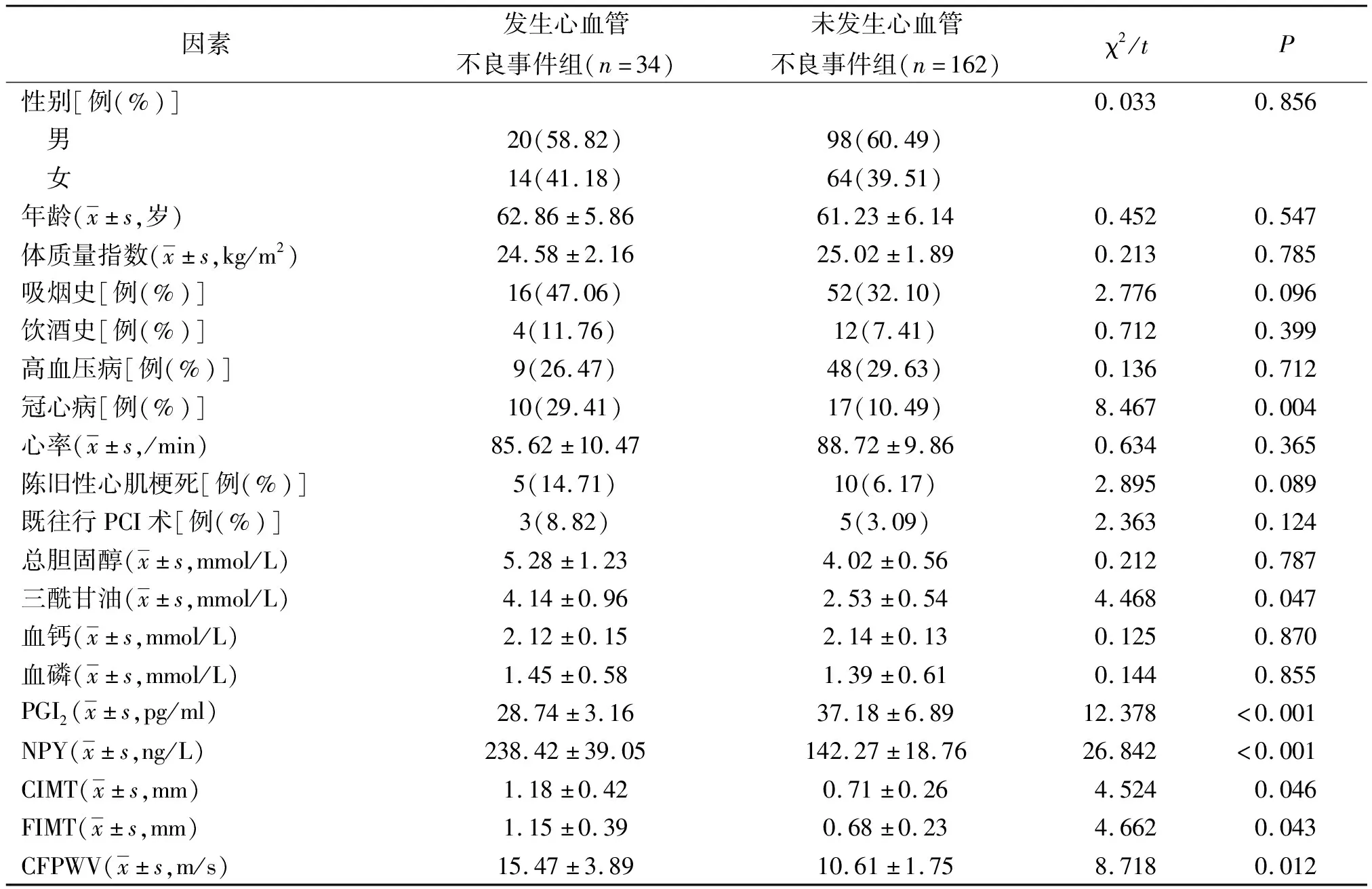
表1 是否发生心血管不良事件糖尿病肾病两组的临床资料比较
2.2多因素Logistic回归分析 以心血管不良事件为因变量,上述单因素分析中差异有统计学意义的指标为自变量,赋值如下:冠心病:有=1,无=0;三酰甘油≥4.14 mmol/L=1,<4.14 mmol/L=0;PGI2≥28.74 pg/ml=1,<28.74 pg/ml=0;NPY≥238.42 ng/L=1,<238.42 ng/L=0;CIMT≥1.18 mm=1,<1.18 mm=0;FIMT≥1.15 mm=1,<1.15 mm=0;CFPWV≥15.47 m/s=1,<15.47 m/s=0。赋值后纳入多因素Logistic回归分析,显示血浆PGI2、NPY和CFPWV均是糖尿病肾病患者发生心血管不良事件的独立危险因素(P<0.01,P<0.05)。见表2。

表2 糖尿病肾病患者发生心血管不良事件的影响因素多因素Logistic回归分析
2.3血浆PGI2、NPY与动脉粥样硬化指标的相关性 经Pearson相关性分析,糖尿病肾病患者CIMT、FIMT、CFPWV均与血浆PGI2水平呈负相关,与NPY水平呈正相关(P<0.05,P<0.01)。见表3。
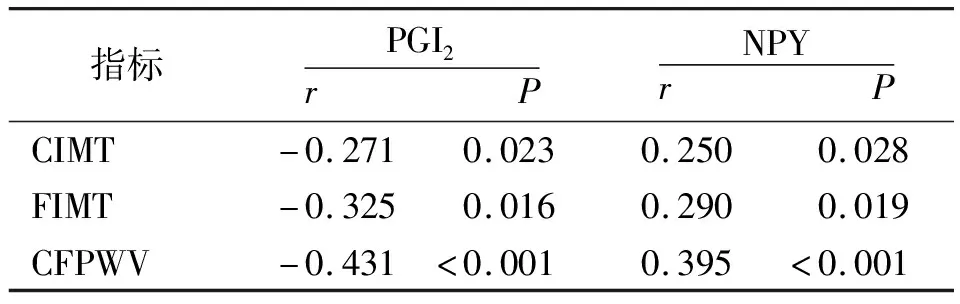
表3 血浆PGI2、NPY与动脉粥样硬化指标的相关性分析
2.4血浆PGI2联合NPY对心血管不良事件的预测效能 经ROC曲线分析显示,血浆PGI2联合NPY预测心血管不良事件发生的AUC均大于血浆PGI2、NPY单独检测及CFPWV(P<0.01)。见表4、图1。

图1 血浆PGI2联合NPY对糖尿病肾病心血管不良事件的预测效能ROC曲线
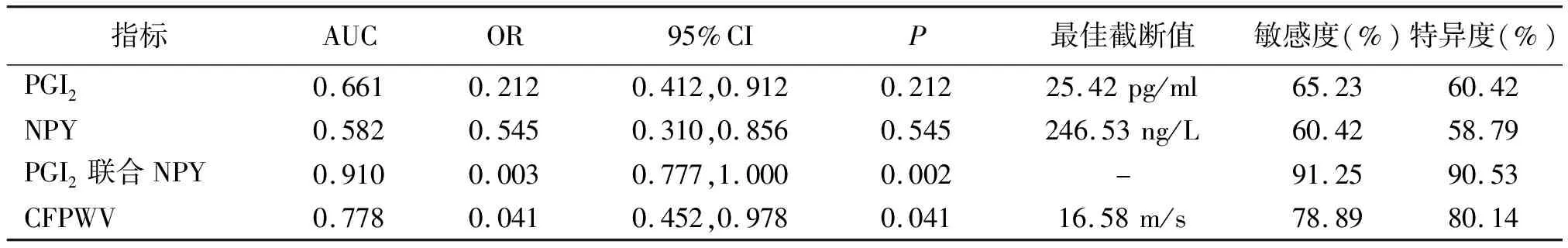
表4 血浆PGI2联合NPY对糖尿病肾病患者心血管不良事件的预测效能
3 讨论
糖尿病肾病患者发生心血管不良事件的机制至今仍未完全阐明,可能与动脉粥样硬化密切相关。PGI2和NPY均为与内皮和血管平滑肌细胞损伤密切相关的血管活性物质,可能对筛查动脉粥样硬化,预测心血管不良事件具有积极作用。既往研究表明,PGI2可通过一系列信号转导,最终发挥舒张血管平滑肌,松弛、扩张血管的作用[8]。在糖尿病肾病这一病理条件下,血管平滑肌细胞合成PGI2的能力减弱。NPY是一种由血管内皮细胞合成的神经肽,具有强烈、持久的血管收缩功能[9]。鉴于长期高血糖不可避免地影响血管张力,在糖尿病肾病患者尤为显著,预示着血管内皮细胞PGI2与NPY的动态平衡已被打破,提示血浆PGI2、NPY水平明显异常。VOCAT等[10]研究显示,糖尿病肾病患者继发的微血管损伤,可导致患者自身代偿引起血浆NPY水平升高,并抑制PGI2生成。本研究结果显示,发生心血管不良事件组血浆PGI2水平低于未发生心血管不良事件组,NPY水平高于未发生心血管不良事件组。与PODZIMKOVA等[11]研究结果相符,提示血浆PGI2水平下降和NPY水平升高可能是糖尿病肾病患者发生心血管不良事件的危险因素。
本研究结果还显示,发生心血管不良事件组CIMT、FIMT、CFPWV均大于未发生心血管不良事件组,与王漪芸等[12]的研究结果相似,然而上述指标易受年龄、血压和血脂等因素的影响,与动脉粥样硬化进程并不平行。基于内皮功能障碍可能早于糖尿病肾病患者伴发动脉粥样硬化的这一观点,本研究发现,糖尿病肾病患者CIMT、FIMT、CFPWV均与血浆PGI2水平呈负相关,究其原因为内皮细胞受损可驱使单核细胞定向黏附于血管壁,进而启动动脉粥样硬化。也有研究显示,在动脉粥样硬化的同时,血管腔内血红蛋白增多并迅速与PGI2结合,耗竭血管平滑肌细胞产生的PGI2,亦佐证了上述观点[13]。本研究结果还显示,糖尿病肾病患者CIMT、FIMT、CFPWV均与血浆NPY水平呈正相关,与CHANG等[14]研究结果相符。分析原因:NPY促进动脉血管平滑肌细胞增殖、巨噬细胞聚集和血小板黏附,从而促进动脉粥样硬化。此外,PGI2与NPY存在负反馈调节机制,当血浆NPY水平升高,对PGI2的抑制作用增强,加剧动脉粥样硬化的病变发展。MAZZONE等[15]研究显示,冠状动脉粥样硬化斑块内巨噬细胞中PGI2含量下调。也有研究显示,NPY与血管炎症反应、血管形成和动脉粥样硬化斑块破裂相关[16]。上述研究均提示血浆PGI2水平下降和NPY水平升高与糖尿病肾病患者动脉粥样硬化有关。
本研究196例糖尿病肾病患者中,均获得36个月的随访,心血管不良事件发生率为17.35%,略低于既往报道数据[16],考虑可能与随访时间不同有关。隋准等[17]研究认为,糖尿病肾病患者随着肾功能下降,内皮功能障碍程度逐渐增高,血浆PGI2水平降低和NPY水平升高。本研究结果显示,血浆PGI2、NPY均是糖尿病肾病患者发生心血管不良事件的独立危险因素。由此认为,糖尿病肾病患者血浆PGI2与NPY水平的动态平衡遭到破坏,需警惕心血管不良事件的发生。本研究ROC曲线分析显示,血浆PGI2联合NPY预测糖尿病肾病患者发生心血管不良事件的效能较好。考虑原因可能在于血浆PGI2和NPY水平失衡,导致血管内皮细胞的异常迁移、增殖和血管新生内膜形成,并促进动脉血管平滑肌细胞增殖、巨噬细胞聚集,增强了血小板的生物学效应,上述机制协同加剧动脉粥样硬化的发生发展。本研究可为临床监测糖尿病肾病患者血浆PGI2、NPY水平变化提供依据,对评估患者病情演变具有积极作用,可指导临床糖尿病肾病患者终点事件的防治。
综上所述,血浆PGI2水平下降和NPY水平升高与糖尿病肾病患者动脉粥样硬化有关,二者联合预测心血管不良事件发生的效能较好。但是,本研究为单中心研究,随访时间较长,且缺少对血浆PGI2和NPY水平的动态观察,未分析二者与患者远期预后的关系,未来还需要扩大研究规模,延长随访时间,在更大范围糖尿病肾病人群中进行PGI2和NPY的动态观察,以深入分析二者在糖尿病肾病患者心血管损伤中的作用机制。

