可用于低中温热能储存的四元硝酸盐/埃洛石/石墨定型复合材料的制备与研究
李钰颖,魏雯珍,李 琦,吴玉庭
(北京工业大学环境与能源工程学院,传热强化与过程节能教育部重点实验室,传热与能源应用北京市重点实验室,北京 100124)
能源的日益消耗和碳排放的日益增长对全球生命系统造成了严重的威胁,节能减排成为了发展的主旋律。优化能源结构,大力发展可再生能源是实现双碳目标的重要举措之一。近年来,作为可调、输出稳定、连续的一种可再生能源,太阳能热发电的发展迅猛,成为中国新能源发展的主力[1-3]。而在发电系统中增加储热环节,可以减小接入电网时带来的系统波动,同时可以按电力系统的供需平衡适时调节功率,既提高了系统运行的安全性和经济性,也增加了灵活性[4]。
储热技术是将太阳能光热、工业余热、地热、废热等热能储存在储热材料中,在需要时释放的一种技术,可以达到时间、空间或热能供需之间的平衡,具有系统结构简单、较低初投资、应用价值较高等优点,成为扩大可再生能源利用规模,提升利用效率的有效途径[5-7]。储热技术中的相变储热技术因工艺简单、储热密度高的优点,成为研究与应用的热点[8-10]。熔融盐相变材料的热容量较大,适用温度范围广、稳定性较好、因此具有巨大的发展潜力,但易泄漏、易腐蚀、热导率较低的缺点阻碍了实际应用[11-13]。
国内外学者对熔融盐储热相变材料进行了广泛的研究。王军涛等[14]通过Toop 模型预测摩尔配比为12.2%NaNO3-54.8%KNO3-33%Ca(NO3)2三元硝酸盐的相图,并用实验验证该熔融盐的熔点为127.1 ℃,分解温度为500 ℃。为防止相变材料堵塞管道、增加运行成本的风险,所需的熔融盐应有较低的熔点。Raade等[15]通过试配法得到由LiNO3、NaNO3、KNO3、CsNO3、Ca(NO3)2组成的五元硝酸盐,其质量比为8∶6∶23∶44∶19,测试得到该五元硝酸盐的熔点低至65 ℃。
为克服硝酸熔融盐易泄漏、易腐蚀的缺点,不少学者在相变蓄热材料中添加支撑材料进行研究。Jiang 等[16]在LiNO3-KNO3-NaNO3-Ca(NO3)2共 晶 硝酸盐中添加10%~40%的硅酸钙作为结构支撑材料,经烧结发现硅酸钙质量比达到20%时复合相变定型材料无泄漏现象。Sang 等[17]将MgO 作为支撑材料,与由碳酸钾、碳酸锂和碳酸钠组成的混合碳酸熔盐分别以3∶7、4∶6、5∶5、6∶4、7∶3的质量比通过冷压-热烧结法制备定型相变材料,结果显示当MgO 的质量比为50%时可以克服泄漏问题。
热导率低是熔融盐实际应用的一大阻碍,提高相变材料的热导率成为研究热点。Ren等[18]以低成本的Ca(NO3)2-NaNO3二元熔盐为相变材料,膨胀石墨(EG)为支撑材料和导热增强剂,实验表明,加入7%(质量分数,下同)的EG可以很好地克服漏液问题,并通过在材料内部形成的导电通道将热导率提高至少7倍。Chen等[19]通过实验确定了二元熔盐中SiO2纳米粒子的最佳粒径和最佳质量分数,发现优化后的熔盐热导率提高了20.2%。Ye 等[20]在60%Na2CO3-40%MgO 混合材料中分别添加0.1%、0.2%、0.3%、0.5%的多壁碳纳米管(MWCNTs),经测试得复合相变材料的热导率随着MWCNTs质量比的增大而提高,120 ℃时,添加0.5% MWCNTs定型材料的热导率高达1.489 W/(m·K)。
邹露璐[21]通过试配法优选出一种熔点为83.4 ℃,分解温度为628.5 ℃,潜热为74.65 kJ/kg,比热容为1.527 J/(g·K)的四元硝酸熔融盐,该优选盐的组分为7%NaNO3-40%NaNO2-53%KNO3-40%Ca(NO3)2。本工作选用该优选盐作为相变蓄热材料,晶体结构为管状的埃洛石作为结构支撑材料,热导率高于金属材料的石墨作为导热增强介质,采用冷压-热烧结方法制备成形状固定的复合蓄热相变材料。
1 样品制备及实验过程
1.1 主要材料
将硝酸钠、亚硝酸钠、硝酸钾和硝酸钙的优选共晶硝酸盐作为储热基体材料,其中4种硝酸盐均为纯度大于99%的分析纯试剂,按照一定的质量配比进行制备。选取具有中空结构的埃洛石纳米管(HNTs,Sigma-Alorich Co.LLC,USA)作为结构支撑材料,并添加一定质量分数的石墨粉提升复合相变材料的导热性能。
1.2 制备方法与实验过程
1.2.1 材料制备
复合相变材料的制备过程主要包括两个部分,分别为四元硝酸盐的制备、复合相变材料的制备。第1步,将硝酸钠、亚硝酸钠、硝酸钾和硝酸钙以质量比7∶40∶53∶20配制混合熔盐,随后放置于温度设定为450 ℃,恒温时间为24 h的马弗炉中进行干燥、加热和熔化过程。恒温结束后,将熔盐从马弗炉中取出,待其自然冷却至固态,使用研磨机研磨至粉末状,得到共晶四元硝酸盐。第2步,将四元硝酸盐与埃洛石纳米管分别按质量比3∶7、4∶6、5∶5、6∶4、7∶3进行配制,放置在密封容器中摇晃20 min 至混合均匀,将其记为样品A1、A2、A3、A4、A5。
1.2.2 实验过程
使用万能试验机将A1~A5的样品以12.229 MPa/s的速率升压至122.29 MPa 并在此压力下持续60 s后形成直径为12.5 mm、厚度为3 mm 的圆薄片,如图1(a)所示。将压制成型的样品放置在马弗炉中进行烧结,马弗炉设置升温速率为5 ℃/min,在150 ℃下恒温30 min,继续加热至250 ℃并恒温60 min。第1 段恒温过程旨在消除样品中的水分,四元硝酸盐在第2段恒温过程中达到熔点后熔化并渗入埃洛石纳米管之中。图1(a)与表1 显示出样品A1、A2、A3、A4、A5 在烧结后的泄漏情况,可以看出样品A4 表面有空隙和鼓包,说明当四元硝酸盐的含量达到60%时会发生一定的泄漏,样品A5 整体膨胀变形,发生了严重泄漏,因此,复合相变材料的最佳配比为5∶5。随后,在样品A3 中添加2%~10%石墨以提升复合相变材料的热导率,烧结前后对比图见图1(b)。

表1 复合相变材料配比及烧结后的泄漏情况Table 1 Ratio of CPCM and leakage after sintering

图1 (a)不同比例QN-HNTs;(b)QN-HNTs-C复合材料烧结前后的形貌对比Fig.1 Appearance comparison of(a)different proportions of QN-HNTs;(b)QN-HNTs-C composites before and after sintering
2 结果讨论与分析
2.1 微观结构及元素分析
2.1.1 微观结构
使用扫描电子显微镜(SEM,S4800,hitachi,日本)对复合相变材料的微观结构进行观察与分析。从图2(a)显示出埃洛石纳米管呈现中空的管状结构,图2(b)、(c)分别为复合相变材料烧结前后的微观形态,可以看出烧结之前四元硝酸盐与埃洛石纳米管为简单物理混合,熔融盐没有浸入埃洛石纳米管之中,经烧结之后埃洛石纳米管内部呈现为黑色,且没有多余块状结构,表明熔融的四元硝酸盐已浸入在埃洛石纳米管中。证明了埃洛石纳米管作为熔融盐的支撑材料时可以有效防止熔融盐发生泄漏和腐蚀。

图2 (a)埃洛石纳米管;(b)复合相变材料烧结前;(c)复合相变材料烧结后扫描电镜图Fig.2 SEM image of(a)HNTs;CPCM before(b)sintering and(c)after sintering
2.1.2 元素分布
复合材料的元素分布图可以通过X 射线能谱仪(EDS,Supra55,Caisi,德国)得到。埃洛石是天然形成的一种硅酸盐水合物,化学分子式为H4Al2O9Si2·2H2O。在复合材料中检测到Si、Al、Na、Ca、K 元素,且几种元素分布均匀,如图3 所示。这说明四元硝酸熔融盐完全浸入埃洛石纳米管之中,且两者连接成稳定的整体。
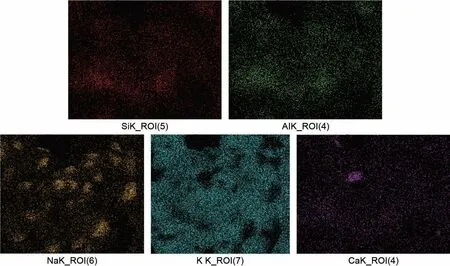
图3 复合相变材料的元素分布Fig.3 EDS elemental mapping images of CPCM
2.2 热物理性能分析
2.2.1 相变特性
分别称取10 mg 的5 种样品使用差示扫描量热仪(DSC,241 Ployma,耐驰,德国)在30~300 ℃的温度区间内进行吸热和放热测试,升温和降温速率均设置为10 K/min。图4 为四元硝酸盐、烧结后四元硝酸盐和埃洛石纳米管复合相变材料、烧结后的四元硝酸盐/埃洛石纳米管/石墨复合相变材料的DSC 曲线,测得四元硝酸盐的相变起始温度为90.9 ℃,相变峰值温度为96.7 ℃,相变终止温度为100.8 ℃,比热容为1.4 J/(g·K),潜热为78.52 kJ/kg。从表2 可以得到添加埃洛石纳米管和石墨后复合相变材料的相变峰值温度降低为94.1 ℃,相变初始温度和相变终止温度变化不足1 ℃,比热容无较大变化,说明支撑材料和导热增强材料对相变材料的热物性无较大影响。而复合材料的测试潜热较理论潜热有所下降,这是因为石墨的添加会导致潜热的少量减小[22]。
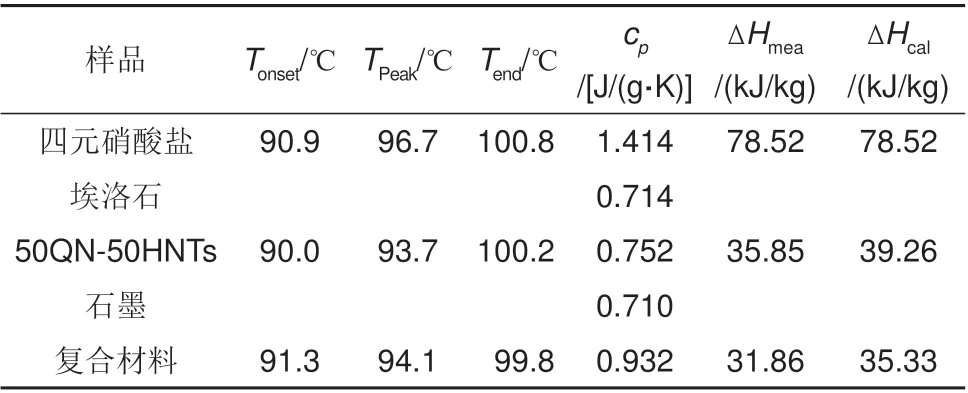
表2 四元硝酸盐、50QN-50HNTs、复合相变材料的热物性Table 2 Thermophysical properties of quaternary nitrate,50QN-50HNTs,and CPCM

图4 四元硝酸盐、50QN-50HNTs、复合相变材料DSC曲线Fig.4 DSC curves of quaternary nitrate,50QN-50-HNTs and CPCM
2.2.2 分解温度
物质的TG曲线通过热重/差热综合分析仪(TG/DTA,labsys evo,塞塔拉姆仪器公司,法国)获得。由于埃洛石是水合物,在100~550 ℃之间烧结会出现吸附水和化学水的消除,同时管壁晶体结构会转变为无定形硅铝结构,但管状形态并不会因此发生改变,且在800 ℃内具有良好的热稳定性[23-24]。因此,将材料A3置于550 ℃的马弗炉中烧结而后进行热重测试。图5显示了四元硝酸盐和复合材料的热重分析,图中可以得到四元硝酸盐将在623 ℃时开始分解,但复合相变材料的分解温度升高至627.5 ℃,这是由埃洛石的硅铝结构对复合物的阻燃作用引起的。结合复合材料的相变温度可以得到该材料的可使用温度区间高达536.2 ℃。

图5 四元硝酸盐、复合相变材料的TG曲线Fig.5 TG curves of quaternary nitrate and CPCM
2.2.3 储热密度
储热密度反映了单位质量材料的储热能力,是评价相变材料储热性能必不可少的参数。对于添加了支撑材料和导热增强材料的复合材料,在计算储热密度时应同时考虑显热和潜热。计算式如下
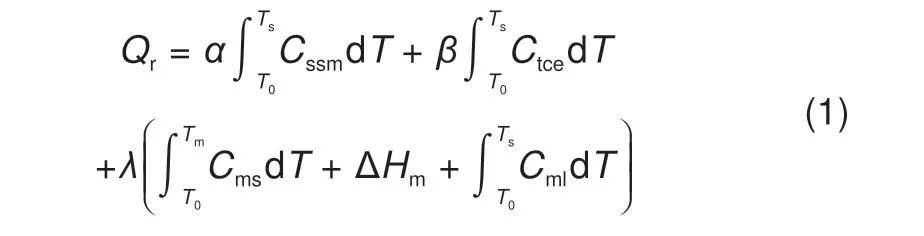
式中,Qr为单位复合材料的储热量;α、β、λ分别为结构支撑材料、导热增强剂和复合相变材料的质量分数;Tm、T0、Ts分别为复合材料的使用下限温度、相变温度和使用上限温度;cssm、ctce、cms、cml分别为结构支撑材料、导热增强介质、固态熔盐和液态熔盐的比热容;ΔHm为相变材料的潜热值。根据表2中的数值计算可得在25~625 ℃的使用温度范围内单位复合相变材料的储热值为630.15 kJ,即该复合相变材料具有非常可观的蓄热能力,应用范围广,市场价值较高。
2.2.4 导热性能
熔融盐导热性的提高是实现其作为相变蓄热材料广泛应用的关键。如图6所示,50 ℃时未加石墨的复合相变材料热导率为0.58156 W/(m·K),添加2%石墨后热导率提高至0.7389 W/(m·K),添加10%石墨后的热导率为1.18 W/(m·K),相较于未添加石墨时提升了103%。总体来看,复合材料的热导率随着石墨质量分数的增加而增大。早在1994年,Pedraza 等[25]就已经指出石墨的热导率随温度的升高而降低,并描述出两者之间的关系式。图中复合材料的热导率随温度的变化趋势与石墨已知行为保持一致,且平均每升高1 ℃,热导率降低约0.3%。

图6 50QN-50HNTs、添加2%石墨和添加10%石墨后复合相变材料的热导率变化Fig.6 Curves of thermal conductivity of 50QN-50HNTs and composite phase change materials with 2%and 10%graphite
2.3 化学性能分析
2.3.1 化学相容性
复合相变材料的化学相容性可以通过傅里叶红外光谱仪(FT-IR,spectrumll,PE,美国)和X射线衍射仪(XRD,D8 ADVANCE,BRUKER/AXS,德国)进行测试和研究。从图7 红外光谱图中可以看出,在1000 cm−1左右的吸收峰为单峰、强峰,根据无机物红外光谱对照表,可以判断该峰为NO3−官能团。同理,在1350 cm−1处的吸收峰为NO2−官能团,在熔融盐中表现为强峰、宽峰;在1635 cm−1处为C—C 官能团和NO3−官能团的吸收峰,在3440 cm−1处的吸收峰为材料吸水所产生的O—H官能团。烧结前后复合材料的特征峰相互对应,表明复合材料在高温时同样具有良好的化学稳定性。
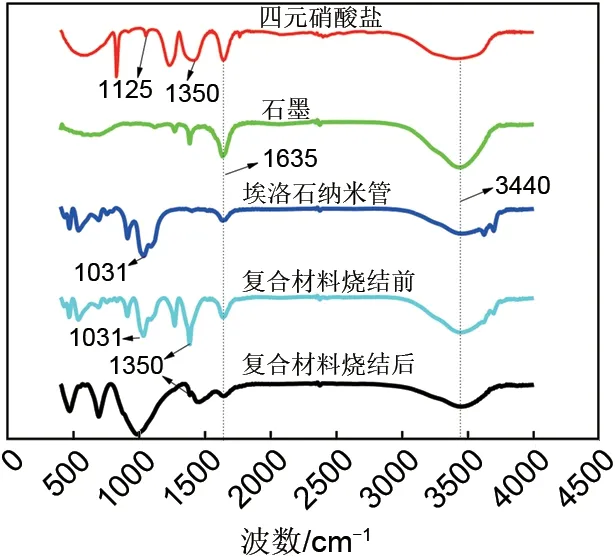
图7 四元硝酸盐、石墨、埃洛石纳米管及复合相变材料烧结前后红外光谱图Fig.7 FTIR patterns of quaternary nitrate,graphite,halloysite nanotubes,and composite phase change materials before and after sintering
2.3.2 化学稳定性
通过X射线衍射仪测试得到复合相变材料的衍射图谱,如图8所示。四元硝酸盐的衍射图谱中可以看出,第2个最强的尖峰为NaNO3的衍射峰,其余标注的强度较小的衍射峰为KNO3,未标注的杂峰则为NaNO2的衍射峰。复合相变材料的衍射图谱中存在对应熔融盐、埃洛石纳米管、石墨的衍射峰。这说明复合相变材料在使用过程中既没有发生化学反应也没有产生新物质,即化学稳定性良好。

图8 四元硝酸盐和复合相变材料的衍射谱图Fig.8 XRD spectra of quaternary nitrate and composite phase change materials
2.4 循环稳定性分析
将制备好的四元硝酸盐/埃洛石纳米管定型复合材料放置在温度设定为500 ℃,升温速率为10 ℃/min 的马弗炉中进行加热,然后取出待其自然冷却,此为一次循环。图9为复合相变材料以及复合相变材料经过30 次和100 次循环后的DSC 曲线,结晶水和其他杂质的影响导致循环前后DSC曲线的差别。由表3可以看出复合相变材料在循环30次和循环100次后相变初始温度、相变峰值温度相较于未循环时浮动最大值为1 ℃,而相变终止温度随着循环次数的增加而有所降低,与潜热的变化趋势保持一致,这是因为在实验过程中不可避免地发生了轻微泄漏,证明了复合定型材料循环稳定性良好。

图9 复合相变材料、复合相变材料循环30次和循环100次后的DSC曲线Fig.9 DSC curves of CPCM and CPCM after 30 times and 100 heating-cooling cycles

表3 复合相变材料、循环30次和循环100次后的相变温度及潜热对比Table 3 Comparison of phase change temperature and latent heat of CPCM and CPCM after 30 times and 100 heating-cooling cycles
3 结 论
通过冷压-热烧结法制备出一种低熔点、低成本、使用范围较广的定型复合相变材料。通过对该复合相变材料的微观结构、元素分布、热物理性质、化学稳定性以及热导率进行测试及表征,得出以下结论。
(1)熔融的四元硝酸盐能很好地浸入埃洛石的管状结构中,并与埃洛石形成结构稳定的复合材料,很好地解决了熔融盐易泄漏、易腐蚀的问题。
(2)复合相变材料的熔点为91.3 ℃,分解温度为627.5 ℃,其可应用温度范围(536.2 ℃)优于文献中已报道数据。在温度范围25~625 ℃内,复合材料储热密度高达630.15 kJ/kg。
(3)四元硝酸盐、埃洛石、石墨3种介质在形成复合材料的过程中没有发生化学反应且没有生成新物质,表明复合材料化学稳定性良好。
(4)复合材料的热导率随着石墨含量的增加而增大,随着温度的升高而降低,50 ℃时添加10%石墨复合相变材料的热导率高达1.18 W/(m·K),较同温度下熔盐材料的热导率提高了44.8%。
(5)复合相变材料经过100次循环后,相变温度及相变潜热无明显变化(波动范围小于3.5%),具有良好的循环稳定性。
符号说明
cml——液态熔盐比热容,J/(g·K)
cms——固态熔盐比热容,J/(g·K)
cp——比热容,J/(g·K)
cssm——结构支撑材料比热容,J/(g·K)
ctce——导热增强材料比热容,J/(g·K)
ΔHcal——相变材料的计算潜热,kJ/kg
ΔHm——相变材料的潜热,kJ/kg
ΔHmea——相变材料的测试潜热,kJ/kg
Qr——单位复合材料储热量,kJ/kg
Tend——相变终止温度,℃
Tm——复合材料相变温度,℃
Tonset——相变初始温度,℃
Tpeak——相变峰值温度,℃
Ts——复合材料使用上限温度,℃
T0——复合材料使用下限温度,℃
α——结构支撑材料质量分数
β——导热增强介质质量分数
λ——相变材料质量分数

