卟啉类光敏剂联合纳米材料在肿瘤光热/光动力治疗中的研究进展*
谢文静,郑 敏,周宏福,王世越,王自瑶,李 玲
(湖北科技学院医学部药学院,湖北 咸宁 437100)
卟啉广泛存在于自然界的动植物体内,早在十九世纪中期,血卟啉就被人类所发现,随后卟啉及其衍生物也因此得到人们的关注。卟啉是一种大分子杂环化合物,它作为一个高度共轭的体系,是由4个吡咯类亚基的α-碳原子通过次甲基桥(=CH-)交联而形成的[1]。科学家们通过将卟啉大环上的吡咯双键进行还原,得到了卟啉类衍生物,如酞菁、卟吩等,促使它们的吸收波长红移至近红外区,激发的波长也能更好的穿透深部组织。基于卟啉类衍生物优良的吸收特性和良好的生物相容性,运用新型纳米材料,巧妙地将其结合在肿瘤光热治疗、光动力治疗中,使卟啉类光敏剂在癌症治疗领域展现出广阔的应用前景。
1 卟啉类光敏剂的发展历程
为了达到理想的治疗效果,人类不断的探索出一代又一代的光敏剂,将其运用于肿瘤的联合治疗之中。而经历了三代变革以后的卟啉类光敏剂,具备结构性质稳定、光毒性强、副作用小、对癌组织靶向性强、光敏化能力强、组织穿透深等优越特性,得到了广泛的运用。
1.1 第一代光敏剂
血卟啉衍生物和光敏素Ⅱ是最早被人们所发现的光敏剂。1841年,Schwartz第一次从血液中提取出了血卟啉,它是由血红蛋白酸水解后产生的内源性卟啉[2],后续的研究者在此基础上进一步证明了血卟啉的光毒性,Allison等[3]对血卟啉衍生物分离纯化,得到了光敏素Ⅱ,此类衍生物吸收波长较短,只有少量光波能透过皮肤直达病灶部位,对肿瘤定位不准确,还会产生皮肤光敏反应,基于以上缺点的限制,第二代光敏剂应运而生。
1.2 第二代光敏剂
第二代光敏剂可实现更长的近红外光的吸收,具有结构单一、靶向性强、活性氧产量高等多重优势,且利用效率也显著提高,并且在无光照条件下,暗毒性很低。
1.2.1 卟啉衍生物
以5-氨基酮戊酸和血卟啉单甲醚为代表的第二代卟啉衍生物最为常见。其中,5-氨基酮戊酸是卟啉在机体代谢而成的中间产物[4]。20世纪90年代初,许德余等[5]独立研发出了一种国产的新型光敏剂——血卟啉单甲醚,相关研究人员进一步将血卟啉单甲醚运用到鲜红斑痣、肺癌诊断、消化道肿瘤等疾病的治疗之中,展现出显著优越的效果。
1.2.2 二氢卟吩类衍生物
二氢卟吩类衍生物,由于其结构中的一个双键被单键取代,所以在近红外光区的光敏效应更好。值得一提的是,自然界中的叶绿素类化合物,核心环都是二氢卟吩,因此,利用这种原料,研究者们合成了叶绿素衍生物,将它运用于肿瘤的治疗,展现出较好的治疗效果。但由于卟吩类光敏剂水溶性差、光谱特征不稳定、清除率低,光毒性强,使其在实际应用中受到限制。
1.2.3 酞菁类光敏剂
酞菁的合成是通过将4个苯环或萘环连接到卟啉环的4个吡咯β位上,再把meso-H对应的C转换为N来实现的,它是一种完全由人工合成的光敏剂[6],可以通过改变取代基和中心配位金属离子来调整结构,使其最大的吸收峰提高。此外,酞菁具有稳定的理化性质,蓄积肿瘤部位速度快,机体清除率高,避免皮肤出现光敏性反应。陈耐生等[7]合成了一种新型酞菁类光敏剂——“福大赛因”,这种锌酞菁抗癌光敏药物已被批准进入临床试验阶段,取得了理想治疗效果。
1.2.4 稠环醌类光敏剂
稠环醌类光敏剂是从菌类植物中提取而成的一种天然光敏剂,在光动力治疗时,可直接产生单线态氧、自由基或超氧阴离子,破坏肿瘤生长缺氧微环境。如云南箭竹中的竹红菌素、贯叶连翘中的金丝桃素和姜科植物中的姜黄素[8],均属于稠环醌类的光敏剂,相比于人工合成的部分卟啉类光敏剂,它的安全性更高、光毒性更低,具有巨大的发展前景。
1.3 第三代光敏剂
第三代光敏剂引入了具有靶向性的官能团或化合物(如多聚体、脂质体、糖类、抗体等),以及卟啉的糖苷化、卟啉与富勒烯复合、与蛋白质复合以及与各种纳米粒子复合,以此来增加在肿瘤细胞中的选择富集作用,提高靶向治疗效果[9]。伴随着纳米技术在肿瘤光热、光动力治疗领域的飞速发展,尤其与光热纳米材料结合的光敏剂,更是具有广阔的前景和未来。
2 光热纳米材料
2.1 无机光热纳米材料
无机光热纳米材料主要包括贵金属材料、金属硫化物材料、金属氧化物材料、量子点、碳基纳米材料等。以金、银、铂等为代表的贵金属,是最早被开发的纳米光热转换材料,尤其是金纳米材料是目前研究最为广泛的贵金属材料,其优点为易合成、易修饰、性质稳定,在808nm处具有良好的光热转换效率,主要是由于金属纳米结构发生了等离子共振吸收,并实现了光能到热能之间的转换,以杀死肿瘤细胞[10];而常见的金属硫化物纳米材料是一种无机半导体的纳米材料,包括二硫化镍、硫化铋、硫化铜等,均有较高的近红外吸收特性和较小的毒副作用[11];而金属氧化物材料,常见的有磁性氧化铁、二氧化锰、过渡金属氧化物二氧化铱等,其中运用较多的磁性氧化铁纳米粒子,不仅在近红外光照射下可以产热,还可以发挥磁热疗的特性,在交变磁场的作用下,定向聚集在肿瘤部位的氧化铁纳米粒子,可以发生磁热效应将癌细胞杀死[12];此外,碳基纳米材料,常见的如碳纳米管、碳纳米球、碳量子点、石墨烯、富勒烯等[13],一般是通过表面改性以及修饰功能化物质拓展其现有性能,在近红外区表现出较强的光吸收特性和较好的稳定性,同时,碳作为人体组成的基本元素之一,生物相容性优于其他重金属纳米材料,并且碳基纳米材料还能有效识别癌细胞的靶向性分子,将其修饰到表面,修饰后的碳基纳米粒子具有很大比表面积,可以负载小分子、药物、基因等[14-15],并选择性的富集到肿瘤组织,既能高效地杀死癌细胞,又能降低治疗中的毒副作用。
2.2 有机光热纳米材料
有机光热纳米材料通常具有良好的组织相容性和生物可降解性,如近红外染料和高分子聚合物等。近红外染料虽然生物相容性好、近红外窗口吸收性强,但它的稳定性差,在肿瘤内靶向蓄积有限,常与纳米载体结合。吲哚菁绿作为一种近红外染料,早在1954年就被美国食品药品监督管理局批准应用于临床诊断[16]。而高分子聚合物纳米材料如聚吡咯、聚多巴胺、聚乙二醇等[17],具有光热转换效率较高、合成成本相对较低等优势,且拥有较高的载药性能,可实现在人体内的缓慢降解。
3 肿瘤的光热治疗、光动力治疗
光热治疗(photothermal therapy ,PPT)是指选用性能较好的光热转换材料,将其注入人体,在靶向性识别技术下富集于肿瘤组织部位,采用近红外光的照射,实现光能与热能的转换,以此达到杀死癌细胞的效果[18]。光动力疗法(photodynamic therapy,PDT)是指使用光敏药物进行激光活化,来治疗肿瘤疾病的新方法。氧、光敏剂和激光是构成光动力治疗的三个基本要素,当采用适当波长光线局部照射,聚集在肿瘤组织的光敏药物被活化,引发光化学反应,并破坏肿瘤细胞,此外,光敏剂有助于生成活性很强的单态氧,单态氧与生物大分子发生氧化反应,引发细胞毒性和微血管损伤,致使肿瘤细胞凋亡[19]。这两种针对肿瘤联合治疗的手段具有毒副作用小、选择性高、创伤小、光学吸收特性高等优势,它们作为有前途的癌症治疗方式,可以明显缩短肿瘤的治疗周期。
4 卟啉类光敏剂联合纳米材料在肿瘤光热/光动力治疗中的应用
4.1 卟啉类光敏剂与金属纳米材料结合——肿瘤光热/光动力治疗
纳米卟啉联合金属有机框架(metal organic frameworks,MOFs)已成为癌症光动力治疗的一个很有前途的治疗平台。金属有机框架具有通用性强、孔隙率高、生物相容性好等特点,结合纳米卟啉的金属有机框架可以有效解决卟啉因水溶性差、不稳定性等问题,并能抑制卟啉化合物自聚集引起的猝灭,促进药物传递。王玉伟等[20]先采用溶剂热法合成卟啉基金属有机框架纳米颗粒,负载高铁酸钾氧化剂,再经牛血清蛋白包覆表面以制得多功能的复合纳米颗粒,模拟肿瘤微环境条件下的细胞培养基,采用CCK-8方法,测试细胞的光-化学动力学联合治疗效果,研究表明它能将肿瘤细胞内过度合成的内源H2O2转化为羟自由基,在660nm激光照射下可以提高单线态氧的产量,增强光动力学效应;崔华媛等[21]制备了一种新型的锰簇卟啉金属有机框架纳米载体,研究其生物学效用,考察它对结肠癌细胞的光毒性,结果显示,光诱导的锰簇卟啉金属有机框架在低氧环境下,对结肠癌肿瘤细胞表现出高水平的细胞杀伤性,H2O2在锰簇作用下分解为O2,产生的氧在近红外光下照射下,进一步转化为具有细胞毒性的单线态氧。
共价有机骨架(covalent organic frameworks,COFs)是一类有机单体通过可逆共价键连接而形成的晶型有机多孔材料[22]。近几年,它作为一种新型材料在合成和性能研究等方面得到了快速发展,这种通过可逆的共价键(C-C、C=N、C-N、C-O和B-O等)连接起来的有机孔材料,相比于以氢键、范德华力等次级键作用力得到的材料而言,具有更好的化学/热稳定性。此外,带有配位基团的共价有机骨架,还可以作为非均相配体与金属配位形成稳定的配合物,从而有助于稳定金属中心,提高过渡金属的催化活性[23]。Wang等[24]制备了卟啉基共价有机骨架纳米颗粒(COF-366 NPs)作为光活性剂,它能降低卟啉的自聚集和猝灭,此外这种共轭结构能增强近红外的吸收,使用COF-366 NPs还可以实现光声成像引导的光动力学和光热学联合癌症治疗,在乳腺癌荷瘤小鼠中,通过一次注射和单一波长光源照射,可实现对大肿瘤的完全抑制(见图1)。
图1 单波长光照射下COF-366 NPs形成和光声成像引导光疗的示意图[16]
4.2 卟啉类光敏剂与聚合物纳米材料结合——肿瘤光热/光动力治疗
卟啉与聚合物纳米复合材料(如胶束、囊泡和微凝胶),通过疏水、静电、配位相互作用、氢键和主客体识别等方式协同自组装,展现出良好的应用价值。在结构上,聚合物可以影响卟啉分子的形式并改变聚合物的构象;在功能上,聚合物组装体为卟啉提供了疏水微环境和亲水外围,并进一步增强了其在生物环境中的稳定性[25]。此外,聚合物的结构多样性可以有效模拟蛋白质残基的结构和功能,增强卟啉的生物活性,与此同时,卟啉又赋予了聚合物各种生物学功能。Shi等[26]采用一种溶液室温老化的方法,制备了基于5,10,15,20-四(4-氨基苯基)-卟啉(Tph)和2,5-二羟基-1,4-苯二甲醛(Dha)的纳米级含卟啉共价有机聚合物(PCOP),它的光热转换效率约为21.7%,在体外和体内分别评估了其协同光动力治疗和光热治疗的抗肿瘤效果,并采用不同激光650nm和808nm进行照射,均可以产生细胞毒性,体内评估PCOP对小鼠的抗肿瘤功效、病理形态学分析结果显示抑瘤效果良好,进一步表明其较低的内毒性,在器官内滞留的浓度在12h达到最大值,随后逐渐下降,可以有效被清除至体外,见图2。
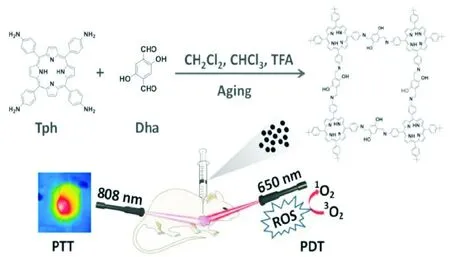
图2 PCOP的制备与PTT和PDT的应用示意图[18]
刘长玲等[27]以四羟基卟啉为原料,制备以卟啉为核的星形链转移剂,以偶氮二异丁腈引发单体N-异丙基丙烯酰胺,制备出了以卟啉为核的四臂星型聚(N-异丙基丙烯酰胺),发现聚合物具有卟啉光敏剂的紫外可见光谱吸收,同时聚合物链段可以防止卟啉分子淬灭,具有良好的生物相容性,并能够有效的杀伤宫颈癌肿瘤细胞;肖潮等[28]通过构建聚乙二醇-聚甲基丙烯酸二异丙基氨基乙酯-四苯基卟啉,使得四苯基卟啉能较好被纳米颗粒所固定,并且包载盐酸阿霉素的纳米胶束,可以实现在肿瘤酸性环境中的缓慢释放,为癌症治疗提供了新的策略;Li等[29]设计了一种芳基硼酯修饰的两亲性共聚物,形成胶束并包覆阿霉素和血卟啉,在特异性的激光照射下,血卟啉会在肿瘤部位产生广泛的活性氧簇,并选择性释放化疗药物阿霉素,这种材料将阿霉素介导的化疗和血卟啉介导的光动力治疗结合,实现了两者的协同抗癌效果。
4.3 卟啉类光敏剂与碳纳米材料结合——肿瘤光热/光动力治疗
Wang等[30]合成了一种基于肿瘤微环境响应的碳纳米管,利用聚丙烯胺盐酸盐和聚丙烯酸钠,通过对多壁碳纳米管进行表面改性,形成以叶酸为端基的胺化聚乙二醇,可以提高其水分散性、生物相容性和抗氧化性以及肿瘤靶向能力,其被内化到肿瘤细胞中,可以迅速释放光敏剂二氢卟吩e6,对肿瘤微环境的低pH和高谷胱甘肽水平的响应,同时在MRI的诱导下,与上述材料结合的MnO2也被催化,将多余的H2O2分解为氧气,缓解缺氧状态,增加过量谷胱甘肽的消耗,协同抑制肿瘤细胞生长,在体内消融肿瘤,见图3。
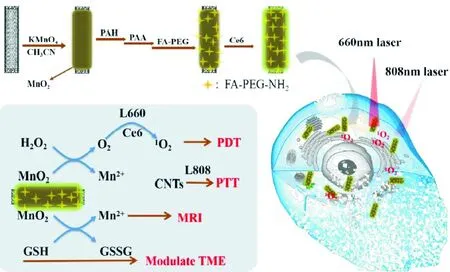
图3 MWNT@MnO2-PEG@Ce6的合成及治疗机制[22]
Gulzar等[31]通过利用聚乙二醇将纳米氧化石墨烯共价植入核壳结构上,然后将二氢卟吩e6负载到石墨烯表面,得到的聚乙二醇包裹石墨烯并负载二氢卟吩的纳米复合材料,不仅可以作为细胞和机体的发光成像探针来进行诊断,同时在808 nm近红外激光诱导下,可产生活性氧,实现对肿瘤的光动力治疗。
4.4 卟啉类光敏剂与脂质体纳米材料结合——肿瘤光热/光动力治疗
卟啉脂质体的优势在于其较好的安全性和酶生物降解性,并且可负载多种药物分子,它作为光敏剂载体,可通过自身快速氧化破坏,促进药物的局部释放,临床应用前景广阔。姜丹等[32]制备了负载血卟啉单甲醚的脂质体,该脂质体粒径大小均一,具有明显的光触发释放性能,在光照条件下,1h释放的百分率为67.36%,表明脂质体作为载体,可以实现血卟啉单甲醚的光触发释放,有利于提高肿瘤光动力学治疗效果;Zhu等[33]构建了一种掺杂原卟啉的载阿霉素多功能脂质体,这种载阿霉素脂质体的脂质双分子层的掺杂,可促进其高效释放,提高阿霉素的核传递效率,并且在进入乳腺癌细胞核时,不易被溶酶体捕获,对于部分耐药性的癌细胞,其强烈的耐药性可以在温和的激光照射下逆转,因为原卟啉的光动力效应破坏了药物外流系统(如p-糖蛋白),并促进阿霉素进入癌细胞核内,见图4。

图4 脂质体激活的药物释放及其光动力疗法(PDT)用于MDR逆转的示意图[25]
5 结 语
综上所述,我们不难发现卟啉类衍生物在癌症治疗领域中的重要作用,其独特的化学结构决定了其易于修饰的特性。与纳米光热材料结合,可以有效地解决卟啉类光敏剂出现的水溶性差、不稳定等问题,同时,还可以更大程度地促使其吸收波长红移至近红外区,激发的波长也能更好的穿透肿瘤深部组织。
因此,在肿瘤的光热治疗中,将卟啉类光敏剂联合的纳米光热材料注入体内,可以很好的靶向富集在肿瘤附近,增强癌组织周围的近红外吸收,光能与热能间转换效率明显提升,以实现杀死癌细胞的目的;而在肿瘤的光动力学治疗中,采用特定波长的激光,可以激活在肿瘤组织内选择性滞留的卟啉类光敏剂,其可以与肿瘤组织内的氧产生反应,生成活性较好的单态氧及一些自由基,这些产物进一步与生物大分子发生作用,破坏癌组织中的细胞、细胞器的结构功能,促使肿瘤细胞发生凋亡、坏死以及过度自噬等过程;而在光热、光动力的协同治疗中,卟啉类光敏剂联合光热纳米材料,既可以增强材料本身在近红外窗口处的吸收和实现较好的光热转换性能,以达到对肿瘤组织的“热消融”,也可以发挥卟啉光敏剂的特性,其反应生成的活性氧与自由基能破坏肿瘤组织内部的缺氧环境,引发细胞毒性和微血管损伤,最终达到良好的癌症治疗效果。
纳米金属卟啉有机框架是目前研究最多、最广的一种形式,其次,聚合物、脂质体以及碳纳米材料也可以很好的与卟啉类光敏剂相结合,协同彼此间的优势,将其运用到肿瘤的光热治疗、光动力治疗之中,均被证实展现出优越的治疗效果。随着科研人员研究的不断深入,近年来,文献报道[34],卟啉类衍生物在肿瘤的声动力治疗(sonodynamic therapy,SDT)中也具有潜在的应用价值。声动力治疗是指一种非侵入性治疗方式,它利用超声波与声敏剂之间的相互作用对肿瘤组织产生损伤。相比于光热治疗、光动力治疗而言,声动力治疗中的超声治疗可以通过控制照射时间、频率、强度,来精确定位肿瘤组织,同时具有更深层的组织穿透力和更小的组织损伤效果。目前,声动力治疗肿瘤的机制有待彻底阐明,现存的观点主要包括活性氧学说、超声空化学说以及免疫学说,有关于卟啉的研究大多还停留在针对肿瘤的光热、光动力治疗领域的应用,缺乏在肿瘤声动力治疗的进一步探索,仅有少量文献报道将卟啉类衍生物运用在声动力治疗,来增强癌症治疗效果。随着肿瘤治疗领域中声动力治疗技术的不断完善和发展,相信这也必将成为未来一个新的研究热点。

