全流程数字化思维模式下的临床研究信息化管理平台应用实践探讨
郑云硉,董宁欣
同济大学附属同济医院信息处, 上海 20065
为切实推进数字化转型工作,进一步落实《关于全面推进上海城市数字化转型的意见》中“推动公共卫生、健康等基本民生保障更均衡、更精准、更充分”“打造智慧医院数字化示范场景”相关工作要求,同济大学附属同济医院以实施“健康上海2030”规划为契机,以加强精准医学、智慧医疗等关键技术为突破,倡导加强医疗大数据的数据挖掘和广泛应用。
以建设“学院型医院”为发展目标,坚持科技兴院,重视临床科研探索,不断加大科技投入、科技奖励,制定学科建设及人才培养系列管理办法、完善知识产权管理、规范继续医学教育。近年来科研工作高速发展,每年医院获批各类科研项目百余项。2019 年,同济大学附属同济医院“临床研究中心”正式以独立部门运行,下辖临床研究中心办公室、药物临床试验管理办公室,在医院领导和学术委员会、伦理委员会的指导下进行临床研究项目的管理。同年,同济大学附属同济医院修正和正式发布《上海市同济医院临床研究管理办法(修订版)》,进一步规范临床研究行为,并启动临床研究信息化管理平台的建设。
1 困境与解决方法
1.1 平台现状
临床研究包括GCP 临床试验和科研类临床科研项目。目前有不少医疗机构研究尝试使用药物临床试验管理系统(CTMS)进行临床试验的流程管理,但是科研类临床研究多以线下纸质化管理为主,信息化程度低,导致临床研究项目管理效率低、数据采集难、数据可靠性差,严重制约着临床研究的发展,也不利于提高临床研究人员的积极性[1-2]。研究者除了承担繁重临床诊疗任务外,还同时承接临床试验项目和科研项目,当前临床研究的管理模式已无法有效促进临床研究的快速发展。利用信息技术为研究者搭建平台,提高项目管理效率,提高研究数据的可及性和可靠性,提高临床管理部门的管理效率,是势在必行也迫在眉睫[3]。
1.2 平台建设的基础与架构
结合同济大学附属同济医院的实际情况,利用信息化手段助力优化GCP 临床试验和科研类临床研究的信息化管理流程[4],创新性地建设一套临床研究管理平台。平台通过4 个层次实现立项审批、启动准备、项目实施、质量监管和结题环节的全流程标准化管理。
受试者数据直取自医疗源数据,包括临床信息系统、影像库、临床数据中心。平台并对受试者临床数据采取数据整合、数据清洗、解析、脱敏等数据治理措施,得到高质量数据后,结合科研数据库进行分析,建立病历信息模型[5]。平台搭建临床研究中心办公室、GCP 机构办公室、临床科室(专业组)、伦理委员会和学术委员会等多个子系统,根据不同类别项目分别建设项目管理流程,同时建设项目监管通道和数据采集与管理通道,见图1。
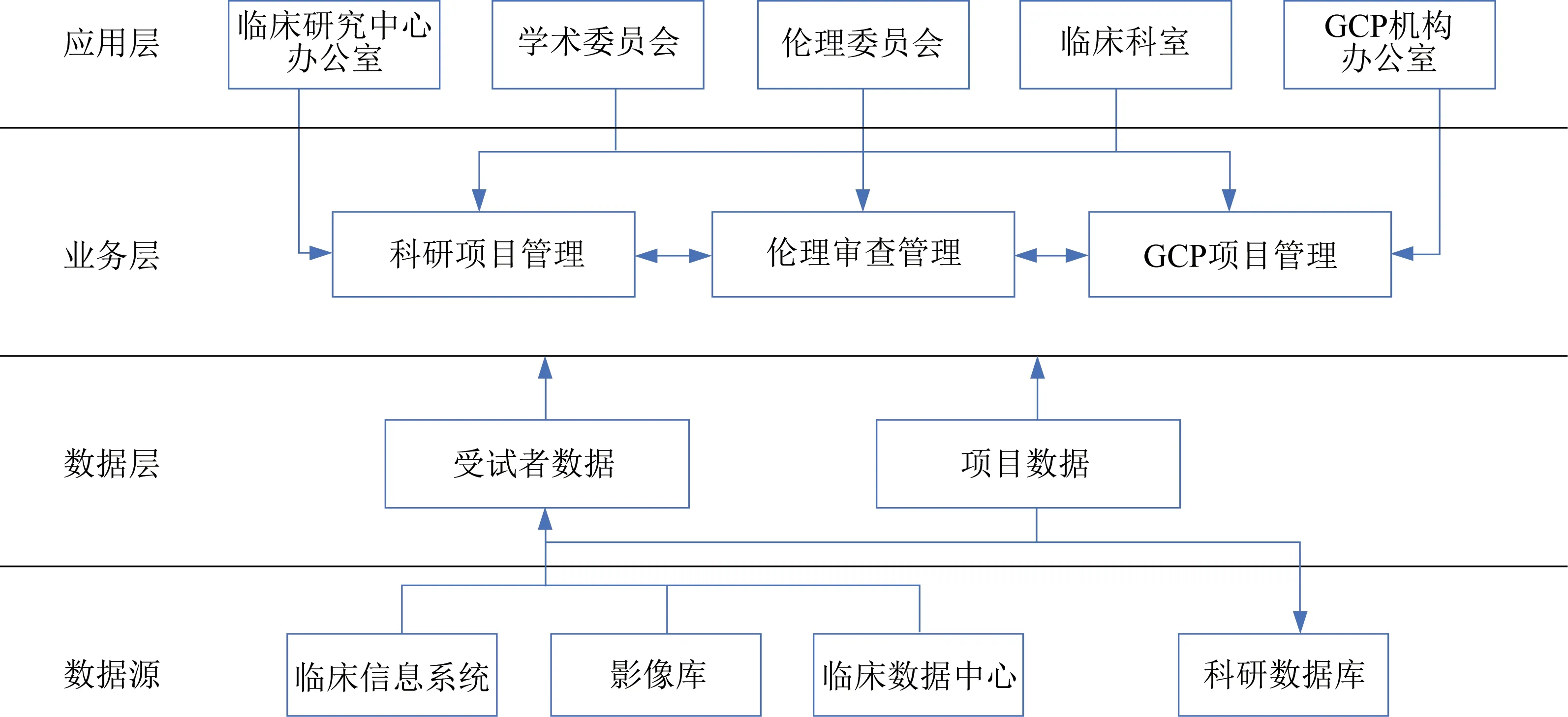
图1 临床研究信息化管理平台框架示意图Fig.1 Diagram of clinical research information management system
2 建设成果
2.1 实现临床研究项目流程管理
该平台设计了两个主要流程,两个流程分别对应科研临床研究项目和GCP 临床试验项目。从研究者角度出发,方便研究者管理项目,临床科室工作站建设同一入口,系统根据研究者选择的类别进入不同的项目管理页面,研究者根据系统指引查看项目立项要求、查看送审文件清单、获取实时任务等,见图2。
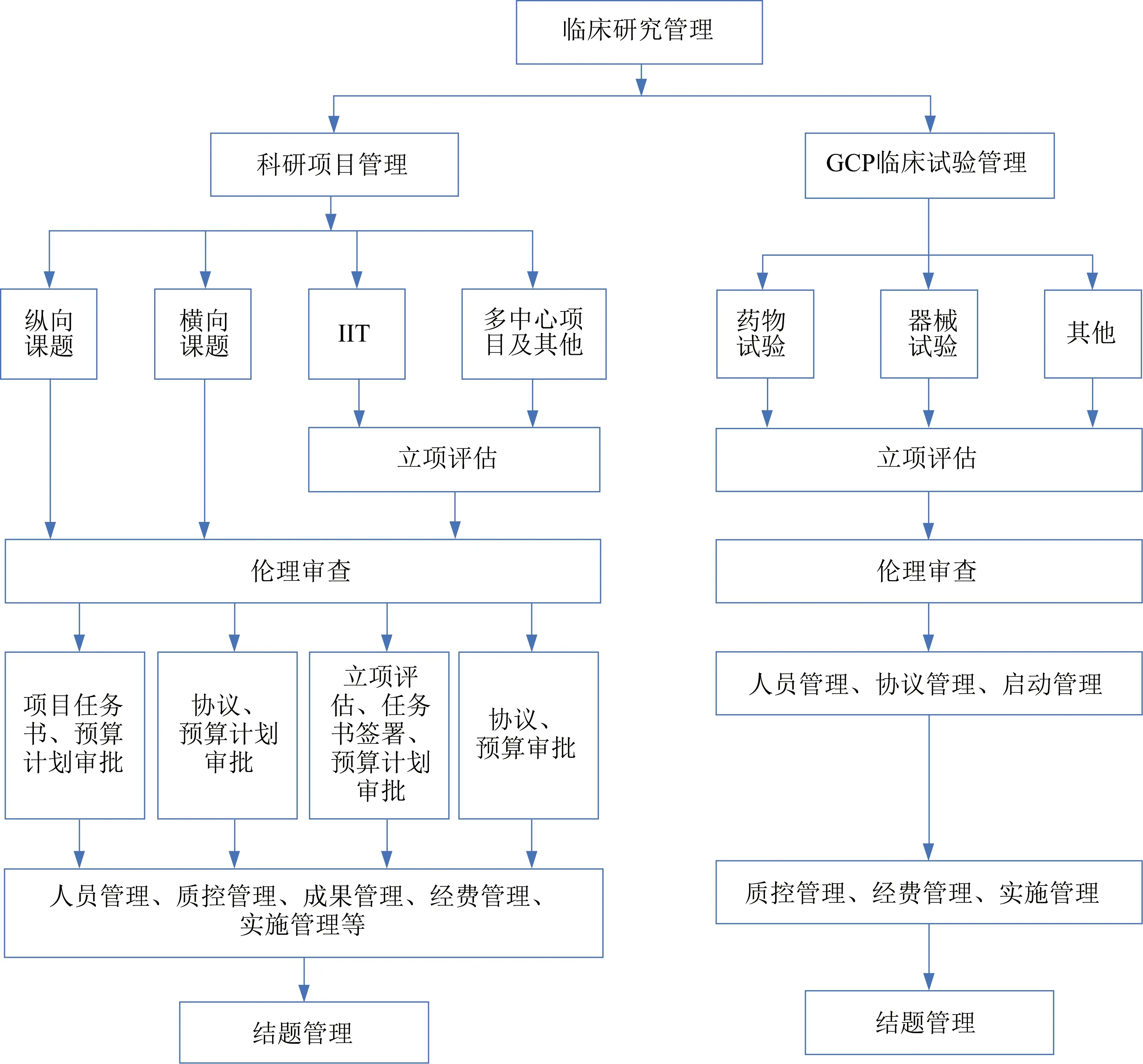
图2 临床研究管理流程示意图Fig.2 Flow chart of clinical research management
根据临床研究管理规范,所有临床研究项目均需立项,平台上线后立项流程均改为信息化审批,所有的审批流程可追溯。科研类临床研究根据项目来源、是否有经费支持进行分类管理。IIT项目经过临床研究中心办公室受理和申请,并组织学术委员性对项目的科学性、安全性和可行性等评估[6],评估通过后送审资料流转到伦理办公室。而纵向课题和横向课题则进行简化立项管理,加快项目立项流程。平台还开发了项目经费管理模块,监督经费使用计划。项目实施过程的管理参照GCP 临床试验管理,建设临床科室自查、临床研究中心监查和抽查流程[7]。建设研究进度监督通道,临床研究中心办公室人员可通过平台查看项目进展情况及入组受试者信息等,可实时监督项目质量。
GCP 机构办公室通过平台受理研究者或申办者递交的项目立项申请。研究者或者申办者根据系统配置的项目立项材料要求上传材料,机构办公室在线受理和立项评估,立项通过后送审材料流程到伦理委员会。伦理委员会承担医院所有临床研究项目的伦理审查工作。伦理委员会分别通过平台受理从临床研究中心办公室和GCP 机构办公室审批通过的审查申请,同时伦理委员会还接受来自研究者递交的严重不良事件报告、违背方案报告、年度跟踪报告等。管理部门和研究者可通过平台查看所有的伦理审查进度及审查结果。通过平台,达到各类临床研究项目管理环节的闭环管理[8]。
2.2 临床研究数据管理
临床研究是以疾病的诊断、治疗、预后、病因和预防为主要研究内容,以患者为主要研究对象,临床研究的结果的可靠性依赖于数据的可靠性。临床研究的数据溯源一直是临床研究质量管理的核心。为了便于临床研究受试者管理,医院建设受试者管理路径和数据溯源通道。通过改造HIS 和EMR 系统实现受试者的快速标记和纳入[9],平台的受试者管理模块实时记录和跟踪试验完成进度,平台与医院数据平台对接实现数据的实时交互[10],平台集成所有受试者的医疗数据,实现数据集成与数据溯源。标准化的流程也为实现各类临床数据的结构化、标准化和归一化奠定基础[9]。
2.3 临床研究质量控制管理
临床研究采用临床科室自查质控和管理部门分级分时质控。平台自动监控项目进展及风险预警,自动触发质控消息和任务。之前,由于临床科室的实施与质量管理脱节,质控不及时或者不到位时常发生[11-12]。采用平台后,所有质控任务及时触发,系统跟踪任务完成情况,有效提高质控的效率。同时,管理部门实施监控项目实施情况,查看项目安全事件报告和受试者数据,必要时可随时抽查。质控不再依赖临床科室的配合,质控记录和报告系统自动生成,快速反馈到临床科室进行整改,管理部门可在线催促整改和查看反馈结果。
2.4 临床研究数据共享及数据安全
临床研究信息化管理平台采用统一平台入口,多个子系统数据共享的模式实现不同类别临床研究项目的管理。平台采用权限分级管理机制,保障数据安全,即不同部门人员在同一入口登录不同工作模块,不同权级的用户,看到的功能模块不同。同一工作站入口,降低研究者的时间成本,有利于平台在全院推广使用。平台不仅为临床研究项目管理带来便利,也通过数据接口与医院其他业务系统数据共享。
3 讨论
3.1 实现全院临床研究的信息化管理
结合医院科研临床研究的管理规范,实现全院各类临床研究项目管理环节的闭环管理。平台的设计理念符合临床研究中心的职责定位,平台的设计与应用符合医院临床和科研信息化发展的趋势。平台自上线以来已经有登记项目近百项,项目立项审批流程顺畅,项目进度监管可视化,项目管理流程化。
3.2 建立医院高质量数据资产
全流程数字化转型的临床科研管理平台,产生了真实性、结构化、标准化临床数据,为医院实现数据应用奠定坚实的数据基础。
3.3 助力医院数字化转型
构建“临床行为产生数据,洞察数据辅助决策,反馈临床研究行为”的数据驱动闭环流程,从而以数据的角度提高医院临床治疗效果与临床质量[12]助力临床科研探索,从而为医院数字化转型发展添砖加瓦。
全流程数字化思维模式下的临床研究信息化管理平台已改造完成并投入使用,平台的建设诚然已取得明显成效,我们也深知信息化建设的道路还很长,比如引入5G+人工智能技术[9]、建设多中心共享平台等,我们将继续利于信息化技术建设更优的管理平台。

