功能离子液体在镧锕系离子萃取分离中的研究进展
蔡益民,郭旭文,袁立华,冯 文
四川大学 原子核科学技术研究所,四川大学 化学学院,辐射物理与技术教育部重点实验室,四川 成都 610064
核电在世界电力生产来源中占比已超过10%,将在未来电力和能源供应中发挥越来越重要的作用[1]。相比于传统能源方式,核能的优势主要体现为清洁、经济、储能高和安全高效等[2]。乏燃料后处理是核燃料循环后段中的关键环节,也是推动核能可持续发展的重要因素[3-4]。目前乏燃料的处理处置主要有两种方式:一次通过式燃料循环和闭式燃料循环。前者将反应堆卸出的乏燃料通过深层地质储藏,而乏燃料的放射性将持续数十万年以上,存在巨大安全隐患的同时还不为公众所接受。闭式燃料循环将乏燃料进行一系列化学分离,回收绝大部分未衰变的铀,并将长半衰期元素分离,极大程度地降低核废液的放射性毒性后再进行处置。例如,在以PUREX(plutonium and uranium extraction)流程为主的乏燃料后处理过程中,首先通过溶剂萃取法将99%以上的U和Pu回收用于循环使用,再依次进行镧锕共萃和次锕系选择性分离,最后通过高能中子射线轰击使次锕系金属嬗变为短半衰期或稳态元素。因此,闭式燃料循环对环境威胁更小,目前世界上大多数核电国家均倾向于采用这种方式[5-6]。
溶剂萃取法是目前乏燃料后处理中较为可靠和唯一商业运行的方法(如PUREX流程)。传统溶剂萃取过程往往会使用有毒、易燃、易挥发的有机分子溶剂作为稀释剂,这对环境造成二次污染的同时也存在巨大的安全隐患。为避免这一系列问题,利用沸点高、毒性低、不易燃的离子液体作为萃取体系稀释剂已成为乏燃料后处理领域的研究热点。而作为离子液体的一个分支,功能离子液体兼具离子液体与萃取剂的双重结构特点,在镧锕分离领域已受到了广泛关注。Mudassir 课题组[7]主要总结了离子液体作为稀释剂时在镧锕系分离领域的应用,并简要介绍了功能离子液体的研究现状,但至今极其缺少相关介绍功能离子液体的结构特征与应用展望的完整综述。本文除了介绍功能离子液体之外,还重点介绍各种用于铀酰离子、钍离子、镧系和次锕系金属离子萃取分离的功能离子液体研究现状,并对该领域工作进行展望。
1 功能离子液体
离子液体是一类由阴阳离子构成的液态有机盐,因其沸点高、难挥发、毒性低等优点被认为是萃取体系中常规有机稀释剂的潜在替代品[8]。离子液体种类随阴/阳离子变化而各异,常见的构成离子液体的阴/阳离子如图1所示。其中,阳离子部分主要有咪唑类、吡啶类和季铵盐类等,阴离子部分主要包括六氟磷酸根、四氟硼酸根和双三氟甲基磺酰亚胺根等。通过改变阴/阳离子组成,可按需调控其水溶性、熔沸点和对有机配体的溶解度等性质。研究表明,离子液体作为萃取体系稀释剂时,往往对有机配体和萃合物展现出良好的溶解性,从而一定程度上避免了萃取过程中沉淀或第三相的形成[9]。此外,在离子液体萃取体系中,金属离子的萃取通常伴随着阴/阳离子交换机理,通过促进萃取过程电荷平衡显著提高体系的萃取性能[10]。然而在常规离子液体萃取体系中,离子液体往往只作为稀释剂使用。

图1 常见的构成离子液体的阳离子(左)和阴离子(右)Fig.1 Common cations(left side) and anions(right side) in ionic liquids
功能离子液体(task-specific ionic liquids, TSILs)是在常规离子液体结构基础上,对其阳离子或阴离子部分进行官能化修饰,使其作为离子液体的同时还呈现出新的特异性功能。这种结构改进方式千变万化,所得TSILs性质也各有不同。例如,在离子液体的咪唑阳离子烷基链上修饰氨基、巯基、硫脲基等不同基团可使其应用于催化、有机合成和萃取等不同领域(图2)。

图2 咪唑阳离子功能离子液体修饰的官能团及其应用Fig.2 Different functional groups of [mim]+ based TSILs and their applications
2 功能离子液体在萃取领域中的重要应用


图3 TSIL-MBT(a)和羧基-咪唑功能离子液体(b)的化学结构式Fig.3 Chemical structures of TSIL-MBT(a) and carboxylic-based TSIL(b)


图4 TOMAS(a)、MTOABEHP(b)和邻苯二甲酸铵盐(c)功能离子液体的化学结构式Fig.4 Chemical structures of TOMAS(a), MTOABEHP(b), and Tri alkyl ammonium hydrogen phthalate(c) based ionic liquid
3 功能离子液体对镧锕系金属的萃取分离
镧系或锕系金属的萃取分离是乏燃料后处理的关键步骤,也一直是亟需解决的科学难题。将功能离子液体用于镧锕系离子分离领域已成为研究热点,其应用研究方向可大致分为四类:对铀酰离子、钍离子、镧系和次锕系金属离子的萃取分离。
3.1 功能离子液体对铀酰离子的萃取



图5 三种季铵盐膦氧类功能离子液体的化学结构式Fig.5 Chemical structures of three phosphine oxide based ionic liquids

图6 铀酰和功能离子液体的相对能量以及DFT优化结构[20]Fig.6 Relative energies of the uranyl/TSIL complexes together with the DFT calculated structures[20]

□——0.05 mol/L PO-TSIL,稀释剂[BMIM]NTf2;○——0.05 mol/L PO-TSIL,稀释剂[OMIM]NTf2;△——0.05 mol/L TOPO,稀释剂[OMIM]NTf2;▽——0.05 mol/L TOPO,稀释剂正十二烷图7 四种氧化膦体系在不同酸度下对铀酰的萃取分配比[21]Fig.7 Dependence of distribution ratios of uranyl ions by four PO extraction systems on acid concentration[21]
Mohapatra课题组[21]对氧化膦功能离子液体PO-TSIL对铀酰的萃取机理进行了研究(图7)。从对照实验可以看出,在三辛基氧化膦(TOPO)体系中,无论使用离子液体[OMIM]NTf2还是[BMIM]NTf2作为稀释剂,当硝酸浓度低于2 mol/L时,随着硝酸浓度增加,铀酰的萃取分配比均逐渐升高,该现象可以解释为铀酰离子和硝酸根作为中性复合物组分被共萃到有机相,因此硝酸根浓度增加可显著促进铀酰离子的萃取,而硝酸浓度进一步升高导致萃取剂质子化严重,萃取性能下降。PO-TSIL体系对铀酰的萃取性能随酸度变化规律与TOPO体系明显不同,较低酸度下其对于铀酰的萃取能力高于TOPO,但随着酸度增加,配位原子质子化导致其萃取能力急剧下降,表明该体系的萃取机理主要为阳离子交换机理。
除膦氧配体外,酰胺类配体也能通过羰基氧对金属体现出配位能力。丙二酰胺(DMDBMA)是一类双齿酰胺配体,被广泛用于锕系金属萃取研究当中[22]。Billard课题组[23]将丙二酰胺基团修饰在离子液体咪唑阳离子上(图8(a)),所得功能离子液体FIL-MA可用于高酸度下铀酰离子的萃取。从图8(b)的性能对比可以看出,FIL-MA对铀酰的分配比比中性分子萃取剂DMDBMA高出一个数量级,这表明向离子液体结构上引入配位基团可以显著提高萃取能力。
类似于丙二酰胺结构,酰胺荚醚(DGA)通过醚键连接两个酰胺基团形成三齿氧配位结构,也被用于金属离子的萃取研究中。2015年,Mohapatra课题组[24]利用DGA修饰的功能离子液体分离酸性溶液中的铀酰离子,并对涉及的萃取机理进行了深入探讨。研究表明,随着水相咪唑阳离子[C8mim]+浓度从0 mmol/L增加到1.0 mmol/L,铀酰萃取分配比从1下降到0.04,这表明萃取过程为阳离子交换机理,水相[C8mim]+的增加抑制了离子交换从而降低萃取性能。硝酸浓度增加导致配位原子严重质子化,同样导致体系萃取性能的显著下降。
除了与铀酰离子的配位萃取,功能离子液体也被应用于超分子铀酰离子萃取体系的构筑当中。彭述明课题组和沈兴海课题组[25]将宏观的超分子自组装思路用于萃取体系中,巧妙地利用羟基功能离子液体独特的类表面活性剂行为和与常规离子液体不同的表面张力特性,提出了一种新颖、高效且环保的铀酰分离策略(图9)。萃取过程中,连续的马拉戈尼效应使得含铀配合物组分发生宏观尺度的自组装,在两相界面处自发形成富铀小球,近乎定量地实现了水溶液中铀酰离子的富集与分离。该策略避免了传统溶剂萃取体系中繁琐的反萃流程,并具有一定的普适性,对铁、铜、锌等其它金属离子同样适用。该体系在乏燃料后处理和其它含金属废液处理等领域有重要应用前景。

(b):c(HNO3)=0.57 mol/L,○——FIL-MA,●——DMDBMA图8 FIL-MA的化学结构式(a)和不同萃取剂浓度对铀酰萃取分配比的影响(b)[22]Fig.8 Chemical structure of FIL-MA(a) and distribution ratios of uranyl ions as a function of ligand concentration(b)[22]

图组分的自组装行为[25]Fig.9 Self-assembly of the uranium-rich SA sample[25]
针对铀酰离子的萃取体系中,以阴离子部分为作用基团的功能离子液体相对较少。Srncik课题组[26]报道了三种基于阴离子作用位点的功能离子液体萃取剂用于铀酰的萃取研究(图10)。溶剂萃取实验表明,[A366][SCN]和[A366][TS]在一定条件下对铀酰的萃取率高达98%,而[A366][Met]仅为56%。实验还发现,[A366][Met]可能在萃取过程中不稳定,这或许是导致其萃取率较低的原因之一。针对实际河水的萃取实验中,[A366][TS]依然能够对铀酰离子定量萃取,而对钙和镁没有明显萃取能力,表明其较好的萃取选择性。相比之下,[A366][SCN]对铀酰离子的萃取率则下降至约30%,说明三种功能离子液体中[A366][TS]更适合铀酰离子的萃取分离。
通过更换阴离子部分,Kandioller课题组[27]利用图11所示的两种功能离子液体[A366][Mal]和[C101][Mal]进行铀酰离子的选择性萃取研究。在pH=2.0条件下,两种体系均能实现对铀酰离子的定量萃取,同时对钋离子的萃取率达到90%,而对铋和铅的萃取率低于20%。两种体系的性能差异主要体现在对钍离子的萃取上,[A336][Mal]对钍的萃取率不到30%,而[C101][Mal]对钍几乎定量萃取,说明[A336][Mal]对铀酰离子的选择性更好。
基于膦氧配位位点,陶国宏课题组[28]将[N14111][DBP](图12(a))用于酸性溶液中铀酰离子的选择性萃取。从图12(b)中可以看出,在pH=2.0~3.5时,由于配体质子化,体系对铀酰离子的萃取性能随酸度增加而降低。相比于其它金属,[N14111][DBP]对铀酰离子体现出较好的选择性。研究还发现,[N14111][DBP]体系与DBP相比,除了萃取能力明显提高之外,选择性也有一定程度的提升。pH=3.5条件下,当配体与金属离子浓度比为20∶1时,[N14111][DBP]体系对铀酰的萃取分配比是DBP体系的200多倍,同时对其它竞争离子均无明显萃取。

图10 三种用于铀酰萃取的功能离子液体的化学结构式[26]Fig.10 Chemical structures of three TSILs used for uranyl extraction[26]

图11 [A366][Mal]和[C101][Mal]的化学结构式[27]Fig.11 Chemical structures of [A366][Mal] and [C101][Mal] [27]

图12 [N14111][DBP]的化学结构式(a)和 [N14111][DBP] 体系对不同金属的萃取(b)[28]Fig.12 Chemical structure of [N14111][DBP](a) and extraction efficiency for different ions at different acidity(b)[28]
3.2 功能离子液体对钍离子的萃取分离
自然界中钍的含量约为铀的3~4倍。相较于传统的铀燃料循环,钍燃料循环产生的超铀元素更少,从而更加环保和安全,有望用于第四代核能系统中[29]。因此,对钍的选择性萃取分离研究具有十分重要的意义。
2020年,杨宇川课题组[30]将两种阳离子上修饰有不同膦氧配位基团的功能离子液体PO-TSIL和PN-TSIL用于钍离子的萃取研究。其中,修饰有膦酰胺基团的PN-TSIL性能明显优于PO-TSIL,对钍的萃取分配比高出数百倍以上(图13)。通过理论计算表明,膦酰胺基团在与硝酸钍发生配位时,酰胺基团和咪唑阳离子中的氢原子可能与硝酸根中的氧原子配位,从而提升其萃取性能。在红外光谱实验中,PN-TSIL与钍离子配位后其NH键对应的红外吸收带从3 621 cm-1移动到3 436 cm-1,进一步证实萃取过程中NH可能以氢键参与配位。


(b):■——TBP-ILs,●——TBP-正十二烷,▲——PO-TSIL,▼——PN-TSIL图13 PO-TSIL和PN-TSIL的化学结构式(a)及其在不同酸度下对Th4+的萃取分配比(b)[30]Fig.13 Chemical structures of PO-TSIL and PN-TSIL(a), and extraction efficiency for Th4+ at different acidity(b)[30]

图14 [DC18DMA][MA]的化学结构式(a)及其在不同酸度下对Th(Ⅳ)的自组装过程(b)[31]Fig.14 Chemical structures of [DC18DMA][MA](a), and self-assembly process for Th(Ⅳ) at different acidity(b)[31]
3.3 功能离子液体对镧系的萃取分离
镧系元素在荧光、电子器件、磁体、催化和冶金领域均有重要用途[32]。镧系收缩使得镧系元素的物化性质十分接近,导致镧系金属之间的相互分离极具挑战性。一系列功能离子液体也被用于镧系元素的萃取分离中。2012年,Venkatesan课题组[33]将一种基于酰胺荚醚阴离子的功能离子液体[A336]+[DGA]-用于Eu(Ⅲ)离子的萃取研究。与等浓度的中性分子HDGA相比,[A336]+[DGA]-的萃取性能在pH=1.0~4.0范围内均明显高于HDGA,对Eu(Ⅲ)离子的萃取分配比高出十倍以上。陈继课题组[34]认为这种现象是离子液体内在的协同作用引起的。
戴胜课题组[35]研究了三种基于膦氧基阴离子的功能离子液体[TBA][DEHP]、[TOMA][DEHP]和[THTP][DEHP]用于镧系金属的相互分离。如图15所示,含中性分子二-(2-乙基己基)磷酸(HDEHP)在内的四种体系对镧系均有较好的分离效果,分离因子SF(M/Eu)最高可达1 000以上。相比之下,功能离子液体体系整体对镧系的分离因子均不同程度地高于HDEHP体系。值得注意的是,HDEHP体系在萃取过程中有沉淀析出,表明其金属萃合物在离子液体中溶解度有限,而功能离子液体体系可避免该问题。此外,功能离子液体以离子液体作为稀释剂时对镧系的分配比比以二异丙苯作为稀释剂时高出了上百倍,这可能是因为“相似相溶”原理,即功能离子液体与金属的萃合物在离子液体中溶解性更佳。
2020年,闫勇胜课题组[36]利用一种含膦氧基阴离子的功能离子液体Cyphos IL 104,通过液膜法实现了对Lu(Ⅲ)/ Yb(Ⅲ)的分离。如图16(a)所示,薄膜左右两相分别为含有金属离子的酸性溶液和含有EDTA的水溶液,通过薄膜中的Cyphos IL 104选择性地在两相界面处不断地配位/解配位金属离子,可实现金属离子的膜分离。从图16(b)可以看出,在一定条件下,该液膜体系对Yb(Ⅲ)的渗透率(156 μm/s) 明显高于Lu(Ⅲ) (114.82 μm/s),由此达到两种镧系金属相互分离的目的。
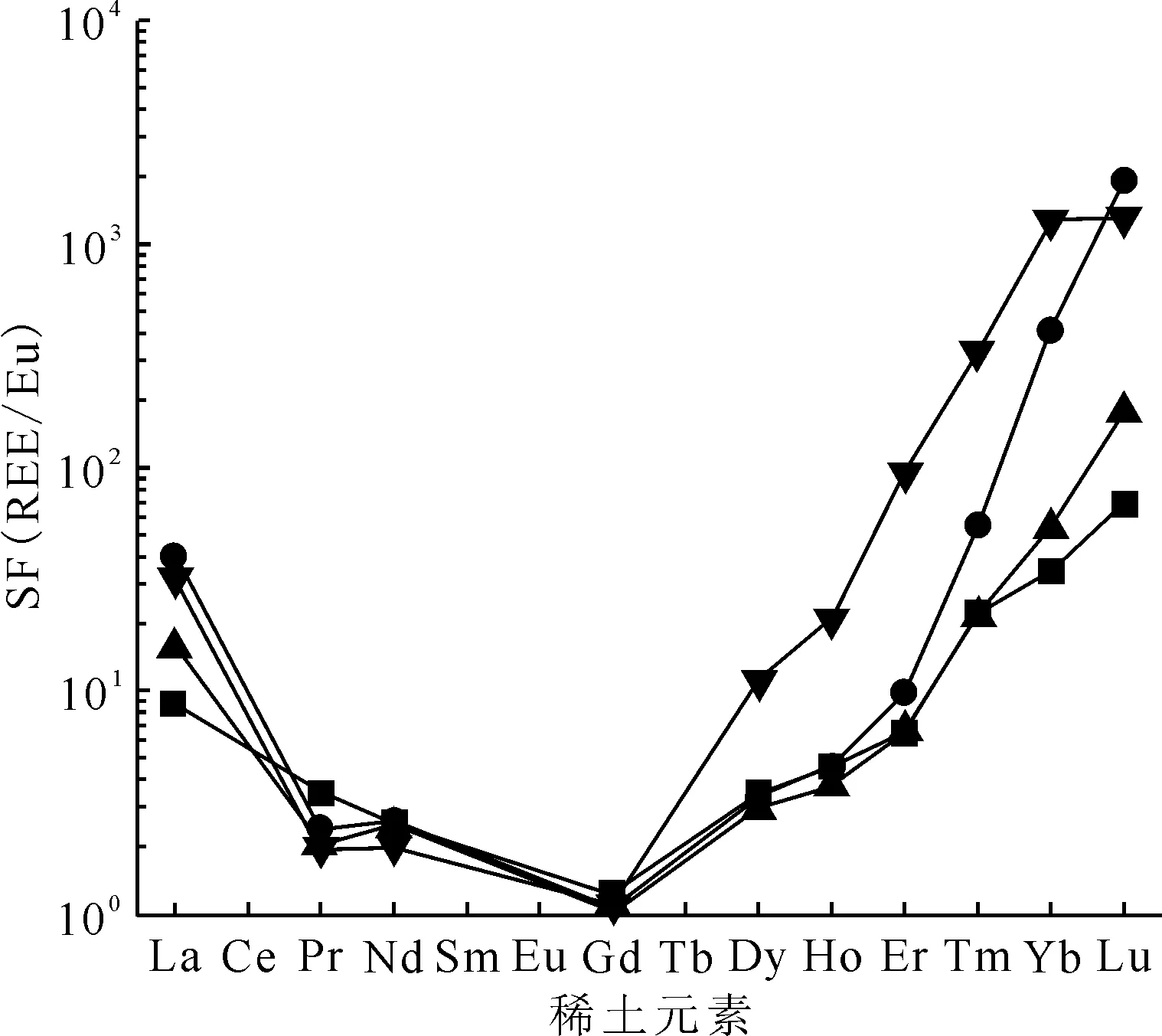
■——HDEHP,●——[TOMA][DEHP],▲——[THTP][DEHP],▼——[TBA][DEHP]图15 HDEHP、 [TBA][DEHP]、 [TOMA][DEHP]和[THTP][DEHP]在[C6mim][NTf2]中萃取不同稀土元素相对于Eu3+的分离因子[35]Fig.15 Separation factors of REEs versus Eu3+ using HDEHP, [TBA][DEHP], [TOMA][DEHP] and [THTP][DEHP] in [C6mim][NTf2][35]


(b):△——Lu(Ⅲ),▽——Yb(Ⅲ)图16 液膜设施示意图(a)和两相中Lu(Ⅲ)和Yb(Ⅲ)的浓度随时间变化曲线[36]Fig.16 Schematic diagram of liquid membrane device(a) and concentration variation of Lu(Ⅲ) and Yb(Ⅲ) in the feed and stripping cells with transport time by PIM-3(b)[36]

图17 离子液体稀释剂(左)和功能离子液体(右)的化学结构式[38]Fig.17 Molecular structures and abbreviations of diluent(left) and ligand(right)[38]
3.4 功能离子液体对次锕系金属的萃取分离



图18 基于2-羟基卞胺的咪唑阳离子功能离子液体(a)和苯二甲酸根功能离子液体(b)Fig.18 Chemical structures of 2-hydroxy-benzylamine-based(a) and hydrogen phthalate-based TSILs(b)

图19 基于DGA(a)、CMPO(b)和羟基乙酰胺(c)的功能离子液体[44]Fig.19 Chemical structures of DGA-based(a), CMPO-based(b), and glycoamide-based(c) TSILs[44]
4 总结与展望
本文详细归纳总结了用于铀酰离子、钍离子、镧系和次锕系金属离子萃取分离的功能离子液体研究现状。基于阴/阳离子配位型的功能离子液体各具特色。对于阴离子配位型功能离子液体而言,虽然在较高酸度下质子化效应会显著降低其萃取性能,但其合成时通常仅需使用目标含氧酸根盐进行阴离子交换,易于大量制备。而阳离子修饰的功能离子液体尽管合成相对繁琐,但其结构中可以引入DGA、CMPO和氧化膦等功能性配位基团,结构选择更为灵活,耐酸性也普遍更好,从而展现出更优良的萃取性能。
鉴于功能离子液体在黏度和选择性等方面仍有待进一步改进,后续研究可从分子结构设计上进行优化,降低黏度并使配位位点与目标金属离子更加匹配,从而提高对金属离子的萃取分离能力;优化功能离子液体的合成条件,提升产率的同时降低合成成本,使其适用于大规模生产, 提高功能离子液体在乏燃料后处理中的应用潜能。

