Duchenne 型肌营养不良171 例临床表型与基因型特征分析
方红军 杨 赛 旷小军 江 志 周 珍 王丽娟 吴丽文 杨理明 刘舒蕾 廖红梅
湖南省儿童医院(湖南长沙 410007)
Duchenne 型肌营养不良(Duchenne muscular dystrophy,DMD)是一种单基因遗传病,DMD基因位于X 染色体上,是目前已知的人类最长的基因,跨越2.5 Mb 以上的基因组序列,由79 个外显子组成。DMD基因编码抗肌萎缩蛋白,后者维持肌纤维在收缩过程中肌膜的完整性,DMD基因变异导致其不完整或者部分功能缺陷从而致病。DMD基因变异会导致DMD或Becker肌营养不良(Becker muscular dystrophy,BMD),统称为肌营养不良[1]。该基因的框架外变异通常使得抗肌萎缩蛋白完全缺失,从而导致严重的表型DMD;相反框内变异通常与轻度BMD相关,伴有截短的抗肌萎缩蛋白表达。阅读框规则适用于90%的病例,通常用于确诊DMD并区分DMD和BMD[2]。DMD患者在儿童早期就出现了运动功能的快速恶化,男孩通常在12岁之前丧失行走能力。临床诊断为DMD的患儿,首先需应用多重连接依赖式探针扩增技术(MLPA)进一步验证,用这种方法在大多数患儿中发现了缺失和重复,其是筛选这些变异的成本最低的方法。MLPA阴性者需要进一步应用外显组测序技术进行测序以检测微小变异[3]。目前最普遍的治疗包括糖皮质激素、心脏保护、呼吸支持和康复功能训练,这些治疗可以改善生活质量,但不能逆转疾病的临床过程及改变结局。目前治疗方法的研究热点集中在基于DNA/ RNA的方法上,例如基于病毒载体的基因治疗(基于DNA)[4]、基于成簇的规则间隔回文重复序列的基因编辑技术(基于DNA)[5]、终止密码子通读方法(基于RNA)和外显子跳跃(基于RNA)[6]。本文总结DMD患儿的临床及基因特点,以充实DMD数据库,为DMD大型研究提供基础数据。
1 对象与方法
1.1 研究对象
收集2014年1月至2020年6月在湖南省儿童医院就诊并通过临床及基因检测确诊的DMD患儿171例的临床资料。纳入标准:①年龄 0~18岁;②符合DMD 临床诊断标准,即进行性四肢近端肌无力,腓肠肌假性肥大,Gowers征阳性,血清肌酸激酶(CK)升高,肌电图呈肌源性损害[7];③应用MLPA、外显组测序及Sanger测序技术进行基因诊断。排除标准:①存在精神病及其他神经遗传性疾病;②基因检测阴性。
本研究获得医院医学伦理委员会批准(No.HCHLL-2021-97)和研究对象法定监护人的知情同意。
1.2 方法
1.2.1 临床资料收集 收集患儿年龄,性别,肌酶包括肌酸激酶(CK)、肌酸激酶同工酶(CKMB)、乳酸脱氢酶(LDH),肝酶包括丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST),发育情况,家族史等临床资料。
1.2.2 标本采集 采集患儿外周静脉血2 mL 于EDTA 抗凝管中,使用血液DNA 提取试剂盒(北京全式金生物技术有限公司),按说明书操作提取患儿全基因组DNA。
1.2.3 MLPA分析 取50 ng DNA 采用1×TE缓冲液定量至5 µL,采用MRC-Holland公司MLPA试剂盒进行DNA 变性、探针杂交、连接反应、扩增,PCR 产物采用ABI 3730XL进行检测,检测结果通过COFFALYSER软件进行数据分析。
1.2.4 外显组测序 将先证者全血用全基因组DNA 提取盒(北京康为世纪生物科技有限公司CWE 9600)提取基因组 DNA,取0.75 μg DNA样本进行超声打断,打断程序为50%强度超声3 s 停1 s,共35 min,得到200~300 bp的DNA片段。采用KAPA高通量文库构建试剂盒构建DNA文库。真空浓缩DNA 文库样本进行杂交捕获,PCR 产物采用Ampure磁珠进行纯化,并进行Qubit定量。取捕获后的DNA样本进行Illumina NovaSeq高通量测序。所有变异均通过Sanger测序验证。
1.2.5 生物信息学分析 测序数据经Illumina序列控制软件评估合格后,进行数据读取和生物信息学分析。
1.2.6 家系成员检测 对同意行基因验证的93例先证者母亲采集外周静脉血2~3 mL,根据先证者检测到致病基因的不同类型选择不同的验证方法。若先证者为缺失、重复水平变异,则选择MLPA方法进行验证;若为单核苷酸水平变异,则用Sanger 测序法进行验证。
1.2.7 ACMG 结果判读 变异致病性判定主要依据ACMG指南2015版[8],将基因变异类型分为良性变异、可能良性变异、临床意义未明变异、致病性变异(包括可能致病变异和致病变异)。
1.3 统计学分析
采用SPSS 23.0 软件进行统计学分析。符合正态分布的计量资料以均数±标准差表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验,两组间比较采用两独立样本t检验;非正态分布计量资料以中位数(P25~P75)表示,组间比较采用秩和检验。计数资料以例数(百分比)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
171 例患儿中男165、女6 例;中位年龄4.1(1.7~7.0)岁,其中<1 岁21 例,~3 岁41 例,~7 岁65例,~13岁44例。23例患儿有相关家族史,5例二胎为DMD。
所有患儿就诊时的CK中位数为4 840.0(1 796.0~8 877.5)U/L,LDH为1 003.0(758.0~1 240.4)IU/L,CKMB 为165.7(99.8~241.9)U/L,ALT 为290.3(191.0~414.1)IU/L,AST为185.0(143.0~288.1)IU/L,均明显升高。
2.2 婴幼儿首次神经内科就诊原因
婴儿组21例,男20例、女1例,因呼吸道、肠道感染等常见疾病或体检发现肌酶升高就诊者15 例(71.4%)、发现肝酶升高就诊者3例(14.3%),因竖头不稳、双手不能主动抓物、不能独坐等运动落后症状就诊者2 例(9.5%),因家族中有DMD 患者就诊者1例(4.8%)。
幼儿组41例,男38例、女3例,因肌酶升高就诊者16例(39.0%),因肝酶升高就诊者7例(17.1%),因不喜自行走路、爬楼需扶行等运动障碍就诊者15例(36.6%),因家族史就诊者3例(7.3%)。
与幼儿组比较,婴儿组因肌酶升高首次至神经内科就诊比例较高(χ2=5.83,P=0.016),因运动落后就诊比例较低(χ2=5.11,P=0.024),差异均有统计学意义。
2.3 DMD基因大片段缺失/重复变异
171 例患儿中,111 例为大缺失变异(64.9%),26例为大重复变异(15.2%)。在111例大缺失变异患儿中,热点变异位于两个缺失区域,即基因中央区外显子45~52区76例(占大缺失变异68.5%),5’端外显子2~28区21例(占大缺失变异18.9%);外显子49~52区缺失(7例,占大缺失变异4.1%)和外显子49~50区缺失(7例,占大缺失变异4.1%)为最常见的缺失。外显子2~26区存在重复热点17例,占所有大重复变异65.4%。大缺失变异中缺失最长的外显子位于17~79 区,大重复变异中重复最长的外显子位于13~44区。
本研究中共60 种缺失类型。其中在中央区外显子45~52 区检测到34 种缺失类型(34/76,占44.74%),而在5’端外显子2~28区检测到19种缺失类型(19/21,90.48%),两个区域间缺失类型比例的差异有统计学意义(χ2=13.89,P<0.001)。26例大重复变异中有24种不同的重复类型(92.3%)。见图1、2。

图1 进行性DMD 111 例致病DMD 基因大缺失定位图

图2 进行性DMD 26 例致病DMD 基因大重复定位图
2.4 DMD基因点变异
171例患儿中34例为点变异(19.9%),其中4例错义变异(2例未被报道)、17例无义变异(7例未报道)、6例移码变异(4例未报道)、7例为非编码区域的剪接变异(6例未报道)。DMD点变异贯穿于整个DMD基因中,第1区域(外显子1~20)7例(20.6%)、第2区域(外显子21~40)8例(23.5%)、第3区域(外显子41~60)5例(14.7%)、第4区域(外显子61~79)7例(20.6%)、第5区域(内含子区)7例(20.6%)。其中外显子10、16、27、34、35、64均出现2个点变异,其余均出现1个点变异。见表1。
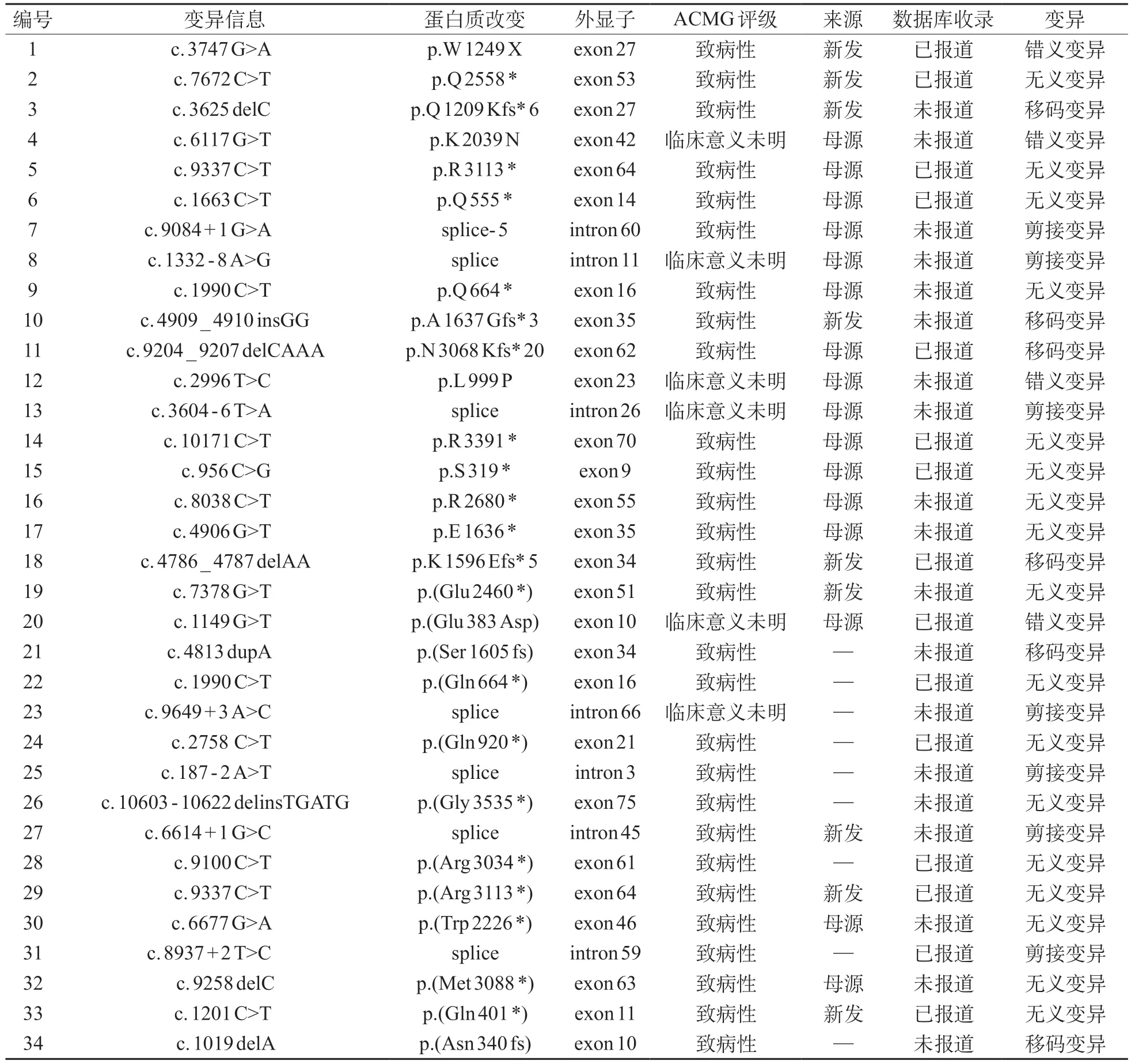
表1 DMD基因单核苷酸水平致病性变异
2.5 先证者母亲携带者状况分析
共93例患儿做了母亲验证,58例母亲为携带者,具有与子女相同的变异,携带率为62.4%。其中大缺失变异35例、大重复变异7例、点变异16例(其中错义变异3例、无义变异9例、剪接变异3例、移码变异1例)。
78 例母亲未完成基因检测,包括无再次生育需求23例、父母离异5例、抽血时母亲不在现场18例、经济原因32例。
2.6 不同基因变异类型组间生化指标比较
按照基因变异类型分成6组,分别为缺失组、重复组、错义变异组、无义变异组、移码变异组、剪接变异组。不同基因变异类型组间发病年龄及生化指标差异无统计学意义(P>0.05)。见表2。
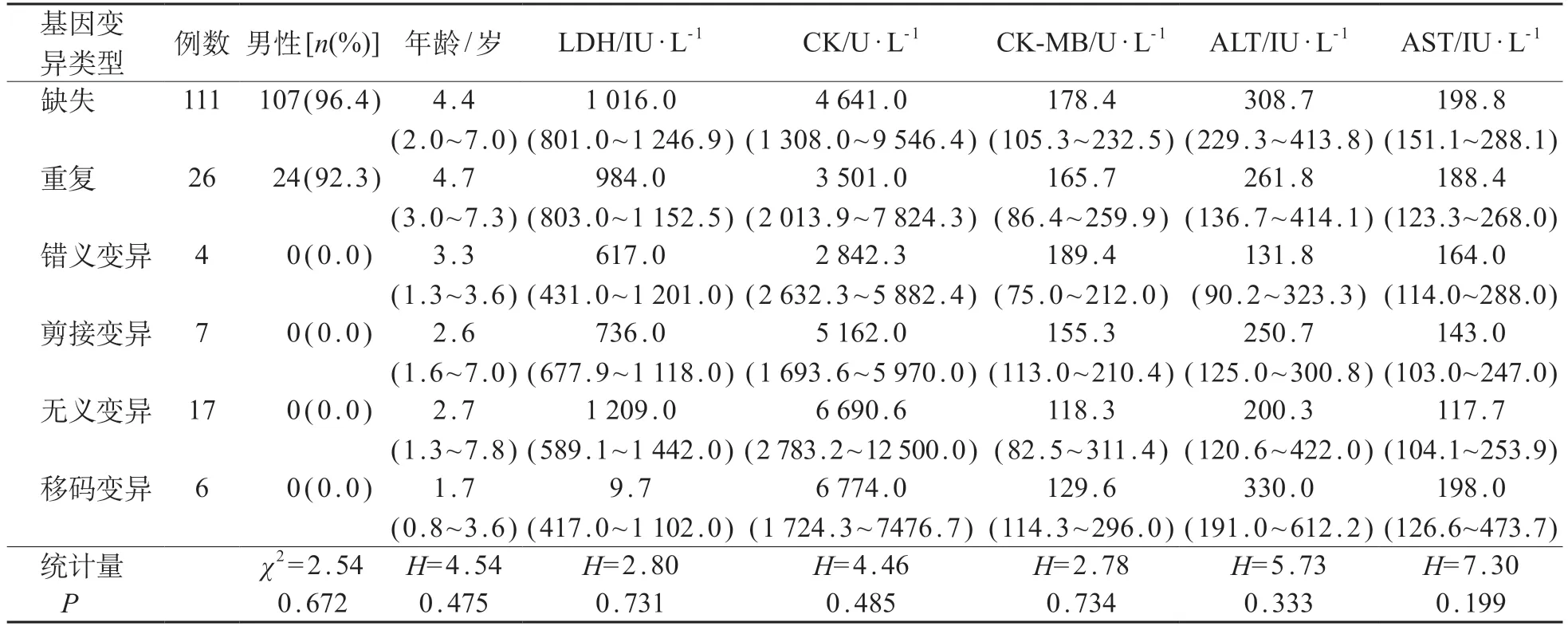
表2 不同基因变异类型对年龄、肌酶和肝酶的影响[M(P25~P75)]
3 讨论
DMD是一种X连锁的隐性神经肌肉疾病,大约每3 500~5 000名男婴中就有1例患病者[2]。由于缺乏维持肌肉细胞膜完整性所需的功能性肌营养不良蛋白,DMD 主要临床表现为运动功能受损,患儿可出现宽基底步态或鸭步、运动发育落后、上楼困难、跑步慢、容易摔跤、抬头无力,Gowers征阳性,一般3~5岁开始逐渐运动倒退,容易疲劳,部分患儿出现肌痛,后期可表现为腓肠肌假性肥大。大部分患儿可出现非运动功能障碍,如注意力不集中、行为异常、认知及语言迟滞[9-10],后期可出现心肺功能障碍,并最终死于心力或呼吸衰竭[11]。DMD起病隐匿,婴幼儿通常不会出现典型的肌无力症状。本研究中婴儿21例,幼儿41例,婴儿因体检或呼吸道感染等常见疾病检查发现肌酶升高而首次至神经内科就诊的比例较高,而幼儿因运动落后首次就诊的比例较高。因此,对于有肌酶升高、运动落后等症状的患儿应警惕,积极完善基因检查。
DMD中最常见的变异是基因缺失。本研究中大缺失(111例,64.9%)和小缺失(6例,3.5%)占所有变异的68.4%;最常见的缺失热点区域位于外显子45~52区(68.5%),其次为外显子2~26区(18.9%),结果与其他研究基本一致[12-13]。尽管在DMD基因的几乎任何地方都可能发生缺失,但两个热点区域位于基因的中心部分和5'末端。与其他热点相比,热点中的某些缺失类型被检测到的频率更高。正如预期的那样,在本研究和前期研究中,外显子2~26和外显子3~7 分别为复制热点和最常见的外显子复制模式[14],与全球范围内的热点区域和最常见的变异类型(重复、缺失)相似,这表明基于种族的DMD 中外显子缺失和重复的比例差异很小[3]。本研究中不同基因变异类型组间患儿发病年龄、CK等生化指标的差异无统计学意义,可能因各种基因变异类型可发生于DMD基因的任何位置且影响基因片段长度不等,无相对固定的发病年龄及疾病严重程度。
DMD呈X连锁隐形遗传病,具有以下特点:患者多为男性,男性患者双亲一般正常,母亲为携带者,患者的兄弟、姨表兄弟、舅舅及外甥可能患病,呈非连续性遗传。携带者状态的确定对于携带者筛查和及时的遗传咨询都是至关重要的。由于缺乏有关遗传咨询和产前诊断的知识,一些DMD家谱包含了多例患者。本研究中23例患儿有相关家族史,5例二胎为DMD。共93 例患儿做了母亲验证,其中58例患儿母亲为携带者,携带率为62.4%。因此,对于DMD家系,应该及时就医,完善基因检测以明确病因,家族中的女性成员均应行携带者检测,积极进行遗传咨询及评估生育风险。当前的遗传咨询将2/3的携带者风险归因于DMD 患儿的母亲[3]。在进行携带者生育风险评估时应该掌握如下原则,男性后代中50%正常,50%患病;而女性后代一般不患病,但50%同为携带者。且新发变异中14%含有生殖腺嵌合体可能,也就是说DMD患儿母亲虽未检测到携带相同的致病基因,仍有产生异常配子的可能。因此新发变异患儿的母亲在再次妊娠前,需进行产前咨询。
目前DMD 常规药物治疗为肾上腺糖皮质激素[15],研究发现长期使用激素利大于弊,激素可以提高肌肉力量,延长步行能力,保持脊柱功能及心脏功能,增加肺功能,从而改善患儿健康状况,延长寿命[16]。如果没有接受皮质类固醇治疗,DMD有90%的机会可发展为进行性脊柱侧弯[17]。DMD 的其他治疗包括内分泌治疗,如睾酮及生长激素的治疗。睾丸激素对骨胳健康以及心理社会情感的发展很重要,睾酮治疗应从低剂量开始,并缓慢增加,以模拟正常青春期[18]。但是没有任何证据或文献评估生长激素在不缺乏生长激素患儿中使用的安全性或有效性。研究表明在无症状的情况下,DMD患儿心肺功能也可能已经受损,因此一旦确诊DMD,需定期做心、肺功能检查,及早发现问题、及早治疗[19-20]。骨骼肌的管理也很重要,走路时保持正确的姿势有助于预防背部、脚和踝关节的挛缩;在轮椅上安装适当的座位系统,及支持脊柱和骨盆的对称性和脊柱的伸展,是至关重要的[21-22]。
目前,基因治疗研究很热。基于RNA 的疗法,例如终止密码子通读疗法和外显子跳跃疗法[23],给无义变异和大缺失变异的患儿带来了希望。阿塔鲁伦(ataluren)为翻译通读诱导药物,能够读取mRNA中的提前终止密码子,从而产生有功能性的肌营养不良蛋白,并已获得欧洲药品管理局的有条件批准,可用于治疗无义变异的DMD 患儿[24]。这项研究中有11.9%的患儿可以从该疗法中获益。反义寡核苷酸(AON)介导的外显子跳跃是DMD患儿的另一种潜在疗法,将框外转录物转换为框内转录物,诱导产生截短但是存在部分功能的肌营养不良蛋白[25-26]。依替普利森(etiplisen)用于外显子51的跳跃[27],已获得FDA有条件批准,多项临床试验证明依替普利森减轻了患儿步行能力的下降程度,使DMD患儿长期受益。同时,针对第53 外显子的吗啉反义寡核苷酸(PMO)golodirsen和针对第45外显子跳跃的临床试验最近已启动[28]。基因添加是一种很有前途的治疗策略,对所有基因变异类型的患儿都具有普遍性。相关研究描述了一种来自外显子50缺失的DMD患儿的诱导多能干细胞中的位点特异性基因添加策略。微型肌营养不良基因片段精确靶向定位于核糖体RNA基因(RDNA)位点。在经过遗传校正的诱导多能干细胞及其衍生心肌细胞中,抗肌萎缩蛋白的表达和膜定位都得到了恢复,在修饰的心肌细胞中观察到了增强的自发收缩[29]。这些结果为DMD 朝着精确治疗迈出重要一步。针对其他外显子的反义寡核苷酸仍处于开发阶段,并面临许多挑战[30]。因此,提供DMD变异详细数据对于应对这些挑战至关重要。
本研究收集了171 例DMD 患儿的临床资料及基因变异信息,对这些数据的分析表明,该人群中的变异分布与以往报道基本一致。本研究数据为DMD的基础研究、临床试验及未来基因治疗提供参考。

